2022-2023学年高中化学苏教版选择性必修1 课时跟踪检测(六) 电解池的工作原理 word版含解析
文档属性
| 名称 | 2022-2023学年高中化学苏教版选择性必修1 课时跟踪检测(六) 电解池的工作原理 word版含解析 |

|
|
| 格式 | doc | ||
| 文件大小 | 391.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-08-24 00:00:00 | ||
图片预览



文档简介
课时跟踪检测(六) 电解池的工作原理
[基础巩固练]
知识点一 电解池的工作原理及构成条件
1.下列有关电解原理的说法正确的是( )
①电解是把电能转化成化学能 ②电解是把化学能转化成电能 ③电解质溶液导电是化学变化,金属导电是物理变化 ④不能自发进行的氧化还原反应,通过电解的原理可以实现 ⑤任何溶液被电解时,必然导致氧化还原反应的发生
A.①②③④ B.②③⑤
C.③④ D.①③④⑤
2.(2021·江苏盐城高二月考)如图是电解氯化铜溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是( )
A.a为负极,b为正极
B.a为阳极,b为阴极
C.电解过程中,d电极质量增加
D.电解过程中,氯离子浓度不变
3.如图所示装置中,属于电解池的是( )
4.为使反应Cu+2H2O===Cu(OH)2+H2↑能够发生,下列设计方案正确的是( )
A.用铜片作负极,石墨电极作正极,氯化钠溶液为电解质溶液构成原电池
B.用铜片作电极,外接直流电源电解硫酸铜溶液
C.用铜片作阳极,铁片作阴极,电解硫酸钠溶液
D.用铜片作阴、阳电极,电解稀硫酸
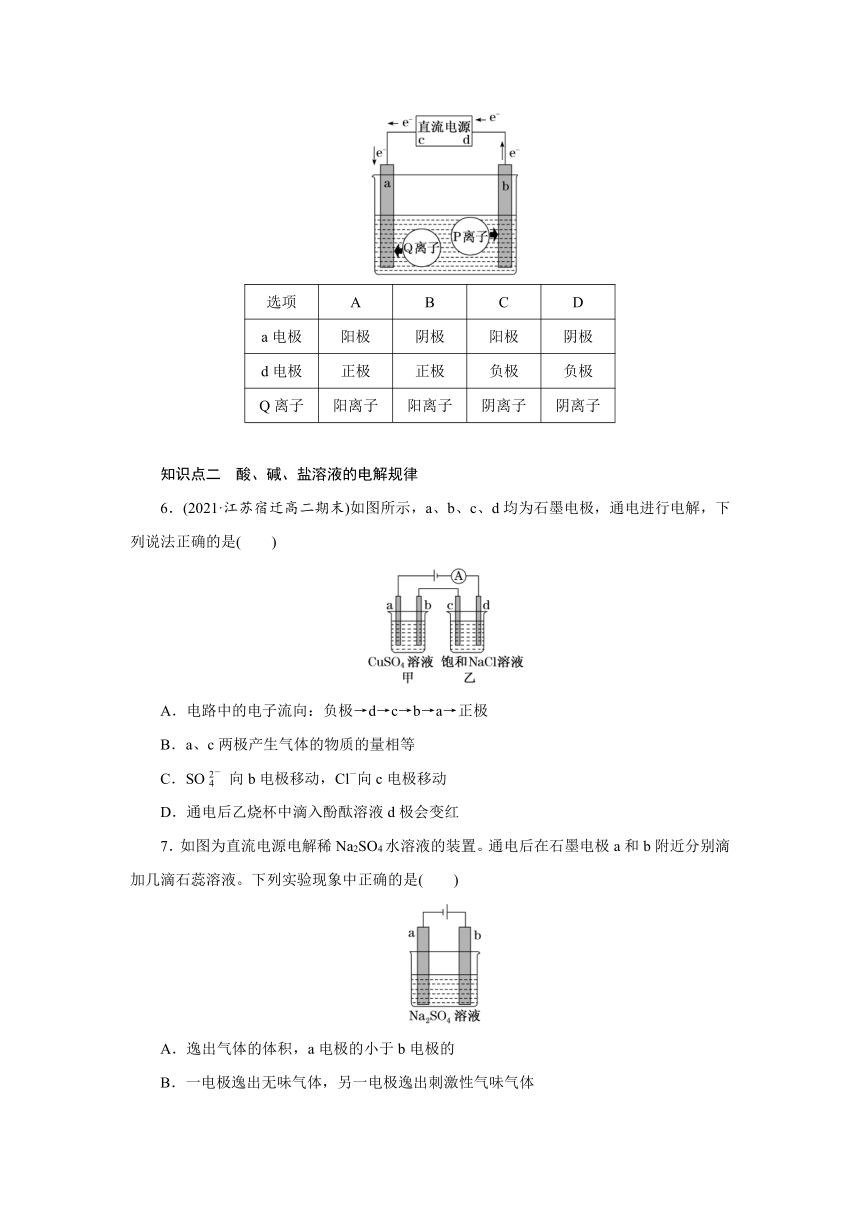
5.(2021·江苏扬州高二检测)某同学将电解池工作时的电子、离子流动方向及电极种类等信息表示在图中,下列有关分析完全正确的是( )
选项 A B C D
a电极 阳极 阴极 阳极 阴极
d电极 正极 正极 负极 负极
Q离子 阳离子 阳离子 阴离子 阴离子
知识点二 酸、碱、盐溶液的电解规律
6.(2021·江苏宿迁高二期末)如图所示,a、b、c、d均为石墨电极,通电进行电解,下列说法正确的是( )
A.电路中的电子流向:负极→d→c→b→a→正极
B.a、c两极产生气体的物质的量相等
C.SO向b电极移动,Cl-向c电极移动
D.通电后乙烧杯中滴入酚酞溶液d极会变红
7.如图为直流电源电解稀Na2SO4水溶液的装置。通电后在石墨电极a和b附近分别滴加几滴石蕊溶液。下列实验现象中正确的是( )
A.逸出气体的体积,a电极的小于b电极的
B.一电极逸出无味气体,另一电极逸出刺激性气味气体
C.a电极附近呈红色,b电极附近呈蓝色
D.a电极附近呈蓝色,b电极附近呈红色
8.(2021·浙江温州高二检测)下列选项中,每种电解质溶液电解时只生成氢气和氧气的是( )
A.HCl、CuCl2、Ba(OH)2
B.NaOH、CuSO4、H2SO4
C.NaOH、H2SO4、Ba(OH)2
D.NaBr、H2SO4、Ba(OH)2
9.用石墨作电极电解下列溶液:
①稀H2SO4 ②K2SO4溶液 ③CuCl2溶液 ④CuSO4溶液 ⑤KOH溶液
(1)阴极、阳极都有气体产生,且体积比(相同条件下)为2∶1 的是__________(填序号),其阳极的电极反应式都是_______________________________________________________,
阴极的电极反应式都是_________________________________________________,
电解反应方程式都是____________________________________________________。
(2)阴极、阳极都有气体产生,其中溶液酸性增强的是____________(填序号)。
(3)一个电极析出金属,另一个电极逸出刺激性气味气体的是________(填序号),其阳极的电极反应式是______________________________________________________
________________________________________________________________________。
[素养提升练]
10.(2021·湖南长沙高二月考)下列有关 2 个电化学装置的叙述不正确的是( )
A.图Ⅰ,在不改变总反应的前提下,可用 Na2SO4 替换 ZnSO4,用石墨替换 Cu 棒
B.图Ⅰ,电流形成的完整过程是负极Zn-2e-===Zn2+,电子经导线流向正极,正极 Cu2++2e-===Cu
C.图Ⅱ,通电后向两极滴加酚酞溶液,左侧变红
D.图Ⅰ,盐桥中 Cl-向左侧移动,图Ⅱ,溶液中 Cl-向右侧移动
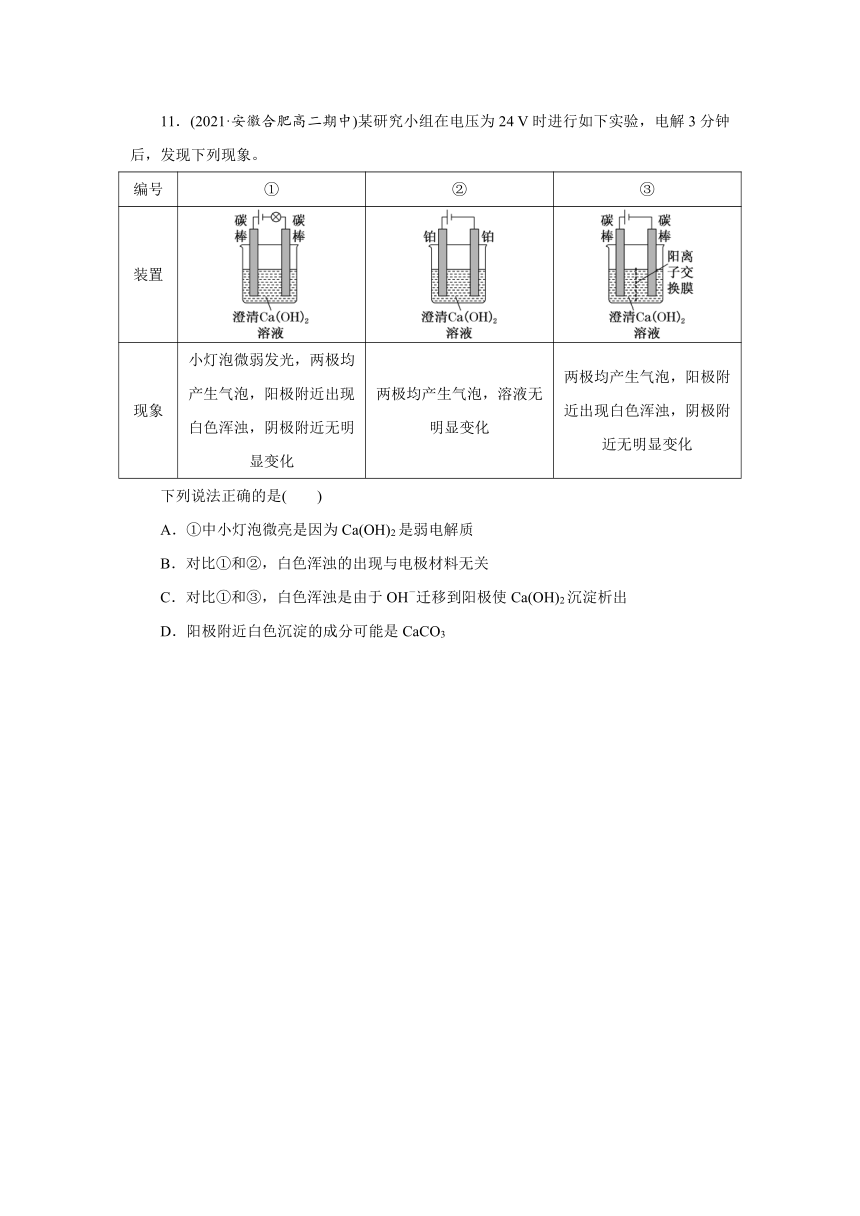
11.(2021·安徽合肥高二期中)某研究小组在电压为24 V时进行如下实验,电解3分钟后,发现下列现象。
编号 ① ② ③
装置
现象 小灯泡微弱发光,两极均产生气泡,阳极附近出现白色浑浊,阴极附近无明显变化 两极均产生气泡,溶液无明显变化 两极均产生气泡,阳极附近出现白色浑浊,阴极附近无明显变化
下列说法正确的是( )
A.①中小灯泡微亮是因为Ca(OH)2是弱电解质
B.对比①和②,白色浑浊的出现与电极材料无关
C.对比①和③,白色浑浊是由于OH-迁移到阳极使Ca(OH)2沉淀析出
D.阳极附近白色沉淀的成分可能是CaCO3
课时跟踪检测(六) 电解池的工作原理
[基础巩固练]
知识点一 电解池的工作原理及构成条件
1.下列有关电解原理的说法正确的是( )
①电解是把电能转化成化学能 ②电解是把化学能转化成电能 ③电解质溶液导电是化学变化,金属导电是物理变化 ④不能自发进行的氧化还原反应,通过电解的原理可以实现 ⑤任何溶液被电解时,必然导致氧化还原反应的发生
A.①②③④ B.②③⑤
C.③④ D.①③④⑤
解析:D 电解时先通电,后发生化学反应,电解是把电能转化成化学能,①正确,②错误;电解质溶液导电时,两个电极上发生氧化还原反应,有新物质生成,发生的是化学变化,金属导电是自由电子的定向移动,没有新物质生成,是物理变化,③、⑤正确;电解不仅能使自发反应进行,也能使非自发反应进行,即无论氧化还原反应是否可以自发进行,都可通过电解的原理实现,④正确;故选D。
2.(2021·江苏盐城高二月考)如图是电解氯化铜溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是( )
A.a为负极,b为正极
B.a为阳极,b为阴极
C.电解过程中,d电极质量增加
D.电解过程中,氯离子浓度不变
解析:C 由图示电流方向可知,a是电源正极,b是电源负极;则c是电解池的阳极,电极反应式为2Cl--2e-===Cl2↑,溶液中氯离子不断减少;d是电解池的阴极,电极反应式为Cu2++2e-===Cu,d电极质量不断增加。
3.如图所示装置中,属于电解池的是( )
解析:C 根据电解池的构成条件进行判断,装置A、B、D中无直流电源,且装置D中不能形成闭合回路,因此A、B、D不能形成电解池。
4.为使反应Cu+2H2O===Cu(OH)2+H2↑能够发生,下列设计方案正确的是( )
A.用铜片作负极,石墨电极作正极,氯化钠溶液为电解质溶液构成原电池
B.用铜片作电极,外接直流电源电解硫酸铜溶液
C.用铜片作阳极,铁片作阴极,电解硫酸钠溶液
D.用铜片作阴、阳电极,电解稀硫酸
解析:C 该反应为不能自发进行的氧化还原反应,必须设计为电解池才能发生。阳极为Cu放电,阴极为H+放电,即用Cu作阳极,电解质溶液中为H2O放电,选项C符合要求。
5.(2021·江苏扬州高二检测)某同学将电解池工作时的电子、离子流动方向及电极种类等信息表示在图中,下列有关分析完全正确的是( )
选项 A B C D
a电极 阳极 阴极 阳极 阴极
d电极 正极 正极 负极 负极
Q离子 阳离子 阳离子 阴离子 阴离子
解析:B 根据题图知,该装置有外接电源,所以属于电解池,根据电子流向知,c是负极,d是正极,a是阴极,b是阳极。电解时,电解质溶液中的阳离子向阴极移动,阴离子向阳极移动,则Q离子是阳离子,P离子是阴离子,故B正确。
知识点二 酸、碱、盐溶液的电解规律
6.(2021·江苏宿迁高二期末)如图所示,a、b、c、d均为石墨电极,通电进行电解,下列说法正确的是( )
A.电路中的电子流向:负极→d→c→b→a→正极
B.a、c两极产生气体的物质的量相等
C.SO向b电极移动,Cl-向c电极移动
D.通电后乙烧杯中滴入酚酞溶液d极会变红
解析:D 电子只能在外电路中移动,故A错误;a极产生O2,c极产生Cl2,根据电子守恒得关系式:O2~2Cl2~4e-,O2和Cl2的物质的量之比为1∶2,故B错误;阴离子向阳极移动,a和c是阳极,所以SO向a电极移动,Cl-向c电极移动,故C错误;d极是阴极,电极反应式为2H2O+2e-===H2↑+2OH-,所以通电后乙烧杯中滴入酚酞溶液d极会变红,故D正确。
7.如图为直流电源电解稀Na2SO4水溶液的装置。通电后在石墨电极a和b附近分别滴加几滴石蕊溶液。下列实验现象中正确的是( )
A.逸出气体的体积,a电极的小于b电极的
B.一电极逸出无味气体,另一电极逸出刺激性气味气体
C.a电极附近呈红色,b电极附近呈蓝色
D.a电极附近呈蓝色,b电极附近呈红色
解析:D a为阴极产生氢气,b为阳极产生氧气,逸出气体的体积,a电极的大于b电极的,故A、B错误;a电极氢离子放电,a电极周围还有大量的氢氧根离子,使a电极附近的石蕊溶液变为蓝色,b电极氢氧根离子放电,b电极周围还有大量的氢离子,使b电极附近的石蕊溶液变为红色,故C错误,D正确。
8.(2021·浙江温州高二检测)下列选项中,每种电解质溶液电解时只生成氢气和氧气的是( )
A.HCl、CuCl2、Ba(OH)2
B.NaOH、CuSO4、H2SO4
C.NaOH、H2SO4、Ba(OH)2
D.NaBr、H2SO4、Ba(OH)2
解析:C A中,2HClCl2↑+H2↑,CuCl2Cu+Cl2↑,错误;B中,2CuSO4+2H2O2Cu+2H2SO4+O2↑,错误;D中,2NaBr+2H2O2NaOH+H2↑+Br2,错误。
9.用石墨作电极电解下列溶液:
①稀H2SO4 ②K2SO4溶液 ③CuCl2溶液 ④CuSO4溶液 ⑤KOH溶液
(1)阴极、阳极都有气体产生,且体积比(相同条件下)为2∶1 的是__________(填序号),其阳极的电极反应式都是_______________________________________________________,
阴极的电极反应式都是_________________________________________________,
电解反应方程式都是____________________________________________________。
(2)阴极、阳极都有气体产生,其中溶液酸性增强的是____________(填序号)。
(3)一个电极析出金属,另一个电极逸出刺激性气味气体的是________(填序号),其阳极的电极反应式是______________________________________________________
________________________________________________________________________。
解析:(1)电解水时,阴极氢离子放电,生成氢气,阳极氢氧根离子放电,生成氧气,两极都有气体产生,且体积比(相同条件下)为2∶1,电解①②⑤时,均相当于电解水,阴极氢离子放电,生成氢气,即2H++2e-===H2↑,阳极氢氧根离子放电,生成氧气,即4OH--4e-===2H2O+O2↑,电解反应为2H2O2H2↑+O2↑;(2)电解①②⑤时,两极都有气体产生,电解③④时,阴极Cu2+放电,没有气体产生,①溶液的浓度增大,pH变小;②溶液的浓度增大,pH不变;⑤溶液的浓度增大,pH变大;(3)电解③④时,阴极都是Cu2+放电,析出金属铜,③中阳极Cl-放电产生的氯气有刺激性气味;④中阳极OH-放电产生的氧气无刺激性气味。
答案:(1)①②⑤ 4OH--4e-===2H2O+O2↑ 2H++2e-===H2↑ 2H2O2H2↑+O2↑
(2)① (3)③ 2Cl--2e-===Cl2↑
[素养提升练]
10.(2021·湖南长沙高二月考)下列有关 2 个电化学装置的叙述不正确的是( )
A.图Ⅰ,在不改变总反应的前提下,可用 Na2SO4 替换 ZnSO4,用石墨替换 Cu 棒
B.图Ⅰ,电流形成的完整过程是负极Zn-2e-===Zn2+,电子经导线流向正极,正极 Cu2++2e-===Cu
C.图Ⅱ,通电后向两极滴加酚酞溶液,左侧变红
D.图Ⅰ,盐桥中 Cl-向左侧移动,图Ⅱ,溶液中 Cl-向右侧移动
解析:B 将图Ⅰ中的ZnSO4替换为Na2SO4,对左侧区反应无影响,将Cu棒替换为石墨棒,仍然是锌为负极,石墨棒为正极,故并不改变总反应,故A正确;图Ⅰ中电流形成的完整过程是负极Zn-2e-===Zn2+,外电路中电子经导线流向正极,正极Cu2++2e-===Cu,内电路的盐桥中的阴离子移向负极,阳离子移向正极,故B错误;图Ⅱ中左侧区是阴极,电极反应为2H2O+2e-===H2↑+2OH-,故阴极区显碱性,加酚酞后溶液变红,故C正确;图Ⅰ中左侧为负极,故盐桥中Cl-向左侧移动,图Ⅱ中右侧是阳极,故溶液中Cl-向右侧移动,故D正确。
11.(2021·安徽合肥高二期中)某研究小组在电压为24 V时进行如下实验,电解3分钟后,发现下列现象。
编号 ① ② ③
装置
现象 小灯泡微弱发光,两极均产生气泡,阳极附近出现白色浑浊,阴极附近无明显变化 两极均产生气泡,溶液无明显变化 两极均产生气泡,阳极附近出现白色浑浊,阴极附近无明显变化
下列说法正确的是( )
A.①中小灯泡微亮是因为Ca(OH)2是弱电解质
B.对比①和②,白色浑浊的出现与电极材料无关
C.对比①和③,白色浑浊是由于OH-迁移到阳极使Ca(OH)2沉淀析出
D.阳极附近白色沉淀的成分可能是CaCO3
解析:D ①中小灯泡微亮是因为Ca(OH)2在水中的溶解度小,实质上Ca(OH)2溶于水后能完全电离,属于强电解质,A错误;对于①,阳极上溶液中OH-失去电子,发生氧化反应,电极反应式为4OH--4e-===O2↑+2H2O,O2与C电极发生反应产生CO2,CO2与溶液中的Ca(OH)2反应产生CaCO3白色沉淀,可见白色浑浊的出现与电极材料有关,B、C错误,D正确。
[基础巩固练]
知识点一 电解池的工作原理及构成条件
1.下列有关电解原理的说法正确的是( )
①电解是把电能转化成化学能 ②电解是把化学能转化成电能 ③电解质溶液导电是化学变化,金属导电是物理变化 ④不能自发进行的氧化还原反应,通过电解的原理可以实现 ⑤任何溶液被电解时,必然导致氧化还原反应的发生
A.①②③④ B.②③⑤
C.③④ D.①③④⑤
2.(2021·江苏盐城高二月考)如图是电解氯化铜溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是( )
A.a为负极,b为正极
B.a为阳极,b为阴极
C.电解过程中,d电极质量增加
D.电解过程中,氯离子浓度不变
3.如图所示装置中,属于电解池的是( )
4.为使反应Cu+2H2O===Cu(OH)2+H2↑能够发生,下列设计方案正确的是( )
A.用铜片作负极,石墨电极作正极,氯化钠溶液为电解质溶液构成原电池
B.用铜片作电极,外接直流电源电解硫酸铜溶液
C.用铜片作阳极,铁片作阴极,电解硫酸钠溶液
D.用铜片作阴、阳电极,电解稀硫酸
5.(2021·江苏扬州高二检测)某同学将电解池工作时的电子、离子流动方向及电极种类等信息表示在图中,下列有关分析完全正确的是( )
选项 A B C D
a电极 阳极 阴极 阳极 阴极
d电极 正极 正极 负极 负极
Q离子 阳离子 阳离子 阴离子 阴离子
知识点二 酸、碱、盐溶液的电解规律
6.(2021·江苏宿迁高二期末)如图所示,a、b、c、d均为石墨电极,通电进行电解,下列说法正确的是( )
A.电路中的电子流向:负极→d→c→b→a→正极
B.a、c两极产生气体的物质的量相等
C.SO向b电极移动,Cl-向c电极移动
D.通电后乙烧杯中滴入酚酞溶液d极会变红
7.如图为直流电源电解稀Na2SO4水溶液的装置。通电后在石墨电极a和b附近分别滴加几滴石蕊溶液。下列实验现象中正确的是( )
A.逸出气体的体积,a电极的小于b电极的
B.一电极逸出无味气体,另一电极逸出刺激性气味气体
C.a电极附近呈红色,b电极附近呈蓝色
D.a电极附近呈蓝色,b电极附近呈红色
8.(2021·浙江温州高二检测)下列选项中,每种电解质溶液电解时只生成氢气和氧气的是( )
A.HCl、CuCl2、Ba(OH)2
B.NaOH、CuSO4、H2SO4
C.NaOH、H2SO4、Ba(OH)2
D.NaBr、H2SO4、Ba(OH)2
9.用石墨作电极电解下列溶液:
①稀H2SO4 ②K2SO4溶液 ③CuCl2溶液 ④CuSO4溶液 ⑤KOH溶液
(1)阴极、阳极都有气体产生,且体积比(相同条件下)为2∶1 的是__________(填序号),其阳极的电极反应式都是_______________________________________________________,
阴极的电极反应式都是_________________________________________________,
电解反应方程式都是____________________________________________________。
(2)阴极、阳极都有气体产生,其中溶液酸性增强的是____________(填序号)。
(3)一个电极析出金属,另一个电极逸出刺激性气味气体的是________(填序号),其阳极的电极反应式是______________________________________________________
________________________________________________________________________。
[素养提升练]
10.(2021·湖南长沙高二月考)下列有关 2 个电化学装置的叙述不正确的是( )
A.图Ⅰ,在不改变总反应的前提下,可用 Na2SO4 替换 ZnSO4,用石墨替换 Cu 棒
B.图Ⅰ,电流形成的完整过程是负极Zn-2e-===Zn2+,电子经导线流向正极,正极 Cu2++2e-===Cu
C.图Ⅱ,通电后向两极滴加酚酞溶液,左侧变红
D.图Ⅰ,盐桥中 Cl-向左侧移动,图Ⅱ,溶液中 Cl-向右侧移动
11.(2021·安徽合肥高二期中)某研究小组在电压为24 V时进行如下实验,电解3分钟后,发现下列现象。
编号 ① ② ③
装置
现象 小灯泡微弱发光,两极均产生气泡,阳极附近出现白色浑浊,阴极附近无明显变化 两极均产生气泡,溶液无明显变化 两极均产生气泡,阳极附近出现白色浑浊,阴极附近无明显变化
下列说法正确的是( )
A.①中小灯泡微亮是因为Ca(OH)2是弱电解质
B.对比①和②,白色浑浊的出现与电极材料无关
C.对比①和③,白色浑浊是由于OH-迁移到阳极使Ca(OH)2沉淀析出
D.阳极附近白色沉淀的成分可能是CaCO3
课时跟踪检测(六) 电解池的工作原理
[基础巩固练]
知识点一 电解池的工作原理及构成条件
1.下列有关电解原理的说法正确的是( )
①电解是把电能转化成化学能 ②电解是把化学能转化成电能 ③电解质溶液导电是化学变化,金属导电是物理变化 ④不能自发进行的氧化还原反应,通过电解的原理可以实现 ⑤任何溶液被电解时,必然导致氧化还原反应的发生
A.①②③④ B.②③⑤
C.③④ D.①③④⑤
解析:D 电解时先通电,后发生化学反应,电解是把电能转化成化学能,①正确,②错误;电解质溶液导电时,两个电极上发生氧化还原反应,有新物质生成,发生的是化学变化,金属导电是自由电子的定向移动,没有新物质生成,是物理变化,③、⑤正确;电解不仅能使自发反应进行,也能使非自发反应进行,即无论氧化还原反应是否可以自发进行,都可通过电解的原理实现,④正确;故选D。
2.(2021·江苏盐城高二月考)如图是电解氯化铜溶液的装置,其中c、d为石墨电极,则下列有关判断正确的是( )
A.a为负极,b为正极
B.a为阳极,b为阴极
C.电解过程中,d电极质量增加
D.电解过程中,氯离子浓度不变
解析:C 由图示电流方向可知,a是电源正极,b是电源负极;则c是电解池的阳极,电极反应式为2Cl--2e-===Cl2↑,溶液中氯离子不断减少;d是电解池的阴极,电极反应式为Cu2++2e-===Cu,d电极质量不断增加。
3.如图所示装置中,属于电解池的是( )
解析:C 根据电解池的构成条件进行判断,装置A、B、D中无直流电源,且装置D中不能形成闭合回路,因此A、B、D不能形成电解池。
4.为使反应Cu+2H2O===Cu(OH)2+H2↑能够发生,下列设计方案正确的是( )
A.用铜片作负极,石墨电极作正极,氯化钠溶液为电解质溶液构成原电池
B.用铜片作电极,外接直流电源电解硫酸铜溶液
C.用铜片作阳极,铁片作阴极,电解硫酸钠溶液
D.用铜片作阴、阳电极,电解稀硫酸
解析:C 该反应为不能自发进行的氧化还原反应,必须设计为电解池才能发生。阳极为Cu放电,阴极为H+放电,即用Cu作阳极,电解质溶液中为H2O放电,选项C符合要求。
5.(2021·江苏扬州高二检测)某同学将电解池工作时的电子、离子流动方向及电极种类等信息表示在图中,下列有关分析完全正确的是( )
选项 A B C D
a电极 阳极 阴极 阳极 阴极
d电极 正极 正极 负极 负极
Q离子 阳离子 阳离子 阴离子 阴离子
解析:B 根据题图知,该装置有外接电源,所以属于电解池,根据电子流向知,c是负极,d是正极,a是阴极,b是阳极。电解时,电解质溶液中的阳离子向阴极移动,阴离子向阳极移动,则Q离子是阳离子,P离子是阴离子,故B正确。
知识点二 酸、碱、盐溶液的电解规律
6.(2021·江苏宿迁高二期末)如图所示,a、b、c、d均为石墨电极,通电进行电解,下列说法正确的是( )
A.电路中的电子流向:负极→d→c→b→a→正极
B.a、c两极产生气体的物质的量相等
C.SO向b电极移动,Cl-向c电极移动
D.通电后乙烧杯中滴入酚酞溶液d极会变红
解析:D 电子只能在外电路中移动,故A错误;a极产生O2,c极产生Cl2,根据电子守恒得关系式:O2~2Cl2~4e-,O2和Cl2的物质的量之比为1∶2,故B错误;阴离子向阳极移动,a和c是阳极,所以SO向a电极移动,Cl-向c电极移动,故C错误;d极是阴极,电极反应式为2H2O+2e-===H2↑+2OH-,所以通电后乙烧杯中滴入酚酞溶液d极会变红,故D正确。
7.如图为直流电源电解稀Na2SO4水溶液的装置。通电后在石墨电极a和b附近分别滴加几滴石蕊溶液。下列实验现象中正确的是( )
A.逸出气体的体积,a电极的小于b电极的
B.一电极逸出无味气体,另一电极逸出刺激性气味气体
C.a电极附近呈红色,b电极附近呈蓝色
D.a电极附近呈蓝色,b电极附近呈红色
解析:D a为阴极产生氢气,b为阳极产生氧气,逸出气体的体积,a电极的大于b电极的,故A、B错误;a电极氢离子放电,a电极周围还有大量的氢氧根离子,使a电极附近的石蕊溶液变为蓝色,b电极氢氧根离子放电,b电极周围还有大量的氢离子,使b电极附近的石蕊溶液变为红色,故C错误,D正确。
8.(2021·浙江温州高二检测)下列选项中,每种电解质溶液电解时只生成氢气和氧气的是( )
A.HCl、CuCl2、Ba(OH)2
B.NaOH、CuSO4、H2SO4
C.NaOH、H2SO4、Ba(OH)2
D.NaBr、H2SO4、Ba(OH)2
解析:C A中,2HClCl2↑+H2↑,CuCl2Cu+Cl2↑,错误;B中,2CuSO4+2H2O2Cu+2H2SO4+O2↑,错误;D中,2NaBr+2H2O2NaOH+H2↑+Br2,错误。
9.用石墨作电极电解下列溶液:
①稀H2SO4 ②K2SO4溶液 ③CuCl2溶液 ④CuSO4溶液 ⑤KOH溶液
(1)阴极、阳极都有气体产生,且体积比(相同条件下)为2∶1 的是__________(填序号),其阳极的电极反应式都是_______________________________________________________,
阴极的电极反应式都是_________________________________________________,
电解反应方程式都是____________________________________________________。
(2)阴极、阳极都有气体产生,其中溶液酸性增强的是____________(填序号)。
(3)一个电极析出金属,另一个电极逸出刺激性气味气体的是________(填序号),其阳极的电极反应式是______________________________________________________
________________________________________________________________________。
解析:(1)电解水时,阴极氢离子放电,生成氢气,阳极氢氧根离子放电,生成氧气,两极都有气体产生,且体积比(相同条件下)为2∶1,电解①②⑤时,均相当于电解水,阴极氢离子放电,生成氢气,即2H++2e-===H2↑,阳极氢氧根离子放电,生成氧气,即4OH--4e-===2H2O+O2↑,电解反应为2H2O2H2↑+O2↑;(2)电解①②⑤时,两极都有气体产生,电解③④时,阴极Cu2+放电,没有气体产生,①溶液的浓度增大,pH变小;②溶液的浓度增大,pH不变;⑤溶液的浓度增大,pH变大;(3)电解③④时,阴极都是Cu2+放电,析出金属铜,③中阳极Cl-放电产生的氯气有刺激性气味;④中阳极OH-放电产生的氧气无刺激性气味。
答案:(1)①②⑤ 4OH--4e-===2H2O+O2↑ 2H++2e-===H2↑ 2H2O2H2↑+O2↑
(2)① (3)③ 2Cl--2e-===Cl2↑
[素养提升练]
10.(2021·湖南长沙高二月考)下列有关 2 个电化学装置的叙述不正确的是( )
A.图Ⅰ,在不改变总反应的前提下,可用 Na2SO4 替换 ZnSO4,用石墨替换 Cu 棒
B.图Ⅰ,电流形成的完整过程是负极Zn-2e-===Zn2+,电子经导线流向正极,正极 Cu2++2e-===Cu
C.图Ⅱ,通电后向两极滴加酚酞溶液,左侧变红
D.图Ⅰ,盐桥中 Cl-向左侧移动,图Ⅱ,溶液中 Cl-向右侧移动
解析:B 将图Ⅰ中的ZnSO4替换为Na2SO4,对左侧区反应无影响,将Cu棒替换为石墨棒,仍然是锌为负极,石墨棒为正极,故并不改变总反应,故A正确;图Ⅰ中电流形成的完整过程是负极Zn-2e-===Zn2+,外电路中电子经导线流向正极,正极Cu2++2e-===Cu,内电路的盐桥中的阴离子移向负极,阳离子移向正极,故B错误;图Ⅱ中左侧区是阴极,电极反应为2H2O+2e-===H2↑+2OH-,故阴极区显碱性,加酚酞后溶液变红,故C正确;图Ⅰ中左侧为负极,故盐桥中Cl-向左侧移动,图Ⅱ中右侧是阳极,故溶液中Cl-向右侧移动,故D正确。
11.(2021·安徽合肥高二期中)某研究小组在电压为24 V时进行如下实验,电解3分钟后,发现下列现象。
编号 ① ② ③
装置
现象 小灯泡微弱发光,两极均产生气泡,阳极附近出现白色浑浊,阴极附近无明显变化 两极均产生气泡,溶液无明显变化 两极均产生气泡,阳极附近出现白色浑浊,阴极附近无明显变化
下列说法正确的是( )
A.①中小灯泡微亮是因为Ca(OH)2是弱电解质
B.对比①和②,白色浑浊的出现与电极材料无关
C.对比①和③,白色浑浊是由于OH-迁移到阳极使Ca(OH)2沉淀析出
D.阳极附近白色沉淀的成分可能是CaCO3
解析:D ①中小灯泡微亮是因为Ca(OH)2在水中的溶解度小,实质上Ca(OH)2溶于水后能完全电离,属于强电解质,A错误;对于①,阳极上溶液中OH-失去电子,发生氧化反应,电极反应式为4OH--4e-===O2↑+2H2O,O2与C电极发生反应产生CO2,CO2与溶液中的Ca(OH)2反应产生CaCO3白色沉淀,可见白色浑浊的出现与电极材料有关,B、C错误,D正确。
