江苏省盐城田中2021-2022学年高一上学期期中考试化学试卷(Word版含答案)
文档属性
| 名称 | 江苏省盐城田中2021-2022学年高一上学期期中考试化学试卷(Word版含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 223.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-08-25 00:00:00 | ||
图片预览



文档简介
盐城田中2021-2022学年高一上学期期中考试
化学试题
说明:1.本试卷共6页,考试时间为75分钟,卷面总分为100分;
2.请将所有客观试题的答案用2B铅笔规范转涂至答题卡上,主观试题的答案填写到答题卷对应区域,否则,答题无效。
可能用到的原子量: H-1 C-12 N-14 O-16 S-32 Cu-64 Mn-55 Ba-137
一、选择题:(每小题只有一个选项符合题目要求,共20题60分)
1. 2020年世界地球日的主题是“珍爱地球,人与自然和谐共生”。下列说法不合理的是
A. 遗弃塑料会污染土壤、地下水和海洋
B. 农业要禁用化肥、农药以防止水污染
C. 车辆排放的氮氧化物会造成空气污染
D. 回收某些垃圾生产煤气、乙醇等燃料
2、下列物质的俗名与化学式相对应的是
A. 纯碱-NaHCO3 B. 苛性钠-NaOH
C. 熟石灰-CaCO3 D. 胆矾-CuSO4
3、用生石灰中和法阻止海水酸化是人们的一种设想。生石灰(CaO)属于
A. 碱 B. 盐
C. 酸性氧化物 D. 碱性氧化物
4、炼铁过程中存在反应:CaO+SiO2CaSiO3。该反应属于
A. 化合反应 B. 分解反应
C. 置换反应 D. 复分解反应
5、用特殊方法把固体物质加工到纳米级(1nm-100nm)的超细粉末粒子,然后制得纳米材料。下列分散系中的分散质的粒子的大小和这种纳米粒子大小具有相同的数量级的是
A. 溶液 B. 悬浊液
C. 胶体 D. 乳浊液
6、下列叙述中,正确的是
A. CO2溶于水能导电,所以CO2是电解质
B. 铜丝、石墨均能导电,所以它们都是电解质
C. KNO3固体不导电,所以KNO3不电解质
D. 熔融的MgCl2能导电,所以MgCl2是电解质
7、遥感三十号07组卫星于2020年10月26日准确送入预定轨道。该导航系统应用了星载氢原子钟和铷原子钟。下列有关铷Rb的说法错误的是
A. 质子数为37 B. 质量数为85
C. 中子数为85 D. 核外电子数为37
8、对于给定物质的量的理想气体,影响其所占体积大小的主要因素是
A.分子直径的大小 B. 分子间距离的大小
C.分子间引力的大小 D. 分子数目的多少
9、下列实验操作中,不能用于物质分离的是
A. B. C. D.
10、下列关于0.1mol/L的Ba(NO3)2溶液的说法中正确的是
A. 1L该溶液中含有Ba2+的质量为1.37 g
B. 该溶液中c(NO)=0.1mol L 1
C. 1L该溶液中含有0.1mol Ba2+
D. 该溶液就是将26.1g 的Ba(NO3)2溶于1L水中所得到的溶液。
11、下列电离方程式中正确的是
A. H2O = 2H+ + O2- B. NaHCO3 = Na+ + H+ + CO32-
C. H2SO4 = 2H+ + SO42- D. MgCl2 = Mg2+ + Cl2-
12、下列叙述正确的是
A.常温常压下,14 g N2含有的分子数约为3.01×1023
B.64 g SO2含有的氧原子数约为6.02×1023
C.标准状况下,22.4 LH2O含有的分子数约为6.02×1023
D.2 L 0.5 mol·L-1MgCl2溶液中,含有的Cl-数约为6.02×1023
13、下列反应不属于氧化还原反应的是
A. Zn+H2SO4===ZnSO4+H2↑ B. Fe2O3+3CO2Fe+3CO2
C. 2HClO2HCl+O2↑ D. FeCl2+2NaOH===Fe(OH)2↓+2NaCl
14、金属钠投入到下列溶液中,既有气体放出,又有沉淀生成的是
A.盐酸 B.硫酸钾溶液 C.氯化铁溶液 D.硝酸铵溶液
15、0.2L1mol·L-1的KCl溶液和0.5L1mol·L-1的FeCl3溶液中,Cl- 的物质的量浓度之比为
A. 1∶3 B. 3∶1 C. 1∶1 D. 2∶15
16、相同条件下,20 mL A2气体与30 mL B2气体恰好完全反应生成20 mL某气体X,则X的化学式为
A.A2B3 B.AB2 C.AB3 D.A3B2
17、下列实验方案能达成目的的是
A. 用乙醇萃取溴水中的溴单质
B. 用焰色反应鉴别KCl和NaOH
C. 用KOH溶液提纯NaCl(其中含有MgCl2)
D. 用Ba(OH)2溶液鉴别Na2CO3溶液与NaHCO3溶液
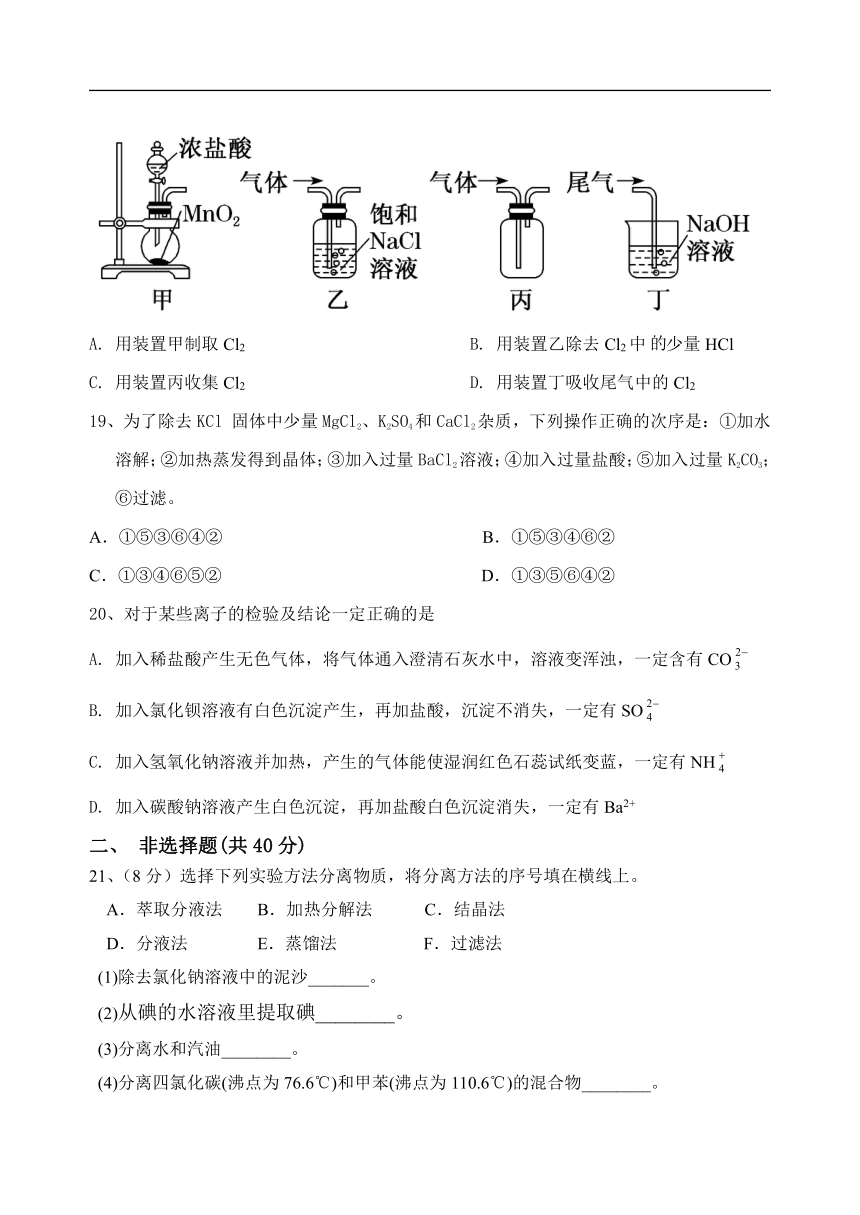
18、实验室用如图装置制取、提纯、收集Cl2、尾气处理,不能达到实验目的的是
A. 用装置甲制取Cl2 B. 用装置乙除去Cl2中少量HCl
C. 用装置丙收集Cl2 D. 用装置丁吸收尾气中的Cl2
19、为了除去KCl 固体中少量MgCl2、K2SO4和CaCl2杂质,下列操作正确的次序是:①加水溶解;②加热蒸发得到晶体;③加入过量BaCl2溶液;④加入过量盐酸;⑤加入过量K2CO3; ⑥过滤。
A.①⑤③⑥④② B.①⑤③④⑥②
C.①③④⑥⑤② D.①③⑤⑥④②
20、对于某些离子的检验及结论一定正确的是
A. 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定含有CO
B. 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO
C. 加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH
D. 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
二、 非选择题(共40分)
21、(8分)选择下列实验方法分离物质,将分离方法的序号填在横线上。
A.萃取分液法 B.加热分解法 C.结晶法
D.分液法 E.蒸馏法 F.过滤法
(1)除去氯化钠溶液中的泥沙_______。
(2)从碘的水溶液里提取碘________。
(3)分离水和汽油________。
(4)分离四氯化碳(沸点为76.6℃)和甲苯(沸点为110.6℃)的混合物________。
22、(10分)用胆矾(CuSO4 5H2O)配制480mL0.1mol L-1的CuSO4溶液,需要用到下列仪器:烧杯、量筒、药匙、玻璃棒、托盘天平、胶头滴管等
(1) 配制时,还缺少的玻璃仪器是_______(填名称)。该实验中两次用到玻璃棒,其作用分别是 和 。
(2) 下列操作对所配溶液的浓度大小有何影响 (填“偏大”、“偏小”或“无影响”)。
①容量瓶未干燥,浓度会_______。
②定容后摇匀,发现液面低于刻度线,又加少量的水至到刻度线,浓度会_______。
(3) 配制该溶液时,可以选择用托盘天平称取固体CuSO4 5H2O的质量为_______g。
23、(12分)一种以生石灰(CaO)为原料制备KClO3的流程如下:
注:氯化过程中Cl2与Ca(OH)2作用生成Ca(ClO)2,Ca(ClO)2进一步转化为Ca(ClO3)2。
(1)制浆过程中发生的化学反应方程式为_____________________。
(2)氯化过程中须缓慢通入Cl2。
①缓慢通入Cl2的目的是_______________________________。
②生成Ca(ClO)2的化学方程式为________________________。
③氯化过程中会有少量无色无味气体生成,该气体可能是_______(填化学式)。
(3)根据右图的溶解度曲线,回答下列问题。
向滤液中加入过量KCl固体可将溶液中Ca(ClO3)2转化为KClO3固体而析出的原因是______________________________。若溶液中KClO3的含量为100 g·L-1,从该溶液中尽可能多地析出KClO3固体的方法是__________________。
24、(8分)实验室用图所示装置制备KClO溶液,并通过KClO溶液与Fe2(SO4)3溶液的反应制备高效水处理剂高铁酸钾(K2FeO4)。
(1)K2FeO4,其中铁元素的化合价为_______。
(2)写出装置A中制备Cl2的化学方程式:_______ 。
(3)8.7 g MnO2和足量的浓盐酸反应,求生成Cl2的体积为_____升(标准状况下)。
盐城田中2021-2022学年高一上学期期中考试
化学参考答案
选择题(共计60分)
1~5 BBDAC 6~10 DCBCC
11~15 CADCA 16~20 ABADC
非选择题(共计40分)
21、(8分) (1)F (2) A (3) D (4) E (每题2分)
22、(12分) (1). 500ml容量瓶 (2). 搅拌 引流 (3). 无影响
(4). 偏低 (5). 125g (每空2分)
23、(12分) (1)CaO+H2O=Ca(OH)2(2分)
(2)①提高Cl2的转化率(2分)
②2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O(2分)
③O2(2分)
(3)相同温度下的KClO3溶解度小于Ca(ClO3)2的溶解度(2分)
蒸发浓缩、降温结晶(2分)
24、(8分) (1). +6价 (2分)
(2). MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O (2分)
(3). 2.24L(4分)
化学试题
说明:1.本试卷共6页,考试时间为75分钟,卷面总分为100分;
2.请将所有客观试题的答案用2B铅笔规范转涂至答题卡上,主观试题的答案填写到答题卷对应区域,否则,答题无效。
可能用到的原子量: H-1 C-12 N-14 O-16 S-32 Cu-64 Mn-55 Ba-137
一、选择题:(每小题只有一个选项符合题目要求,共20题60分)
1. 2020年世界地球日的主题是“珍爱地球,人与自然和谐共生”。下列说法不合理的是
A. 遗弃塑料会污染土壤、地下水和海洋
B. 农业要禁用化肥、农药以防止水污染
C. 车辆排放的氮氧化物会造成空气污染
D. 回收某些垃圾生产煤气、乙醇等燃料
2、下列物质的俗名与化学式相对应的是
A. 纯碱-NaHCO3 B. 苛性钠-NaOH
C. 熟石灰-CaCO3 D. 胆矾-CuSO4
3、用生石灰中和法阻止海水酸化是人们的一种设想。生石灰(CaO)属于
A. 碱 B. 盐
C. 酸性氧化物 D. 碱性氧化物
4、炼铁过程中存在反应:CaO+SiO2CaSiO3。该反应属于
A. 化合反应 B. 分解反应
C. 置换反应 D. 复分解反应
5、用特殊方法把固体物质加工到纳米级(1nm-100nm)的超细粉末粒子,然后制得纳米材料。下列分散系中的分散质的粒子的大小和这种纳米粒子大小具有相同的数量级的是
A. 溶液 B. 悬浊液
C. 胶体 D. 乳浊液
6、下列叙述中,正确的是
A. CO2溶于水能导电,所以CO2是电解质
B. 铜丝、石墨均能导电,所以它们都是电解质
C. KNO3固体不导电,所以KNO3不电解质
D. 熔融的MgCl2能导电,所以MgCl2是电解质
7、遥感三十号07组卫星于2020年10月26日准确送入预定轨道。该导航系统应用了星载氢原子钟和铷原子钟。下列有关铷Rb的说法错误的是
A. 质子数为37 B. 质量数为85
C. 中子数为85 D. 核外电子数为37
8、对于给定物质的量的理想气体,影响其所占体积大小的主要因素是
A.分子直径的大小 B. 分子间距离的大小
C.分子间引力的大小 D. 分子数目的多少
9、下列实验操作中,不能用于物质分离的是
A. B. C. D.
10、下列关于0.1mol/L的Ba(NO3)2溶液的说法中正确的是
A. 1L该溶液中含有Ba2+的质量为1.37 g
B. 该溶液中c(NO)=0.1mol L 1
C. 1L该溶液中含有0.1mol Ba2+
D. 该溶液就是将26.1g 的Ba(NO3)2溶于1L水中所得到的溶液。
11、下列电离方程式中正确的是
A. H2O = 2H+ + O2- B. NaHCO3 = Na+ + H+ + CO32-
C. H2SO4 = 2H+ + SO42- D. MgCl2 = Mg2+ + Cl2-
12、下列叙述正确的是
A.常温常压下,14 g N2含有的分子数约为3.01×1023
B.64 g SO2含有的氧原子数约为6.02×1023
C.标准状况下,22.4 LH2O含有的分子数约为6.02×1023
D.2 L 0.5 mol·L-1MgCl2溶液中,含有的Cl-数约为6.02×1023
13、下列反应不属于氧化还原反应的是
A. Zn+H2SO4===ZnSO4+H2↑ B. Fe2O3+3CO2Fe+3CO2
C. 2HClO2HCl+O2↑ D. FeCl2+2NaOH===Fe(OH)2↓+2NaCl
14、金属钠投入到下列溶液中,既有气体放出,又有沉淀生成的是
A.盐酸 B.硫酸钾溶液 C.氯化铁溶液 D.硝酸铵溶液
15、0.2L1mol·L-1的KCl溶液和0.5L1mol·L-1的FeCl3溶液中,Cl- 的物质的量浓度之比为
A. 1∶3 B. 3∶1 C. 1∶1 D. 2∶15
16、相同条件下,20 mL A2气体与30 mL B2气体恰好完全反应生成20 mL某气体X,则X的化学式为
A.A2B3 B.AB2 C.AB3 D.A3B2
17、下列实验方案能达成目的的是
A. 用乙醇萃取溴水中的溴单质
B. 用焰色反应鉴别KCl和NaOH
C. 用KOH溶液提纯NaCl(其中含有MgCl2)
D. 用Ba(OH)2溶液鉴别Na2CO3溶液与NaHCO3溶液
18、实验室用如图装置制取、提纯、收集Cl2、尾气处理,不能达到实验目的的是
A. 用装置甲制取Cl2 B. 用装置乙除去Cl2中少量HCl
C. 用装置丙收集Cl2 D. 用装置丁吸收尾气中的Cl2
19、为了除去KCl 固体中少量MgCl2、K2SO4和CaCl2杂质,下列操作正确的次序是:①加水溶解;②加热蒸发得到晶体;③加入过量BaCl2溶液;④加入过量盐酸;⑤加入过量K2CO3; ⑥过滤。
A.①⑤③⑥④② B.①⑤③④⑥②
C.①③④⑥⑤② D.①③⑤⑥④②
20、对于某些离子的检验及结论一定正确的是
A. 加入稀盐酸产生无色气体,将气体通入澄清石灰水中,溶液变浑浊,一定含有CO
B. 加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,一定有SO
C. 加入氢氧化钠溶液并加热,产生的气体能使湿润红色石蕊试纸变蓝,一定有NH
D. 加入碳酸钠溶液产生白色沉淀,再加盐酸白色沉淀消失,一定有Ba2+
二、 非选择题(共40分)
21、(8分)选择下列实验方法分离物质,将分离方法的序号填在横线上。
A.萃取分液法 B.加热分解法 C.结晶法
D.分液法 E.蒸馏法 F.过滤法
(1)除去氯化钠溶液中的泥沙_______。
(2)从碘的水溶液里提取碘________。
(3)分离水和汽油________。
(4)分离四氯化碳(沸点为76.6℃)和甲苯(沸点为110.6℃)的混合物________。
22、(10分)用胆矾(CuSO4 5H2O)配制480mL0.1mol L-1的CuSO4溶液,需要用到下列仪器:烧杯、量筒、药匙、玻璃棒、托盘天平、胶头滴管等
(1) 配制时,还缺少的玻璃仪器是_______(填名称)。该实验中两次用到玻璃棒,其作用分别是 和 。
(2) 下列操作对所配溶液的浓度大小有何影响 (填“偏大”、“偏小”或“无影响”)。
①容量瓶未干燥,浓度会_______。
②定容后摇匀,发现液面低于刻度线,又加少量的水至到刻度线,浓度会_______。
(3) 配制该溶液时,可以选择用托盘天平称取固体CuSO4 5H2O的质量为_______g。
23、(12分)一种以生石灰(CaO)为原料制备KClO3的流程如下:
注:氯化过程中Cl2与Ca(OH)2作用生成Ca(ClO)2,Ca(ClO)2进一步转化为Ca(ClO3)2。
(1)制浆过程中发生的化学反应方程式为_____________________。
(2)氯化过程中须缓慢通入Cl2。
①缓慢通入Cl2的目的是_______________________________。
②生成Ca(ClO)2的化学方程式为________________________。
③氯化过程中会有少量无色无味气体生成,该气体可能是_______(填化学式)。
(3)根据右图的溶解度曲线,回答下列问题。
向滤液中加入过量KCl固体可将溶液中Ca(ClO3)2转化为KClO3固体而析出的原因是______________________________。若溶液中KClO3的含量为100 g·L-1,从该溶液中尽可能多地析出KClO3固体的方法是__________________。
24、(8分)实验室用图所示装置制备KClO溶液,并通过KClO溶液与Fe2(SO4)3溶液的反应制备高效水处理剂高铁酸钾(K2FeO4)。
(1)K2FeO4,其中铁元素的化合价为_______。
(2)写出装置A中制备Cl2的化学方程式:_______ 。
(3)8.7 g MnO2和足量的浓盐酸反应,求生成Cl2的体积为_____升(标准状况下)。
盐城田中2021-2022学年高一上学期期中考试
化学参考答案
选择题(共计60分)
1~5 BBDAC 6~10 DCBCC
11~15 CADCA 16~20 ABADC
非选择题(共计40分)
21、(8分) (1)F (2) A (3) D (4) E (每题2分)
22、(12分) (1). 500ml容量瓶 (2). 搅拌 引流 (3). 无影响
(4). 偏低 (5). 125g (每空2分)
23、(12分) (1)CaO+H2O=Ca(OH)2(2分)
(2)①提高Cl2的转化率(2分)
②2Cl2+2Ca(OH)2=Ca(ClO)2+CaCl2+2H2O(2分)
③O2(2分)
(3)相同温度下的KClO3溶解度小于Ca(ClO3)2的溶解度(2分)
蒸发浓缩、降温结晶(2分)
24、(8分) (1). +6价 (2分)
(2). MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O (2分)
(3). 2.24L(4分)
同课章节目录
