浙江省舟山市普陀二中2022-2023学年初八升九期始考科学试题卷(含答案)
文档属性
| 名称 | 浙江省舟山市普陀二中2022-2023学年初八升九期始考科学试题卷(含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 1.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2022-08-29 00:00:00 | ||
图片预览

文档简介
浙江省舟山市普陀二中2022-2023学年八升九期始考科学试题卷
注意事项:
1.本试题卷分卷I(选择题)和卷II(非选择题)两部分,满分180分,考试时间为120分钟。
2.本卷g取10牛/千克。
3.本卷可能用到的相对原子质量:H-1 C-12 N-14 0-16 Na-23 Mg-24 Al-27 S-32 Cl-35.5 Ca-40 Fe-56 Cu-64 Ag-108 I-127 Ba-233
4.答题时请仔细阅读答题卷上的注意事项,认真审题,细心答题。
第I卷(选择题50分)
一、选择题(本题有15小题,第1-10小题,每小题3分,第11-15小题,每小题4分,共50分。请选出一个符合题意的正确选项,不选、多选、错选、均不给分)
1.建立模型是学习科学的重要方法,下列不属于模型的是( )
A.原子结构 B.空气成分 C.细胞结构 D.注意行人
2.辨别家庭电路中的火线与零线,应该选用( )
A.放大镜B.测电笔 C.指南针 D.弹簧测力计
3.规范操作是科学实验成功的关键,下列实验操作错误的是( )
A.倾倒液体 B.取用粉末状固体 C.闻气体气味 D.检查气密性
4.乐乐通过无土栽培的技术培养富贵竹时,发现植株矮小,叶色发黄。为改善富贵竹的生长状况,应添加的无机盐是( )
A.含氮无机盐 B.含磷无机盐 C.含钾无机盐 D.含铁无机盐
5.新鲜果汁是常见的饮料,下列四种饮料呈弱碱性的是( )
A.柠檬汁(pH:2~3) B.苹果汁(pH:3~4)
C.西瓜汁(pH:5~6) D.玉米汁(pH:7~8)
6.如图,小敏用条形磁铁使铁钉竖直静止在空中,细线紧绷且质量不计,下列说法正确的是( )
A.铁钉上端被磁化成N极
B.铁钉受到的磁力与自身重力大小相等
C.桌面对石头的支持力和石头的重力是一对平衡力
D.细线对石头的拉力和石头对细线的拉力是一对相互作用力
7.如图为Fe元素的化合价和物质类别的二维图。下列说法正确的是( )
A.物质C的化学式为Fe2O3
B.物质D的化学式为Fe(OH)3
C.物质A在氧气中燃烧生成物质B
D.物质B比物质C的铁元素含量低
8.某小组使用数据采集器探究“铁丝在O2中燃烧”,集气瓶内O2的体积分数随时间的变化关系如图所示。下列说法正确的是( )
A.反应为:铁+氧气三氧化二铁 B.瓶中放少量水,用于吸收有毒物质
C.开始采集数据时,瓶内是纯净的O2 D.铁丝停止燃烧时,瓶内O2未耗尽
9.植物对水分的吸收、运输与细胞液及土壤溶液的溶质质量分数相关,图中箭头表示水分渗透的方向,由此可判断①、②、③三处溶液溶质质量分数大小关系是( )
①>②>③ B.③>②>①
C.①>③>② D.③>①>②
10.乙醇是酒精的主要成分,其分子式为C2H5OH。则下列有关乙醇的说法正确的是( )
A.乙醇分子中C,H,O三种原子的个数比为2∶5∶1 B.乙醇由三种元素组成
C.乙醇由9个原子构成 D.乙醇分子由碳原子和水分子构成
11.对于图中所示的四幅图,以下说法不正确的是( )
A.图甲所示的风光互补式路灯,太阳能发电装置是将太阳能转化为电能,风力发电机的工作原理是电磁感应
B.图乙中,铁钉B吸引的大头针比A多,说明电磁铁的磁性强弱与电流大小有关
C.图丙是一种自动测定油箱内油面高度的装置,油量减少时油量表示数变小
D.图丁是电流表的内部结构图,指针偏转角度随线圈中电流增大而增大,它是利用磁场对电流的作用的原理工作的
12.为探究植物种子呼吸作用的产物,用如图装置进行对照实验:先在A、B试管中加入等量的澄清石灰水,再往A试管中加入适量的已浸水及消毒的蚕豆种子,则试管B中应加入等量的( )
A.已浸水及消毒的绿豆种子
B.已浸水及未消毒的蚕豆种子
C.已煮熟及未消毒的蚕豆种子
D.已煮熟及消毒的蚕豆种子
13.在一密闭容器中发生某反应,其中甲、乙、丙、丁四种物质的质量变化如表所示,下列判断不正确的是( )
物质 甲 乙 丙 丁
反应前质量(g) 10 16 0 0
反应中质量(g) 1.6
反应后质量(g) 0 15.2 6.4
A.的值是4.4 B.的值是4
C.甲和乙是反应物 D.甲、丁间反应的质量比为7:8
14.2022年第24届冬季奥运会将由北京市和张家口市联合举行。如图所示,“五环”中相交两环中的物质间能够发生化学反应,其中A、B、C、D分别是HCl、Fe2O3、H2、CuSO4中的一种。下列说法中正确的是( )
A.A物质与B物质间发生的反应是工业炼铁的主要反应原理
B.B物质与C物质间发生反应的化学方程式为:4HCl+Fe2O3═2H2O+2FeCl2
C.C物质与NaOH溶液发生反应时无明显现象
D.D物质的溶液与NaOH溶液发生反应时产生红褐色沉淀
15.某混合物X由Al2O3,Fe2O3,Cu,SiO2中的一种或几种组成。分别对X进行如下实验,有关说法错误的是( )
A.由I可知,X中一定存在Fe2O3、Cu B.由II和III可得出结论,混合物中无Al2O3
C.1.92g固体为SiO2和Cu的混合物 D.原混合物中Fe2O3和Cu的质量比为1:1
第II卷(非选择题130分)
二、填空题(本题有9小题20空格,每空2分,共40分)
16.医用消毒酒精为75%的乙醇溶液,化工生产中可用A(主要成分的化学式为C8H18)作原料,经以下流程制取乙醇:
(1)步骤①的转化属于______(选填“化学”或“物理”)变化。
(2)步骤②是乙烯和含两种元素的化合物B发生化合反应,则B中所含元素是______。
17.酸、碱、盐等是我们学过的重要物质,请根据相关知识回答下列问题:
(1)稀盐酸能除铁锈(铁锈的主要成分是Fe2O3),写出稀盐酸除锈反应的化学方程式_____________________。
(2)服用含氢氧化铝[Al(OH)3]的药物可以治疗胃酸过多症,该反应的化学方程式为_____________________。
18.随着全民健身活动的兴起,有更多的人参加马拉松运动。马拉松已经远远不只是一场比赛,它是你认识自己,认识一座城市,认识这个世界的方式。因参赛选手很多,无法在同一起跑线出发而计时困难。近年常采用感应 芯片计时,参赛者须按要求正确佩带计时芯片,当参赛者通过起点和终点 设置有磁场的感应带时,芯片里的线圈中就会产生________,工作原理是_________,从而激发芯片发送编码信息,系统实时获取计时信息。
19.据报道,我国科学家发现治疗新冠的新药——中药千金藤素,获得国家发明专利授权。千金藤素来自千金藤,其化学式为C37H38N2O6,白色固体,难溶于水,易氧化,需密封避光低温保存。
(1)根据上述信息,写出千金藤素的一条物理性质:___________。
(2)千金藤素中各元素质量分数如图甲所示,其中表示碳元素的是___________。(填序号)
20.如图是自然界中碳、氧循环简图(其中Y为葡萄糖C6H12O6)。
(1)图一中的X是________(用化学式表示)。
(2)图二中的转化3是自然界中碳、氧循环的重要反应即绿色植物光合作用的过程,涉及的能量转化情况为________。
(3)生物体的呼吸作用对应的是图中的________。(填“转化2”或“转化4”)
21.如图所示是蔬菜无土栽培装置。在培育过程中,需要适时添加含有硝酸钾、磷酸二氢钾等物质的培养液。
(1)磷酸二氢铵(NH4H2PO4)中氮元素的化合价是-3价,磷元素的化合价是______。
(2)若蔬菜的根细胞液浓度______培养液的浓度(选填“大于”、“小于”、“等于”),会导致蔬菜细胞内水分含量下降而发生萎蔫。
22.1823年,德国化学家德贝莱纳发现氢气遇到金属铂会起火,根据此原理制成了世界上第一支打火机(如图甲)。
(1)当关闭开关,堵住喷嘴时打火机火焰熄灭,其灭火原理是___________;
(2)氢气和氧气遇铂在常温下就会反应,原理如乙图所示,铂在反应中起___________的作用。
23.如图甲所示为某智能扫地机器人部分工作原理图,其中R为光敏电阻:如图乙所示为光敏电阻R的阻值随照度变化的图线(照度表示物体被照明的程度,照度越大被照明的程度越大)。
(1)上述智能扫地机器人工作原理如下:接通电源,当地面灰尘较多时,使照射到光敏电阻R上的照度变小,光敏电阻R的阻值________(选填“变大”或“变小”),电磁铁的磁性________(选填“增强”或“减弱”),此时电动机旋转产生高速气流将灰尘等吸入集尘盒;当灰尘清扫到一定程度时,电动机停止工作,指示灯亮,该智能扫地机器人处于待机状态;
(2)根据其工作原理可知,电动机应接入________(选填“ab”或“cd”)之间。
24.小李同学用如下图总结NaOH的四类化学性质(即NaOH能够与四类物质发生化学反应)。
为验证性质④,他选择了二氧化碳与其反应,为探究两者是否发生了化学反应,小李设计了如图所示的A、B实验进行验证。实验现象为:A中试管内液面上升,B中___________。
李莉提出质疑,她认为A实验不严谨,应做一个对比实验:_________________________________。
三、实验探究题(本题有5小题,15空,25、26题每空2分,27-29题每空3分,共40分)
25.在研究酸和碱的化学性质时,某科学兴趣小组进行了如下探究实验:
(1)探究稀硫酸与氢氧化钠溶液的反应:
(2)探究上述稀硫酸与氢氧化钠溶液反应后烧杯中的硫酸是否过量:根据上述反应过程中溶液变成无色,不能确定稀硫酸是否过量。他们又分别选取氯化钡溶液、紫色石蕊试液设计实验方案,如下表:
实验方案 实验步骤 实验现象 实验结论
实验一 取样,滴入适量的氯化钡溶液 出现白色沉淀 稀硫酸过量
实验二 取样,滴入几滴紫色石蕊试液 溶液变红 稀硫酸过量
①上述实验方案中,方案一不合理,理由是___________________________________________________。
②请你再设计一个确定稀硫酸是否过量的实验方案,写出选用的药品、预期实验现象及结论___________
__________________________________________________________________________________________。
26.磁场看不见、摸不着,小科想利用铁屑和小磁针(黑色一端为极)来探究通电螺线管外部磁场特点。请你解答以下问题:
(1)实验中,小磁针的作用是为了研究通电螺线管周围的___________。(填“磁场强弱”或“磁场方向”)
(2)小科在奥斯特实验的启发下,只改变通电螺线管中的电流方向,实验现象如图乙所示。对比两次的实验现象可知:通电螺线管两端的磁极性质与通电螺线管中的电流方向___________。(填“有关”或“无关”)
(3)下列操作中能增强通电螺线管磁性的是___________
A.增大通电螺线管中的电流 B.改变通电螺线管中的电流方向
C.在通电螺线管内插入铁棒 D.减少通电螺线管的匝数
27.科学小组将制得的CO2分别通入澄清石灰水和氢氧化钠溶液中,他们观察到前者变浑浊,后者无明显现象。那么CO2和NaOH是否发生了化学反应?
(1)小明设计了甲、乙两个实验来验证CO2与NaOH发生了化学反应,如图所示。实验现象为:甲——软塑料瓶变瘪,乙——“瓶吞鸡蛋”。
①小林认为上述实验是可行的,其共同原理是____________________________________;
②小华提出质疑,她认为上述实验还不足以说明CO2和NaOH发生了反应,其理由是_______________________;小明同学针对小华的质疑又补充了一个对照实验,请简单写出实验方案_________________________________
__________________________________________________________________________________________。
(2)为进一步比较,老师用三个相同的烧瓶收集等量的CO2气体,注入等量的三种液体,用气压传感器测定内部气压变化,得到烧瓶内压强与时间的关系曲线如图丙所示。其中曲线2代表澄清石灰水,曲线3代表氢氧化钠溶液,由此曲线,你可以得出的结论是______。
A.CO2能与氢氧化钠溶液反应
B.CO2能使澄清石灰水变浑浊
C.此氢氧化钠溶液比澄清石灰水更适合用于吸收CO2
28.袁隆平院士(图甲)是中国杂交水稻事业的开创者和领导者,被誉为“杂交水稻之父”,为我国粮食生产和农业科学的发展作出了杰出贡献。缅怀袁老最好的方式是——“珍惜每一粒粮食”。
下表为常规水稻和杂交水稻的对比。
类别 常规水稻 杂交水稻
定义 通过选育、提纯、保持亲本品种的特征和特性不变,可以留种且后代不分离 选用两个在遗传上有一定差异,同时它们的优良性状又能互补的水稻品种,进行杂交,生产具有杂种优势的第一代
产量 一般较低(<300kg/亩) 一般较高(>700kg/亩)
品质 质软,粘而腻 质地硬,粘性小
特点 不需要年年换种,但需要提纯复壮,抗性差 生长旺盛,根系发达,穗大粒多,抗逆性强等
(1)请根据表一的内容写出支持种植杂交水稻的一个理由:_______________________________。
(2)据乙图,水和无机盐在水稻体内运输途径可以用文字表示为:根中导管→___________→叶中导管。
(3)乐乐把丙装置放在晴朗的室外环境,测得密闭玻璃钟罩内一天的氧气和二氧化碳浓度变化如图丁所示。已知空气中含氧量相对较高时,人会觉得更舒适。那么据图分析,你建议人们到田埂、公园等绿色植物较多的地方散步、游玩的时间应在___________时左右。
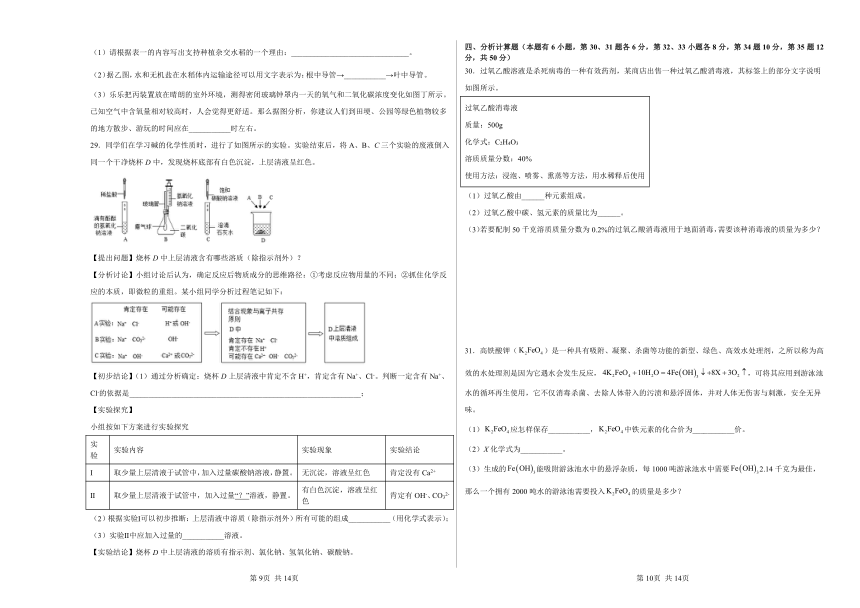
29.同学们在学习碱的化学性质时,进行了如图所示的实验。实验结束后,将A、B、C三个实验的废液倒入同一个干净烧杯D中,发现烧杯底部有白色沉淀,上层清液呈红色。
【提出问题】烧杯D中上层清液含有哪些溶质(除指示剂外)?
【分析讨论】小组讨论后认为,确定反应后物质成分的思维路径:①考虑反应物用量的不同;②抓住化学反应的本质,即微粒的重组。某小组同学分析过程笔记如下:
【初步结论】(1)通过分析确定:烧杯D上层清液中肯定不含H+,肯定含有Na+、Cl-。判断一定含有Na+、Cl-的依据是_____________________________________________________________;
【实验探究】
小组按如下方案进行实验探究
实验 实验内容 实验现象 实验结论
Ⅰ 取少量上层清液于试管中,加入过量碳酸钠溶液,静置。 无沉淀,溶液呈红色 肯定没有Ca2+
Ⅱ 取少量上层清液于试管中,加入过量“?”溶液,静置。 有白色沉淀,溶液呈红色 肯定有OH-、CO32-
(2)根据实验Ⅰ可以初步推断:上层清液中溶质(除指示剂外)所有可能的组成___________(用化学式表示);
(3)实验Ⅱ中应加入过量的___________溶液。
【实验结论】烧杯D中上层清液的溶质有指示剂、氯化钠、氢氧化钠、碳酸钠。
四、分析计算题(本题有6小题,第30、31题各6分,第32、33小题各8分,第34题10分,第35题12分,共50分)
30.过氧乙酸溶液是杀死病毒的一种有效药剂,某商店出售一种过氧乙酸消毒液,其标签上的部分文字说明如图所示。
过氧乙酸消毒液 质量:500g 化学式:C2H4O3 溶质质量分数:40% 使用方法:浸泡、喷雾、熏蒸等方法,用水稀释后使用
(1)过氧乙酸由______种元素组成。
(2)过氧乙酸中碳、氢元素的质量比为______。
(3)若要配制50千克溶质质量分数为0.2%的过氧乙酸消毒液用于地面消毒,需要该种消毒液的质量为多少?
31.高铁酸钾()是一种具有吸附、凝聚、杀菌等功能的新型、绿色、高效水处理剂,之所以称为高效的水处理剂是因为它遇水会发生反应,,可将其应用到游泳池水的循环再生使用,它不仅消毒杀菌、去除人体带入的污渍和悬浮固体,并对人体无伤害与刺激,安全无异味。
(1)应怎样保存___________,中铁元素的化合价为___________价。
(2)X化学式为___________。
(3)生成的能吸附游泳池水中的悬浮杂质,每1000吨游泳池水中需要2.14千克为最佳,那么一个拥有2000吨水的游泳池需要投入的质量是多少?
32.中国政府提出2060年前实现碳中和的目标。“碳中和”指二氧化碳等温室气体的排放总量等于吸收总量,达到“零排放”。为此,某科学兴趣小组经过“前期调查、原理选择、药量测算和装置设计”等环节,制定了二氧化碳吸收方案。
【前期调查】为分析自然界中碳排放与吸收的主要途径,小组成员经调查绘制了自然界部分碳循环示意图。
【原理选择】小组成员经比较分析,最终确定利用氢氧化钠吸收二氧化碳的思路(化学方程式为:2NaOH+CO2==Na2CO3+H2O)。
【药量测算】考虑操作的便捷性、可行性,设定一次性至少吸收二氧化碳4.4千克,并计算了装载氢氧化钠的质量。
【装置设计】结合吸收效果等因素,兴趣小组成员设计了图乙所示A、B两种吸收装置。
(1)图甲为小组成员绘制的碳排放与吸收示意图,其中碳排放的途径有___________。
(2)根据小组设定的一次性二氧化碳吸收量的要求,在装置A中至少要加入多少千克的氢氧化钠?
(3)请选择A、B两种装置的其中一种进行推广,并简要说明理由:_______________________________。
33.科学实验提倡绿色环保,对实验装置进行微型化改进是一条很好的途径。图甲是实验室制取并检验CO2的装置,图乙是对图甲实验装置进行“微型”化改进后的装置。
(1)图乙中微型塑料滴管在实验中的作用与图甲中的______仪器相同(填字母编号);
(2)通常用甲装置完成该实验需要的盐酸是“微型”实验装置用量的10倍,采用“微型”实验装置具有的优点是________________________________________________________;
(3)某学校化学兴趣小组的同学对实验室用石灰石和稀盐酸制取二氧化碳后的废液进行溶质成分的鉴定.取废液上层清液50克,逐滴加入质量分数为26.5%的碳酸钠溶液,出现气泡,滴加至10克时开始出现白色沉淀,继续滴加至沉淀不再产生,对沉淀进行对应处理后,测得沉淀的质量为5克,并绘制了如图像。则废液中含有的溶质有______(写化学式)。废液中属于盐类溶质的质量分数是多少?
34.四位同学元旦去仙华山风景区游玩,带回了几小块石灰石样品。为了检测样品中碳酸钙的含量,甲、乙、丙、丁四位同学用浓度相同的稀盐酸与样品充分反应来进行实验测定,(样品中的杂质不溶于水,且不与盐酸反应)测定数据如下:
甲同学 乙同学 丙同学 丁同学
所取石灰石样品的质量(g) 12.0 12.0 12.0 12.0
加入盐酸的质量(g)烧杯中 10.0 20.0 30.0 40.0
剩余物质的总质量(g) 21.0 30.0 39.0 48.7
试回答:
(1)四位同学里面,___________同学的石灰石样品完全反应了;12.0g石灰石样品与___________g稀盐酸恰好完全反应;
(2)样品中碳酸钙的质量分数为多少?(写出计算过程)
(3)请在图中大致画出生成气体的质量与加入稀盐酸质量的变化关系(标注必要的数值)。
35.随着家庭电气化程度越来越高,用电安全是一个十分突出的问题,下表提供了一组人体电阻的数据。如图所示,用电器R(阻值为44欧),电路中还有熔断电流为8A的保险丝。则:
测量项目 手和手之间电阻 手与脚之间电阻 手与塑料鞋底之间电阻
完全干燥时 200千欧 300千欧 8000千欧
出汗或潮湿时 1千欧 1千欧 10千欧
(1)一个全身潮湿的人,赤脚站在地上,由于不小心,手接触火线,发生触电事故,则通过人体的电流是___________A,通过计算分析此时保险丝是否熔断___________;
(2)当发现有人触电时,应该第一时间___________,在触电者未脱离电源前,严禁直接用手去触及伤员;
(3)为用电安全,有的电热水器安装了防电墙。防电墙技术就是在电热水器内部形成永久性电阻,从而降低异常情况下经过人体的电流值。经过防电墙处理后,发生异常情况时,人体承受的电压约10V,如图所示,这就保证了人体安全。若人体的最大电组约为20兆欧,求防电墙的电阻大约是多少?第1页 共4页 第2页 共4页
第1页 共4页 第2页 共4页
参考答案
一、选择题(本题有15小题,1-10题每小题3分,11-15题每小题4分,共50分。请选出各题中一个符合题意的正确选项,不选、多选、错选,均不给分)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案 D B A A D D D D B B B D B C C
二、填空题(本题有9小题,每空2分,共40分)
16. 化学 氢元素、氧元素
17. Fe2O3+6HCl═2FeCl3+3H2O Al(OH)3+3HCl═AlCl3+3H2O
18. 感应电流 电磁感应
19. 白色固体##难溶于水 ① 被子
20. H2CO3 太阳能转化为化学能 转化4
21. +5 小于
22. 隔离可燃物 催化
23. 变大 减弱 ab
24. 气球胀大 将A中氢氧化钠溶液换成等量的水
三、实验探究题(本题有5小题15空格,第25-26小题,每空2分,第27-29小题,每空3分,共40分)
25. 硫酸钠也能和氯化钡反应生成白色沉淀硫酸钡 加入锌粒等活泼金属(或碳酸钠等),若有气体放出,证明稀硫酸过量,反之稀硫酸不过量
26. 磁场方向 有关 AC
27. 二氧化碳与氢氧化钠反应后装置中的压强减小 二氧化碳能够溶于水 将氢氧化钠溶液换为等体积的水 AC
28. 产量高 茎中导管 18
29. Na+和Cl-在整个过程中没有参与反应 NaCl、NaOH ;NaCl、Na2CO3 ;NaCl、NaOH、Na2CO3 BaCl2(或CaCl2或Ca(NO3)2或Ba(NO3)2)
四、分析计算题(本题有6小题,第30、31题各6分,第32、33小题各8分,第34题10分,第35题12分,共50分)
30. 3 6:1 0.25kg
31. 干燥 +6 KOH 设需要投入K2FeO4 的质量为x,
,
x=3.96kg,
答:一个拥有 2000 吨水的游泳池需要投入K2FeO4 的质量是7.92kg。
32.(1)植物的呼吸作用、动物的呼吸作用、燃料的燃烧
(2)①解:设至少加入氢氧化钠质量为x。
x=8kg。
答:至少加入8kg的氢氧化钠。
②理由支持所选装置
装置A:无水泵,无需耗电,节约能量;装置结构较简单;相同质量固体比溶液吸收更多CO2
装置B:利用氢氧化钠喷雾,增大接触面积,吸收更加充分,未反应的氢氧化钠喷雾还可以通过水泵循环利用,节约原料。
33. A 药品用量少,产生的废弃物也少,方便操作 HCl、CaCl2 设废液中氯化钙的质量为x
x=5.55g
废液中氯化钙的质量分数为:×100%=11.1%
34.(1)丁; 33.0
(2)设样品中含有碳酸钙的质量为x,
x=7.5克
CaCO3%=;
(3)。
35. 【详解】(1)[1]由表格数据可知,一个潮湿的人手和脚之间的电阻R人=1000Ω,则手接触火线时通过人体的电流
[2]熔断丝的额定电流为8A,通过熔断丝的电流远远小于熔断丝的额定电流,所以熔断丝不会断。
(2)[3]发现有人触电时,需要切断电源或用干燥竿子将火线与人分离。
(3)[4]人体与防电墙串联,通过它们的电流相等,则
R墙=420MΩ
答案第1页,共2页
答案第1页,共2页
注意事项:
1.本试题卷分卷I(选择题)和卷II(非选择题)两部分,满分180分,考试时间为120分钟。
2.本卷g取10牛/千克。
3.本卷可能用到的相对原子质量:H-1 C-12 N-14 0-16 Na-23 Mg-24 Al-27 S-32 Cl-35.5 Ca-40 Fe-56 Cu-64 Ag-108 I-127 Ba-233
4.答题时请仔细阅读答题卷上的注意事项,认真审题,细心答题。
第I卷(选择题50分)
一、选择题(本题有15小题,第1-10小题,每小题3分,第11-15小题,每小题4分,共50分。请选出一个符合题意的正确选项,不选、多选、错选、均不给分)
1.建立模型是学习科学的重要方法,下列不属于模型的是( )
A.原子结构 B.空气成分 C.细胞结构 D.注意行人
2.辨别家庭电路中的火线与零线,应该选用( )
A.放大镜B.测电笔 C.指南针 D.弹簧测力计
3.规范操作是科学实验成功的关键,下列实验操作错误的是( )
A.倾倒液体 B.取用粉末状固体 C.闻气体气味 D.检查气密性
4.乐乐通过无土栽培的技术培养富贵竹时,发现植株矮小,叶色发黄。为改善富贵竹的生长状况,应添加的无机盐是( )
A.含氮无机盐 B.含磷无机盐 C.含钾无机盐 D.含铁无机盐
5.新鲜果汁是常见的饮料,下列四种饮料呈弱碱性的是( )
A.柠檬汁(pH:2~3) B.苹果汁(pH:3~4)
C.西瓜汁(pH:5~6) D.玉米汁(pH:7~8)
6.如图,小敏用条形磁铁使铁钉竖直静止在空中,细线紧绷且质量不计,下列说法正确的是( )
A.铁钉上端被磁化成N极
B.铁钉受到的磁力与自身重力大小相等
C.桌面对石头的支持力和石头的重力是一对平衡力
D.细线对石头的拉力和石头对细线的拉力是一对相互作用力
7.如图为Fe元素的化合价和物质类别的二维图。下列说法正确的是( )
A.物质C的化学式为Fe2O3
B.物质D的化学式为Fe(OH)3
C.物质A在氧气中燃烧生成物质B
D.物质B比物质C的铁元素含量低
8.某小组使用数据采集器探究“铁丝在O2中燃烧”,集气瓶内O2的体积分数随时间的变化关系如图所示。下列说法正确的是( )
A.反应为:铁+氧气三氧化二铁 B.瓶中放少量水,用于吸收有毒物质
C.开始采集数据时,瓶内是纯净的O2 D.铁丝停止燃烧时,瓶内O2未耗尽
9.植物对水分的吸收、运输与细胞液及土壤溶液的溶质质量分数相关,图中箭头表示水分渗透的方向,由此可判断①、②、③三处溶液溶质质量分数大小关系是( )
①>②>③ B.③>②>①
C.①>③>② D.③>①>②
10.乙醇是酒精的主要成分,其分子式为C2H5OH。则下列有关乙醇的说法正确的是( )
A.乙醇分子中C,H,O三种原子的个数比为2∶5∶1 B.乙醇由三种元素组成
C.乙醇由9个原子构成 D.乙醇分子由碳原子和水分子构成
11.对于图中所示的四幅图,以下说法不正确的是( )
A.图甲所示的风光互补式路灯,太阳能发电装置是将太阳能转化为电能,风力发电机的工作原理是电磁感应
B.图乙中,铁钉B吸引的大头针比A多,说明电磁铁的磁性强弱与电流大小有关
C.图丙是一种自动测定油箱内油面高度的装置,油量减少时油量表示数变小
D.图丁是电流表的内部结构图,指针偏转角度随线圈中电流增大而增大,它是利用磁场对电流的作用的原理工作的
12.为探究植物种子呼吸作用的产物,用如图装置进行对照实验:先在A、B试管中加入等量的澄清石灰水,再往A试管中加入适量的已浸水及消毒的蚕豆种子,则试管B中应加入等量的( )
A.已浸水及消毒的绿豆种子
B.已浸水及未消毒的蚕豆种子
C.已煮熟及未消毒的蚕豆种子
D.已煮熟及消毒的蚕豆种子
13.在一密闭容器中发生某反应,其中甲、乙、丙、丁四种物质的质量变化如表所示,下列判断不正确的是( )
物质 甲 乙 丙 丁
反应前质量(g) 10 16 0 0
反应中质量(g) 1.6
反应后质量(g) 0 15.2 6.4
A.的值是4.4 B.的值是4
C.甲和乙是反应物 D.甲、丁间反应的质量比为7:8
14.2022年第24届冬季奥运会将由北京市和张家口市联合举行。如图所示,“五环”中相交两环中的物质间能够发生化学反应,其中A、B、C、D分别是HCl、Fe2O3、H2、CuSO4中的一种。下列说法中正确的是( )
A.A物质与B物质间发生的反应是工业炼铁的主要反应原理
B.B物质与C物质间发生反应的化学方程式为:4HCl+Fe2O3═2H2O+2FeCl2
C.C物质与NaOH溶液发生反应时无明显现象
D.D物质的溶液与NaOH溶液发生反应时产生红褐色沉淀
15.某混合物X由Al2O3,Fe2O3,Cu,SiO2中的一种或几种组成。分别对X进行如下实验,有关说法错误的是( )
A.由I可知,X中一定存在Fe2O3、Cu B.由II和III可得出结论,混合物中无Al2O3
C.1.92g固体为SiO2和Cu的混合物 D.原混合物中Fe2O3和Cu的质量比为1:1
第II卷(非选择题130分)
二、填空题(本题有9小题20空格,每空2分,共40分)
16.医用消毒酒精为75%的乙醇溶液,化工生产中可用A(主要成分的化学式为C8H18)作原料,经以下流程制取乙醇:
(1)步骤①的转化属于______(选填“化学”或“物理”)变化。
(2)步骤②是乙烯和含两种元素的化合物B发生化合反应,则B中所含元素是______。
17.酸、碱、盐等是我们学过的重要物质,请根据相关知识回答下列问题:
(1)稀盐酸能除铁锈(铁锈的主要成分是Fe2O3),写出稀盐酸除锈反应的化学方程式_____________________。
(2)服用含氢氧化铝[Al(OH)3]的药物可以治疗胃酸过多症,该反应的化学方程式为_____________________。
18.随着全民健身活动的兴起,有更多的人参加马拉松运动。马拉松已经远远不只是一场比赛,它是你认识自己,认识一座城市,认识这个世界的方式。因参赛选手很多,无法在同一起跑线出发而计时困难。近年常采用感应 芯片计时,参赛者须按要求正确佩带计时芯片,当参赛者通过起点和终点 设置有磁场的感应带时,芯片里的线圈中就会产生________,工作原理是_________,从而激发芯片发送编码信息,系统实时获取计时信息。
19.据报道,我国科学家发现治疗新冠的新药——中药千金藤素,获得国家发明专利授权。千金藤素来自千金藤,其化学式为C37H38N2O6,白色固体,难溶于水,易氧化,需密封避光低温保存。
(1)根据上述信息,写出千金藤素的一条物理性质:___________。
(2)千金藤素中各元素质量分数如图甲所示,其中表示碳元素的是___________。(填序号)
20.如图是自然界中碳、氧循环简图(其中Y为葡萄糖C6H12O6)。
(1)图一中的X是________(用化学式表示)。
(2)图二中的转化3是自然界中碳、氧循环的重要反应即绿色植物光合作用的过程,涉及的能量转化情况为________。
(3)生物体的呼吸作用对应的是图中的________。(填“转化2”或“转化4”)
21.如图所示是蔬菜无土栽培装置。在培育过程中,需要适时添加含有硝酸钾、磷酸二氢钾等物质的培养液。
(1)磷酸二氢铵(NH4H2PO4)中氮元素的化合价是-3价,磷元素的化合价是______。
(2)若蔬菜的根细胞液浓度______培养液的浓度(选填“大于”、“小于”、“等于”),会导致蔬菜细胞内水分含量下降而发生萎蔫。
22.1823年,德国化学家德贝莱纳发现氢气遇到金属铂会起火,根据此原理制成了世界上第一支打火机(如图甲)。
(1)当关闭开关,堵住喷嘴时打火机火焰熄灭,其灭火原理是___________;
(2)氢气和氧气遇铂在常温下就会反应,原理如乙图所示,铂在反应中起___________的作用。
23.如图甲所示为某智能扫地机器人部分工作原理图,其中R为光敏电阻:如图乙所示为光敏电阻R的阻值随照度变化的图线(照度表示物体被照明的程度,照度越大被照明的程度越大)。
(1)上述智能扫地机器人工作原理如下:接通电源,当地面灰尘较多时,使照射到光敏电阻R上的照度变小,光敏电阻R的阻值________(选填“变大”或“变小”),电磁铁的磁性________(选填“增强”或“减弱”),此时电动机旋转产生高速气流将灰尘等吸入集尘盒;当灰尘清扫到一定程度时,电动机停止工作,指示灯亮,该智能扫地机器人处于待机状态;
(2)根据其工作原理可知,电动机应接入________(选填“ab”或“cd”)之间。
24.小李同学用如下图总结NaOH的四类化学性质(即NaOH能够与四类物质发生化学反应)。
为验证性质④,他选择了二氧化碳与其反应,为探究两者是否发生了化学反应,小李设计了如图所示的A、B实验进行验证。实验现象为:A中试管内液面上升,B中___________。
李莉提出质疑,她认为A实验不严谨,应做一个对比实验:_________________________________。
三、实验探究题(本题有5小题,15空,25、26题每空2分,27-29题每空3分,共40分)
25.在研究酸和碱的化学性质时,某科学兴趣小组进行了如下探究实验:
(1)探究稀硫酸与氢氧化钠溶液的反应:
(2)探究上述稀硫酸与氢氧化钠溶液反应后烧杯中的硫酸是否过量:根据上述反应过程中溶液变成无色,不能确定稀硫酸是否过量。他们又分别选取氯化钡溶液、紫色石蕊试液设计实验方案,如下表:
实验方案 实验步骤 实验现象 实验结论
实验一 取样,滴入适量的氯化钡溶液 出现白色沉淀 稀硫酸过量
实验二 取样,滴入几滴紫色石蕊试液 溶液变红 稀硫酸过量
①上述实验方案中,方案一不合理,理由是___________________________________________________。
②请你再设计一个确定稀硫酸是否过量的实验方案,写出选用的药品、预期实验现象及结论___________
__________________________________________________________________________________________。
26.磁场看不见、摸不着,小科想利用铁屑和小磁针(黑色一端为极)来探究通电螺线管外部磁场特点。请你解答以下问题:
(1)实验中,小磁针的作用是为了研究通电螺线管周围的___________。(填“磁场强弱”或“磁场方向”)
(2)小科在奥斯特实验的启发下,只改变通电螺线管中的电流方向,实验现象如图乙所示。对比两次的实验现象可知:通电螺线管两端的磁极性质与通电螺线管中的电流方向___________。(填“有关”或“无关”)
(3)下列操作中能增强通电螺线管磁性的是___________
A.增大通电螺线管中的电流 B.改变通电螺线管中的电流方向
C.在通电螺线管内插入铁棒 D.减少通电螺线管的匝数
27.科学小组将制得的CO2分别通入澄清石灰水和氢氧化钠溶液中,他们观察到前者变浑浊,后者无明显现象。那么CO2和NaOH是否发生了化学反应?
(1)小明设计了甲、乙两个实验来验证CO2与NaOH发生了化学反应,如图所示。实验现象为:甲——软塑料瓶变瘪,乙——“瓶吞鸡蛋”。
①小林认为上述实验是可行的,其共同原理是____________________________________;
②小华提出质疑,她认为上述实验还不足以说明CO2和NaOH发生了反应,其理由是_______________________;小明同学针对小华的质疑又补充了一个对照实验,请简单写出实验方案_________________________________
__________________________________________________________________________________________。
(2)为进一步比较,老师用三个相同的烧瓶收集等量的CO2气体,注入等量的三种液体,用气压传感器测定内部气压变化,得到烧瓶内压强与时间的关系曲线如图丙所示。其中曲线2代表澄清石灰水,曲线3代表氢氧化钠溶液,由此曲线,你可以得出的结论是______。
A.CO2能与氢氧化钠溶液反应
B.CO2能使澄清石灰水变浑浊
C.此氢氧化钠溶液比澄清石灰水更适合用于吸收CO2
28.袁隆平院士(图甲)是中国杂交水稻事业的开创者和领导者,被誉为“杂交水稻之父”,为我国粮食生产和农业科学的发展作出了杰出贡献。缅怀袁老最好的方式是——“珍惜每一粒粮食”。
下表为常规水稻和杂交水稻的对比。
类别 常规水稻 杂交水稻
定义 通过选育、提纯、保持亲本品种的特征和特性不变,可以留种且后代不分离 选用两个在遗传上有一定差异,同时它们的优良性状又能互补的水稻品种,进行杂交,生产具有杂种优势的第一代
产量 一般较低(<300kg/亩) 一般较高(>700kg/亩)
品质 质软,粘而腻 质地硬,粘性小
特点 不需要年年换种,但需要提纯复壮,抗性差 生长旺盛,根系发达,穗大粒多,抗逆性强等
(1)请根据表一的内容写出支持种植杂交水稻的一个理由:_______________________________。
(2)据乙图,水和无机盐在水稻体内运输途径可以用文字表示为:根中导管→___________→叶中导管。
(3)乐乐把丙装置放在晴朗的室外环境,测得密闭玻璃钟罩内一天的氧气和二氧化碳浓度变化如图丁所示。已知空气中含氧量相对较高时,人会觉得更舒适。那么据图分析,你建议人们到田埂、公园等绿色植物较多的地方散步、游玩的时间应在___________时左右。
29.同学们在学习碱的化学性质时,进行了如图所示的实验。实验结束后,将A、B、C三个实验的废液倒入同一个干净烧杯D中,发现烧杯底部有白色沉淀,上层清液呈红色。
【提出问题】烧杯D中上层清液含有哪些溶质(除指示剂外)?
【分析讨论】小组讨论后认为,确定反应后物质成分的思维路径:①考虑反应物用量的不同;②抓住化学反应的本质,即微粒的重组。某小组同学分析过程笔记如下:
【初步结论】(1)通过分析确定:烧杯D上层清液中肯定不含H+,肯定含有Na+、Cl-。判断一定含有Na+、Cl-的依据是_____________________________________________________________;
【实验探究】
小组按如下方案进行实验探究
实验 实验内容 实验现象 实验结论
Ⅰ 取少量上层清液于试管中,加入过量碳酸钠溶液,静置。 无沉淀,溶液呈红色 肯定没有Ca2+
Ⅱ 取少量上层清液于试管中,加入过量“?”溶液,静置。 有白色沉淀,溶液呈红色 肯定有OH-、CO32-
(2)根据实验Ⅰ可以初步推断:上层清液中溶质(除指示剂外)所有可能的组成___________(用化学式表示);
(3)实验Ⅱ中应加入过量的___________溶液。
【实验结论】烧杯D中上层清液的溶质有指示剂、氯化钠、氢氧化钠、碳酸钠。
四、分析计算题(本题有6小题,第30、31题各6分,第32、33小题各8分,第34题10分,第35题12分,共50分)
30.过氧乙酸溶液是杀死病毒的一种有效药剂,某商店出售一种过氧乙酸消毒液,其标签上的部分文字说明如图所示。
过氧乙酸消毒液 质量:500g 化学式:C2H4O3 溶质质量分数:40% 使用方法:浸泡、喷雾、熏蒸等方法,用水稀释后使用
(1)过氧乙酸由______种元素组成。
(2)过氧乙酸中碳、氢元素的质量比为______。
(3)若要配制50千克溶质质量分数为0.2%的过氧乙酸消毒液用于地面消毒,需要该种消毒液的质量为多少?
31.高铁酸钾()是一种具有吸附、凝聚、杀菌等功能的新型、绿色、高效水处理剂,之所以称为高效的水处理剂是因为它遇水会发生反应,,可将其应用到游泳池水的循环再生使用,它不仅消毒杀菌、去除人体带入的污渍和悬浮固体,并对人体无伤害与刺激,安全无异味。
(1)应怎样保存___________,中铁元素的化合价为___________价。
(2)X化学式为___________。
(3)生成的能吸附游泳池水中的悬浮杂质,每1000吨游泳池水中需要2.14千克为最佳,那么一个拥有2000吨水的游泳池需要投入的质量是多少?
32.中国政府提出2060年前实现碳中和的目标。“碳中和”指二氧化碳等温室气体的排放总量等于吸收总量,达到“零排放”。为此,某科学兴趣小组经过“前期调查、原理选择、药量测算和装置设计”等环节,制定了二氧化碳吸收方案。
【前期调查】为分析自然界中碳排放与吸收的主要途径,小组成员经调查绘制了自然界部分碳循环示意图。
【原理选择】小组成员经比较分析,最终确定利用氢氧化钠吸收二氧化碳的思路(化学方程式为:2NaOH+CO2==Na2CO3+H2O)。
【药量测算】考虑操作的便捷性、可行性,设定一次性至少吸收二氧化碳4.4千克,并计算了装载氢氧化钠的质量。
【装置设计】结合吸收效果等因素,兴趣小组成员设计了图乙所示A、B两种吸收装置。
(1)图甲为小组成员绘制的碳排放与吸收示意图,其中碳排放的途径有___________。
(2)根据小组设定的一次性二氧化碳吸收量的要求,在装置A中至少要加入多少千克的氢氧化钠?
(3)请选择A、B两种装置的其中一种进行推广,并简要说明理由:_______________________________。
33.科学实验提倡绿色环保,对实验装置进行微型化改进是一条很好的途径。图甲是实验室制取并检验CO2的装置,图乙是对图甲实验装置进行“微型”化改进后的装置。
(1)图乙中微型塑料滴管在实验中的作用与图甲中的______仪器相同(填字母编号);
(2)通常用甲装置完成该实验需要的盐酸是“微型”实验装置用量的10倍,采用“微型”实验装置具有的优点是________________________________________________________;
(3)某学校化学兴趣小组的同学对实验室用石灰石和稀盐酸制取二氧化碳后的废液进行溶质成分的鉴定.取废液上层清液50克,逐滴加入质量分数为26.5%的碳酸钠溶液,出现气泡,滴加至10克时开始出现白色沉淀,继续滴加至沉淀不再产生,对沉淀进行对应处理后,测得沉淀的质量为5克,并绘制了如图像。则废液中含有的溶质有______(写化学式)。废液中属于盐类溶质的质量分数是多少?
34.四位同学元旦去仙华山风景区游玩,带回了几小块石灰石样品。为了检测样品中碳酸钙的含量,甲、乙、丙、丁四位同学用浓度相同的稀盐酸与样品充分反应来进行实验测定,(样品中的杂质不溶于水,且不与盐酸反应)测定数据如下:
甲同学 乙同学 丙同学 丁同学
所取石灰石样品的质量(g) 12.0 12.0 12.0 12.0
加入盐酸的质量(g)烧杯中 10.0 20.0 30.0 40.0
剩余物质的总质量(g) 21.0 30.0 39.0 48.7
试回答:
(1)四位同学里面,___________同学的石灰石样品完全反应了;12.0g石灰石样品与___________g稀盐酸恰好完全反应;
(2)样品中碳酸钙的质量分数为多少?(写出计算过程)
(3)请在图中大致画出生成气体的质量与加入稀盐酸质量的变化关系(标注必要的数值)。
35.随着家庭电气化程度越来越高,用电安全是一个十分突出的问题,下表提供了一组人体电阻的数据。如图所示,用电器R(阻值为44欧),电路中还有熔断电流为8A的保险丝。则:
测量项目 手和手之间电阻 手与脚之间电阻 手与塑料鞋底之间电阻
完全干燥时 200千欧 300千欧 8000千欧
出汗或潮湿时 1千欧 1千欧 10千欧
(1)一个全身潮湿的人,赤脚站在地上,由于不小心,手接触火线,发生触电事故,则通过人体的电流是___________A,通过计算分析此时保险丝是否熔断___________;
(2)当发现有人触电时,应该第一时间___________,在触电者未脱离电源前,严禁直接用手去触及伤员;
(3)为用电安全,有的电热水器安装了防电墙。防电墙技术就是在电热水器内部形成永久性电阻,从而降低异常情况下经过人体的电流值。经过防电墙处理后,发生异常情况时,人体承受的电压约10V,如图所示,这就保证了人体安全。若人体的最大电组约为20兆欧,求防电墙的电阻大约是多少?第1页 共4页 第2页 共4页
第1页 共4页 第2页 共4页
参考答案
一、选择题(本题有15小题,1-10题每小题3分,11-15题每小题4分,共50分。请选出各题中一个符合题意的正确选项,不选、多选、错选,均不给分)
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案 D B A A D D D D B B B D B C C
二、填空题(本题有9小题,每空2分,共40分)
16. 化学 氢元素、氧元素
17. Fe2O3+6HCl═2FeCl3+3H2O Al(OH)3+3HCl═AlCl3+3H2O
18. 感应电流 电磁感应
19. 白色固体##难溶于水 ① 被子
20. H2CO3 太阳能转化为化学能 转化4
21. +5 小于
22. 隔离可燃物 催化
23. 变大 减弱 ab
24. 气球胀大 将A中氢氧化钠溶液换成等量的水
三、实验探究题(本题有5小题15空格,第25-26小题,每空2分,第27-29小题,每空3分,共40分)
25. 硫酸钠也能和氯化钡反应生成白色沉淀硫酸钡 加入锌粒等活泼金属(或碳酸钠等),若有气体放出,证明稀硫酸过量,反之稀硫酸不过量
26. 磁场方向 有关 AC
27. 二氧化碳与氢氧化钠反应后装置中的压强减小 二氧化碳能够溶于水 将氢氧化钠溶液换为等体积的水 AC
28. 产量高 茎中导管 18
29. Na+和Cl-在整个过程中没有参与反应 NaCl、NaOH ;NaCl、Na2CO3 ;NaCl、NaOH、Na2CO3 BaCl2(或CaCl2或Ca(NO3)2或Ba(NO3)2)
四、分析计算题(本题有6小题,第30、31题各6分,第32、33小题各8分,第34题10分,第35题12分,共50分)
30. 3 6:1 0.25kg
31. 干燥 +6 KOH 设需要投入K2FeO4 的质量为x,
,
x=3.96kg,
答:一个拥有 2000 吨水的游泳池需要投入K2FeO4 的质量是7.92kg。
32.(1)植物的呼吸作用、动物的呼吸作用、燃料的燃烧
(2)①解:设至少加入氢氧化钠质量为x。
x=8kg。
答:至少加入8kg的氢氧化钠。
②理由支持所选装置
装置A:无水泵,无需耗电,节约能量;装置结构较简单;相同质量固体比溶液吸收更多CO2
装置B:利用氢氧化钠喷雾,增大接触面积,吸收更加充分,未反应的氢氧化钠喷雾还可以通过水泵循环利用,节约原料。
33. A 药品用量少,产生的废弃物也少,方便操作 HCl、CaCl2 设废液中氯化钙的质量为x
x=5.55g
废液中氯化钙的质量分数为:×100%=11.1%
34.(1)丁; 33.0
(2)设样品中含有碳酸钙的质量为x,
x=7.5克
CaCO3%=;
(3)。
35. 【详解】(1)[1]由表格数据可知,一个潮湿的人手和脚之间的电阻R人=1000Ω,则手接触火线时通过人体的电流
[2]熔断丝的额定电流为8A,通过熔断丝的电流远远小于熔断丝的额定电流,所以熔断丝不会断。
(2)[3]发现有人触电时,需要切断电源或用干燥竿子将火线与人分离。
(3)[4]人体与防电墙串联,通过它们的电流相等,则
R墙=420MΩ
答案第1页,共2页
答案第1页,共2页
同课章节目录
