物质的溶解(第一课时)
图片预览




文档简介
课件19张PPT。老爸,我要喝最甜的糖水,还要加,一直加……儿子,现在最甜的了,再加也不会再变甜了……嘿,别吵了,我给个建议吧:
学习物质的溶解性!第5节 物质的溶解(1) 遂昌湖山风景 〔联想与启示〕
在日常生活中,我们常观察到这样的事实:
1.在相同条件下,面粉在水中不易溶解,而食盐、
蔗糖在水中易于溶解。(一)溶解性:一种物质溶解在另一种物质里的能力。2.衣服上的油渍在水中很难洗去,而在汽油或酒精
中易于洗去。一、物质的溶解性─ 物质的一种特性蔗糖全部溶解仍有少量蔗糖
未能溶解(二)影响物质溶解性的因素1.提出问题:
根据研究的内容,提出探究的问题: ?
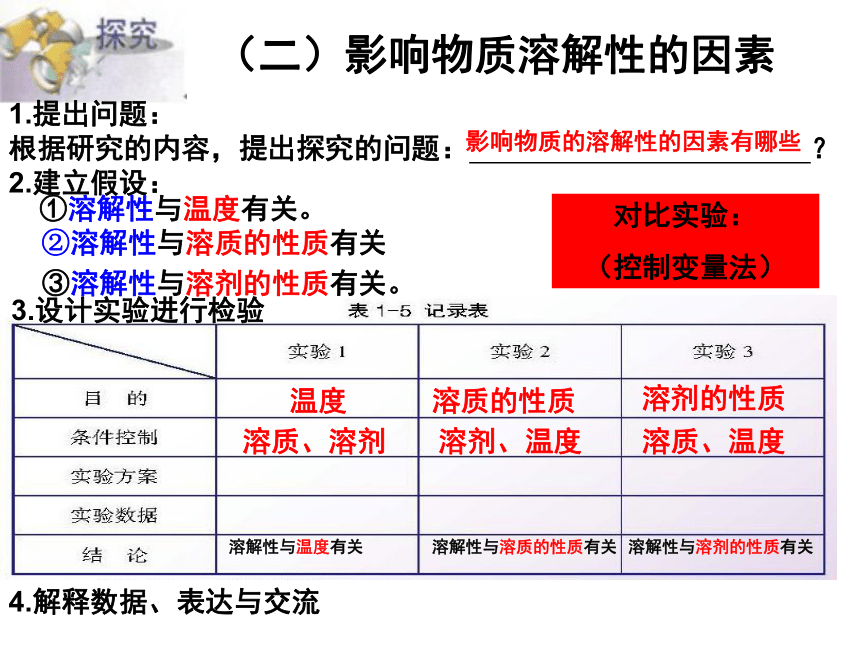
2.建立假设:影响物质的溶解性的因素有哪些①溶解性与温度有关。溶剂、温度③溶解性与溶剂的性质有关。温度溶质的性质溶剂的性质溶质、溶剂溶质、温度②溶解性与溶质的性质有关3.设计实验进行检验4.解释数据、表达与交流对比实验:
(控制变量法)溶解性与溶质的性质有关溶解性与温度有关溶解性与溶剂的性质有关实验1:
取1支试管,加入5mL水,然后加入20g蔗糖,充分振荡,蔗糖是否能完全溶解?如不能完全溶解,将试管加热,观察实验现象。固体没有全部溶解固体全部溶解溶解性与温度有关注意:
⑴.多数固体物质的溶解性随着温度的升高而增强,如,硝酸钾
⑵.极少数固体物质的溶解性随着温度的升高而减弱,如,消石灰1.同一物质在同一溶剂中的溶解性与温度有关;[实验2]
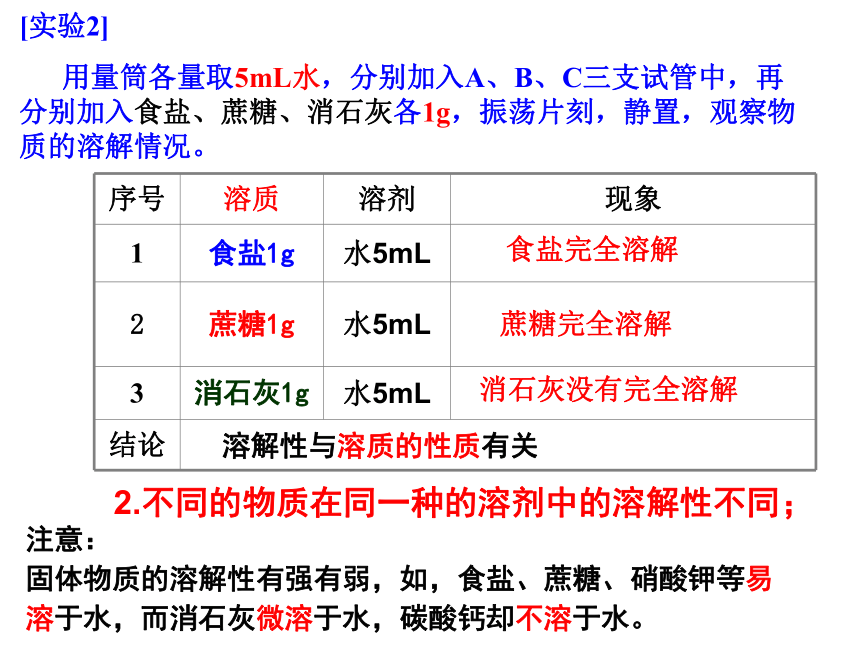
用量筒各量取5mL水,分别加入A、B、C三支试管中,再分别加入食盐、蔗糖、消石灰各1g,振荡片刻,静置,观察物质的溶解情况。食盐完全溶解蔗糖完全溶解消石灰没有完全溶解注意:
固体物质的溶解性有强有弱,如,食盐、蔗糖、硝酸钾等易溶于水,而消石灰微溶于水,碳酸钙却不溶于水。溶解性与溶质的性质有关2.不同的物质在同一种的溶剂中的溶解性不同;[实验3]
取A、B两支试管,分别滴入少量食用油。往试管A中加入少量水,往试管B中加入少量汽油,振荡,观察现象。食用油不溶于水食用油溶于汽油中注意:
在生活和生产中,人们常用酒精、汽油、氯仿、苯、香蕉水等溶剂溶解某些在水中难以溶解的物质。溶解性与溶剂的性质有关3.同一物质在不同的溶剂中的溶解性不同; 影响固体物质溶解性的因素有①溶质的性质;②溶剂的性质;③温度。与溶质的多少、溶剂的多少、溶液是否饱和、是否搅拌、颗粒大小无关。影响气体溶解性的因素哪些?①溶质的性质;
②溶剂的性质;
③温度;
④气压;气体溶解性随温度升高而减小 气体溶解性随气压增大而增大 (三)溶解时的吸热或放热现象有的物质(氢氧化钠、硫酸)溶解时,会放出热量,使溶液温度升高;
有的物质(硝酸铵)溶解时,会吸收热量,使溶液温度降低;
也有许多物质(食盐)溶解时,溶液的温度没有明显变化。实验表明:二、饱和溶液在一定的温度下,在一定量的溶剂中,物质能够溶解的量是有限的。饱和溶液在一定温度、一定量的溶剂中, 不能再溶解某种溶质的溶液,称为这种溶质的饱和溶液。不饱和溶液在一定温度、一定量的溶剂中, 还能继续溶解某种溶质的溶液,称为这种溶质的不饱和溶液。思考:
1.饱和溶液的前提条件是什么?
2.在上面的前提条件下,关键看什么?
3.为什么必须说明是“这种溶质”的饱和溶液?[实验1]
取一瓶底部留有硝酸钾晶体的硝酸钾溶液,分别取出适量加入A、B两支试管中,再分别向试管中加入少量硝酸钾晶体,振荡,观察固体是否溶解。
[实验2]
在A试管中再加入适量水,观察未溶解的硝酸钾是否继续溶解。
[实验3]
在酒精灯上加热B试管,观察未溶解的硝酸钾是否继续溶解。 1.如何用实验证明两瓶溶液中,一瓶是饱和溶液,二另一瓶是不饱和溶液? 答:添加少量溶质,若该溶质不能继续溶解,则原溶液是饱和溶液;若该溶质能继续溶解,则原溶液是不饱和溶液;观察底部是否为溶解的溶质。2.如何将不饱和的硝酸钾转化为饱和的硝酸钾溶液?一定温度、一定量的溶剂中、某溶质饱和溶液 不饱和溶液加溶质蒸发溶剂加溶剂升温降温练习、下列说法是否正确
(1)不能再溶解某种溶质的溶液叫饱和溶液。
(2)装有饱和溶液的瓶底,一定有这种溶质的固体。
(3)含有未溶溶质的溶液,一定是这种溶质的饱和溶液。
(4)使一接近饱和的溶液变成饱和溶液,可倒出一些溶液。
(5)在同一温度下,某物质的饱和溶液,一定会比不饱和溶液含有的溶质多。
(6)在相同温度下,食盐的饱和溶液比它的不饱和溶液要浓。
(7)60℃时的硝酸钾饱和溶液,当温度降低到20℃时,其它条件不变,该溶液还是饱和溶液 。
√√√交流讨论:饱和溶液一定
是浓溶液稀溶液一定是
不饱和溶液同学们说说他们谁是正确的?有的溶液溶有较多的溶质,称为浓溶液;
有的溶液溶有较少的溶质,称为稀溶液。结论:
1.浓、稀溶液与饱和、不饱和溶液无绝对关系;
饱和溶液不一定是浓溶液;不饱和溶液不一定是稀溶液。
2.同种溶质在相同温度下饱和溶液的浓度一定大于不饱和溶液。课堂小结:一、溶解性:1、影响物质溶解性的因素:①溶质性质②溶剂性质③温度一种物质(溶质)溶解在另一种物质(溶剂)里的能力。4、浓溶液和稀溶液:3、检验饱和溶液方法:取样,加入少量该溶质,观察能否继续溶解。⑴饱和溶液不一定是浓溶液,不饱和溶液也不一定是稀溶液;
⑵相同温度,同一溶质的溶液,饱和溶液比不饱和溶液要浓一些。加溶质蒸发溶剂降温加溶剂升温2、在一定温度下,某物质的饱和溶液一定是( )
A.浓溶液 B.不能溶解任何物质的溶液
C.稀溶液 D.不能继续溶解该物质的溶液D1、 下列因素不会影响物质溶解性的是( )
A.溶质的性质 B.溶剂的质量
C.溶剂的性质 D.温度B3、 下列措施不能使不饱和溶液转变为饱和溶液的是( )
A.蒸发溶剂 B.增加溶质
C.改变温度 D.加速搅拌D4、现有20℃时的硝酸钾饱和溶液100克,能使该溶液变为
不饱和溶液的方法是( )
A.恒温蒸发掉20克水 B.温度不变,加入20克硝酸钾
C.降低温度到10℃ D.升高温度到30℃ D练习:Thank you!
学习物质的溶解性!第5节 物质的溶解(1) 遂昌湖山风景 〔联想与启示〕
在日常生活中,我们常观察到这样的事实:
1.在相同条件下,面粉在水中不易溶解,而食盐、
蔗糖在水中易于溶解。(一)溶解性:一种物质溶解在另一种物质里的能力。2.衣服上的油渍在水中很难洗去,而在汽油或酒精
中易于洗去。一、物质的溶解性─ 物质的一种特性蔗糖全部溶解仍有少量蔗糖
未能溶解(二)影响物质溶解性的因素1.提出问题:
根据研究的内容,提出探究的问题: ?
2.建立假设:影响物质的溶解性的因素有哪些①溶解性与温度有关。溶剂、温度③溶解性与溶剂的性质有关。温度溶质的性质溶剂的性质溶质、溶剂溶质、温度②溶解性与溶质的性质有关3.设计实验进行检验4.解释数据、表达与交流对比实验:
(控制变量法)溶解性与溶质的性质有关溶解性与温度有关溶解性与溶剂的性质有关实验1:
取1支试管,加入5mL水,然后加入20g蔗糖,充分振荡,蔗糖是否能完全溶解?如不能完全溶解,将试管加热,观察实验现象。固体没有全部溶解固体全部溶解溶解性与温度有关注意:
⑴.多数固体物质的溶解性随着温度的升高而增强,如,硝酸钾
⑵.极少数固体物质的溶解性随着温度的升高而减弱,如,消石灰1.同一物质在同一溶剂中的溶解性与温度有关;[实验2]
用量筒各量取5mL水,分别加入A、B、C三支试管中,再分别加入食盐、蔗糖、消石灰各1g,振荡片刻,静置,观察物质的溶解情况。食盐完全溶解蔗糖完全溶解消石灰没有完全溶解注意:
固体物质的溶解性有强有弱,如,食盐、蔗糖、硝酸钾等易溶于水,而消石灰微溶于水,碳酸钙却不溶于水。溶解性与溶质的性质有关2.不同的物质在同一种的溶剂中的溶解性不同;[实验3]
取A、B两支试管,分别滴入少量食用油。往试管A中加入少量水,往试管B中加入少量汽油,振荡,观察现象。食用油不溶于水食用油溶于汽油中注意:
在生活和生产中,人们常用酒精、汽油、氯仿、苯、香蕉水等溶剂溶解某些在水中难以溶解的物质。溶解性与溶剂的性质有关3.同一物质在不同的溶剂中的溶解性不同; 影响固体物质溶解性的因素有①溶质的性质;②溶剂的性质;③温度。与溶质的多少、溶剂的多少、溶液是否饱和、是否搅拌、颗粒大小无关。影响气体溶解性的因素哪些?①溶质的性质;
②溶剂的性质;
③温度;
④气压;气体溶解性随温度升高而减小 气体溶解性随气压增大而增大 (三)溶解时的吸热或放热现象有的物质(氢氧化钠、硫酸)溶解时,会放出热量,使溶液温度升高;
有的物质(硝酸铵)溶解时,会吸收热量,使溶液温度降低;
也有许多物质(食盐)溶解时,溶液的温度没有明显变化。实验表明:二、饱和溶液在一定的温度下,在一定量的溶剂中,物质能够溶解的量是有限的。饱和溶液在一定温度、一定量的溶剂中, 不能再溶解某种溶质的溶液,称为这种溶质的饱和溶液。不饱和溶液在一定温度、一定量的溶剂中, 还能继续溶解某种溶质的溶液,称为这种溶质的不饱和溶液。思考:
1.饱和溶液的前提条件是什么?
2.在上面的前提条件下,关键看什么?
3.为什么必须说明是“这种溶质”的饱和溶液?[实验1]
取一瓶底部留有硝酸钾晶体的硝酸钾溶液,分别取出适量加入A、B两支试管中,再分别向试管中加入少量硝酸钾晶体,振荡,观察固体是否溶解。
[实验2]
在A试管中再加入适量水,观察未溶解的硝酸钾是否继续溶解。
[实验3]
在酒精灯上加热B试管,观察未溶解的硝酸钾是否继续溶解。 1.如何用实验证明两瓶溶液中,一瓶是饱和溶液,二另一瓶是不饱和溶液? 答:添加少量溶质,若该溶质不能继续溶解,则原溶液是饱和溶液;若该溶质能继续溶解,则原溶液是不饱和溶液;观察底部是否为溶解的溶质。2.如何将不饱和的硝酸钾转化为饱和的硝酸钾溶液?一定温度、一定量的溶剂中、某溶质饱和溶液 不饱和溶液加溶质蒸发溶剂加溶剂升温降温练习、下列说法是否正确
(1)不能再溶解某种溶质的溶液叫饱和溶液。
(2)装有饱和溶液的瓶底,一定有这种溶质的固体。
(3)含有未溶溶质的溶液,一定是这种溶质的饱和溶液。
(4)使一接近饱和的溶液变成饱和溶液,可倒出一些溶液。
(5)在同一温度下,某物质的饱和溶液,一定会比不饱和溶液含有的溶质多。
(6)在相同温度下,食盐的饱和溶液比它的不饱和溶液要浓。
(7)60℃时的硝酸钾饱和溶液,当温度降低到20℃时,其它条件不变,该溶液还是饱和溶液 。
√√√交流讨论:饱和溶液一定
是浓溶液稀溶液一定是
不饱和溶液同学们说说他们谁是正确的?有的溶液溶有较多的溶质,称为浓溶液;
有的溶液溶有较少的溶质,称为稀溶液。结论:
1.浓、稀溶液与饱和、不饱和溶液无绝对关系;
饱和溶液不一定是浓溶液;不饱和溶液不一定是稀溶液。
2.同种溶质在相同温度下饱和溶液的浓度一定大于不饱和溶液。课堂小结:一、溶解性:1、影响物质溶解性的因素:①溶质性质②溶剂性质③温度一种物质(溶质)溶解在另一种物质(溶剂)里的能力。4、浓溶液和稀溶液:3、检验饱和溶液方法:取样,加入少量该溶质,观察能否继续溶解。⑴饱和溶液不一定是浓溶液,不饱和溶液也不一定是稀溶液;
⑵相同温度,同一溶质的溶液,饱和溶液比不饱和溶液要浓一些。加溶质蒸发溶剂降温加溶剂升温2、在一定温度下,某物质的饱和溶液一定是( )
A.浓溶液 B.不能溶解任何物质的溶液
C.稀溶液 D.不能继续溶解该物质的溶液D1、 下列因素不会影响物质溶解性的是( )
A.溶质的性质 B.溶剂的质量
C.溶剂的性质 D.温度B3、 下列措施不能使不饱和溶液转变为饱和溶液的是( )
A.蒸发溶剂 B.增加溶质
C.改变温度 D.加速搅拌D4、现有20℃时的硝酸钾饱和溶液100克,能使该溶液变为
不饱和溶液的方法是( )
A.恒温蒸发掉20克水 B.温度不变,加入20克硝酸钾
C.降低温度到10℃ D.升高温度到30℃ D练习:Thank you!
同课章节目录
- 第1章 水和水的溶液
- 第1节 地球上的水
- 第2节 水的组成
- 第3节 水的浮力
- 第4节 物质在水中的分散状况
- 第5节 物质的溶解
- 第6节 物质的分离
- 第7节 水资源的利用、开发和保护
- 第2章 天气与气候
- 第1节 大气层
- 第2节 气温
- 第3节 大气的压强
- 第4节 风和降水
- 第5节 天气预报
- 第6节 气候和影响气候的因素
- 第7节 我国的气候特征与主要气象灾害
- 第3章 生命活动的调节
- 第1节 植物生命活动的调节
- 第2节 人体的激素调节
- 第3节 神经调节
- 第4节 动物的行为
- 第5节 体温的控制
- 第4章 电路探秘
- 第1节 电荷与电流
- 第2节 电流的测量
- 第3节 物质的导电性与电阻
- 第4节 变阻器
- 第5节 电压的测量
- 第6节 电流与电压、电阻的关系
- 第7节 电路分析与应用
- 研究性学习课题
- 一 测定本地区的“酸雨”情况及分析原因
- 二 太阳黑子活动与本地区降水的关系
- 三 训练小动物建立某种条件反射
- 四 调查在自然界或生命活动中的电现象
