人类对原子结构的认识
图片预览







文档简介
课件26张PPT。第三单元
人类对原子结构的认识第一课时 原子结构模型的演变
及核外电子排布武义二中 涂王伟 在化学家眼里,璀璨夺目的钻石和墨黑墨黑的木炭、石墨一样都是碳原子构成的 。这怎叫人相信?
英国的托斯卡纳伯爵就不相信。 说别人的钻石是假的,我这五彩缤纷、灿烂夺目的钻石一定不是碳原子构成的。
于是,化学家戴维用大聚光镜,在阳光下聚焦,随着温度的升高,钻石和木炭、石墨都不翼而飞了。
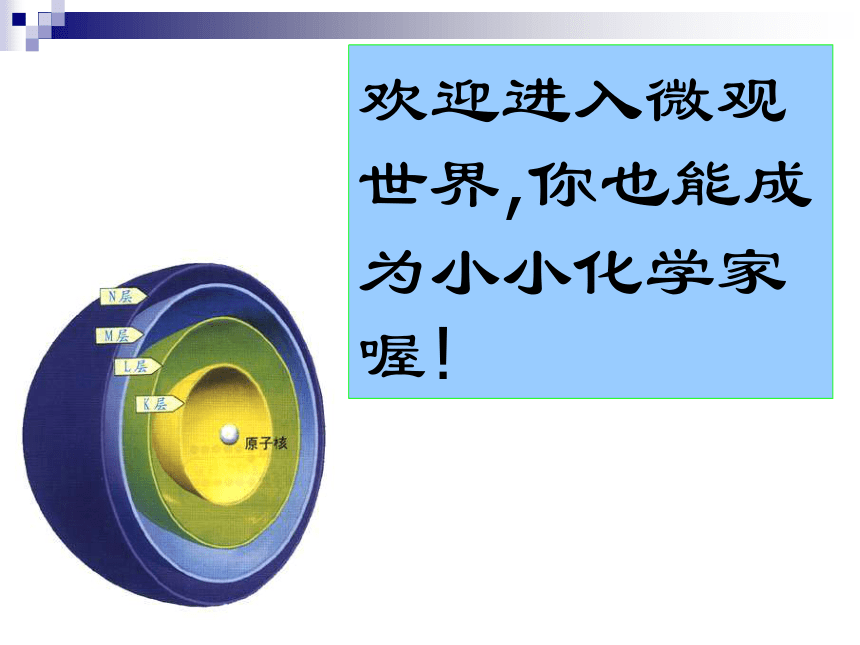
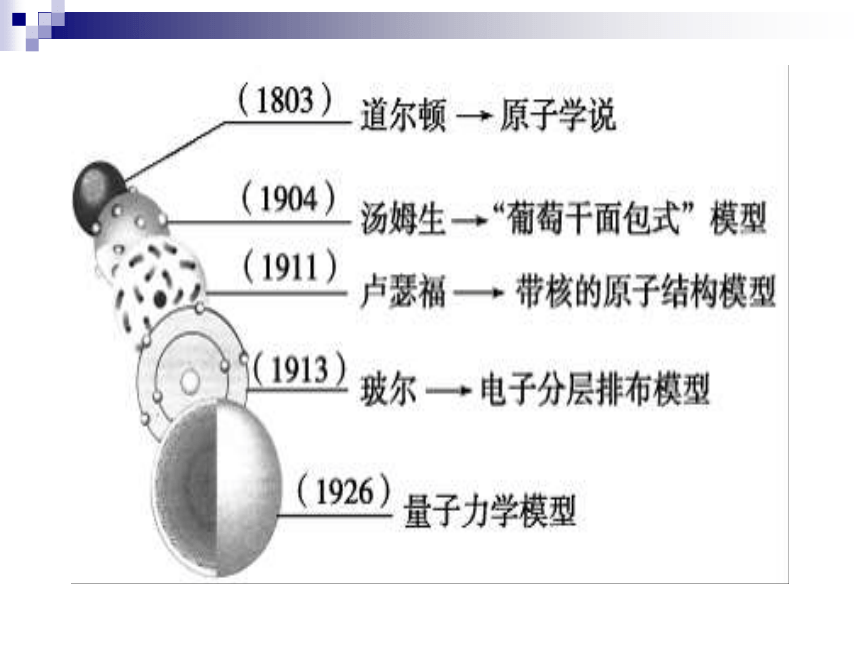
伯爵用昂贵的代价明白了道理。 化学典故构成物质的基本粒子有哪些?分子、原子、离子欢迎进入微观世界,你也能成为小小化学家喔!历史演绎:再现原子结构探索的历史 一、原子结构模型的演变 从化学史“原子结构模型的演变”学习中你获得了什么?(结合你的学习实际)道尔顿的原子理论汤姆生的 葡萄干面包式卢瑟福的带核原子结构模型
通过研究α粒子散射现象波尔的原子结构模型
通过研究氢原子光谱连连看:道尔顿 汤姆生 卢瑟福 玻 尔 “葡萄干面包式”原子结构模型 带核原子结构模型 核外电子分层排布结构模型 实心球结构模型 排排看:二、原子核外电子排布 实验:镁条的燃烧现象:化学方程式:【探究情景】 【探求新知】 氧化镁的化学式为什么写成MgO,而不是Mg2O、MgO2呢?剧烈燃烧,发出耀眼的白光,放出大量的热。[提出问题]: 核外电子是如何分层排布的?它的排布有没有规律呢? (一)、原子核外电子排布规律 [思考归纳]:
1、第一层最多排2个;第二层最多排8个。
2、稀有气体每层都达到饱和,处于稳定状态。所以化学性质稳定。
3、
4、
…(一)、原子核外电子排布规律 12第1层第2层第3层K层L层M层282+(二)、原子结构示意图小组合作:练习书写原子结构示意图并展示成果: Na 、 Al 、 N、 Cl (三)、元素性质与原子核外最外层电子排布的关系[提出问题]:
1、He、Ne、Ar等稀有气体(惰性气体)为什么很难与其它元素发生化学反应?而Mg和O2为什么点燃后会剧烈反应? 温馨提示:①分析He、Ne、Ar 原子结构示意图,请问有什么共同特点?②其它原子的“人生追求”是什么? 原子最外层的电子数小于8个时,在化学反应中总是得到或失去电子而达到最外层8电子的稳定结构。离子结构示意图原子结构示意图结论1、活泼金属元素的原子容易失去最外层上的电子变为带正电荷的阳离子。2、活泼非金属元素的原子容易得到电子变为带负电荷的阴离子。[提出问题]: 2、在活泼非金属与活泼金属化合的过程中,原子在反应中得失电子的数目与其在化合物中呈现的化合价之间存在什么关系? (完成教材P30页问题解决)⒈金属单质Na、Mg能分别与非金属单质O2、Cl2反应生成氧化物和氯化物,请写出这些氧化物和氯化物的化学式。
得e- 7-1Cl得得2e-6 -2O 失 2e-2 +2Mg失1失 e- +1Na失去(或得到)电子的数目原子最外层电子数目化合价元素⒉根据Na、Mg、O、Cl原子在反应中失去或得到电子的数目和该原子的最外层电子数目,推断其氧化物和氯化物中元素的化合价,将结果填入下表:
一些元素的原子得失电子的情况
Na2O、MgO、NaCl、MgCl2问题解决 1元素化合价与原子核外电子排布的关系 1、金属元素(如钠、镁、铝):
正化合价=失电子数=最外层电子数。
2、非金属元素(如氧、氟、氯):
=得电子数=8-最外层电子数。【典型例题】 元素A的原子最外层有6个电子,元素B的原子最外层有3个电子,则A与B形成的化合物可能的化学式是 ( )
A、B2A3 B、B2A C、BA2 D、BA课堂小结:(一)、原子核外电子排布规律(二)、原子结构示意图、离子结构示意图(三)、元素性质与原子核外最外层电子排布的关系 一、原子结构模型的演变二、原子核外电子排布谢谢大家
人类对原子结构的认识第一课时 原子结构模型的演变
及核外电子排布武义二中 涂王伟 在化学家眼里,璀璨夺目的钻石和墨黑墨黑的木炭、石墨一样都是碳原子构成的 。这怎叫人相信?
英国的托斯卡纳伯爵就不相信。 说别人的钻石是假的,我这五彩缤纷、灿烂夺目的钻石一定不是碳原子构成的。
于是,化学家戴维用大聚光镜,在阳光下聚焦,随着温度的升高,钻石和木炭、石墨都不翼而飞了。
伯爵用昂贵的代价明白了道理。 化学典故构成物质的基本粒子有哪些?分子、原子、离子欢迎进入微观世界,你也能成为小小化学家喔!历史演绎:再现原子结构探索的历史 一、原子结构模型的演变 从化学史“原子结构模型的演变”学习中你获得了什么?(结合你的学习实际)道尔顿的原子理论汤姆生的 葡萄干面包式卢瑟福的带核原子结构模型
通过研究α粒子散射现象波尔的原子结构模型
通过研究氢原子光谱连连看:道尔顿 汤姆生 卢瑟福 玻 尔 “葡萄干面包式”原子结构模型 带核原子结构模型 核外电子分层排布结构模型 实心球结构模型 排排看:二、原子核外电子排布 实验:镁条的燃烧现象:化学方程式:【探究情景】 【探求新知】 氧化镁的化学式为什么写成MgO,而不是Mg2O、MgO2呢?剧烈燃烧,发出耀眼的白光,放出大量的热。[提出问题]: 核外电子是如何分层排布的?它的排布有没有规律呢? (一)、原子核外电子排布规律 [思考归纳]:
1、第一层最多排2个;第二层最多排8个。
2、稀有气体每层都达到饱和,处于稳定状态。所以化学性质稳定。
3、
4、
…(一)、原子核外电子排布规律 12第1层第2层第3层K层L层M层282+(二)、原子结构示意图小组合作:练习书写原子结构示意图并展示成果: Na 、 Al 、 N、 Cl (三)、元素性质与原子核外最外层电子排布的关系[提出问题]:
1、He、Ne、Ar等稀有气体(惰性气体)为什么很难与其它元素发生化学反应?而Mg和O2为什么点燃后会剧烈反应? 温馨提示:①分析He、Ne、Ar 原子结构示意图,请问有什么共同特点?②其它原子的“人生追求”是什么? 原子最外层的电子数小于8个时,在化学反应中总是得到或失去电子而达到最外层8电子的稳定结构。离子结构示意图原子结构示意图结论1、活泼金属元素的原子容易失去最外层上的电子变为带正电荷的阳离子。2、活泼非金属元素的原子容易得到电子变为带负电荷的阴离子。[提出问题]: 2、在活泼非金属与活泼金属化合的过程中,原子在反应中得失电子的数目与其在化合物中呈现的化合价之间存在什么关系? (完成教材P30页问题解决)⒈金属单质Na、Mg能分别与非金属单质O2、Cl2反应生成氧化物和氯化物,请写出这些氧化物和氯化物的化学式。
得e- 7-1Cl得得2e-6 -2O 失 2e-2 +2Mg失1失 e- +1Na失去(或得到)电子的数目原子最外层电子数目化合价元素⒉根据Na、Mg、O、Cl原子在反应中失去或得到电子的数目和该原子的最外层电子数目,推断其氧化物和氯化物中元素的化合价,将结果填入下表:
一些元素的原子得失电子的情况
Na2O、MgO、NaCl、MgCl2问题解决 1元素化合价与原子核外电子排布的关系 1、金属元素(如钠、镁、铝):
正化合价=失电子数=最外层电子数。
2、非金属元素(如氧、氟、氯):
=得电子数=8-最外层电子数。【典型例题】 元素A的原子最外层有6个电子,元素B的原子最外层有3个电子,则A与B形成的化合物可能的化学式是 ( )
A、B2A3 B、B2A C、BA2 D、BA课堂小结:(一)、原子核外电子排布规律(二)、原子结构示意图、离子结构示意图(三)、元素性质与原子核外最外层电子排布的关系 一、原子结构模型的演变二、原子核外电子排布谢谢大家
