福建省德化县2022-2023学年高二上学期8月开学检测化学试题(Word版含答案)
文档属性
| 名称 | 福建省德化县2022-2023学年高二上学期8月开学检测化学试题(Word版含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-08-30 00:00:00 | ||
图片预览

文档简介
德化县2022-2023学年高二上学期8月开学检测
化学试题
(考试时间:75分钟总分:100分)
相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Cl-35.5 Zn-65
第Ⅰ卷(选择题,共48分)
一、选择题(本大题共12小题,每小题4分,共48分。在每小题列出的四个选项中,只有一项是最符合题目要求的。)
1.各种形式的能量转换为生活提供便利,下列选项主要依靠化学能转化为热能的是( )
A.一次性速冷冰袋 B.自热饭速食米饭 C.新能源汽车 D.麒麟970芯片
2.下列制备金属单质的方法正确的是( )
A.在高温条件下,用还原制备单质
B.在通电条件下,电解饱和食盐水制备单质
C.在通电条件下,电解熔融制备单质
D.加强热,使在高温条件下分解制备单质
3.一种外壳为纸层包装的电池,印有如图所示的文字。下列有关说法错误的是( )
A.该电池是一次电池
B.该电池工作时,电子由负极通过外电路流入正极
C.该电池含有的金属元素中毒性最大的是
D.该电池工作时,外电路中每通过0.2电子,锌的质量理论上减少3.25g
4.工业上常采用氨脱硝法处理电厂排放的氮氧化物()污染物。以处理为例,原理为:
常用的催化剂有和,其中的催化效率更好一些。下列表示两种催化剂在反应催化过程中的能量变化示意图合理的是( )
A B C D
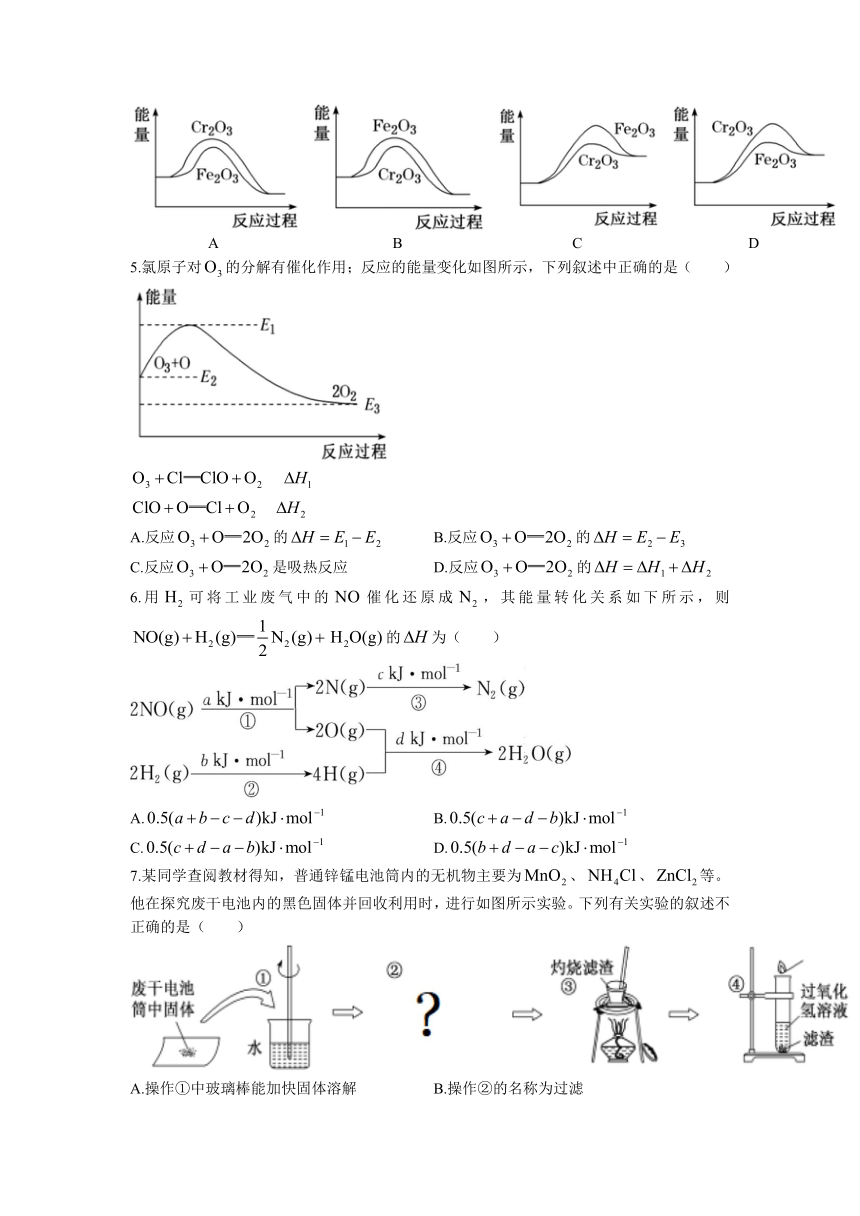
5.氯原子对的分解有催化作用;反应的能量变化如图所示,下列叙述中正确的是( )
A.反应的 B.反应的
C.反应是吸热反应 D.反应的
6.用可将工业废气中的催化还原成,其能量转化关系如下所示,则的为( )
A. B.
C. D.
7.某同学查阅教材得知,普通锌锰电池筒内的无机物主要为、、等。他在探究废干电池内的黑色固体并回收利用时,进行如图所示实验。下列有关实验的叙述不正确的是( )
A.操作①中玻璃棒能加快固体溶解 B.操作②的名称为过滤
C.操作③盛放滤渣的仪器是坩埚 D.操作④的目的是除去滤渣中的杂质
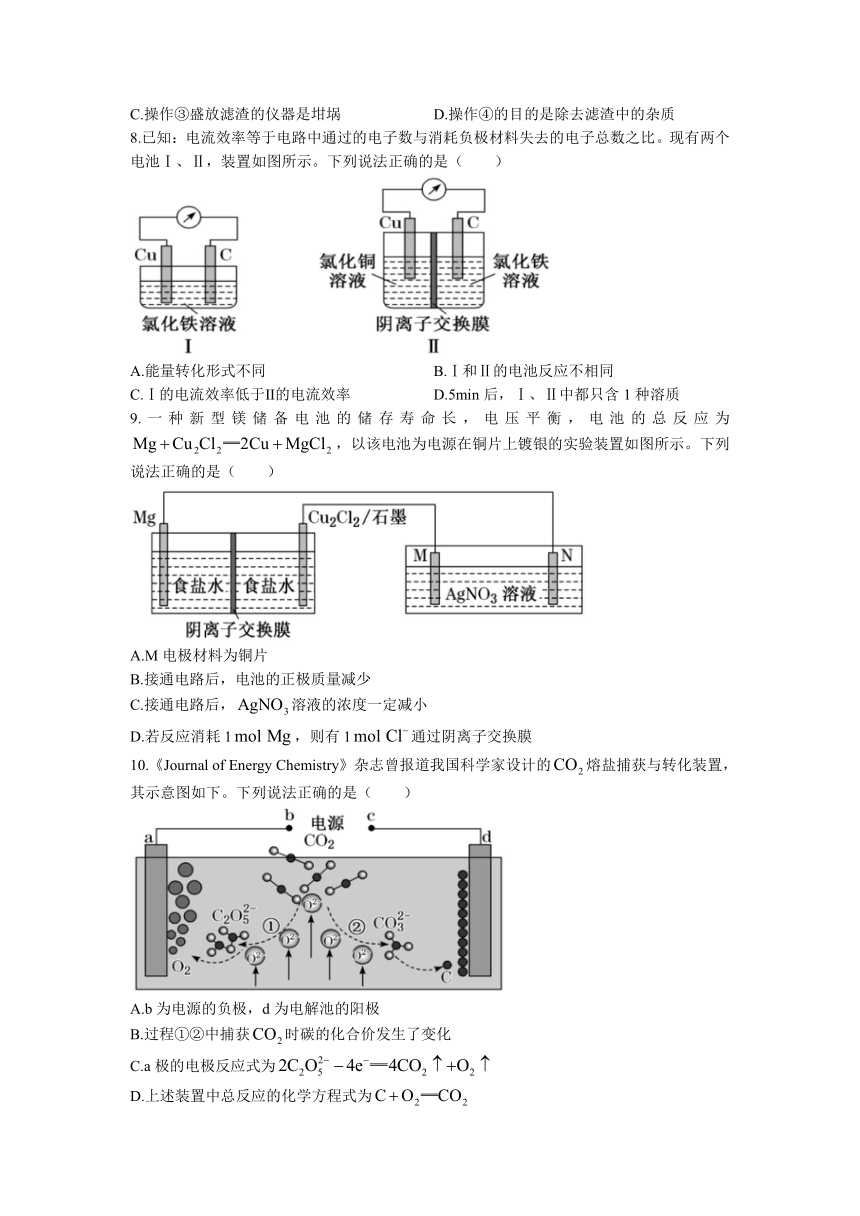
8.已知:电流效率等于电路中通过的电子数与消耗负极材料失去的电子总数之比。现有两个电池Ⅰ、Ⅱ,装置如图所示。下列说法正确的是( )
A.能量转化形式不同 B.Ⅰ和Ⅱ的电池反应不相同
C.Ⅰ的电流效率低于Ⅱ的电流效率 D.5min后,Ⅰ、Ⅱ中都只含1种溶质
9.一种新型镁储备电池的储存寿命长,电压平衡,电池的总反应为,以该电池为电源在铜片上镀银的实验装置如图所示。下列说法正确的是( )
A.M电极材料为铜片
B.接通电路后,电池的正极质量减少
C.接通电路后,溶液的浓度一定减小
D.若反应消耗1,则有1通过阴离子交换膜
10.《Journal of Energy Chemistry》杂志曾报道我国科学家设计的熔盐捕获与转化装置,其示意图如下。下列说法正确的是( )
A.b为电源的负极,d为电解池的阳极
B.过程①②中捕获时碳的化合价发生了变化
C.a极的电极反应式为
D.上述装置中总反应的化学方程式为
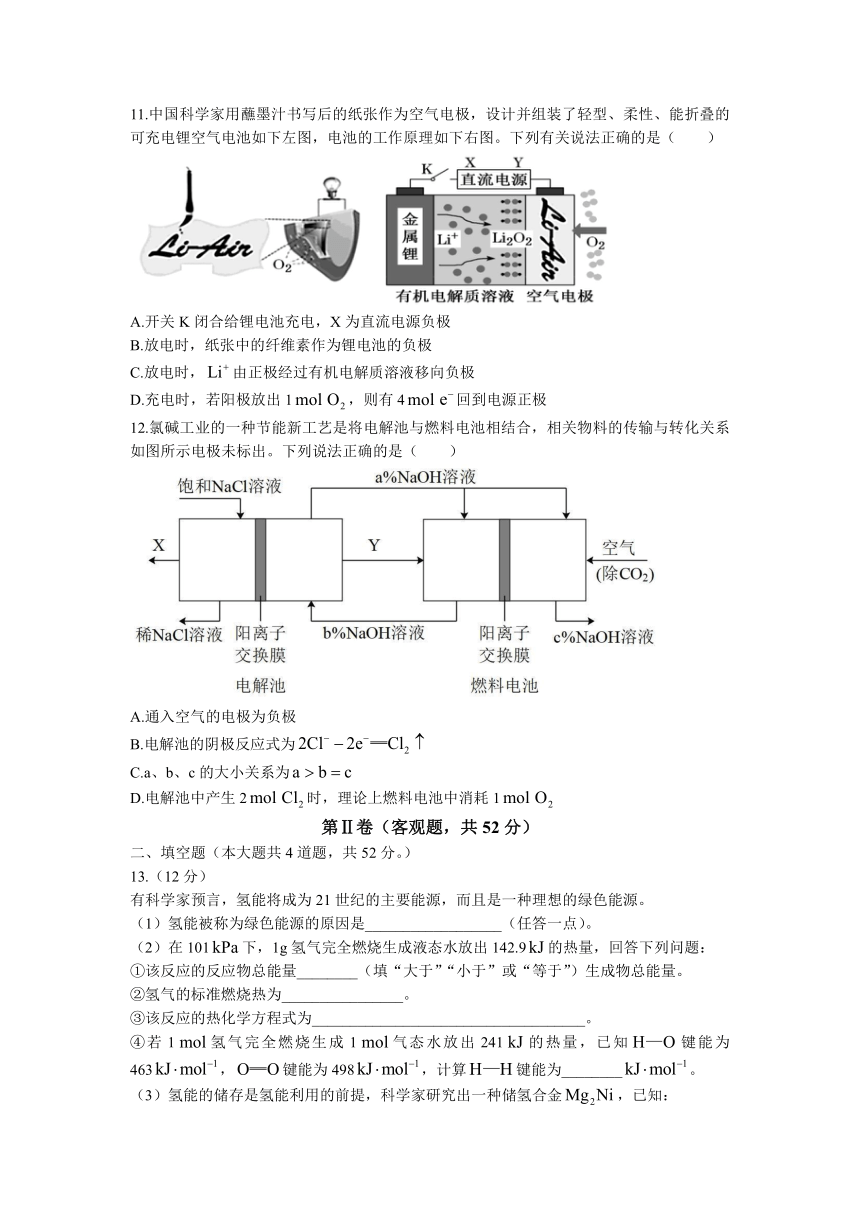
11.中国科学家用蘸墨汁书写后的纸张作为空气电极,设计并组装了轻型、柔性、能折叠的可充电锂空气电池如下左图,电池的工作原理如下右图。下列有关说法正确的是( )
A.开关K闭合给锂电池充电,X为直流电源负极
B.放电时,纸张中的纤维素作为锂电池的负极
C.放电时,由正极经过有机电解质溶液移向负极
D.充电时,若阳极放出1,则有4回到电源正极
12.氯碱工业的一种节能新工艺是将电解池与燃料电池相结合,相关物料的传输与转化关系如图所示电极未标出。下列说法正确的是( )
A.通入空气的电极为负极
B.电解池的阴极反应式为
C.a、b、c的大小关系为
D.电解池中产生2时,理论上燃料电池中消耗1
第Ⅱ卷(客观题,共52分)
二、填空题(本大题共4道题,共52分。)
13.(12分)
有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。
(1)氢能被称为绿色能源的原因是__________________(任答一点)。
(2)在101下,1g氢气完全燃烧生成液态水放出142.9的热量,回答下列问题:
①该反应的反应物总能量________(填“大于”“小于”或“等于”)生成物总能量。
②氢气的标准燃烧热为________________。
③该反应的热化学方程式为____________________________________。
④若1氢气完全燃烧生成1气态水放出241的热量,已知键能为463,键能为498,计算键能为________。
(3)氢能的储存是氢能利用的前提,科学家研究出一种储氢合金,已知:
;
;
。
则________。
14.(12分)
纳米级由于具有优良的催化性能而受关注,下表为制取的两种方法:
方法a 用炭粉在高温条件下还原
方法b 电解法,反应为
(1)工业上常用方法b制取而很少用方法a,其原因是反应条件不易控制,若控温不当易生成__________而使产率降低。
(2)已知:①
②
③
则方法a中发生的反应: ________。
(3)方法b是用液态肼燃料电池为电源,通过离子交换膜电解法控制电解液中的浓度来制备纳米,装置如图所示:
①上述装置中B电极应连__________(填“C”或“D”)电极。
②该离子交换膜为________(填“阴”或“阳”)离子交换膜,
该电解池的阴极反应式_____________________________________。
③原电池中负极反应式为________________________________________________。
15.(16分)
反应热的研究对于化学学科发展具有重要意义。
I.已知反应:①101,
②稀溶液中,
下列结论中正确的是________。
A.碳的燃烧热等于110.5
B.稀硫酸与稀溶液反应的中和热为114.6
C.含20.0g的稀溶液与稀盐酸完全中和,放出28.65的热量
Ⅱ.利用如图所示装置测定中和热的实验步骤如下:
①用量筒量取1000.50盐酸倒入小烧杯中,测出盐酸温度;
②用另一量筒量取1000.55溶液,并用同一温度计测出其温度;
③将和盐酸溶液一并倒入小烧杯中,设法使之混合均匀,测混合液最高温度。
(1)仪器a的名称是___________;烧杯间填满碎泡沫塑料的作用是___________。
(2)配制1000.55的氢氧化钠溶液,需要用到的仪器有托盘天平、烧杯、药匙、镊子、玻璃棒、量筒以及___________。
(3)实验中改用800.50盐酸跟800.55溶液进行反应,与上述实验相比,所放出的热量____________(填“相等”“不相等”)。用溶液和硫酸代替上述试剂,所测中和热的数值________。(填“偏大”、“偏小”或“不变”)
(4)倒入和盐酸溶液的正确操作是________(填字母)。
A.沿玻璃棒缓慢倒入 B.分多次倒入 C.一次迅速倒入
(5)现将一定量稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别与1L1.0的稀盐酸恰好完全反应,其反应热分别为、、ΔH3,则、、的大小关系为____________________。
16.(12分)
电化学在现代生活、生产和科学技术的发展中发挥着越来越重要的作用。
(1)绿色环保的全钒液流电池工作原理如图所示:
①电池放电时电极A为正极。充电时,A电极反应式为__________________,移动方向为________(填“A→B”或“B→A”)。
②电极A与电极B之间质子交换膜的作用___________________________________。
(2)利用微生物燃料电池处理某废水的工作原理如图所示。
①该电池的正极为_________(填“a”或“b”),a电极反应式为_____________________。
②当电路中有0.6转移时,通过质子交接膜的数目为_____________。
德化县2022-2023学年高二上学期8月开学检测
化学参考答案
选择题(本题共有12小题,每小题4分,共48分,每小题只有一个选项符合题意)
1 2 3 4 5 6 7 8 9 10 11 12
B C D B D A D C B C A D
非选择题(共4题,共52分)
13.(12分)
(1)产物无污染(答案合理均可)
(2)①大于 ②285.8 ③ ④436
(3)+84.6
14.(12分)
(1)
(2)+34.5
(3)①D ②阴
③
15.(16分)
Ⅰ.C
Ⅱ.(1)环形玻璃搅拌棒 保温、隔热,减少实验过程中的热量损失
(2)100容量瓶、胶头滴管
(3)不相等 偏大
(4)C
(5)
16.(12分)
(1)① A→B
②避免氧化剂与还原剂直接接触(其他合理答案也可)
(2)①b
②0.6或
化学试题
(考试时间:75分钟总分:100分)
相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Cl-35.5 Zn-65
第Ⅰ卷(选择题,共48分)
一、选择题(本大题共12小题,每小题4分,共48分。在每小题列出的四个选项中,只有一项是最符合题目要求的。)
1.各种形式的能量转换为生活提供便利,下列选项主要依靠化学能转化为热能的是( )
A.一次性速冷冰袋 B.自热饭速食米饭 C.新能源汽车 D.麒麟970芯片
2.下列制备金属单质的方法正确的是( )
A.在高温条件下,用还原制备单质
B.在通电条件下,电解饱和食盐水制备单质
C.在通电条件下,电解熔融制备单质
D.加强热,使在高温条件下分解制备单质
3.一种外壳为纸层包装的电池,印有如图所示的文字。下列有关说法错误的是( )
A.该电池是一次电池
B.该电池工作时,电子由负极通过外电路流入正极
C.该电池含有的金属元素中毒性最大的是
D.该电池工作时,外电路中每通过0.2电子,锌的质量理论上减少3.25g
4.工业上常采用氨脱硝法处理电厂排放的氮氧化物()污染物。以处理为例,原理为:
常用的催化剂有和,其中的催化效率更好一些。下列表示两种催化剂在反应催化过程中的能量变化示意图合理的是( )
A B C D
5.氯原子对的分解有催化作用;反应的能量变化如图所示,下列叙述中正确的是( )
A.反应的 B.反应的
C.反应是吸热反应 D.反应的
6.用可将工业废气中的催化还原成,其能量转化关系如下所示,则的为( )
A. B.
C. D.
7.某同学查阅教材得知,普通锌锰电池筒内的无机物主要为、、等。他在探究废干电池内的黑色固体并回收利用时,进行如图所示实验。下列有关实验的叙述不正确的是( )
A.操作①中玻璃棒能加快固体溶解 B.操作②的名称为过滤
C.操作③盛放滤渣的仪器是坩埚 D.操作④的目的是除去滤渣中的杂质
8.已知:电流效率等于电路中通过的电子数与消耗负极材料失去的电子总数之比。现有两个电池Ⅰ、Ⅱ,装置如图所示。下列说法正确的是( )
A.能量转化形式不同 B.Ⅰ和Ⅱ的电池反应不相同
C.Ⅰ的电流效率低于Ⅱ的电流效率 D.5min后,Ⅰ、Ⅱ中都只含1种溶质
9.一种新型镁储备电池的储存寿命长,电压平衡,电池的总反应为,以该电池为电源在铜片上镀银的实验装置如图所示。下列说法正确的是( )
A.M电极材料为铜片
B.接通电路后,电池的正极质量减少
C.接通电路后,溶液的浓度一定减小
D.若反应消耗1,则有1通过阴离子交换膜
10.《Journal of Energy Chemistry》杂志曾报道我国科学家设计的熔盐捕获与转化装置,其示意图如下。下列说法正确的是( )
A.b为电源的负极,d为电解池的阳极
B.过程①②中捕获时碳的化合价发生了变化
C.a极的电极反应式为
D.上述装置中总反应的化学方程式为
11.中国科学家用蘸墨汁书写后的纸张作为空气电极,设计并组装了轻型、柔性、能折叠的可充电锂空气电池如下左图,电池的工作原理如下右图。下列有关说法正确的是( )
A.开关K闭合给锂电池充电,X为直流电源负极
B.放电时,纸张中的纤维素作为锂电池的负极
C.放电时,由正极经过有机电解质溶液移向负极
D.充电时,若阳极放出1,则有4回到电源正极
12.氯碱工业的一种节能新工艺是将电解池与燃料电池相结合,相关物料的传输与转化关系如图所示电极未标出。下列说法正确的是( )
A.通入空气的电极为负极
B.电解池的阴极反应式为
C.a、b、c的大小关系为
D.电解池中产生2时,理论上燃料电池中消耗1
第Ⅱ卷(客观题,共52分)
二、填空题(本大题共4道题,共52分。)
13.(12分)
有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。
(1)氢能被称为绿色能源的原因是__________________(任答一点)。
(2)在101下,1g氢气完全燃烧生成液态水放出142.9的热量,回答下列问题:
①该反应的反应物总能量________(填“大于”“小于”或“等于”)生成物总能量。
②氢气的标准燃烧热为________________。
③该反应的热化学方程式为____________________________________。
④若1氢气完全燃烧生成1气态水放出241的热量,已知键能为463,键能为498,计算键能为________。
(3)氢能的储存是氢能利用的前提,科学家研究出一种储氢合金,已知:
;
;
。
则________。
14.(12分)
纳米级由于具有优良的催化性能而受关注,下表为制取的两种方法:
方法a 用炭粉在高温条件下还原
方法b 电解法,反应为
(1)工业上常用方法b制取而很少用方法a,其原因是反应条件不易控制,若控温不当易生成__________而使产率降低。
(2)已知:①
②
③
则方法a中发生的反应: ________。
(3)方法b是用液态肼燃料电池为电源,通过离子交换膜电解法控制电解液中的浓度来制备纳米,装置如图所示:
①上述装置中B电极应连__________(填“C”或“D”)电极。
②该离子交换膜为________(填“阴”或“阳”)离子交换膜,
该电解池的阴极反应式_____________________________________。
③原电池中负极反应式为________________________________________________。
15.(16分)
反应热的研究对于化学学科发展具有重要意义。
I.已知反应:①101,
②稀溶液中,
下列结论中正确的是________。
A.碳的燃烧热等于110.5
B.稀硫酸与稀溶液反应的中和热为114.6
C.含20.0g的稀溶液与稀盐酸完全中和,放出28.65的热量
Ⅱ.利用如图所示装置测定中和热的实验步骤如下:
①用量筒量取1000.50盐酸倒入小烧杯中,测出盐酸温度;
②用另一量筒量取1000.55溶液,并用同一温度计测出其温度;
③将和盐酸溶液一并倒入小烧杯中,设法使之混合均匀,测混合液最高温度。
(1)仪器a的名称是___________;烧杯间填满碎泡沫塑料的作用是___________。
(2)配制1000.55的氢氧化钠溶液,需要用到的仪器有托盘天平、烧杯、药匙、镊子、玻璃棒、量筒以及___________。
(3)实验中改用800.50盐酸跟800.55溶液进行反应,与上述实验相比,所放出的热量____________(填“相等”“不相等”)。用溶液和硫酸代替上述试剂,所测中和热的数值________。(填“偏大”、“偏小”或“不变”)
(4)倒入和盐酸溶液的正确操作是________(填字母)。
A.沿玻璃棒缓慢倒入 B.分多次倒入 C.一次迅速倒入
(5)现将一定量稀氢氧化钠溶液、稀氢氧化钙溶液、稀氨水分别与1L1.0的稀盐酸恰好完全反应,其反应热分别为、、ΔH3,则、、的大小关系为____________________。
16.(12分)
电化学在现代生活、生产和科学技术的发展中发挥着越来越重要的作用。
(1)绿色环保的全钒液流电池工作原理如图所示:
①电池放电时电极A为正极。充电时,A电极反应式为__________________,移动方向为________(填“A→B”或“B→A”)。
②电极A与电极B之间质子交换膜的作用___________________________________。
(2)利用微生物燃料电池处理某废水的工作原理如图所示。
①该电池的正极为_________(填“a”或“b”),a电极反应式为_____________________。
②当电路中有0.6转移时,通过质子交接膜的数目为_____________。
德化县2022-2023学年高二上学期8月开学检测
化学参考答案
选择题(本题共有12小题,每小题4分,共48分,每小题只有一个选项符合题意)
1 2 3 4 5 6 7 8 9 10 11 12
B C D B D A D C B C A D
非选择题(共4题,共52分)
13.(12分)
(1)产物无污染(答案合理均可)
(2)①大于 ②285.8 ③ ④436
(3)+84.6
14.(12分)
(1)
(2)+34.5
(3)①D ②阴
③
15.(16分)
Ⅰ.C
Ⅱ.(1)环形玻璃搅拌棒 保温、隔热,减少实验过程中的热量损失
(2)100容量瓶、胶头滴管
(3)不相等 偏大
(4)C
(5)
16.(12分)
(1)① A→B
②避免氧化剂与还原剂直接接触(其他合理答案也可)
(2)①b
②0.6或
同课章节目录
