人教版化学九年级上册 第一单元 课题1 物质的变化和性质 (第2课时) 课件(共23张PPT)
文档属性
| 名称 | 人教版化学九年级上册 第一单元 课题1 物质的变化和性质 (第2课时) 课件(共23张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-09-01 00:00:00 | ||
图片预览







文档简介
(共23张PPT)
第一单元 走进化学世界
导入新课
讲授新课
课堂小结
随堂训练
课题1 物质的变化和性质
第2课时 物质的性质
导入新课
观察与思考
日常生活中,常见一些人用医用酒精来降温,以达到退烧的目的,也经常用工业酒精炖小锅美食。这都是利用了酒精的特性。
思考:根据你的观察和生活经验,酒精有哪些性质?
导入新课
根据观察和生活经验,酒精具有以下性质:
颜色:
状态:
气味:
密度:
水溶性:
是否挥发:
点燃时在空气中
无色
液体
有特殊气味
0.8g/ml
能与水互溶
易挥发
能燃烧
讨论:以上性质可以怎样分类?
1.了解物理性质和化学性质的概念,并能识别。(重点)
2.能区分物质的物理变化与物理性质,化学变化与化学
性质。(难点)
3.明确物质用途所运用的性质,判断该性质属于物理性
质还是化学性质。
学习目标
导入新课
物理性质和化学性质的定义
一
讲授新课
合作探究
通过对酒精性质的了解,我们知道物质本身有许多固有的属性,哪些是通过化学变化表现出来的性质,哪些不是通过化学变化表现出来的本身就固有的性质呢?
物理性质
化学性质
归纳与小结
1.物质在化学变化中表现出来的性质叫做化学性质。
2.物质不需要发生化学变化就表现出来的性质叫做物理性质。
如:颜色、状态、气味、熔点、沸点、硬度、溶解性、挥发性、密度、导热性、导电性等。
如:可燃性、助燃性、毒性、氧化性、稳定性、腐蚀性、酸性、碱性等。
讲授新课
知识链接
⑴ 熔点和沸点
① 熔点:物质的熔化温度(固态变液体),如:固态的冰在0℃
时会熔化成液态的水,即冰的熔点为0℃。
② 沸点:液体沸腾时的温度(液态变气态),如:液态水加热
到100℃时会沸腾,即水的沸点为100℃。(沸点会
随着大气压的减小而降低)
101kPa的压强称为标准大气压,上述水的熔点和沸点是在标准大气压下测定的;若压强低于101kPa,则水的沸点低于100℃。
讲授新课
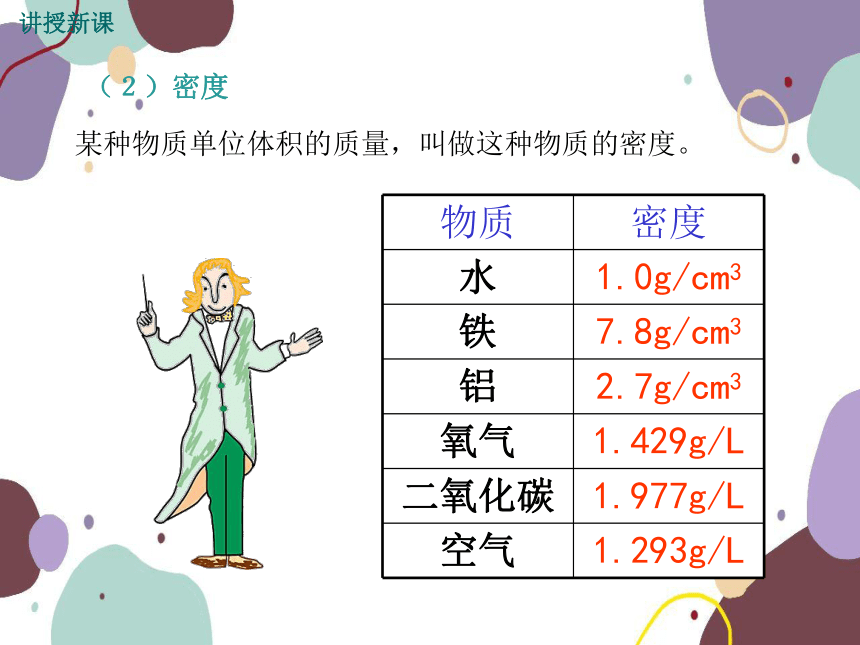
(2)密度
某种物质单位体积的质量,叫做这种物质的密度。
物质 密度
水 1.0g/cm3
铁 7.8g/cm3
铝 2.7g/cm3
氧气 1.429g/L
二氧化碳 1.977g/L
空气 1.293g/L
讲授新课
典例精析
例1 下列物质表现出的性质属于化学性质的是( )
A. 氧气为无色无味的气体 B.碳在常温下的性质稳定
C. 铁可以打成铁片 D.4℃时水的密度最大
解析:
A. 颜色、气味、状态属于物理性质;
B.稳定性指不易与其他物质发生化学反应,属于化学性质;
C.说明铁具有延展性,属于物理性质;
D.密度属于物理性质。
B
讲授新课
归纳与小结
讲授新课
物理性质
化学性质
区别
性质判断
性质内容
物质是否需通过化学变化表现出来的性质
直接(眼看、鼻闻、
耳听、手掂量等)
或由仪器间接观察
必须通过化学变化才
可判断。在叙述物质
的化学性质时,往往
有下列字:能、会、
可以、易、难等
颜色、状态、气味、
熔点、沸点、硬度、
密度、溶解度、挥发性、
导电性、导热性等
根据物质的化学变化
判断其化学性质,如
可燃性、稳定性(如
受热是否易分解)等
实验与探究
实验1:分别取一集气瓶氧气和一集气瓶二氧化碳气体,仔细观察它们的颜色和状态,闻一闻气味。
讲授新课
初步认识氧气和二氧化碳的性质
二
实验与探究
讲授新课
实验2:取一根小木条在空气中点燃,分别慢慢地放入盛有氧气和二氧化碳的集气瓶中,观察木条燃烧情况的变化。
实验现象 实验结论 性质类别
实验1
实验2
均为无色、
无味的气体
在标准情况下,氧气和二氧化碳均为无色、无味的气体
木条在氧气中
燃烧得更旺;
木条在二氧化
碳中熄灭
氧气能支持燃烧;二氧化碳一般不燃烧也不支持燃烧
讲授新课
实验记录
物理性质
化学性质
思考:
(1) 如何正确闻气味?
(2)如何鉴别O2和CO2两种气体?
扇闻法
燃着的木条
讲授新课
物质的性质、变化和用途间的关系
三
讲授新课
观察与思考
生活中,我们除了用水灭火之外,
还常用二氧化碳灭火器进行灭火,
这是根据二氧化碳不能燃烧也不能支
持燃烧的特性制作而成。那么在二氧化
碳灭火的过程中,物质发生了
什么变化?体现出了什么性质?二者
之间有怎样的区别和联系呢?与用途
之间呢?
讲授新课
性质
用途
决定
体现
变化
体现
决定
二氧化碳既不能燃烧也不能支持燃烧
可制作二氧化碳灭火器进行灭火
二氧化碳使燃着的木条熄灭
典例精析
例2 分析下列语句,指出其表现出的是物质的性质、变化还是用途?
(1)汽油可燃烧
(2)汽油在燃烧
(3)汽油易挥发
(4)汽油挥发了
(5)汽油可作汽车燃料
物质的性质
物质的性质
物质的变化
物质的变化
物质的用途
讲授新课
讲授新课
物质的变化 物质的性质
区别 物质运动的形式,是一个过程,是动
态的,其中包括物理变化和化学变化 物质本身固有的属性,是物质在满足一定条件下发生某种变化的可能性,是静态的
联系 物质的性质决定着变化,而变化又体现出性质。
归纳与小结
课堂小结
物质的用途
决定
体现
铜丝作导线
氢气作燃料
随堂训练
1.下列用途只要应用化学性质的是( )
A.生铁制成铁锅
B.金刚石作装饰品
C.铜丝作导线
D.用煤气烹饪
D
2.下列描述哪些是物理变化( )
哪些是化学变化( )
哪些是物理性质( )
哪些是化学性质( )
A.铜能生锈生成铜绿;
B.纯净的水是无色无味的液体;
C.以粮食为原料酿酒;
D.胆矾是一种蓝色固体;
E.木棒受力折断。
E
C
BD
A
随堂训练
3.铜是人类发现最早的金属之一,也是较好的纯金属之一。①呈紫红色光泽;②熔点为1 083.4 ℃;③沸点为2 567 ℃;④密度8.9 g/cm3;⑤具有很好的延展性;⑥导电、导热性较好,但含杂质时则导电性大受影响;⑦在干燥的空气里很稳定;⑧在潮湿的空气里表面可生成一层绿色物质,俗称铜绿;⑨高温时可被氧化,生成一层黑色氧化铜; ⑩铜溶于硝酸和热浓硫酸。阅读完这段话后,请回答下列问题:
铜的物理性质有:
铜的化学性质有:
①、②、③、④、⑤、⑥
⑦、⑧、⑨、⑩
第一单元 走进化学世界
导入新课
讲授新课
课堂小结
随堂训练
课题1 物质的变化和性质
第2课时 物质的性质
导入新课
观察与思考
日常生活中,常见一些人用医用酒精来降温,以达到退烧的目的,也经常用工业酒精炖小锅美食。这都是利用了酒精的特性。
思考:根据你的观察和生活经验,酒精有哪些性质?
导入新课
根据观察和生活经验,酒精具有以下性质:
颜色:
状态:
气味:
密度:
水溶性:
是否挥发:
点燃时在空气中
无色
液体
有特殊气味
0.8g/ml
能与水互溶
易挥发
能燃烧
讨论:以上性质可以怎样分类?
1.了解物理性质和化学性质的概念,并能识别。(重点)
2.能区分物质的物理变化与物理性质,化学变化与化学
性质。(难点)
3.明确物质用途所运用的性质,判断该性质属于物理性
质还是化学性质。
学习目标
导入新课
物理性质和化学性质的定义
一
讲授新课
合作探究
通过对酒精性质的了解,我们知道物质本身有许多固有的属性,哪些是通过化学变化表现出来的性质,哪些不是通过化学变化表现出来的本身就固有的性质呢?
物理性质
化学性质
归纳与小结
1.物质在化学变化中表现出来的性质叫做化学性质。
2.物质不需要发生化学变化就表现出来的性质叫做物理性质。
如:颜色、状态、气味、熔点、沸点、硬度、溶解性、挥发性、密度、导热性、导电性等。
如:可燃性、助燃性、毒性、氧化性、稳定性、腐蚀性、酸性、碱性等。
讲授新课
知识链接
⑴ 熔点和沸点
① 熔点:物质的熔化温度(固态变液体),如:固态的冰在0℃
时会熔化成液态的水,即冰的熔点为0℃。
② 沸点:液体沸腾时的温度(液态变气态),如:液态水加热
到100℃时会沸腾,即水的沸点为100℃。(沸点会
随着大气压的减小而降低)
101kPa的压强称为标准大气压,上述水的熔点和沸点是在标准大气压下测定的;若压强低于101kPa,则水的沸点低于100℃。
讲授新课
(2)密度
某种物质单位体积的质量,叫做这种物质的密度。
物质 密度
水 1.0g/cm3
铁 7.8g/cm3
铝 2.7g/cm3
氧气 1.429g/L
二氧化碳 1.977g/L
空气 1.293g/L
讲授新课
典例精析
例1 下列物质表现出的性质属于化学性质的是( )
A. 氧气为无色无味的气体 B.碳在常温下的性质稳定
C. 铁可以打成铁片 D.4℃时水的密度最大
解析:
A. 颜色、气味、状态属于物理性质;
B.稳定性指不易与其他物质发生化学反应,属于化学性质;
C.说明铁具有延展性,属于物理性质;
D.密度属于物理性质。
B
讲授新课
归纳与小结
讲授新课
物理性质
化学性质
区别
性质判断
性质内容
物质是否需通过化学变化表现出来的性质
直接(眼看、鼻闻、
耳听、手掂量等)
或由仪器间接观察
必须通过化学变化才
可判断。在叙述物质
的化学性质时,往往
有下列字:能、会、
可以、易、难等
颜色、状态、气味、
熔点、沸点、硬度、
密度、溶解度、挥发性、
导电性、导热性等
根据物质的化学变化
判断其化学性质,如
可燃性、稳定性(如
受热是否易分解)等
实验与探究
实验1:分别取一集气瓶氧气和一集气瓶二氧化碳气体,仔细观察它们的颜色和状态,闻一闻气味。
讲授新课
初步认识氧气和二氧化碳的性质
二
实验与探究
讲授新课
实验2:取一根小木条在空气中点燃,分别慢慢地放入盛有氧气和二氧化碳的集气瓶中,观察木条燃烧情况的变化。
实验现象 实验结论 性质类别
实验1
实验2
均为无色、
无味的气体
在标准情况下,氧气和二氧化碳均为无色、无味的气体
木条在氧气中
燃烧得更旺;
木条在二氧化
碳中熄灭
氧气能支持燃烧;二氧化碳一般不燃烧也不支持燃烧
讲授新课
实验记录
物理性质
化学性质
思考:
(1) 如何正确闻气味?
(2)如何鉴别O2和CO2两种气体?
扇闻法
燃着的木条
讲授新课
物质的性质、变化和用途间的关系
三
讲授新课
观察与思考
生活中,我们除了用水灭火之外,
还常用二氧化碳灭火器进行灭火,
这是根据二氧化碳不能燃烧也不能支
持燃烧的特性制作而成。那么在二氧化
碳灭火的过程中,物质发生了
什么变化?体现出了什么性质?二者
之间有怎样的区别和联系呢?与用途
之间呢?
讲授新课
性质
用途
决定
体现
变化
体现
决定
二氧化碳既不能燃烧也不能支持燃烧
可制作二氧化碳灭火器进行灭火
二氧化碳使燃着的木条熄灭
典例精析
例2 分析下列语句,指出其表现出的是物质的性质、变化还是用途?
(1)汽油可燃烧
(2)汽油在燃烧
(3)汽油易挥发
(4)汽油挥发了
(5)汽油可作汽车燃料
物质的性质
物质的性质
物质的变化
物质的变化
物质的用途
讲授新课
讲授新课
物质的变化 物质的性质
区别 物质运动的形式,是一个过程,是动
态的,其中包括物理变化和化学变化 物质本身固有的属性,是物质在满足一定条件下发生某种变化的可能性,是静态的
联系 物质的性质决定着变化,而变化又体现出性质。
归纳与小结
课堂小结
物质的用途
决定
体现
铜丝作导线
氢气作燃料
随堂训练
1.下列用途只要应用化学性质的是( )
A.生铁制成铁锅
B.金刚石作装饰品
C.铜丝作导线
D.用煤气烹饪
D
2.下列描述哪些是物理变化( )
哪些是化学变化( )
哪些是物理性质( )
哪些是化学性质( )
A.铜能生锈生成铜绿;
B.纯净的水是无色无味的液体;
C.以粮食为原料酿酒;
D.胆矾是一种蓝色固体;
E.木棒受力折断。
E
C
BD
A
随堂训练
3.铜是人类发现最早的金属之一,也是较好的纯金属之一。①呈紫红色光泽;②熔点为1 083.4 ℃;③沸点为2 567 ℃;④密度8.9 g/cm3;⑤具有很好的延展性;⑥导电、导热性较好,但含杂质时则导电性大受影响;⑦在干燥的空气里很稳定;⑧在潮湿的空气里表面可生成一层绿色物质,俗称铜绿;⑨高温时可被氧化,生成一层黑色氧化铜; ⑩铜溶于硝酸和热浓硫酸。阅读完这段话后,请回答下列问题:
铜的物理性质有:
铜的化学性质有:
①、②、③、④、⑤、⑥
⑦、⑧、⑨、⑩
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
