2022-2023学年人教版九年级化学上册 第六单元 碳和碳的氧化物 综合检测卷(word版 有答案)
文档属性
| 名称 | 2022-2023学年人教版九年级化学上册 第六单元 碳和碳的氧化物 综合检测卷(word版 有答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 879.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-09-01 00:00:00 | ||
图片预览


文档简介
第六单元综合检测卷
可能用到的相对原子质量:C-12 O-16 Ca-40
一、选择题:本大题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.低碳生活是一种绿色、健康、环保的生活方式。这里的“碳”指的是( )
A.碳元素 B.碳单质
C.二氧化碳 D.所有含碳化合物
2.下列物质经仔细打磨后,可成为钻石的是( )
A.焦炭 B.活性炭 C.石墨 D.金刚石
3.下列关于金刚石、石墨和C60的叙述中,正确的是( )
A.都有导电性 B.都属于纯净物
C.都有滑腻感 D.都是黑色固体
4.性质决定用途。下列有关“物质-性质-用途”的叙述中,不相符的是( )
选项 物质 性质 用途
A 二氧化碳 酸性 用于制碳酸饮料
B 金刚石 硬度大 用于裁玻璃
C 炭黑 稳定性 用于制墨汁
D 一氧化碳 还原性 用于冶炼金属
5.归纳与比较是学习化学常用的方法。下列关于CO2和CO的归纳与比较中,错误的是( )
A.构成:CO2分子和CO分子中碳、氧原子的个数比不同
B.性质:CO2不能燃烧,CO可以燃烧
C.用途:CO2可作气体肥料,CO可用于人工降雨
D.危害:CO2过多会增强温室效应,CO是空气污染物
6.下列有关实验室制取CO2的图示中,正确的是( )
7.下列有关碳和碳的氧化物的说法正确的是( )
A.金刚石和石墨物理性质不同的原因是构成它们的原子不同
B.CO2和CO化学性质不同的原因是它们的分子构成不同
C.碳在空气中燃烧生成CO,在氧气中燃烧生成CO2
D.CO2通入紫色石蕊溶液中,溶液变红,再加热,溶液变为无色
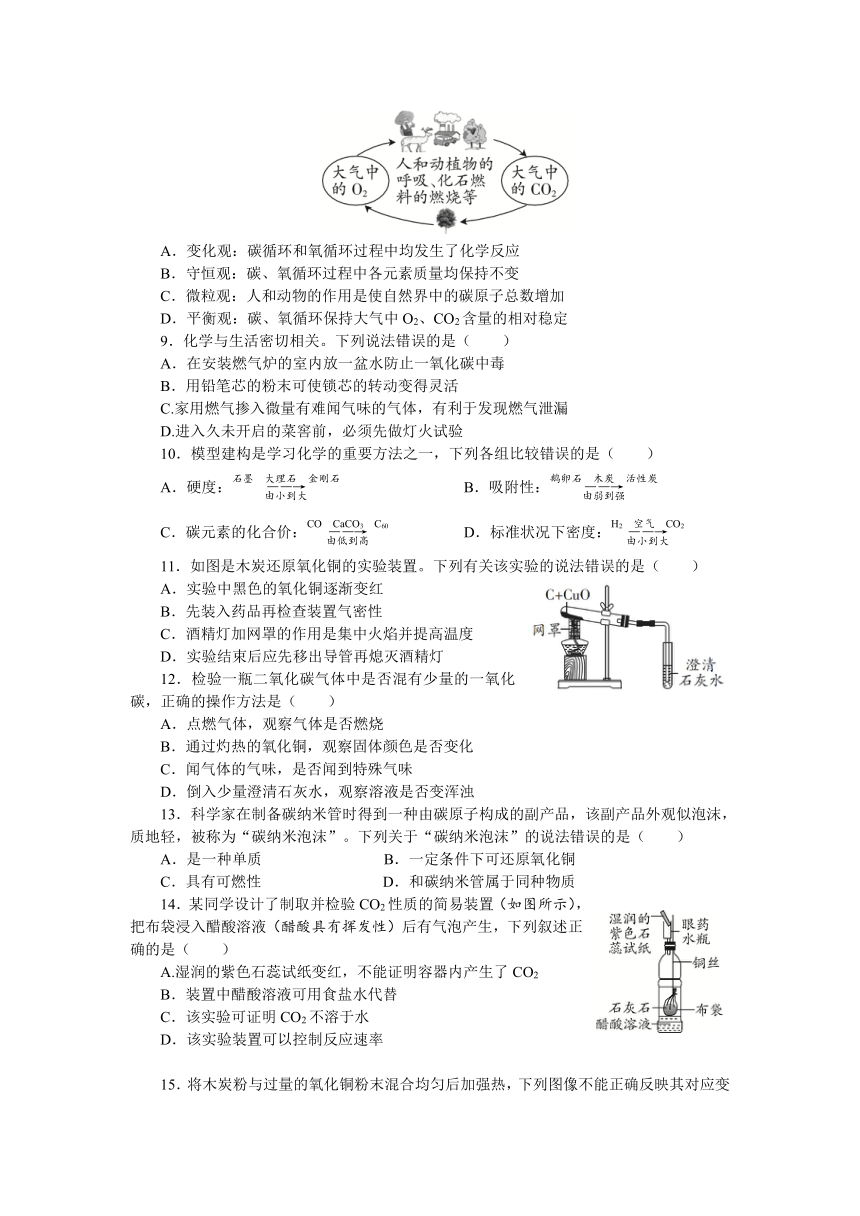
8.碳循环和氧循环是自然界中的重要循环。下列有关分析中,错误的是( )
A.变化观:碳循环和氧循环过程中均发生了化学反应
B.守恒观:碳、氧循环过程中各元素质量均保持不变
C.微粒观:人和动物的作用是使自然界中的碳原子总数增加
D.平衡观:碳、氧循环保持大气中O2、CO2含量的相对稳定
9.化学与生活密切相关。下列说法错误的是( )
A.在安装燃气炉的室内放一盆水防止一氧化碳中毒
B.用铅笔芯的粉末可使锁芯的转动变得灵活
C.家用燃气掺入微量有难闻气味的气体,有利于发现燃气泄漏
D.进入久未开启的菜窖前,必须先做灯火试验
10.模型建构是学习化学的重要方法之一,下列各组比较错误的是( )
A.硬度: B.吸附性:
C.碳元素的化合价: D.标准状况下密度:
11.如图是木炭还原氧化铜的实验装置。下列有关该实验的说法错误的是( )
A.实验中黑色的氧化铜逐渐变红
B.先装入药品再检查装置气密性
C.酒精灯加网罩的作用是集中火焰并提高温度
D.实验结束后应先移出导管再熄灭酒精灯
12.检验一瓶二氧化碳气体中是否混有少量的一氧化碳,正确的操作方法是( )
A.点燃气体,观察气体是否燃烧
B.通过灼热的氧化铜,观察固体颜色是否变化
C.闻气体的气味,是否闻到特殊气味
D.倒入少量澄清石灰水,观察溶液是否变浑浊
13.科学家在制备碳纳米管时得到一种由碳原子构成的副产品,该副产品外观似泡沫,质地轻,被称为“碳纳米泡沫”。下列关于“碳纳米泡沫”的说法错误的是( )
A.是一种单质 B.一定条件下可还原氧化铜
C.具有可燃性 D.和碳纳米管属于同种物质
14.某同学设计了制取并检验CO2性质的简易装置(如图所示),把布袋浸入醋酸溶液(醋酸具有挥发性)后有气泡产生,下列叙述正确的是( )
A.湿润的紫色石蕊试纸变红,不能证明容器内产生了CO2
B.装置中醋酸溶液可用食盐水代替
C.该实验可证明CO2不溶于水
D.该实验装置可以控制反应速率
15.将木炭粉与过量的氧化铜粉末混合均匀后加强热,下列图像不能正确反映其对应变化关系的是( )
二、非选择题:本大题共6小题,第16小题7分,第17小题8分,第18~21小题各10分,共55分。
16.CO2对人类的生活有着重大影响,CO2的捕集与资源化利用是当今化学研究的一项热点。
(1)一种捕集CO2的方法是将其封入蓄水层中,封入时CO2会部分与水发生反应,化学方程式为___________________________________________________。
(2)CO2可用于食品保鲜,智能化食品包装通过颜色变化显示包装内CO2气体含量的变化,举出一种可用于该智能化包装的物质:________________。
(3)据悉,2022年北京冬奥会国家速滑馆“冰丝带”采用当前最先进的CO2跨临界直冷制冰技术,可实现CO2循环利用和碳排放趋近于零。固态CO2能制冷的原因是____________________________________;CO2气体制成干冰时,从微观角度看,发生改变的是________________。
(4)2021年9月24日,《科学》在线发表了我国科研人员在国际上首次实现了CO2到淀粉的从头合成。
①在自然界中绿色植物可以通过____________将CO2转化为淀粉。
②实验分析表明人工合成的淀粉与天然淀粉非常接近,该项研究成果的实际应用价值有________(填序号)。
降低空气中CO2的含量 B.缓解人类粮食短缺问题
C.节约耕地资源
17.如图是碳的几种单质的结构示意图,图中小圆圈均代表碳原子。
甲 乙 丙
(1)碳原子的结构示意图为,其最外层电子数是___________。
(2)甲、乙、丙三种物质物理性质有较大差异的原因是________________________,物质甲的名称是__________,物质丙是由________(填“分子”或“原子”)构成的。
(3)一定条件下,物质乙可转变为物质甲,该过程中发生了________(填“物理”或“化学”)变化。
(4)物质乙制成的坩埚被广泛用于金属的冶炼和熔炼,说明其具有的性质是__________________(写一条)。坩埚外表层常覆盖特制的釉层和致密的成型材料,其目的是________________________________________。
18.实验室部分仪器和装置如下,请回答下列问题:
已知:浓硫酸具有强吸水性。
(1)图中标号B的仪器名称为____________。
(2)用大理石与稀盐酸制取二氧化碳,并要求获得平稳气流,发生和收集装置需要用到的仪器有________(填序号,从图中A~I选择),反应的化学方程式为_________________。
(3)实验室制取的二氧化碳中常含有水蒸气,为获得干燥的二氧化碳气体,可选用装置J进行干燥,则气体应从______(填“a”或“b”)端通入。若用装置K收集二氧化碳,请将K中的导管补画完整。
(4)查阅资料得知:实验室用加热氯化铵和氢氧化钙的固体混合物的方法制取氨气,氨气是一种密度小于空气且极易溶于水的气体。图中组装制取氨气的发生装置还缺少的仪器是________;收集氨气应采用______________法。
19.实验是进行科学探究的重要方式。同学们设计如下实验探究二氧化碳的性质,请你参与探究并填空。
【实验记录与分析】
实验一 实验二 实验三
实验操作
实验现象 蜡烛__________ ______________ 乙中澄清石灰水变浑浊,软塑料瓶变瘪程度较大的是______(填“甲”或“乙”) 干石蕊纸花__________,湿石蕊纸花________
实验结论 ①__________________________; ②二氧化碳不燃烧,也不支持燃烧 二氧化碳能与氢氧化钙发生反应 二氧化碳能与水反应
【反思与拓展】
(1)根据实验一,写出二氧化碳的一条用途:________。
(2)由实验二的结论分析得出:实验室中保存氢氧化钙溶液要注意____________。写出二氧化碳与氢氧化钙反应的化学方程式:______________________________________。
(3)在设计上述三组实验时,都只改变一个影响因素,保持其他因素不变,这是运用了科学探究中__________的方法。
20.如图是二氧化碳的知识网络图,其中“→”表示某种物质经一步反应可以转化为另一种物质(反应条件已略去),请回答问题:
(1)完善该网络图:物质a的化学式是______,其常见用途为_____________(写一条)。
(2)转化②的基本反应类型是________反应。
(3)写出转化⑤的化学方程式:________________________。
(4)写出符合转化⑦且是分解反应的化学方程式:______________________,该反应不适用于实验室制取CO2的原因是____________________________。
(5)小明认为存在O2CO2的相互转化关系,你认为此观点________(填“正确”或“错误”)。
21.阅读材料,回答问题。
“碳中和”指通过各种捕捉技术使排放到大气中的CO2气体净增量为零。目前,CO2捕捉技术主要分为物理吸收法和化学吸收法。物理吸收法可用活性炭、沸石等吸收CO2。化学吸收剂主要有氨水吸收剂(主要成分为NH3·H2O)、钙基吸收剂(主要成分为CaO)等。
(1)活性炭、沸石等能够吸收CO2,是因为它们具有____________的结构。
(2)采用氨水吸收CO2时,温度不宜太高的原因是________________________。
(3)钙基吸收CO2时发生反应的化学方程式为CaO+CO2CaCO3。请计算用
11.2 g CaO可以吸收CO2的质量。
(4)下列措施不利于实现“碳中和”目标的是______(填序号)。
a.电脑长时间待机 b.推广新能源汽车
c.鼓励乘坐公交出行 d.多植树造林
参考答案
一、选择题:本大题共15小题,每小题3分,共45分。
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案 C D B A C D B C A C B B D A B
二、非选择题:本大题共6小题,共55分。
16.(7分)(1)CO2+H2O=== H2CO3(2分) (2)紫色石蕊溶液(1分)
(3)固态CO2升华吸热,使环境温度降低(1分) 分子间的间隔(1分)
(4)①光合作用(1分) ②ABC(1分)
17.(8分)(1)4(1分)
(2)碳原子的排列方式不同(1分) 金刚石(1分) 分子(1分)
(3)化学(1分)
(4)熔点高(或导热性好)(1分) 防止加热时石墨与空气中的氧气反应(2分)
18.(10分)(1)长颈漏斗(1分) (2)ADEG(2分)
CaCO3+2HCl=== CaCl2+H2O+CO2↑(2分)
(3)a(1分) 如图(2分)
(4)试管(1分) 向下排空气(1分)
19.(10分)【实验记录与分析】自下而上依次熄灭(1分) 乙(1分)
不变色(1分) 变红(1分) 二氧化碳的密度比空气大(1分)
【反思与拓展】(1)灭火(1分)
(2)密封保存(1分) CO2+Ca(OH)2=== CaCO3↓+H2O(2分)
(3)控制变量(1分)
20.(10分)(1)CO(1分) 冶炼金属等(1分) (2)化合(1分)
(3)CO2+C 2CO(2分)
(4)CaCO3 CaO+CO2↑(2分) 反应条件是高温,耗能大(2分)
(5)正确(1分)
21.(10分)(1)疏松多孔(1分)
(2)防止氨水挥发影响吸收(2分)
(3)解:设用11.2 g CaO可以吸收CO2的质量为x。(1分)
CaO + CO2 CaCO3
56 44
11.2 g x(1分)
=(1分),x=8.8 g(1分)
答:用11.2 g CaO可以吸收CO2的质量为8.8 g。(1分)
(4)a(2分)
可能用到的相对原子质量:C-12 O-16 Ca-40
一、选择题:本大题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1.低碳生活是一种绿色、健康、环保的生活方式。这里的“碳”指的是( )
A.碳元素 B.碳单质
C.二氧化碳 D.所有含碳化合物
2.下列物质经仔细打磨后,可成为钻石的是( )
A.焦炭 B.活性炭 C.石墨 D.金刚石
3.下列关于金刚石、石墨和C60的叙述中,正确的是( )
A.都有导电性 B.都属于纯净物
C.都有滑腻感 D.都是黑色固体
4.性质决定用途。下列有关“物质-性质-用途”的叙述中,不相符的是( )
选项 物质 性质 用途
A 二氧化碳 酸性 用于制碳酸饮料
B 金刚石 硬度大 用于裁玻璃
C 炭黑 稳定性 用于制墨汁
D 一氧化碳 还原性 用于冶炼金属
5.归纳与比较是学习化学常用的方法。下列关于CO2和CO的归纳与比较中,错误的是( )
A.构成:CO2分子和CO分子中碳、氧原子的个数比不同
B.性质:CO2不能燃烧,CO可以燃烧
C.用途:CO2可作气体肥料,CO可用于人工降雨
D.危害:CO2过多会增强温室效应,CO是空气污染物
6.下列有关实验室制取CO2的图示中,正确的是( )
7.下列有关碳和碳的氧化物的说法正确的是( )
A.金刚石和石墨物理性质不同的原因是构成它们的原子不同
B.CO2和CO化学性质不同的原因是它们的分子构成不同
C.碳在空气中燃烧生成CO,在氧气中燃烧生成CO2
D.CO2通入紫色石蕊溶液中,溶液变红,再加热,溶液变为无色
8.碳循环和氧循环是自然界中的重要循环。下列有关分析中,错误的是( )
A.变化观:碳循环和氧循环过程中均发生了化学反应
B.守恒观:碳、氧循环过程中各元素质量均保持不变
C.微粒观:人和动物的作用是使自然界中的碳原子总数增加
D.平衡观:碳、氧循环保持大气中O2、CO2含量的相对稳定
9.化学与生活密切相关。下列说法错误的是( )
A.在安装燃气炉的室内放一盆水防止一氧化碳中毒
B.用铅笔芯的粉末可使锁芯的转动变得灵活
C.家用燃气掺入微量有难闻气味的气体,有利于发现燃气泄漏
D.进入久未开启的菜窖前,必须先做灯火试验
10.模型建构是学习化学的重要方法之一,下列各组比较错误的是( )
A.硬度: B.吸附性:
C.碳元素的化合价: D.标准状况下密度:
11.如图是木炭还原氧化铜的实验装置。下列有关该实验的说法错误的是( )
A.实验中黑色的氧化铜逐渐变红
B.先装入药品再检查装置气密性
C.酒精灯加网罩的作用是集中火焰并提高温度
D.实验结束后应先移出导管再熄灭酒精灯
12.检验一瓶二氧化碳气体中是否混有少量的一氧化碳,正确的操作方法是( )
A.点燃气体,观察气体是否燃烧
B.通过灼热的氧化铜,观察固体颜色是否变化
C.闻气体的气味,是否闻到特殊气味
D.倒入少量澄清石灰水,观察溶液是否变浑浊
13.科学家在制备碳纳米管时得到一种由碳原子构成的副产品,该副产品外观似泡沫,质地轻,被称为“碳纳米泡沫”。下列关于“碳纳米泡沫”的说法错误的是( )
A.是一种单质 B.一定条件下可还原氧化铜
C.具有可燃性 D.和碳纳米管属于同种物质
14.某同学设计了制取并检验CO2性质的简易装置(如图所示),把布袋浸入醋酸溶液(醋酸具有挥发性)后有气泡产生,下列叙述正确的是( )
A.湿润的紫色石蕊试纸变红,不能证明容器内产生了CO2
B.装置中醋酸溶液可用食盐水代替
C.该实验可证明CO2不溶于水
D.该实验装置可以控制反应速率
15.将木炭粉与过量的氧化铜粉末混合均匀后加强热,下列图像不能正确反映其对应变化关系的是( )
二、非选择题:本大题共6小题,第16小题7分,第17小题8分,第18~21小题各10分,共55分。
16.CO2对人类的生活有着重大影响,CO2的捕集与资源化利用是当今化学研究的一项热点。
(1)一种捕集CO2的方法是将其封入蓄水层中,封入时CO2会部分与水发生反应,化学方程式为___________________________________________________。
(2)CO2可用于食品保鲜,智能化食品包装通过颜色变化显示包装内CO2气体含量的变化,举出一种可用于该智能化包装的物质:________________。
(3)据悉,2022年北京冬奥会国家速滑馆“冰丝带”采用当前最先进的CO2跨临界直冷制冰技术,可实现CO2循环利用和碳排放趋近于零。固态CO2能制冷的原因是____________________________________;CO2气体制成干冰时,从微观角度看,发生改变的是________________。
(4)2021年9月24日,《科学》在线发表了我国科研人员在国际上首次实现了CO2到淀粉的从头合成。
①在自然界中绿色植物可以通过____________将CO2转化为淀粉。
②实验分析表明人工合成的淀粉与天然淀粉非常接近,该项研究成果的实际应用价值有________(填序号)。
降低空气中CO2的含量 B.缓解人类粮食短缺问题
C.节约耕地资源
17.如图是碳的几种单质的结构示意图,图中小圆圈均代表碳原子。
甲 乙 丙
(1)碳原子的结构示意图为,其最外层电子数是___________。
(2)甲、乙、丙三种物质物理性质有较大差异的原因是________________________,物质甲的名称是__________,物质丙是由________(填“分子”或“原子”)构成的。
(3)一定条件下,物质乙可转变为物质甲,该过程中发生了________(填“物理”或“化学”)变化。
(4)物质乙制成的坩埚被广泛用于金属的冶炼和熔炼,说明其具有的性质是__________________(写一条)。坩埚外表层常覆盖特制的釉层和致密的成型材料,其目的是________________________________________。
18.实验室部分仪器和装置如下,请回答下列问题:
已知:浓硫酸具有强吸水性。
(1)图中标号B的仪器名称为____________。
(2)用大理石与稀盐酸制取二氧化碳,并要求获得平稳气流,发生和收集装置需要用到的仪器有________(填序号,从图中A~I选择),反应的化学方程式为_________________。
(3)实验室制取的二氧化碳中常含有水蒸气,为获得干燥的二氧化碳气体,可选用装置J进行干燥,则气体应从______(填“a”或“b”)端通入。若用装置K收集二氧化碳,请将K中的导管补画完整。
(4)查阅资料得知:实验室用加热氯化铵和氢氧化钙的固体混合物的方法制取氨气,氨气是一种密度小于空气且极易溶于水的气体。图中组装制取氨气的发生装置还缺少的仪器是________;收集氨气应采用______________法。
19.实验是进行科学探究的重要方式。同学们设计如下实验探究二氧化碳的性质,请你参与探究并填空。
【实验记录与分析】
实验一 实验二 实验三
实验操作
实验现象 蜡烛__________ ______________ 乙中澄清石灰水变浑浊,软塑料瓶变瘪程度较大的是______(填“甲”或“乙”) 干石蕊纸花__________,湿石蕊纸花________
实验结论 ①__________________________; ②二氧化碳不燃烧,也不支持燃烧 二氧化碳能与氢氧化钙发生反应 二氧化碳能与水反应
【反思与拓展】
(1)根据实验一,写出二氧化碳的一条用途:________。
(2)由实验二的结论分析得出:实验室中保存氢氧化钙溶液要注意____________。写出二氧化碳与氢氧化钙反应的化学方程式:______________________________________。
(3)在设计上述三组实验时,都只改变一个影响因素,保持其他因素不变,这是运用了科学探究中__________的方法。
20.如图是二氧化碳的知识网络图,其中“→”表示某种物质经一步反应可以转化为另一种物质(反应条件已略去),请回答问题:
(1)完善该网络图:物质a的化学式是______,其常见用途为_____________(写一条)。
(2)转化②的基本反应类型是________反应。
(3)写出转化⑤的化学方程式:________________________。
(4)写出符合转化⑦且是分解反应的化学方程式:______________________,该反应不适用于实验室制取CO2的原因是____________________________。
(5)小明认为存在O2CO2的相互转化关系,你认为此观点________(填“正确”或“错误”)。
21.阅读材料,回答问题。
“碳中和”指通过各种捕捉技术使排放到大气中的CO2气体净增量为零。目前,CO2捕捉技术主要分为物理吸收法和化学吸收法。物理吸收法可用活性炭、沸石等吸收CO2。化学吸收剂主要有氨水吸收剂(主要成分为NH3·H2O)、钙基吸收剂(主要成分为CaO)等。
(1)活性炭、沸石等能够吸收CO2,是因为它们具有____________的结构。
(2)采用氨水吸收CO2时,温度不宜太高的原因是________________________。
(3)钙基吸收CO2时发生反应的化学方程式为CaO+CO2CaCO3。请计算用
11.2 g CaO可以吸收CO2的质量。
(4)下列措施不利于实现“碳中和”目标的是______(填序号)。
a.电脑长时间待机 b.推广新能源汽车
c.鼓励乘坐公交出行 d.多植树造林
参考答案
一、选择题:本大题共15小题,每小题3分,共45分。
题号 1 2 3 4 5 6 7 8 9 10 11 12 13 14 15
答案 C D B A C D B C A C B B D A B
二、非选择题:本大题共6小题,共55分。
16.(7分)(1)CO2+H2O=== H2CO3(2分) (2)紫色石蕊溶液(1分)
(3)固态CO2升华吸热,使环境温度降低(1分) 分子间的间隔(1分)
(4)①光合作用(1分) ②ABC(1分)
17.(8分)(1)4(1分)
(2)碳原子的排列方式不同(1分) 金刚石(1分) 分子(1分)
(3)化学(1分)
(4)熔点高(或导热性好)(1分) 防止加热时石墨与空气中的氧气反应(2分)
18.(10分)(1)长颈漏斗(1分) (2)ADEG(2分)
CaCO3+2HCl=== CaCl2+H2O+CO2↑(2分)
(3)a(1分) 如图(2分)
(4)试管(1分) 向下排空气(1分)
19.(10分)【实验记录与分析】自下而上依次熄灭(1分) 乙(1分)
不变色(1分) 变红(1分) 二氧化碳的密度比空气大(1分)
【反思与拓展】(1)灭火(1分)
(2)密封保存(1分) CO2+Ca(OH)2=== CaCO3↓+H2O(2分)
(3)控制变量(1分)
20.(10分)(1)CO(1分) 冶炼金属等(1分) (2)化合(1分)
(3)CO2+C 2CO(2分)
(4)CaCO3 CaO+CO2↑(2分) 反应条件是高温,耗能大(2分)
(5)正确(1分)
21.(10分)(1)疏松多孔(1分)
(2)防止氨水挥发影响吸收(2分)
(3)解:设用11.2 g CaO可以吸收CO2的质量为x。(1分)
CaO + CO2 CaCO3
56 44
11.2 g x(1分)
=(1分),x=8.8 g(1分)
答:用11.2 g CaO可以吸收CO2的质量为8.8 g。(1分)
(4)a(2分)
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
