第六单元碳和碳的氧化物同步巩固测试 九年级化学人教版上册(word版 有答案)
文档属性
| 名称 | 第六单元碳和碳的氧化物同步巩固测试 九年级化学人教版上册(word版 有答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 403.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-09-02 00:00:00 | ||
图片预览


文档简介
第六单元 碳和碳的氧化物 同步巩固测试
一、单选题
1.为测定石灰石与稀盐酸产生的CO2的体积,某学生拟用如图实验装置,对于该实验,下列说法错误的是
A.若量气管中液体为水,会使测定结果偏小
B.为使测量较准确,读数前应上下移动水准管,使水准管内液面与量气管中液面相平
C.所加稀盐酸的体积对测定结果无影响
D.实验测得CO2的体积偏小可能是因为左侧Y型管中有二氧化碳残留
2.“碳达峰、碳中和”是我国重要的生态战略目标,下列做法不利于实现该目标的是
A.分类回收垃圾 B.推广使用清洁能源
C.焚烧口罩等医用品 D.积极植树造林
3.下列4个实验方案的设计中,不正确的是
A.用二氧化锰区分水和过氧化氢溶液
B.用水除去CO和CO2混合气体中的CO2
C.用燃着的木条鉴别氧气、空气和二氧化碳3瓶气体
D.用闻气味的方法区分食醋与酒精
4.下列有关碳和碳的氧化物的说法,错误的是
A.金刚石和石墨都是由原子构成的物质
B.一氧化碳可用做气体燃料,二氧化碳可用于灭火
C.一氧化碳和二氧化碳组成元素相同,所以它们的化学性质也相同
D.古代用墨书写的字画长久不变色,是因为常温下碳的化学性质不活泼
5.下列关于二氧化碳、一氧化碳的比较错误的是
A.组成:均由碳元素和氧元素组成
B.性质:CO2、CO都可以与NaOH溶液反应
C.用途:干冰可用于人工降雨;一氧化碳气体可作燃料
D.危害:二氧化碳会导致“温室效应”;一氧化碳会引起中毒
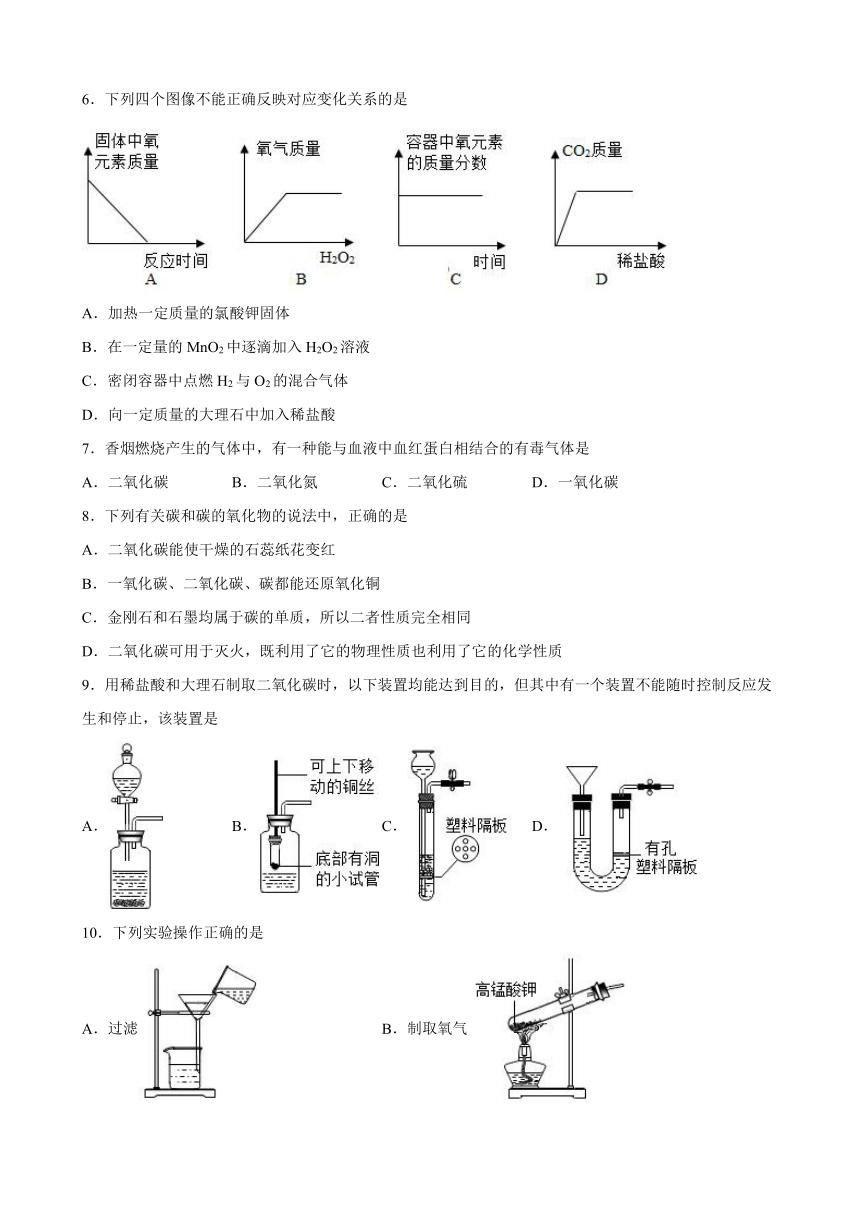
6.下列四个图像不能正确反映对应变化关系的是
A.加热一定质量的氯酸钾固体
B.在一定量的MnO2中逐滴加入H2O2溶液
C.密闭容器中点燃H2与O2的混合气体
D.向一定质量的大理石中加入稀盐酸
7.香烟燃烧产生的气体中,有一种能与血液中血红蛋白相结合的有毒气体是
A.二氧化碳 B.二氧化氮 C.二氧化硫 D.一氧化碳
8.下列有关碳和碳的氧化物的说法中,正确的是
A.二氧化碳能使干燥的石蕊纸花变红
B.一氧化碳、二氧化碳、碳都能还原氧化铜
C.金刚石和石墨均属于碳的单质,所以二者性质完全相同
D.二氧化碳可用于灭火,既利用了它的物理性质也利用了它的化学性质
9.用稀盐酸和大理石制取二氧化碳时,以下装置均能达到目的,但其中有一个装置不能随时控制反应发生和停止,该装置是
A. B. C. D.
10.下列实验操作正确的是
A.过滤 B.制取氧气
C.验满气体 D.移走蒸发皿
11.关于碳的单质的说法,错误的是
A.碳纳米管 石墨烯是新形态的碳单质 B.金刚石 石墨 C60 都直接由碳原子构成
C.木炭 活性炭都具有吸附能力 D.碳单质的性质的不同是因为原子的排列方式不同
12.如图所示的装置有很多用途,下列使用方法不正确的是
A.排水法收集氧气时,由a口进气
B.装置中装入适量石灰水并且检验二氧化碳,由a口进气
C.排水法收集氢气时,由b口进气
D.排空气法收集二氧化碳时,由a口进气
13.关于C、CO、CO2三种物质,有下列说法:①三种物质都含有碳元素,都具有还原性;②CO、CO2都是没有颜色、没有气味的气体;③CO2可用于光合作用,CO可用于人工降雨;④CO2能产生温室效应,CO易于血液中的血红蛋白结合引起中毒;⑤CO2可用来做肥料,CO可用作燃料。上述说法中正确的是
A.①②③ B.②④⑤ C.②③④ D.①③⑤
14.下列有关二氧化碳的说法错误的是
A.二氧化碳是一种有毒气体 B.二氧化碳能使澄清石灰水变浑浊
C.液态二氧化碳可用于灭火 D.干冰可用于人工降雨
二、填空题
15.化学是一门研究物质的科学,我们一般从物质的组成(或构成)、性质、用途等方面研究一种物质。以二氧化碳为例,请回答相关问题。
(1)从微观上看,二氧化碳由______构成。
(2)①如图1所示实验中,a、d为用紫色石蕊溶液润湿的棉球,b、c为用石蕊溶液染成紫色的干燥棉球。缓慢通入CO2一段时间后观察到:d比a先变红,b、c不变红,此现象说明CO2具有的物理性质是______,化学性质是______。
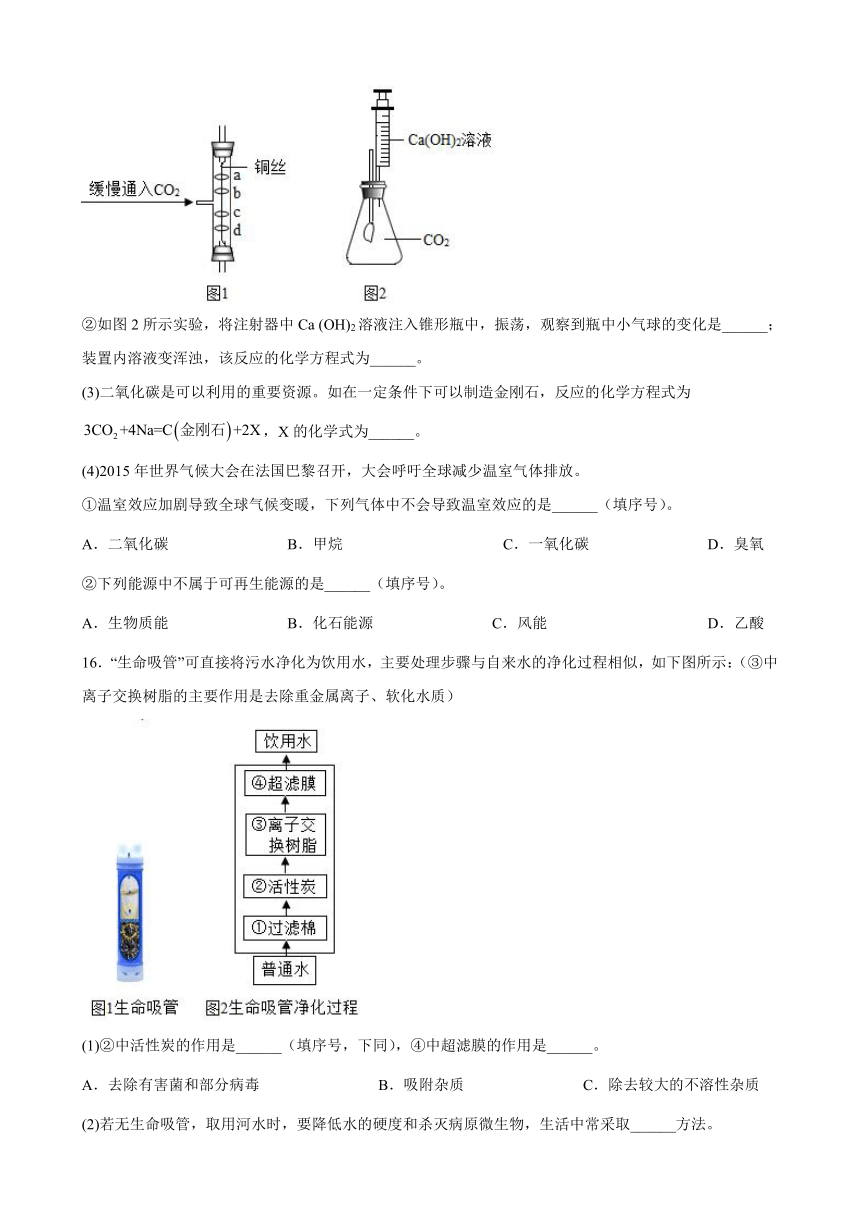
②如图2所示实验,将注射器中Ca (OH)2溶液注入锥形瓶中,振荡,观察到瓶中小气球的变化是______;装置内溶液变浑浊,该反应的化学方程式为______。
(3)二氧化碳是可以利用的重要资源。如在一定条件下可以制造金刚石,反应的化学方程式为,X的化学式为______。
(4)2015年世界气候大会在法国巴黎召开,大会呼吁全球减少温室气体排放。
①温室效应加剧导致全球气候变暖,下列气体中不会导致温室效应的是______(填序号)。
A.二氧化碳 B.甲烷 C.一氧化碳 D.臭氧
②下列能源中不属于可再生能源的是______(填序号)。
A.生物质能 B.化石能源 C.风能 D.乙酸
16.“生命吸管”可直接将污水净化为饮用水,主要处理步骤与自来水的净化过程相似,如下图所示:(③中离子交换树脂的主要作用是去除重金属离子、软化水质)
(1)②中活性炭的作用是______(填序号,下同),④中超滤膜的作用是______。
A.去除有害菌和部分病毒 B.吸附杂质 C.除去较大的不溶性杂质
(2)若无生命吸管,取用河水时,要降低水的硬度和杀灭病原微生物,生活中常采取______方法。
(3)经过生命吸管净化后的水是否是软水,你认为可以用______来检验。
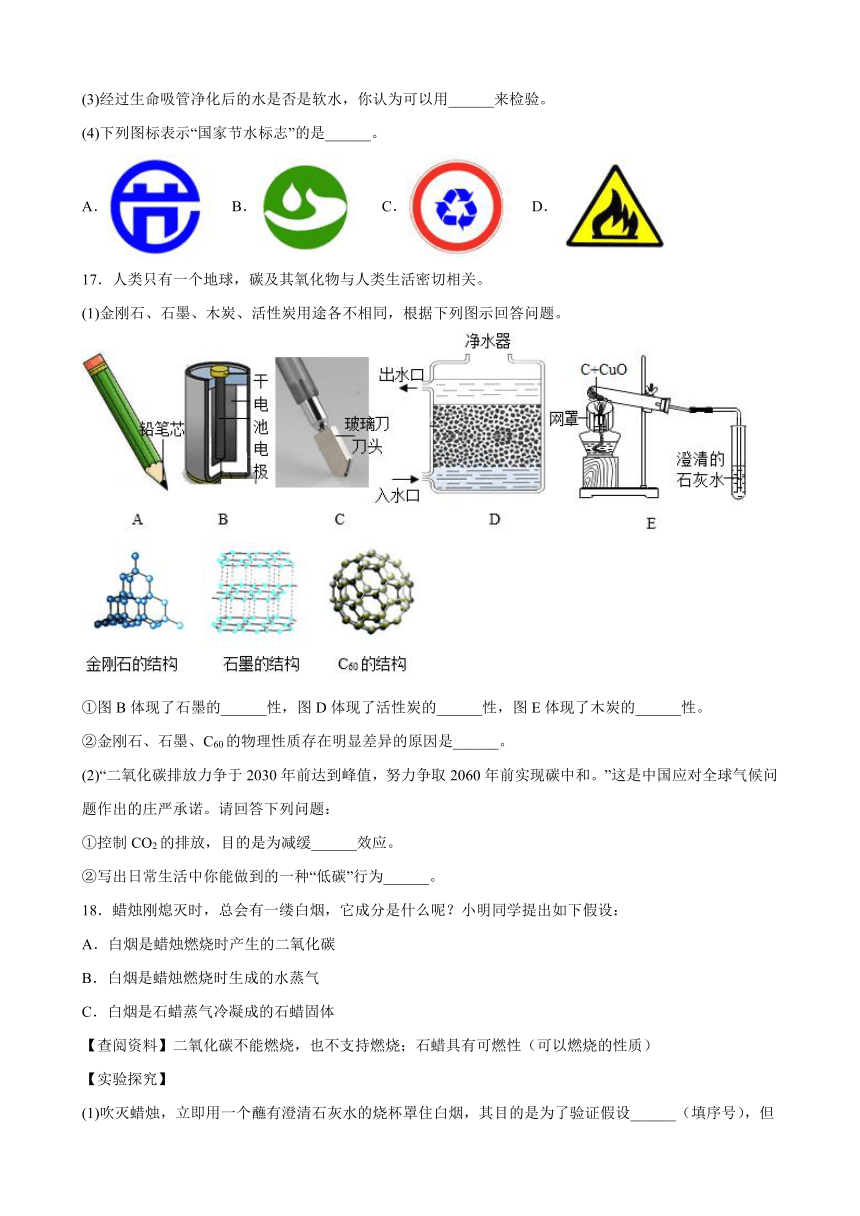
(4)下列图标表示“国家节水标志”的是______。
A. B. C. D.
17.人类只有一个地球,碳及其氧化物与人类生活密切相关。
(1)金刚石、石墨、木炭、活性炭用途各不相同,根据下列图示回答问题。
①图B体现了石墨的______性,图D体现了活性炭的______性,图E体现了木炭的______性。
②金刚石、石墨、C60的物理性质存在明显差异的原因是______。
(2)“二氧化碳排放力争于2030年前达到峰值,努力争取2060年前实现碳中和。”这是中国应对全球气候问题作出的庄严承诺。请回答下列问题:
①控制CO2的排放,目的是为减缓______效应。
②写出日常生活中你能做到的一种“低碳”行为______。
18.蜡烛刚熄灭时,总会有一缕白烟,它成分是什么呢?小明同学提出如下假设:
A.白烟是蜡烛燃烧时产生的二氧化碳
B.白烟是蜡烛燃烧时生成的水蒸气
C.白烟是石蜡蒸气冷凝成的石蜡固体
【查阅资料】二氧化碳不能燃烧,也不支持燃烧;石蜡具有可燃性(可以燃烧的性质)
【实验探究】
(1)吹灭蜡烛,立即用一个蘸有澄清石灰水的烧杯罩住白烟,其目的是为了验证假设______(填序号),但这样做并不能得出正确的结论,原因是______。
(2)吹灭蜡烛,立即用一块干而冷的玻璃片放在白烟上,玻璃片没有水雾,说明白烟不是______。
(3)吹灭蜡烛,立即用燃着的木条去点燃白烟,发现蜡烛重新被点燃,说明白烟具有______性,这为假设______提供了证据,因为______。
19.二氧化碳在大气循环中起着重要作用,如图1是产生二氧化碳的途径,其中甲是一种黑色固体单质,乙是天然气的主要成分,丙是一种大气污染物,请回答下列问题:
(1)丙的化学式为______。
(2)实验室CaCO3→CO2的化学反应方程式为______。
(3)列举甲的一种用途是______。的反应属于______反应(填“放热”或“吸热”)。
(4)大气中的二氧化碳过多会引发的环境问题是______。
(5)某同学设计了如图2简易CO2捕捉器流程图,图中固体和液体分离的操作方法是______;请用化学方程式表示捕捉CO2的原理______;流程中可循环利用的物质为______(填化学式)。
三、实验题
20.请结合下图回答问题:
(1)写出有标号仪器的名称:①___________,②___________。
(2)用氯酸钾和二氧化锰制取O2,选用发生装置是___________(填字母),该反应化学方程式是___________;若要收集相对纯度较高的O2可用___________(填字母)装置收集。
(3)实验室制取CO2若用F装置代替B装置进行实验,其优点为___________,要获得纯净、干燥的CO2,除杂装置(如图)的导管按气流方向连接顺序是___________(选填字母)。
A.a→b→d→c B.d→c→a→b
C.b→a→c→d D.c→d→b→a
21.实验室现有石灰石、氯酸钾、二氧化锰、稀硫酸、稀盐酸等药品及相关仪器和用品,请结合下列装置回答问题:
(1)仪器 a 的名称是__________ 。
(2)选用上述药品和 B、E 装置制取 O2,气体收集完毕时,应先 _________(填“从水中移出导管”或“熄灭酒精灯”)。
(3)选用上述仪器和药品制取二氧化碳,发生反应的化学方程式是__________。
(4)为了得到纯净、干燥的 CO2,除杂装置〔如图 2)的导管口按气流方向连接顺序是__________(填序号)。
①1→2→4→3 ②2→1→3→4 ③4→3→1→2 ④3→4→2→1
四、计算题
22.长久使用的热水壶底部有一层水垢,主要成分是碳酸钙(CaCO3),某化学兴趣小组为了测定水垢中碳酸钙的质量分数,取25g水垢放入过量的稀盐酸的烧杯中,立即将烧杯放在天平上,称其质量。在以后的5min内,每一分钟读一次数。结果如下表,试回答下列问题:
时间/min 1 2 3 4 5
质量/g 100g 95g 92g 91.2g 91.2g
(1)反应生成的二氧化碳的质量为多少?______
(2)该水垢中CaCO3的质量分数为多少?______
23.为测定实验室废弃氧化铜样品中氧化铜的质量分数,兴趣小组同学取5g样品在右图装置进行实验(样品中其它杂质不反应),充分反应后测得B质量增加2.2g。回答下列问题:
(1)氧化铜样品中氧化铜的质量分数是多少?(写出计算过程)
(2)小华同学认为测定反应前后A中固体的质量变化也可以测出样品中氧化铜的质量分数,则小华测得充分反应后A中固体的质量应是_________。
参考答案:
1.D
2.C
3.B
4.C
5.B
6.B
7.D
8.D
9.A
10.C
11.B
12.A
13.B
14.A
15.(1)二氧化碳分子
(2) 密度比空气大 能与水反应生成酸 小气球逐渐胀大
(3)Na2CO3
(4) C B
16.(1) B A
(2)煮沸
(3)肥皂水
(4)B
17.(1) 导电 吸附 还原 碳原子的排列方式不同
(2) 温室 使用自行车或公共交通出行,节约用电等
18.(1) A 蜡烛燃烧产生的二氧化碳会使澄清石灰水变浑浊
(2)水蒸气
(3) 可燃 C 只有石蜡具有可燃性
19.(1)CO
(2)
(3) 燃料(合理即可) 吸热
(4)温室效应
(5) 过滤 CaO
20.(1) 长颈漏斗 集气瓶
(2) A D
(3) 可控制反应的发生或停止 B
21.(1)试管
(2)从水中移出导管
(3)
(4)③
22.(1)8.8g
(2)80%
23.(1)设样品中CuO的质量为x。
x=4g
样品中氧化铜的质量分数=×100%=80%。
答:样品中氧化铜的质量分数是80%
(2)4.2g
一、单选题
1.为测定石灰石与稀盐酸产生的CO2的体积,某学生拟用如图实验装置,对于该实验,下列说法错误的是
A.若量气管中液体为水,会使测定结果偏小
B.为使测量较准确,读数前应上下移动水准管,使水准管内液面与量气管中液面相平
C.所加稀盐酸的体积对测定结果无影响
D.实验测得CO2的体积偏小可能是因为左侧Y型管中有二氧化碳残留
2.“碳达峰、碳中和”是我国重要的生态战略目标,下列做法不利于实现该目标的是
A.分类回收垃圾 B.推广使用清洁能源
C.焚烧口罩等医用品 D.积极植树造林
3.下列4个实验方案的设计中,不正确的是
A.用二氧化锰区分水和过氧化氢溶液
B.用水除去CO和CO2混合气体中的CO2
C.用燃着的木条鉴别氧气、空气和二氧化碳3瓶气体
D.用闻气味的方法区分食醋与酒精
4.下列有关碳和碳的氧化物的说法,错误的是
A.金刚石和石墨都是由原子构成的物质
B.一氧化碳可用做气体燃料,二氧化碳可用于灭火
C.一氧化碳和二氧化碳组成元素相同,所以它们的化学性质也相同
D.古代用墨书写的字画长久不变色,是因为常温下碳的化学性质不活泼
5.下列关于二氧化碳、一氧化碳的比较错误的是
A.组成:均由碳元素和氧元素组成
B.性质:CO2、CO都可以与NaOH溶液反应
C.用途:干冰可用于人工降雨;一氧化碳气体可作燃料
D.危害:二氧化碳会导致“温室效应”;一氧化碳会引起中毒
6.下列四个图像不能正确反映对应变化关系的是
A.加热一定质量的氯酸钾固体
B.在一定量的MnO2中逐滴加入H2O2溶液
C.密闭容器中点燃H2与O2的混合气体
D.向一定质量的大理石中加入稀盐酸
7.香烟燃烧产生的气体中,有一种能与血液中血红蛋白相结合的有毒气体是
A.二氧化碳 B.二氧化氮 C.二氧化硫 D.一氧化碳
8.下列有关碳和碳的氧化物的说法中,正确的是
A.二氧化碳能使干燥的石蕊纸花变红
B.一氧化碳、二氧化碳、碳都能还原氧化铜
C.金刚石和石墨均属于碳的单质,所以二者性质完全相同
D.二氧化碳可用于灭火,既利用了它的物理性质也利用了它的化学性质
9.用稀盐酸和大理石制取二氧化碳时,以下装置均能达到目的,但其中有一个装置不能随时控制反应发生和停止,该装置是
A. B. C. D.
10.下列实验操作正确的是
A.过滤 B.制取氧气
C.验满气体 D.移走蒸发皿
11.关于碳的单质的说法,错误的是
A.碳纳米管 石墨烯是新形态的碳单质 B.金刚石 石墨 C60 都直接由碳原子构成
C.木炭 活性炭都具有吸附能力 D.碳单质的性质的不同是因为原子的排列方式不同
12.如图所示的装置有很多用途,下列使用方法不正确的是
A.排水法收集氧气时,由a口进气
B.装置中装入适量石灰水并且检验二氧化碳,由a口进气
C.排水法收集氢气时,由b口进气
D.排空气法收集二氧化碳时,由a口进气
13.关于C、CO、CO2三种物质,有下列说法:①三种物质都含有碳元素,都具有还原性;②CO、CO2都是没有颜色、没有气味的气体;③CO2可用于光合作用,CO可用于人工降雨;④CO2能产生温室效应,CO易于血液中的血红蛋白结合引起中毒;⑤CO2可用来做肥料,CO可用作燃料。上述说法中正确的是
A.①②③ B.②④⑤ C.②③④ D.①③⑤
14.下列有关二氧化碳的说法错误的是
A.二氧化碳是一种有毒气体 B.二氧化碳能使澄清石灰水变浑浊
C.液态二氧化碳可用于灭火 D.干冰可用于人工降雨
二、填空题
15.化学是一门研究物质的科学,我们一般从物质的组成(或构成)、性质、用途等方面研究一种物质。以二氧化碳为例,请回答相关问题。
(1)从微观上看,二氧化碳由______构成。
(2)①如图1所示实验中,a、d为用紫色石蕊溶液润湿的棉球,b、c为用石蕊溶液染成紫色的干燥棉球。缓慢通入CO2一段时间后观察到:d比a先变红,b、c不变红,此现象说明CO2具有的物理性质是______,化学性质是______。
②如图2所示实验,将注射器中Ca (OH)2溶液注入锥形瓶中,振荡,观察到瓶中小气球的变化是______;装置内溶液变浑浊,该反应的化学方程式为______。
(3)二氧化碳是可以利用的重要资源。如在一定条件下可以制造金刚石,反应的化学方程式为,X的化学式为______。
(4)2015年世界气候大会在法国巴黎召开,大会呼吁全球减少温室气体排放。
①温室效应加剧导致全球气候变暖,下列气体中不会导致温室效应的是______(填序号)。
A.二氧化碳 B.甲烷 C.一氧化碳 D.臭氧
②下列能源中不属于可再生能源的是______(填序号)。
A.生物质能 B.化石能源 C.风能 D.乙酸
16.“生命吸管”可直接将污水净化为饮用水,主要处理步骤与自来水的净化过程相似,如下图所示:(③中离子交换树脂的主要作用是去除重金属离子、软化水质)
(1)②中活性炭的作用是______(填序号,下同),④中超滤膜的作用是______。
A.去除有害菌和部分病毒 B.吸附杂质 C.除去较大的不溶性杂质
(2)若无生命吸管,取用河水时,要降低水的硬度和杀灭病原微生物,生活中常采取______方法。
(3)经过生命吸管净化后的水是否是软水,你认为可以用______来检验。
(4)下列图标表示“国家节水标志”的是______。
A. B. C. D.
17.人类只有一个地球,碳及其氧化物与人类生活密切相关。
(1)金刚石、石墨、木炭、活性炭用途各不相同,根据下列图示回答问题。
①图B体现了石墨的______性,图D体现了活性炭的______性,图E体现了木炭的______性。
②金刚石、石墨、C60的物理性质存在明显差异的原因是______。
(2)“二氧化碳排放力争于2030年前达到峰值,努力争取2060年前实现碳中和。”这是中国应对全球气候问题作出的庄严承诺。请回答下列问题:
①控制CO2的排放,目的是为减缓______效应。
②写出日常生活中你能做到的一种“低碳”行为______。
18.蜡烛刚熄灭时,总会有一缕白烟,它成分是什么呢?小明同学提出如下假设:
A.白烟是蜡烛燃烧时产生的二氧化碳
B.白烟是蜡烛燃烧时生成的水蒸气
C.白烟是石蜡蒸气冷凝成的石蜡固体
【查阅资料】二氧化碳不能燃烧,也不支持燃烧;石蜡具有可燃性(可以燃烧的性质)
【实验探究】
(1)吹灭蜡烛,立即用一个蘸有澄清石灰水的烧杯罩住白烟,其目的是为了验证假设______(填序号),但这样做并不能得出正确的结论,原因是______。
(2)吹灭蜡烛,立即用一块干而冷的玻璃片放在白烟上,玻璃片没有水雾,说明白烟不是______。
(3)吹灭蜡烛,立即用燃着的木条去点燃白烟,发现蜡烛重新被点燃,说明白烟具有______性,这为假设______提供了证据,因为______。
19.二氧化碳在大气循环中起着重要作用,如图1是产生二氧化碳的途径,其中甲是一种黑色固体单质,乙是天然气的主要成分,丙是一种大气污染物,请回答下列问题:
(1)丙的化学式为______。
(2)实验室CaCO3→CO2的化学反应方程式为______。
(3)列举甲的一种用途是______。的反应属于______反应(填“放热”或“吸热”)。
(4)大气中的二氧化碳过多会引发的环境问题是______。
(5)某同学设计了如图2简易CO2捕捉器流程图,图中固体和液体分离的操作方法是______;请用化学方程式表示捕捉CO2的原理______;流程中可循环利用的物质为______(填化学式)。
三、实验题
20.请结合下图回答问题:
(1)写出有标号仪器的名称:①___________,②___________。
(2)用氯酸钾和二氧化锰制取O2,选用发生装置是___________(填字母),该反应化学方程式是___________;若要收集相对纯度较高的O2可用___________(填字母)装置收集。
(3)实验室制取CO2若用F装置代替B装置进行实验,其优点为___________,要获得纯净、干燥的CO2,除杂装置(如图)的导管按气流方向连接顺序是___________(选填字母)。
A.a→b→d→c B.d→c→a→b
C.b→a→c→d D.c→d→b→a
21.实验室现有石灰石、氯酸钾、二氧化锰、稀硫酸、稀盐酸等药品及相关仪器和用品,请结合下列装置回答问题:
(1)仪器 a 的名称是__________ 。
(2)选用上述药品和 B、E 装置制取 O2,气体收集完毕时,应先 _________(填“从水中移出导管”或“熄灭酒精灯”)。
(3)选用上述仪器和药品制取二氧化碳,发生反应的化学方程式是__________。
(4)为了得到纯净、干燥的 CO2,除杂装置〔如图 2)的导管口按气流方向连接顺序是__________(填序号)。
①1→2→4→3 ②2→1→3→4 ③4→3→1→2 ④3→4→2→1
四、计算题
22.长久使用的热水壶底部有一层水垢,主要成分是碳酸钙(CaCO3),某化学兴趣小组为了测定水垢中碳酸钙的质量分数,取25g水垢放入过量的稀盐酸的烧杯中,立即将烧杯放在天平上,称其质量。在以后的5min内,每一分钟读一次数。结果如下表,试回答下列问题:
时间/min 1 2 3 4 5
质量/g 100g 95g 92g 91.2g 91.2g
(1)反应生成的二氧化碳的质量为多少?______
(2)该水垢中CaCO3的质量分数为多少?______
23.为测定实验室废弃氧化铜样品中氧化铜的质量分数,兴趣小组同学取5g样品在右图装置进行实验(样品中其它杂质不反应),充分反应后测得B质量增加2.2g。回答下列问题:
(1)氧化铜样品中氧化铜的质量分数是多少?(写出计算过程)
(2)小华同学认为测定反应前后A中固体的质量变化也可以测出样品中氧化铜的质量分数,则小华测得充分反应后A中固体的质量应是_________。
参考答案:
1.D
2.C
3.B
4.C
5.B
6.B
7.D
8.D
9.A
10.C
11.B
12.A
13.B
14.A
15.(1)二氧化碳分子
(2) 密度比空气大 能与水反应生成酸 小气球逐渐胀大
(3)Na2CO3
(4) C B
16.(1) B A
(2)煮沸
(3)肥皂水
(4)B
17.(1) 导电 吸附 还原 碳原子的排列方式不同
(2) 温室 使用自行车或公共交通出行,节约用电等
18.(1) A 蜡烛燃烧产生的二氧化碳会使澄清石灰水变浑浊
(2)水蒸气
(3) 可燃 C 只有石蜡具有可燃性
19.(1)CO
(2)
(3) 燃料(合理即可) 吸热
(4)温室效应
(5) 过滤 CaO
20.(1) 长颈漏斗 集气瓶
(2) A D
(3) 可控制反应的发生或停止 B
21.(1)试管
(2)从水中移出导管
(3)
(4)③
22.(1)8.8g
(2)80%
23.(1)设样品中CuO的质量为x。
x=4g
样品中氧化铜的质量分数=×100%=80%。
答:样品中氧化铜的质量分数是80%
(2)4.2g
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
