化学人教版2019必修第一册2.3.1 物质的量的单位——摩尔(共25张ppt)
文档属性
| 名称 | 化学人教版2019必修第一册2.3.1 物质的量的单位——摩尔(共25张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-09-02 00:00:00 | ||
图片预览







文档简介
(共25张PPT)
第三节 物质的量
第一课时 物质的量的单位——摩尔
第二章 海水中的重要元素——钠和氯
本课件内嵌有高清视频供老师参考使用
视频:认识物质的量
认识阿伏伽德罗常数
认识摩尔质量
本页可自行删除
【考纲要求】
了解物质的量、阿伏加德罗常数、摩尔质量的含义和应用,体会定量研究对化学科学的重要作用。
能基于物质的量认识物质组成及其化学变化,并运用物质的量、摩尔质量之间的相互关系进行简单计算。
知识导航
一粒大米
一堆大米
一袋大米
课堂导入
课堂导入
水是由水分子构成
…
…
课堂导入
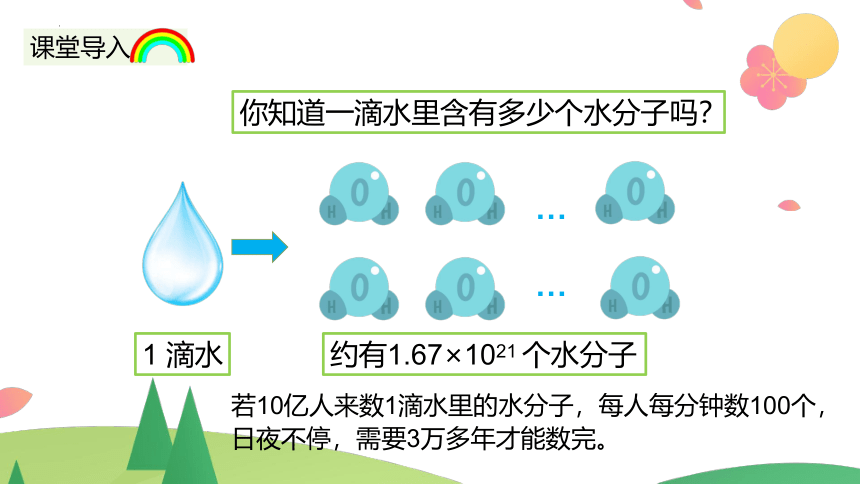
你知道一滴水里含有多少个水分子吗?
1 滴水
约有1.67×1021 个水分子
若10亿人来数1滴水里的水分子,每人每分钟数100个,日夜不停,需要3万多年才能数完。
大量的分子用什么计量更方便呢?
化学家在研究中发现,虽然参加化学反应的微粒质量很小,但实际参加反应的微粒数往往很大(如1滴水中大约含有17万亿亿个水分子)。
为了将一定数目的微观粒子与可称量的宏观物质联系起来,
在化学上引入了物质的量。
1.了解国际单位制的七个基本单位。
例如:用米、厘米等来计量长度;用千克、毫克 等来计量质量。
2.想一想,微观粒子包括哪些?
原子、分子、离子、电子、中子、质子、原子团等。
人们用摩尔作为计量原子、离子或分子等微观粒子的“物质的量”的单位。
物理量 长度 质量 时间 电流 热力学温度 物质的量 发光强度
单位(符号) 米(m) 千克(kg) 秒(s) 安(A) 开(K) 摩(mol) 坎(cd)
1.意义:国际单位制中7个基本物理量之一,它表示含有一定数目粒子的集合体。
2. 符号:n
3. 单位:摩尔,简称摩,符号为mol
一.物质的量
4.物质的量研究对象:
粒子集体可以是原子、分子、离子、质子、中子、电子或原子团等微观粒子。
例如1mol Fe 、1mol O2 、 、1mol SO42- 、1mol e- 等。
【注意】
(1)物质的量是国际单位制中七个基本物理量之一,是衡量微观粒子的物理量。物质的量可将宏观可称量的物质与微观粒子联系起来。
(2)“物质的量”同长度、质量、时间等物理量一样,是一个整体名词,不可分割或插入其它字,比如不能将其理解为“物质的质量”或“物质的数量”,也不能写成“物质量”。
(3)使用摩尔表示物质的量时,表述要确切,指代需明确。
例如:1molH表示 ,
1molH2表示 ,
1mol H+ 表示 。
(4)摩尔作为物质的量的单位,可以计量所有的微观粒子(包括原子、分子、离子、质子、中子、电子、原子团等),但不能表示宏观物质,例如,
“1mol小米”、“1mol乒乓球”描述 错误
1mol氢原子
1mol氢气分子
1mol氢离子
二.阿伏伽德罗常数
1.定义:6.02×1023 mol- 叫做阿伏伽德罗常数,是个物理量。
2.符号: NA
3.意义:1 mol任何粒子的粒子数
与阿伏伽德罗常数数值相等。
1摩尔粒子集合体所含的粒子数与 12C中所含的碳原子数相同,约为 。
0.012kg
6.02×1023
4. 18gH2O,27gAl所含的粒子(分子或原子)均约为 个。
大量实验证明,任何粒子或物质的质量以 为单位,在数值上与该粒子的 或者 相等时,所含粒子的数目都约为 个。
6.02×1023
克
相对原子质量
相对分子质量
6.02×1023
含有 个粒子的任何粒子的集体,计量为1mol。
1mol任何粒子集体的粒子数目都为 个。
例如:1 mol 水含有 6.02×1023个水分子。
6.02×1023
6.02×1023
【例题1】下列叙述正确的是( )
①2 mol铁原子 ②1 mol Fe3+ ③0.5 mol 氧
④0.5 mol 氮分子 ⑤氨的摩尔质量是17 g
A.①③④ B.①②④⑤
C.①②④ D.①②③④⑤
【答案】C
【总结】
微观粒子数目、阿伏伽德罗常数和物质的量的关系
1.微观粒子数:符号 。
2.含有 个或者 个粒子的任何粒子的集体,计量为 1 mol;
1mol任何粒子集体的粒子数目都约为 个或者 个。
3.关系式:
N
6.02×1023
6.02×1023
NA
NA
【例题2】正确填写下列数据
(1)1mol O2 中约含有 个氧分子;
(2)2mol C 中约含有 个碳原子;
(3)1mol H2SO4 中约含有 个硫酸分子;
(4)1.5molNaOH中约含有 个Na+,
个OH-;
(5)n mol 某微粒集合体中约含有该微粒约为
个 ;
(6)1.204×1024 个水分子的物质的量 mol;
(7)9.03×1023个铁原子的物质的量 mol。
6.02×1023(NA)
2×6.02×1023(2NA)
6.02×1023
1.5×6.02×1023
1.5×6.02×1023
n×6.02×1023(nNA)
2
1.5
1. 定义:单位物质的量的物质所具有的质量
2. 单位: g/mol 或 g﹒mol-1
3. 1mol任何粒子或物质的质量以 克 为单位时,在数值上都与与该粒子的相对原子质量或者相对分子质量相等。
4. n 、m、M数学表达式
三.摩尔质量
【总结】
物质的量是——
连接微观粒子和宏观可称量质量的桥梁。
【例题3】C的摩尔质量为 ,
12克C含有 个碳原子;
Na+的摩尔质量为 ,
0.1molNa+的质量为 。
12g/mol
6.02×1023(NA)
23g/mol
2.3g
效果检测
1.下列与物质的量有关的说法中正确的是
A.物质的量是物质所含粒子数量的简称
B.物质的量适用于计量分子、原子、离子等粒子
C.摩尔是表示物质所含微粒个数的物理量
D.物质的量就是指物质的质量
【答案】B
2.(2021·上海市新中高级中学高一阶段练习)将物质的质量跟它所包含的微粒数相联系的物理量是
A.摩尔质量 B.摩尔 C.物质的量 D.阿伏加德罗常数
【答案】C
3.(2021·上海师范大学附属中学闵行分校高一期中)已知0.25molX的质量为11g,则X的摩尔质量是
A.22g B.44g C.22g mol-1 D.44g mol-1
【答案】D
4.(2021·河北·武安市第一中学高一阶段练习)下列说法正确的是
A.摩尔是表示物质所含质量多少的单位
B.摩尔质量就等于物质相对分子质量的6.02×1023倍
C.HNO3的摩尔质量是63g
D.硫酸和磷酸的摩尔质量相等
【答案】D
5.(2021·广东·阳西县第一中学高一阶段练习)下列叙述正确的是
A.OH-的摩尔质量为17g·mol-1
B.1mol物质的质量就是该物质的相对分子质量
C.摩尔是七个基本物理量之一
D.阿伏伽德罗常数就是6.02×1023mol-1
【答案】A
6.(2021·上海·华东理工大学附属闵行科技高级中学高一期中)下列说法正确的是
A.H2O的摩尔质量是18
B.1molO2的质量是32g/mol
C.0.5mol氮
D.含有3.01×1024个CO2分子的CO2物质的量为5mol
【答案】D
本课结束
第三节 物质的量
第一课时 物质的量的单位——摩尔
第二章 海水中的重要元素——钠和氯
本课件内嵌有高清视频供老师参考使用
视频:认识物质的量
认识阿伏伽德罗常数
认识摩尔质量
本页可自行删除
【考纲要求】
了解物质的量、阿伏加德罗常数、摩尔质量的含义和应用,体会定量研究对化学科学的重要作用。
能基于物质的量认识物质组成及其化学变化,并运用物质的量、摩尔质量之间的相互关系进行简单计算。
知识导航
一粒大米
一堆大米
一袋大米
课堂导入
课堂导入
水是由水分子构成
…
…
课堂导入
你知道一滴水里含有多少个水分子吗?
1 滴水
约有1.67×1021 个水分子
若10亿人来数1滴水里的水分子,每人每分钟数100个,日夜不停,需要3万多年才能数完。
大量的分子用什么计量更方便呢?
化学家在研究中发现,虽然参加化学反应的微粒质量很小,但实际参加反应的微粒数往往很大(如1滴水中大约含有17万亿亿个水分子)。
为了将一定数目的微观粒子与可称量的宏观物质联系起来,
在化学上引入了物质的量。
1.了解国际单位制的七个基本单位。
例如:用米、厘米等来计量长度;用千克、毫克 等来计量质量。
2.想一想,微观粒子包括哪些?
原子、分子、离子、电子、中子、质子、原子团等。
人们用摩尔作为计量原子、离子或分子等微观粒子的“物质的量”的单位。
物理量 长度 质量 时间 电流 热力学温度 物质的量 发光强度
单位(符号) 米(m) 千克(kg) 秒(s) 安(A) 开(K) 摩(mol) 坎(cd)
1.意义:国际单位制中7个基本物理量之一,它表示含有一定数目粒子的集合体。
2. 符号:n
3. 单位:摩尔,简称摩,符号为mol
一.物质的量
4.物质的量研究对象:
粒子集体可以是原子、分子、离子、质子、中子、电子或原子团等微观粒子。
例如1mol Fe 、1mol O2 、 、1mol SO42- 、1mol e- 等。
【注意】
(1)物质的量是国际单位制中七个基本物理量之一,是衡量微观粒子的物理量。物质的量可将宏观可称量的物质与微观粒子联系起来。
(2)“物质的量”同长度、质量、时间等物理量一样,是一个整体名词,不可分割或插入其它字,比如不能将其理解为“物质的质量”或“物质的数量”,也不能写成“物质量”。
(3)使用摩尔表示物质的量时,表述要确切,指代需明确。
例如:1molH表示 ,
1molH2表示 ,
1mol H+ 表示 。
(4)摩尔作为物质的量的单位,可以计量所有的微观粒子(包括原子、分子、离子、质子、中子、电子、原子团等),但不能表示宏观物质,例如,
“1mol小米”、“1mol乒乓球”描述 错误
1mol氢原子
1mol氢气分子
1mol氢离子
二.阿伏伽德罗常数
1.定义:6.02×1023 mol- 叫做阿伏伽德罗常数,是个物理量。
2.符号: NA
3.意义:1 mol任何粒子的粒子数
与阿伏伽德罗常数数值相等。
1摩尔粒子集合体所含的粒子数与 12C中所含的碳原子数相同,约为 。
0.012kg
6.02×1023
4. 18gH2O,27gAl所含的粒子(分子或原子)均约为 个。
大量实验证明,任何粒子或物质的质量以 为单位,在数值上与该粒子的 或者 相等时,所含粒子的数目都约为 个。
6.02×1023
克
相对原子质量
相对分子质量
6.02×1023
含有 个粒子的任何粒子的集体,计量为1mol。
1mol任何粒子集体的粒子数目都为 个。
例如:1 mol 水含有 6.02×1023个水分子。
6.02×1023
6.02×1023
【例题1】下列叙述正确的是( )
①2 mol铁原子 ②1 mol Fe3+ ③0.5 mol 氧
④0.5 mol 氮分子 ⑤氨的摩尔质量是17 g
A.①③④ B.①②④⑤
C.①②④ D.①②③④⑤
【答案】C
【总结】
微观粒子数目、阿伏伽德罗常数和物质的量的关系
1.微观粒子数:符号 。
2.含有 个或者 个粒子的任何粒子的集体,计量为 1 mol;
1mol任何粒子集体的粒子数目都约为 个或者 个。
3.关系式:
N
6.02×1023
6.02×1023
NA
NA
【例题2】正确填写下列数据
(1)1mol O2 中约含有 个氧分子;
(2)2mol C 中约含有 个碳原子;
(3)1mol H2SO4 中约含有 个硫酸分子;
(4)1.5molNaOH中约含有 个Na+,
个OH-;
(5)n mol 某微粒集合体中约含有该微粒约为
个 ;
(6)1.204×1024 个水分子的物质的量 mol;
(7)9.03×1023个铁原子的物质的量 mol。
6.02×1023(NA)
2×6.02×1023(2NA)
6.02×1023
1.5×6.02×1023
1.5×6.02×1023
n×6.02×1023(nNA)
2
1.5
1. 定义:单位物质的量的物质所具有的质量
2. 单位: g/mol 或 g﹒mol-1
3. 1mol任何粒子或物质的质量以 克 为单位时,在数值上都与与该粒子的相对原子质量或者相对分子质量相等。
4. n 、m、M数学表达式
三.摩尔质量
【总结】
物质的量是——
连接微观粒子和宏观可称量质量的桥梁。
【例题3】C的摩尔质量为 ,
12克C含有 个碳原子;
Na+的摩尔质量为 ,
0.1molNa+的质量为 。
12g/mol
6.02×1023(NA)
23g/mol
2.3g
效果检测
1.下列与物质的量有关的说法中正确的是
A.物质的量是物质所含粒子数量的简称
B.物质的量适用于计量分子、原子、离子等粒子
C.摩尔是表示物质所含微粒个数的物理量
D.物质的量就是指物质的质量
【答案】B
2.(2021·上海市新中高级中学高一阶段练习)将物质的质量跟它所包含的微粒数相联系的物理量是
A.摩尔质量 B.摩尔 C.物质的量 D.阿伏加德罗常数
【答案】C
3.(2021·上海师范大学附属中学闵行分校高一期中)已知0.25molX的质量为11g,则X的摩尔质量是
A.22g B.44g C.22g mol-1 D.44g mol-1
【答案】D
4.(2021·河北·武安市第一中学高一阶段练习)下列说法正确的是
A.摩尔是表示物质所含质量多少的单位
B.摩尔质量就等于物质相对分子质量的6.02×1023倍
C.HNO3的摩尔质量是63g
D.硫酸和磷酸的摩尔质量相等
【答案】D
5.(2021·广东·阳西县第一中学高一阶段练习)下列叙述正确的是
A.OH-的摩尔质量为17g·mol-1
B.1mol物质的质量就是该物质的相对分子质量
C.摩尔是七个基本物理量之一
D.阿伏伽德罗常数就是6.02×1023mol-1
【答案】A
6.(2021·上海·华东理工大学附属闵行科技高级中学高一期中)下列说法正确的是
A.H2O的摩尔质量是18
B.1molO2的质量是32g/mol
C.0.5mol氮
D.含有3.01×1024个CO2分子的CO2物质的量为5mol
【答案】D
本课结束
