化学人教版(2019)必修第一册1.1.1 物质的分类(共23张ppt)
文档属性
| 名称 | 化学人教版(2019)必修第一册1.1.1 物质的分类(共23张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 993.3KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-09-03 00:00:00 | ||
图片预览






文档简介
(共23张PPT)
第一章 物质及其变化
第1节 物质的分类与转化
(1)物质的分类
超市里有成千上万种商品,为了顾客迅速找到“可比克”薯片?超市做了哪些工作?
图书馆里有许许多多的书籍,为什么你很快就找到你需要的书?
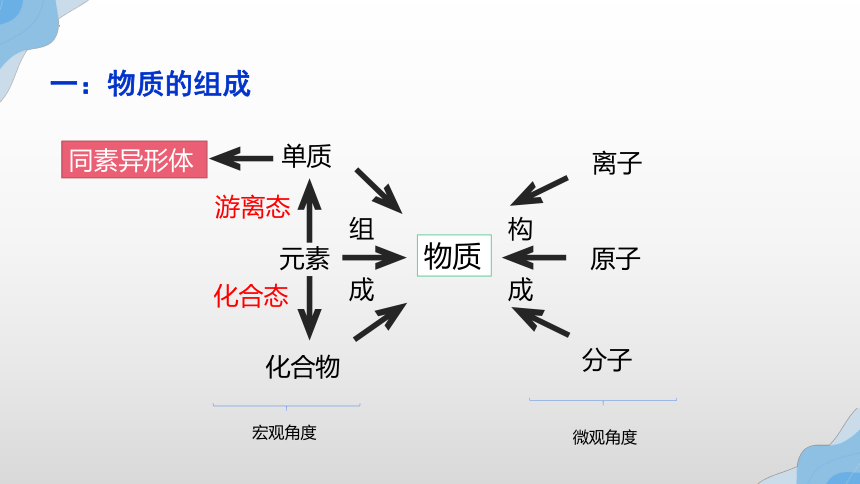
一:物质的组成
物质
元素
单质
游离态
同素异形体
化合物
化合态
组
成
构
成
原子
离子
分子
宏观角度
微观角度
二:同素异形体
由同一种元素形成的几种性质不同的单质。
例:金刚石、石墨、C60
氧气 (O2) 、臭氧(O3)
白磷(P4) 、红磷(P)
注意:
由同一种元素组成的物质可能是纯净物,也可能是混合物。
互为同素异形体的物质之间转化属于化学变化,而不是物理变化。
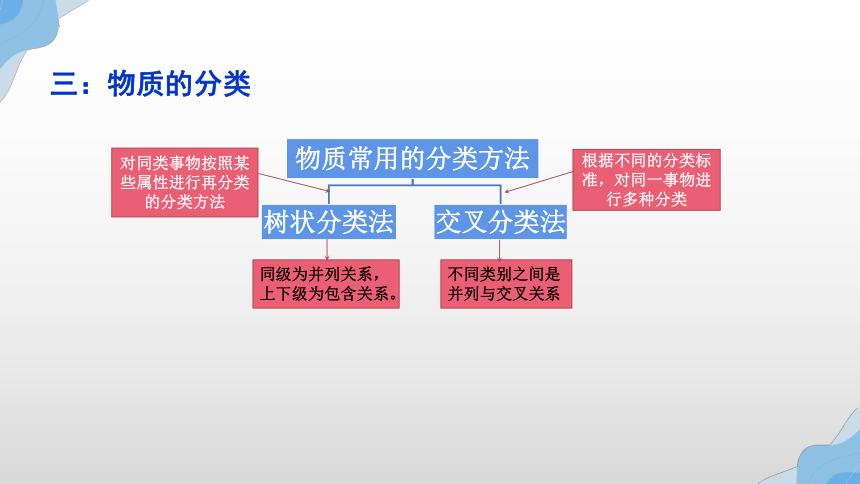
三:物质的分类
根据不同的分类标准,对同一事物进行多种分类
对同类事物按照某些属性进行再分类的分类方法
同级为并列关系,
上下级为包含关系。
不同类别之间是
并列与交叉关系
1.树状分类法
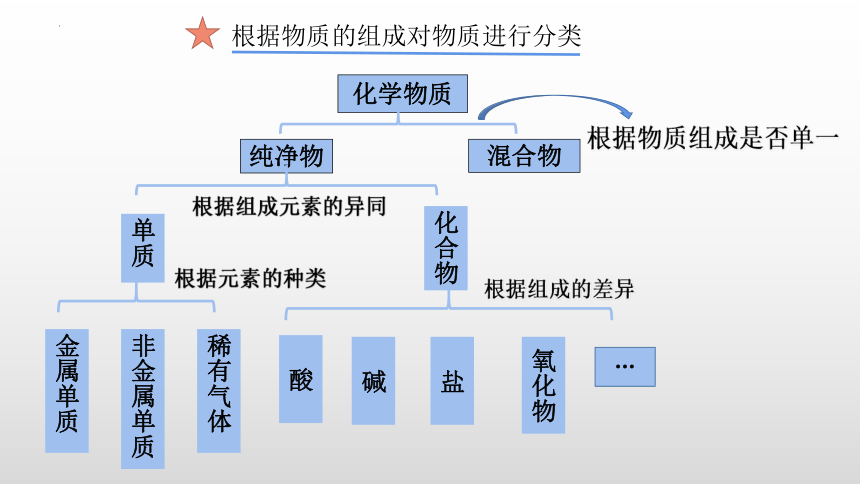
根据物质的组成对物质进行分类
化学物质
根据物质组成是否单一
纯净物
混合物
根据组成元素的异同
单质
根据元素的种类
金属单质
非金属单质
稀有气体
化合物
氧化物
盐
碱
酸
…
根据组成的差异
用树状分类法对酸碱盐氧化物进行分类
HCl H2S
H2SO4
HNO3
HCl H2SO4 HNO3
HCl HNO3
H3PO4
H2SO4 H2CO3
H2CO3 CH3COOH
NaOH KOH
Cu(OH)2 Fe(OH )3
NaOH KOH
Ba(OH)2 Ca(OH)2
NH3 ·H2O
Cu(OH)2 Fe(OH )3
NaOH KOH LiOH
Ba(OH)2 Ca(OH)2
Fe(OH )3
NaCl KCl Na2 SO4
AgCl CaCO3 BaSO4
NaCl KCl Na2 SO4
NaHCO 3 NaHSO4
Cu2(OH)2 CO3
KAl(SO4) 2
H2O2 Na2O2
CuO Fe2O3
SO2 CO2
酸性氧化物:与碱反应生成盐(同价态)和水
CO2 + 2NaOH Na2CO3 + H2O
SO3 + 2NaOH Na2SO4 + H2O
碱性氧化物:与酸反应生成盐(同价态)和水
CaO + 2HCl CaCl2 + H2O
Fe2O3 + 6HCl 2FeCl3 + 3H2O
Na2O + 2HCl 2NaCl + H2O
酸性氧化物、碱性氧化物的通性
酸性氧化物
碱性氧化物
+ 水 相应的酸
+ 碱 盐和水
+碱性氧化物 盐
+ 水 相应的碱
+ 酸 盐和水
注意:
有的酸性氧化物(SiO2)和碱性氧化物(CuO)不溶于水,即不能跟水发生化学反应。
能和水反应生成酸、碱的氧化物也不一定是酸性氧化物、碱性氧化物,如:NO2、Na2O2
不成盐氧化物:既不和酸反应生成盐和水又不和碱反应生成 盐和水
例如: NO CO
两性氧化物:既和酸反应生成盐和水又和碱反应生成盐和水
例如: Al2O3
概念区分
1.非金属氧化物不一定是酸性氧化物;
例如:CO NO
2.酸性氧化物也不一定是非金属氧化物;
例如:Mn2O7
3.金属氧化物不一定是碱性氧化物;
例如: Mn2O7
4.碱性氧化物一定是金属氧化物。
1.下列有关物质的分类正确的是 ( )
A.混合物:空气、矿泉水、水银
B.碱:Ba(OH)2、 Cu2(OH)2CO3、 NH3·H2O
C.盐:硫酸钠、氯化铵、 纯碱
D.氧化物:H2O、 CO、 HCOOH
练习
C
2.下列有关概念说法正确的是( )
A.酸性氧化物均能溶于水生成相应的酸
B.金属氧化物均为碱性氧化物,非金属氧化物均为酸性氧化物
C.由一种元素组成的物质是纯净物
D.CuSO4 5H2O属于纯净物
D
练习
2.交叉分类法
从不同角度对物质进行分类
Na2CO3
根据阳离子区分
根据阴离子区分
钠盐
碳酸盐
一个物质从不同的分类角度来看,可以从属于多个类别
Na2CO3
Na2SO4
硫酸盐
钠盐
K2SO4
碳酸盐
K2CO3
钾盐
根据阳离子区分
根据阴离子区分
硫酸盐
钠盐
碳酸盐
钾盐
① ② ③ ④
A NaCl K2SO4 KCl (NH4)2SO4
B Na2SO4 K2SO4 KCl NH4Cl
C NaCl K2SO4 KCl NH4Cl
D Na2SO4 K2SO4 KCl (NH4)2SO4
3.奥运五环代表着全世界五大洲的人民团结在一起。下列各项中的物质,能满足如图中阴影部分关系的是( )
练习
B
第一章 物质及其变化
第1节 物质的分类与转化
(1)物质的分类
超市里有成千上万种商品,为了顾客迅速找到“可比克”薯片?超市做了哪些工作?
图书馆里有许许多多的书籍,为什么你很快就找到你需要的书?
一:物质的组成
物质
元素
单质
游离态
同素异形体
化合物
化合态
组
成
构
成
原子
离子
分子
宏观角度
微观角度
二:同素异形体
由同一种元素形成的几种性质不同的单质。
例:金刚石、石墨、C60
氧气 (O2) 、臭氧(O3)
白磷(P4) 、红磷(P)
注意:
由同一种元素组成的物质可能是纯净物,也可能是混合物。
互为同素异形体的物质之间转化属于化学变化,而不是物理变化。
三:物质的分类
根据不同的分类标准,对同一事物进行多种分类
对同类事物按照某些属性进行再分类的分类方法
同级为并列关系,
上下级为包含关系。
不同类别之间是
并列与交叉关系
1.树状分类法
根据物质的组成对物质进行分类
化学物质
根据物质组成是否单一
纯净物
混合物
根据组成元素的异同
单质
根据元素的种类
金属单质
非金属单质
稀有气体
化合物
氧化物
盐
碱
酸
…
根据组成的差异
用树状分类法对酸碱盐氧化物进行分类
HCl H2S
H2SO4
HNO3
HCl H2SO4 HNO3
HCl HNO3
H3PO4
H2SO4 H2CO3
H2CO3 CH3COOH
NaOH KOH
Cu(OH)2 Fe(OH )3
NaOH KOH
Ba(OH)2 Ca(OH)2
NH3 ·H2O
Cu(OH)2 Fe(OH )3
NaOH KOH LiOH
Ba(OH)2 Ca(OH)2
Fe(OH )3
NaCl KCl Na2 SO4
AgCl CaCO3 BaSO4
NaCl KCl Na2 SO4
NaHCO 3 NaHSO4
Cu2(OH)2 CO3
KAl(SO4) 2
H2O2 Na2O2
CuO Fe2O3
SO2 CO2
酸性氧化物:与碱反应生成盐(同价态)和水
CO2 + 2NaOH Na2CO3 + H2O
SO3 + 2NaOH Na2SO4 + H2O
碱性氧化物:与酸反应生成盐(同价态)和水
CaO + 2HCl CaCl2 + H2O
Fe2O3 + 6HCl 2FeCl3 + 3H2O
Na2O + 2HCl 2NaCl + H2O
酸性氧化物、碱性氧化物的通性
酸性氧化物
碱性氧化物
+ 水 相应的酸
+ 碱 盐和水
+碱性氧化物 盐
+ 水 相应的碱
+ 酸 盐和水
注意:
有的酸性氧化物(SiO2)和碱性氧化物(CuO)不溶于水,即不能跟水发生化学反应。
能和水反应生成酸、碱的氧化物也不一定是酸性氧化物、碱性氧化物,如:NO2、Na2O2
不成盐氧化物:既不和酸反应生成盐和水又不和碱反应生成 盐和水
例如: NO CO
两性氧化物:既和酸反应生成盐和水又和碱反应生成盐和水
例如: Al2O3
概念区分
1.非金属氧化物不一定是酸性氧化物;
例如:CO NO
2.酸性氧化物也不一定是非金属氧化物;
例如:Mn2O7
3.金属氧化物不一定是碱性氧化物;
例如: Mn2O7
4.碱性氧化物一定是金属氧化物。
1.下列有关物质的分类正确的是 ( )
A.混合物:空气、矿泉水、水银
B.碱:Ba(OH)2、 Cu2(OH)2CO3、 NH3·H2O
C.盐:硫酸钠、氯化铵、 纯碱
D.氧化物:H2O、 CO、 HCOOH
练习
C
2.下列有关概念说法正确的是( )
A.酸性氧化物均能溶于水生成相应的酸
B.金属氧化物均为碱性氧化物,非金属氧化物均为酸性氧化物
C.由一种元素组成的物质是纯净物
D.CuSO4 5H2O属于纯净物
D
练习
2.交叉分类法
从不同角度对物质进行分类
Na2CO3
根据阳离子区分
根据阴离子区分
钠盐
碳酸盐
一个物质从不同的分类角度来看,可以从属于多个类别
Na2CO3
Na2SO4
硫酸盐
钠盐
K2SO4
碳酸盐
K2CO3
钾盐
根据阳离子区分
根据阴离子区分
硫酸盐
钠盐
碳酸盐
钾盐
① ② ③ ④
A NaCl K2SO4 KCl (NH4)2SO4
B Na2SO4 K2SO4 KCl NH4Cl
C NaCl K2SO4 KCl NH4Cl
D Na2SO4 K2SO4 KCl (NH4)2SO4
3.奥运五环代表着全世界五大洲的人民团结在一起。下列各项中的物质,能满足如图中阴影部分关系的是( )
练习
B
