广西壮族自治区南宁市2022-2023学年高二上学期9月开学质量调研化学试题(Word版含答案)
文档属性
| 名称 | 广西壮族自治区南宁市2022-2023学年高二上学期9月开学质量调研化学试题(Word版含答案) |
|
|
| 格式 | docx | ||
| 文件大小 | 644.7KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-09-03 00:00:00 | ||
图片预览


文档简介
南宁市2022-2023学年高二上学期9月开学质量调研
化学
注意事项:
1.本试卷满分100分,考试时间90分钟。
2.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑;非选择题请用直径0.5毫米黑色墨水签字笔在答题卡上各题的答题区域内作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
可能用到的相对原子质量:O-16 Na-23
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
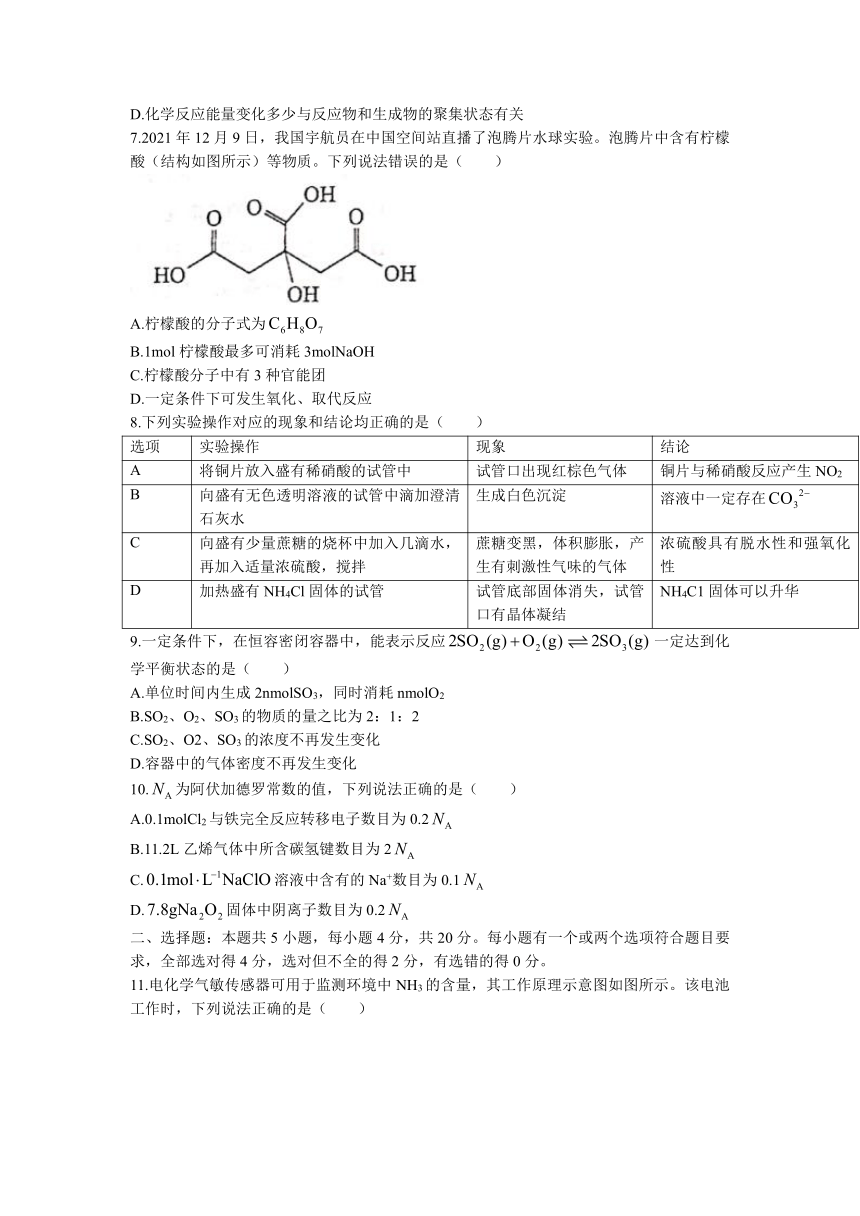
1.“十四五”时期生态文明建设强调绿色发展、减少碳排放和改善生态环境质量。下列关于碳排放的说法错误的是( )
A.我国科学家利用CO2合成淀粉,能促进实现2030年“碳达峰”的目标
B.大力推进新能源汽车代替传统燃油汽车,有利于实现“碳中和”,改善生态环境
C.通过煤的干馏、煤的气化和煤的液化,可以从根本上杜绝碳排放
D.积极开发使用风能、太阳能、生物能等新型能源,有利于减少碳排放
2.按照物质的组成分类,KIO3属于( )
A.氧化物 B.酸 C.碱 D.盐
3.在100ml小烧杯中加入40ml蒸馏水,将烧杯中蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴FeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热,得到的分散系为( )
A.浊液 B.溶液 C.胶体 D.无法确定
4.下列与实验相关的操作或方案正确的是( )
A.配制一定物质的量浓度的溶液 B.组成Zn-Cu原电池 C.实验室制取乙酸乙酯 D.比较S、C、Si的非金属性强弱
A.A B.B C.C D.D
5.下列离子方程式中,正确的是( )
A.将铜片插入溶液中:
B.将醋酸滴在石灰石上:
C.将一块绿豆大的钠放入水中:
D.将硝酸银溶液与氯化钠溶液混合:
6.下列说法错误的是( )
A.在化学反应过程中,发生物质变化的同时不一定发生能量变化
B.化学键的断裂与形成是化学反应中能量变化的主要原因
C.当生成物总能量高于反应物总能量时,反应吸热
D.化学反应能量变化多少与反应物和生成物的聚集状态有关
7.2021年12月9日,我国宇航员在中国空间站直播了泡腾片水球实验。泡腾片中含有柠檬酸(结构如图所示)等物质。下列说法错误的是( )
A.柠檬酸的分子式为
B.1mol柠檬酸最多可消耗3molNaOH
C.柠檬酸分子中有3种官能团
D.一定条件下可发生氧化、取代反应
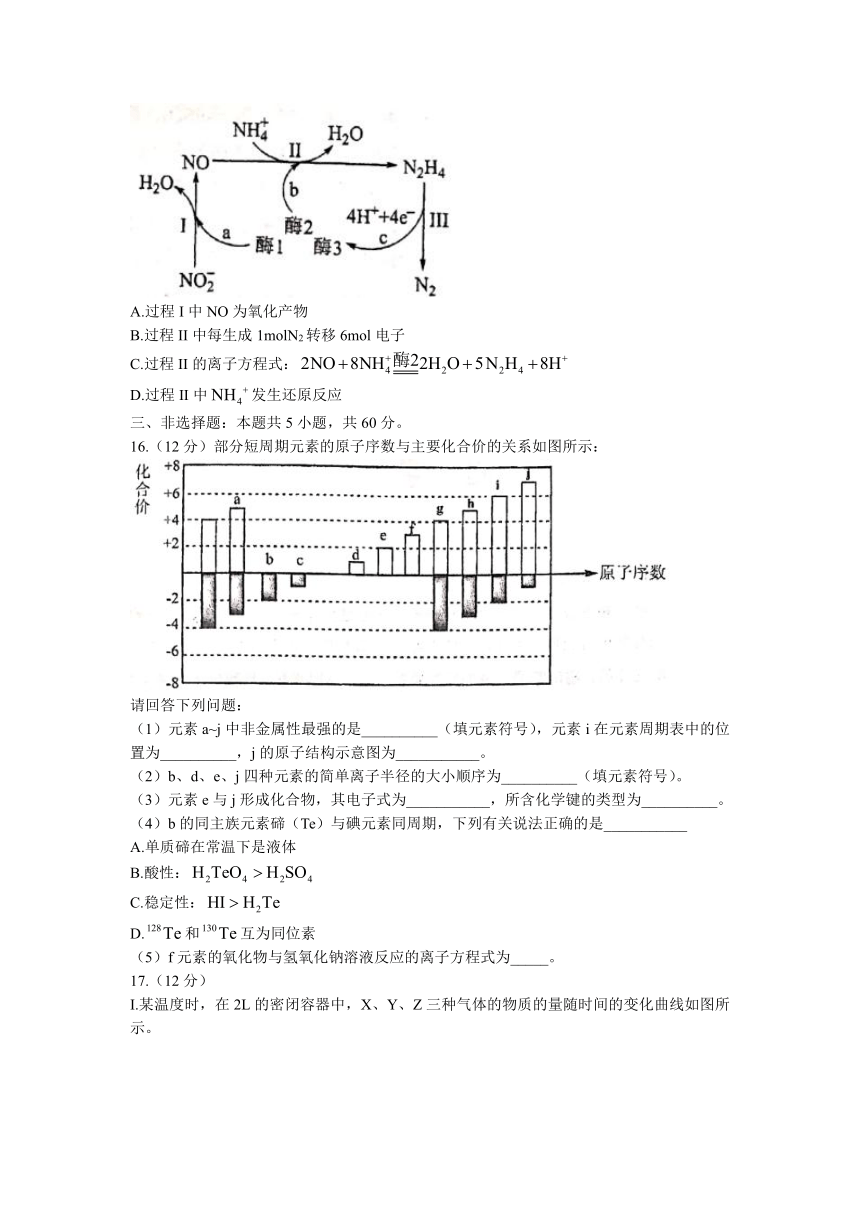
8.下列实验操作对应的现象和结论均正确的是( )
选项 实验操作 现象 结论
A 将铜片放入盛有稀硝酸的试管中 试管口出现红棕色气体 铜片与稀硝酸反应产生NO2
B 向盛有无色透明溶液的试管中滴加澄清石灰水 生成白色沉淀 溶液中一定存在
C 向盛有少量蔗糖的烧杯中加入几滴水,再加入适量浓硫酸,搅拌 蔗糖变黑,体积膨胀,产生有刺激性气味的气体 浓硫酸具有脱水性和强氧化性
D 加热盛有NH4Cl固体的试管 试管底部固体消失,试管口有晶体凝结 NH4C1固体可以升华
9.一定条件下,在恒容密闭容器中,能表示反应一定达到化学平衡状态的是( )
A.单位时间内生成2nmolSO3,同时消耗nmolO2
B.SO2、O2、SO3的物质的量之比为2:1:2
C.SO2、O2、SO3的浓度不再发生变化
D.容器中的气体密度不再发生变化
10.为阿伏加德罗常数的值,下列说法正确的是( )
A.0.1molCl2与铁完全反应转移电子数目为0.2
B.11.2L乙烯气体中所含碳氢键数目为2
C.溶液中含有的Na+数目为0.1
D.固体中阴离子数目为0.2
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,全部选对得4分,选对但不全的得2分,有选错的得0分。
11.电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如图所示。该电池工作时,下列说法正确的是( )
A.电极(a)为正极
B.NH3在电极(a)_上发生氧化反应
C.电子由电极(a)经导线移动向电极(b)
D.K+向电极(a)移动
12.短周期主族元素X、Y、Z、W在元素周期表中的位置如图所示,Y原子最外层电子数是其电子层数的3倍。下列关于这四种元素及其化合物的说法中正确的是( )
A.X、Y、z、W中可能存在金属元素
B.化合物ZW2分子中所有原子都达到8电子稳定结构
C.气态氢化物的稳定性:Z>W>X>Y
D.Y、Z可形成具有漂白性的化合物
13.下列物质的制备与工业生产不相符的是( )
A.NH3NOHNO3
B.海水→MgOMg
C.饱和食盐水
D.石油乙烯聚乙烯塑料
14.室温下,下列各组离子在指定条件下一定能大量共存的是( )
A.与铝反应产生氢气的溶液:
B.无色透明溶液:
C.pH=1的溶液:
D.新制饱和氯水:
15.科学家发现某些生物酶体系可以促进和的转移(如a、b和c),能将海洋中的转化为N2进入大气层,反应过程如图所示。下列说法正确的是( )
A.过程I中NO为氧化产物
B.过程II中每生成1molN2转移6mol电子
C.过程II的离子方程式:
D.过程II中发生还原反应
三、非选择题:本题共5小题,共60分。
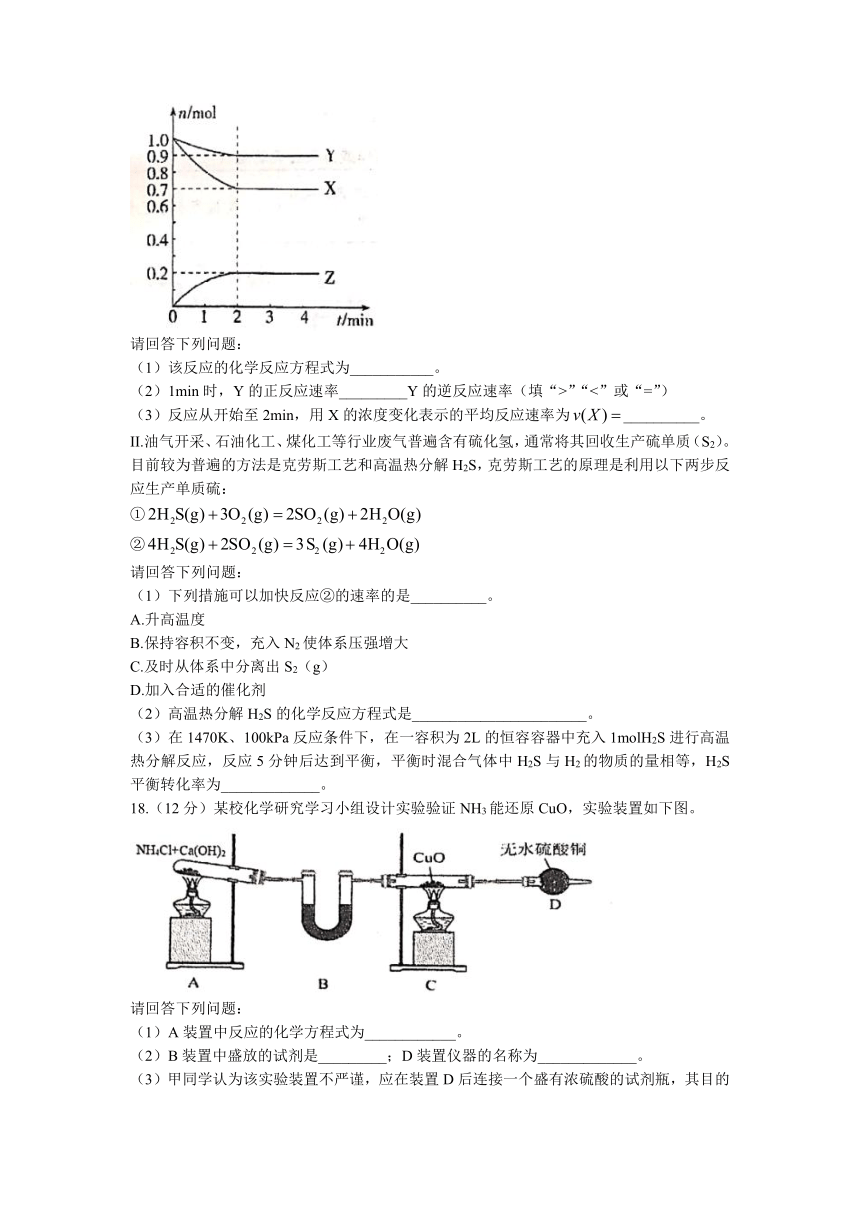
16.(12分)部分短周期元素的原子序数与主要化合价的关系如图所示:
请回答下列问题:
(1)元素a~j中非金属性最强的是__________(填元素符号),元素i在元素周期表中的位置为__________,j的原子结构示意图为___________。
(2)b、d、e、j四种元素的简单离子半径的大小顺序为__________(填元素符号)。
(3)元素e与j形成化合物,其电子式为___________,所含化学键的类型为__________。
(4)b的同主族元素碲(Te)与碘元素同周期,下列有关说法正确的是___________
A.单质碲在常温下是液体
B.酸性:
C.稳定性:
D.和互为同位素
(5)f元素的氧化物与氢氧化钠溶液反应的离子方程式为_____。
17.(12分)
I.某温度时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。
请回答下列问题:
(1)该反应的化学反应方程式为___________。
(2)1min时,Y的正反应速率_________Y的逆反应速率(填“>”“<”或“=”)
(3)反应从开始至2min,用X的浓度变化表示的平均反应速率为__________。
II.油气开采、石油化工、煤化工等行业废气普遍含有硫化氢,通常将其回收生产硫单质(S2)。目前较为普遍的方法是克劳斯工艺和高温热分解H2S,克劳斯工艺的原理是利用以下两步反应生产单质硫:
①
②
请回答下列问题:
(1)下列措施可以加快反应②的速率的是__________。
A.升高温度
B.保持容积不变,充入N2使体系压强增大
C.及时从体系中分离出S2(g)
D.加入合适的催化剂
(2)高温热分解H2S的化学反应方程式是_______________________。
(3)在1470K、100kPa反应条件下,在一容积为2L的恒容容器中充入1molH2S进行高温热分解反应,反应5分钟后达到平衡,平衡时混合气体中H2S与H2的物质的量相等,H2S平衡转化率为_____________。
18.(12分)某校化学研究学习小组设计实验验证NH3能还原CuO,实验装置如下图。
请回答下列问题:
(1)A装置中反应的化学方程式为____________。
(2)B装置中盛放的试剂是_________;D装置仪器的名称为_____________。
(3)甲同学认为该实验装置不严谨,应在装置D后连接一个盛有浓硫酸的试剂瓶,其目的是____________。
(4)证明NH3能与CuO反应的实验现象是__________________。
(5)若NH3还原CuO的还原产物唯一且生成无毒无污染气体,则C反应中氧化产物与还原产物的物质的量之比为__________________。
(6)已知该反应受NH3用量和反应温度影响,有时会生成副产物Cu2O,Cu2O为砖红色,易对实验结论产生干扰。已知Cu2O在酸性溶液中不稳定:,请设计实验方案验证CuO完全反应后的红色固体产物中是否含有Cu2O________________。
19.(12分)金属及其化合物在生产生活中占有极其重要的地位,请结合金属及其化合物的相关知识回答下列问题:
(1)目前使用量最大的合金是____________。
A.钢 B.青铜 C.镁合金 D.铝合金
(2)某溶液中有Mg2+、Fe2+、Al3+、Cu2+等离子,向其中加入足量的Na2O2后,过滤,将滤渣投入足量的盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是__________。
A.Mg2+ B.Fe2+ C.A13+ D.Cu2+
(3)高铁酸钠()是一种新型水处理剂。某兴趣小组欲利用废金属屑(主要成分为Fe和Cu,含有少量)制取高铁酸钠并回收金属Cu,其工艺流程如下:
①试剂a为__________(填化学式,下同),滤渣II的主要成分为_________。
②在过滤操作中要使用玻璃棒,其作用是__________。
③检验滤液I中是否存在Fe3+的试剂是___________。
④制备的反应原理是:当反应中转移电子总数约为时,则生成的物质的量为_________mol。
(4)纳米铁粉可用于处理废水中的。酸性条件下,纳米铁粉与废水中反应生成Fe3+与,其反应的离子方程式是________________。
20.(12分)烃A(结构简式:)是有机化学工业的基本原料,可从石油中获得。烃A可发生如下图所示的一系列化学反应。
请回答下列问题:
(l)B的分子式为__________,①的反应类型是__________。
(2)E的名称是_________,可鉴别A、E两种物质的试剂是__________________(填一种)。
(3)C是A通过加聚反应制得的有机高分子材料,其结构简式为_________。
(4)G的官能团是__________(填名称),D与F反应的化学方程式是___________。
南宁市2022-2023学年高二上学期9月开学质量调研
化学评分细则
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
题号 1 2 3 4 5 6 7 8 9 10
答案 C D C D B A C C C A
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要得求,全部选对得4分,选对但不全的得2分,有选错的得0分。
题号 11 12 13 14 15
答案 BC BD B BD C
16.评分细则
(1)第一空 F(1分)
细则:写成小写或名称给0分。
第二空:第3周期VIA族(2分)
细则:“3”写成“三”“Ⅲ”,“VIA族”写成“第六主族”、“第6主族”、“VI主族”均不扣分,其他情况给0分。
第三空:(1分)
细则:其他情况均给0分。
(2)(2分)
细则:写成“”也给2分,其余答案给0分。
(33)第一空:(1分)
细则:电子式写错或少电荷数均给0分。
第二空:离子键(1分)
细则:其他答案给0分
(4)CD(2分)
细则:选对一个给1分,选错一个倒扣1分,扣完为止。
(5)(2分)
细则:化学式正确但配平错误给1分;化学式错误给0分。
17.评分细则
I.(1)(2分)
细则:反应物生成物对,没配平或把可逆符号写成等号给1分,其他情况给0分。
(2)>(2分)
细则:填“大于”给2分,其他答案给0分。
(3)(2分)
细则:数字(含分数)和单位都正确给2分,数字正确单位错误或没写单位给1分,数字错误单位正确给0分,其他情况也给0分。
II.(1)AD(2分)
细则:选对一个给1分,选错一个倒扣1分,扣完为止。
(2)(2分)
细则:化学式正确但配平错误给1分;化学式错误给0分。
(3)50%(2分)
细则:写成“0.5”或“1/2”或化简后得到“0.5”给2分,其他给0分。
18.评分细则
(1)(2分)
细则:化学式正确但配平错误给1分;化学式错误给0分。反应条件不写或错误不扣分。
(2)第一空:碱石灰(1分)
细则:写成“NaOH和CaO的混合物”给1分,其他情况给0分。
第二空:球形干燥管(1分)
细则:写成“干燥管”给1分,其他情况给0分。
(3)①防止空气中的水分进入装置D干扰实验,②除去尾气氨气(2分)
细则:写成有除去氨气之意的给1分,写成有防止空气中的水蒸气进入干燥管(装置D)之意的给1分;其他情况给0分。
(4)①装置C中的黑色固体变为红色②装置D中的白色固体变为蓝色(2分)
细则:答出装置C的实验现象且正确给1分;答出装置D的实验现象且正确给1分。其他情况给0分。
(5)1:3(2分)
细则:写成“1/3”或“0.33”或化简后得到“0.33”给2分,其他情况给0分。
(6)取少量的样品于试管中,加入稀硫酸,若溶液中出现蓝色,说明红色固体产物中含有Cu2O,反之没有。(2分)
细则:操作正确给1分;现象描述正确给1分,不写结论不扣分;“硫酸”写成“盐酸或酸”且操作同样给1分,“硫酸”写成“硝酸”操作给0分。
19.评分细则
(1)A(1分)
细则:其他答案给0分
(2)BC(2分)
细则:选对一个给1分,选错一个倒扣1分,扣完为止。
(3)①第一空:H2SO4(1分)
细则:写成“稀H2SO4”给1分,其他答案给0分。
第二空:Cu(1分)
细则:写成“铜”或“金属铜”或“铜粉”给1分,其他答案不给分。
②引流(1分)
细则:有表达“引流”之意的给1分,如“让液体沿着玻璃棒流入漏斗中”等。
③KSCN溶液(2分)
细则:写成“硫氰化钾溶液”给2分,“硫氰化钾”或“KSCN”给1分,其他答案给0分。
④0.3mol(2分);
细则:写成“0.3”或“3/10”给2分,数字正确多写单位且正确不扣分,数字正确多写单位但单位错误给1分,其他答案给0分。
(4)(2分)
细则:化学式正确但配平错误给1分;化学式错误给0分。
20.(12分)
(1)第一空:C3H6Br2(2分)
细则:写成结构简式、结构式均给0分。
第二空:加成反应(1分)
细则:写成“加成”给2分,若有多答以第一个答案为准给分,其他答案给0分。
(2)第一空:丙烷(1分)
细则:其他答案均给0分。
第二空:溴水(或溴的CCl4溶液或酸性高锰酸钾溶液)(2分)
细则:答任意一种试剂且正确给2分,若有其他合理答案也给2分。
(3)(2分)
细则:写成或结构简式中少氢原子或甲基位置错误均给0分。
(4)第一空:碳碳双键、酯基(2分)
细则:写成结构简式或结构式不得分,答对一个给1分,多答以第一、第二个答案为准给分。
第二空:(2分)
细则:
①有机物结构简式都写对,不写可逆符号(写等号或箭头),不扣分;
②有机物结构简式都写对,不写反应条件或反应条件写错,不扣分;
③少写H2O,给1分;
④有机物结构简式写分子式给0分。
化学
注意事项:
1.本试卷满分100分,考试时间90分钟。
2.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑;非选择题请用直径0.5毫米黑色墨水签字笔在答题卡上各题的答题区域内作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
可能用到的相对原子质量:O-16 Na-23
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
1.“十四五”时期生态文明建设强调绿色发展、减少碳排放和改善生态环境质量。下列关于碳排放的说法错误的是( )
A.我国科学家利用CO2合成淀粉,能促进实现2030年“碳达峰”的目标
B.大力推进新能源汽车代替传统燃油汽车,有利于实现“碳中和”,改善生态环境
C.通过煤的干馏、煤的气化和煤的液化,可以从根本上杜绝碳排放
D.积极开发使用风能、太阳能、生物能等新型能源,有利于减少碳排放
2.按照物质的组成分类,KIO3属于( )
A.氧化物 B.酸 C.碱 D.盐
3.在100ml小烧杯中加入40ml蒸馏水,将烧杯中蒸馏水加热至沸腾,向沸水中逐滴加入5~6滴FeCl3饱和溶液,继续煮沸至液体呈红褐色,停止加热,得到的分散系为( )
A.浊液 B.溶液 C.胶体 D.无法确定
4.下列与实验相关的操作或方案正确的是( )
A.配制一定物质的量浓度的溶液 B.组成Zn-Cu原电池 C.实验室制取乙酸乙酯 D.比较S、C、Si的非金属性强弱
A.A B.B C.C D.D
5.下列离子方程式中,正确的是( )
A.将铜片插入溶液中:
B.将醋酸滴在石灰石上:
C.将一块绿豆大的钠放入水中:
D.将硝酸银溶液与氯化钠溶液混合:
6.下列说法错误的是( )
A.在化学反应过程中,发生物质变化的同时不一定发生能量变化
B.化学键的断裂与形成是化学反应中能量变化的主要原因
C.当生成物总能量高于反应物总能量时,反应吸热
D.化学反应能量变化多少与反应物和生成物的聚集状态有关
7.2021年12月9日,我国宇航员在中国空间站直播了泡腾片水球实验。泡腾片中含有柠檬酸(结构如图所示)等物质。下列说法错误的是( )
A.柠檬酸的分子式为
B.1mol柠檬酸最多可消耗3molNaOH
C.柠檬酸分子中有3种官能团
D.一定条件下可发生氧化、取代反应
8.下列实验操作对应的现象和结论均正确的是( )
选项 实验操作 现象 结论
A 将铜片放入盛有稀硝酸的试管中 试管口出现红棕色气体 铜片与稀硝酸反应产生NO2
B 向盛有无色透明溶液的试管中滴加澄清石灰水 生成白色沉淀 溶液中一定存在
C 向盛有少量蔗糖的烧杯中加入几滴水,再加入适量浓硫酸,搅拌 蔗糖变黑,体积膨胀,产生有刺激性气味的气体 浓硫酸具有脱水性和强氧化性
D 加热盛有NH4Cl固体的试管 试管底部固体消失,试管口有晶体凝结 NH4C1固体可以升华
9.一定条件下,在恒容密闭容器中,能表示反应一定达到化学平衡状态的是( )
A.单位时间内生成2nmolSO3,同时消耗nmolO2
B.SO2、O2、SO3的物质的量之比为2:1:2
C.SO2、O2、SO3的浓度不再发生变化
D.容器中的气体密度不再发生变化
10.为阿伏加德罗常数的值,下列说法正确的是( )
A.0.1molCl2与铁完全反应转移电子数目为0.2
B.11.2L乙烯气体中所含碳氢键数目为2
C.溶液中含有的Na+数目为0.1
D.固体中阴离子数目为0.2
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要求,全部选对得4分,选对但不全的得2分,有选错的得0分。
11.电化学气敏传感器可用于监测环境中NH3的含量,其工作原理示意图如图所示。该电池工作时,下列说法正确的是( )
A.电极(a)为正极
B.NH3在电极(a)_上发生氧化反应
C.电子由电极(a)经导线移动向电极(b)
D.K+向电极(a)移动
12.短周期主族元素X、Y、Z、W在元素周期表中的位置如图所示,Y原子最外层电子数是其电子层数的3倍。下列关于这四种元素及其化合物的说法中正确的是( )
A.X、Y、z、W中可能存在金属元素
B.化合物ZW2分子中所有原子都达到8电子稳定结构
C.气态氢化物的稳定性:Z>W>X>Y
D.Y、Z可形成具有漂白性的化合物
13.下列物质的制备与工业生产不相符的是( )
A.NH3NOHNO3
B.海水→MgOMg
C.饱和食盐水
D.石油乙烯聚乙烯塑料
14.室温下,下列各组离子在指定条件下一定能大量共存的是( )
A.与铝反应产生氢气的溶液:
B.无色透明溶液:
C.pH=1的溶液:
D.新制饱和氯水:
15.科学家发现某些生物酶体系可以促进和的转移(如a、b和c),能将海洋中的转化为N2进入大气层,反应过程如图所示。下列说法正确的是( )
A.过程I中NO为氧化产物
B.过程II中每生成1molN2转移6mol电子
C.过程II的离子方程式:
D.过程II中发生还原反应
三、非选择题:本题共5小题,共60分。
16.(12分)部分短周期元素的原子序数与主要化合价的关系如图所示:
请回答下列问题:
(1)元素a~j中非金属性最强的是__________(填元素符号),元素i在元素周期表中的位置为__________,j的原子结构示意图为___________。
(2)b、d、e、j四种元素的简单离子半径的大小顺序为__________(填元素符号)。
(3)元素e与j形成化合物,其电子式为___________,所含化学键的类型为__________。
(4)b的同主族元素碲(Te)与碘元素同周期,下列有关说法正确的是___________
A.单质碲在常温下是液体
B.酸性:
C.稳定性:
D.和互为同位素
(5)f元素的氧化物与氢氧化钠溶液反应的离子方程式为_____。
17.(12分)
I.某温度时,在2L的密闭容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。
请回答下列问题:
(1)该反应的化学反应方程式为___________。
(2)1min时,Y的正反应速率_________Y的逆反应速率(填“>”“<”或“=”)
(3)反应从开始至2min,用X的浓度变化表示的平均反应速率为__________。
II.油气开采、石油化工、煤化工等行业废气普遍含有硫化氢,通常将其回收生产硫单质(S2)。目前较为普遍的方法是克劳斯工艺和高温热分解H2S,克劳斯工艺的原理是利用以下两步反应生产单质硫:
①
②
请回答下列问题:
(1)下列措施可以加快反应②的速率的是__________。
A.升高温度
B.保持容积不变,充入N2使体系压强增大
C.及时从体系中分离出S2(g)
D.加入合适的催化剂
(2)高温热分解H2S的化学反应方程式是_______________________。
(3)在1470K、100kPa反应条件下,在一容积为2L的恒容容器中充入1molH2S进行高温热分解反应,反应5分钟后达到平衡,平衡时混合气体中H2S与H2的物质的量相等,H2S平衡转化率为_____________。
18.(12分)某校化学研究学习小组设计实验验证NH3能还原CuO,实验装置如下图。
请回答下列问题:
(1)A装置中反应的化学方程式为____________。
(2)B装置中盛放的试剂是_________;D装置仪器的名称为_____________。
(3)甲同学认为该实验装置不严谨,应在装置D后连接一个盛有浓硫酸的试剂瓶,其目的是____________。
(4)证明NH3能与CuO反应的实验现象是__________________。
(5)若NH3还原CuO的还原产物唯一且生成无毒无污染气体,则C反应中氧化产物与还原产物的物质的量之比为__________________。
(6)已知该反应受NH3用量和反应温度影响,有时会生成副产物Cu2O,Cu2O为砖红色,易对实验结论产生干扰。已知Cu2O在酸性溶液中不稳定:,请设计实验方案验证CuO完全反应后的红色固体产物中是否含有Cu2O________________。
19.(12分)金属及其化合物在生产生活中占有极其重要的地位,请结合金属及其化合物的相关知识回答下列问题:
(1)目前使用量最大的合金是____________。
A.钢 B.青铜 C.镁合金 D.铝合金
(2)某溶液中有Mg2+、Fe2+、Al3+、Cu2+等离子,向其中加入足量的Na2O2后,过滤,将滤渣投入足量的盐酸中,所得溶液与原溶液相比,溶液中大量减少的阳离子是__________。
A.Mg2+ B.Fe2+ C.A13+ D.Cu2+
(3)高铁酸钠()是一种新型水处理剂。某兴趣小组欲利用废金属屑(主要成分为Fe和Cu,含有少量)制取高铁酸钠并回收金属Cu,其工艺流程如下:
①试剂a为__________(填化学式,下同),滤渣II的主要成分为_________。
②在过滤操作中要使用玻璃棒,其作用是__________。
③检验滤液I中是否存在Fe3+的试剂是___________。
④制备的反应原理是:当反应中转移电子总数约为时,则生成的物质的量为_________mol。
(4)纳米铁粉可用于处理废水中的。酸性条件下,纳米铁粉与废水中反应生成Fe3+与,其反应的离子方程式是________________。
20.(12分)烃A(结构简式:)是有机化学工业的基本原料,可从石油中获得。烃A可发生如下图所示的一系列化学反应。
请回答下列问题:
(l)B的分子式为__________,①的反应类型是__________。
(2)E的名称是_________,可鉴别A、E两种物质的试剂是__________________(填一种)。
(3)C是A通过加聚反应制得的有机高分子材料,其结构简式为_________。
(4)G的官能团是__________(填名称),D与F反应的化学方程式是___________。
南宁市2022-2023学年高二上学期9月开学质量调研
化学评分细则
一、选择题:本题共10小题,每小题2分,共20分。每小题只有一个选项符合题目要求。
题号 1 2 3 4 5 6 7 8 9 10
答案 C D C D B A C C C A
二、选择题:本题共5小题,每小题4分,共20分。每小题有一个或两个选项符合题目要得求,全部选对得4分,选对但不全的得2分,有选错的得0分。
题号 11 12 13 14 15
答案 BC BD B BD C
16.评分细则
(1)第一空 F(1分)
细则:写成小写或名称给0分。
第二空:第3周期VIA族(2分)
细则:“3”写成“三”“Ⅲ”,“VIA族”写成“第六主族”、“第6主族”、“VI主族”均不扣分,其他情况给0分。
第三空:(1分)
细则:其他情况均给0分。
(2)(2分)
细则:写成“”也给2分,其余答案给0分。
(33)第一空:(1分)
细则:电子式写错或少电荷数均给0分。
第二空:离子键(1分)
细则:其他答案给0分
(4)CD(2分)
细则:选对一个给1分,选错一个倒扣1分,扣完为止。
(5)(2分)
细则:化学式正确但配平错误给1分;化学式错误给0分。
17.评分细则
I.(1)(2分)
细则:反应物生成物对,没配平或把可逆符号写成等号给1分,其他情况给0分。
(2)>(2分)
细则:填“大于”给2分,其他答案给0分。
(3)(2分)
细则:数字(含分数)和单位都正确给2分,数字正确单位错误或没写单位给1分,数字错误单位正确给0分,其他情况也给0分。
II.(1)AD(2分)
细则:选对一个给1分,选错一个倒扣1分,扣完为止。
(2)(2分)
细则:化学式正确但配平错误给1分;化学式错误给0分。
(3)50%(2分)
细则:写成“0.5”或“1/2”或化简后得到“0.5”给2分,其他给0分。
18.评分细则
(1)(2分)
细则:化学式正确但配平错误给1分;化学式错误给0分。反应条件不写或错误不扣分。
(2)第一空:碱石灰(1分)
细则:写成“NaOH和CaO的混合物”给1分,其他情况给0分。
第二空:球形干燥管(1分)
细则:写成“干燥管”给1分,其他情况给0分。
(3)①防止空气中的水分进入装置D干扰实验,②除去尾气氨气(2分)
细则:写成有除去氨气之意的给1分,写成有防止空气中的水蒸气进入干燥管(装置D)之意的给1分;其他情况给0分。
(4)①装置C中的黑色固体变为红色②装置D中的白色固体变为蓝色(2分)
细则:答出装置C的实验现象且正确给1分;答出装置D的实验现象且正确给1分。其他情况给0分。
(5)1:3(2分)
细则:写成“1/3”或“0.33”或化简后得到“0.33”给2分,其他情况给0分。
(6)取少量的样品于试管中,加入稀硫酸,若溶液中出现蓝色,说明红色固体产物中含有Cu2O,反之没有。(2分)
细则:操作正确给1分;现象描述正确给1分,不写结论不扣分;“硫酸”写成“盐酸或酸”且操作同样给1分,“硫酸”写成“硝酸”操作给0分。
19.评分细则
(1)A(1分)
细则:其他答案给0分
(2)BC(2分)
细则:选对一个给1分,选错一个倒扣1分,扣完为止。
(3)①第一空:H2SO4(1分)
细则:写成“稀H2SO4”给1分,其他答案给0分。
第二空:Cu(1分)
细则:写成“铜”或“金属铜”或“铜粉”给1分,其他答案不给分。
②引流(1分)
细则:有表达“引流”之意的给1分,如“让液体沿着玻璃棒流入漏斗中”等。
③KSCN溶液(2分)
细则:写成“硫氰化钾溶液”给2分,“硫氰化钾”或“KSCN”给1分,其他答案给0分。
④0.3mol(2分);
细则:写成“0.3”或“3/10”给2分,数字正确多写单位且正确不扣分,数字正确多写单位但单位错误给1分,其他答案给0分。
(4)(2分)
细则:化学式正确但配平错误给1分;化学式错误给0分。
20.(12分)
(1)第一空:C3H6Br2(2分)
细则:写成结构简式、结构式均给0分。
第二空:加成反应(1分)
细则:写成“加成”给2分,若有多答以第一个答案为准给分,其他答案给0分。
(2)第一空:丙烷(1分)
细则:其他答案均给0分。
第二空:溴水(或溴的CCl4溶液或酸性高锰酸钾溶液)(2分)
细则:答任意一种试剂且正确给2分,若有其他合理答案也给2分。
(3)(2分)
细则:写成或结构简式中少氢原子或甲基位置错误均给0分。
(4)第一空:碳碳双键、酯基(2分)
细则:写成结构简式或结构式不得分,答对一个给1分,多答以第一、第二个答案为准给分。
第二空:(2分)
细则:
①有机物结构简式都写对,不写可逆符号(写等号或箭头),不扣分;
②有机物结构简式都写对,不写反应条件或反应条件写错,不扣分;
③少写H2O,给1分;
④有机物结构简式写分子式给0分。
同课章节目录
