第四章 环烃
图片预览




文档简介
课件65张PPT。第四章 环烃2主 要 内 容4.1 脂环烃
一、环烷烃命名、结构
二、环己烷及其衍生物构象
三、脂环烃性质
四、金刚烷 4.2 芳香烃
一、芳香烃分类及命名
二、单环芳烃
三、稠环芳烃
4.3 煤焦油和石油31、掌握环烃的命名,分子结构,环烷烃取代与开环反应;苯
的结构及芳香性,闭合共轭体系及大π键,苯环亲电取代
反应及其定位法则与电子效应,苯同系物侧链卤代与氧 化。
2、熟悉环己烷及其衍生物的优势构象,环烷烃的稳定性,萘,
蒽,菲及环戊烷多氢菲的结构,萘的取代反应与加氢反应。
3、了解十氢化萘的构象,苯及其主要同系物,萘,蒽,菲的
物理性质;萘,蒽,菲的氧化反应;致癌烃,煤焦油和石
油的基本知识。 教学目的要求 4.1 脂环烃一、脂环烃的分类、同分异构和命名(一)分类 1. 按饱和程度可分为:环烷烃、环烯烃、环炔烃 2. 按环大小可分为:大环(12个以上C原子的环);
中环(8-11个C原子的环);
一般环(5-7个C原子的环);
小环(3-4个C原子的环)。 3. 按碳环的数目可分为:
单环;
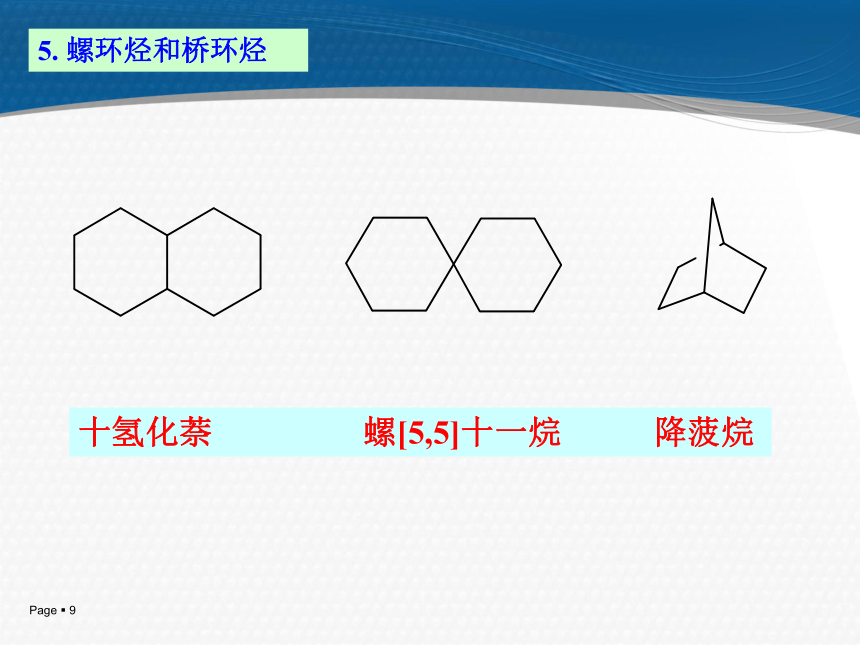
桥环(两个环共用两个C原子);
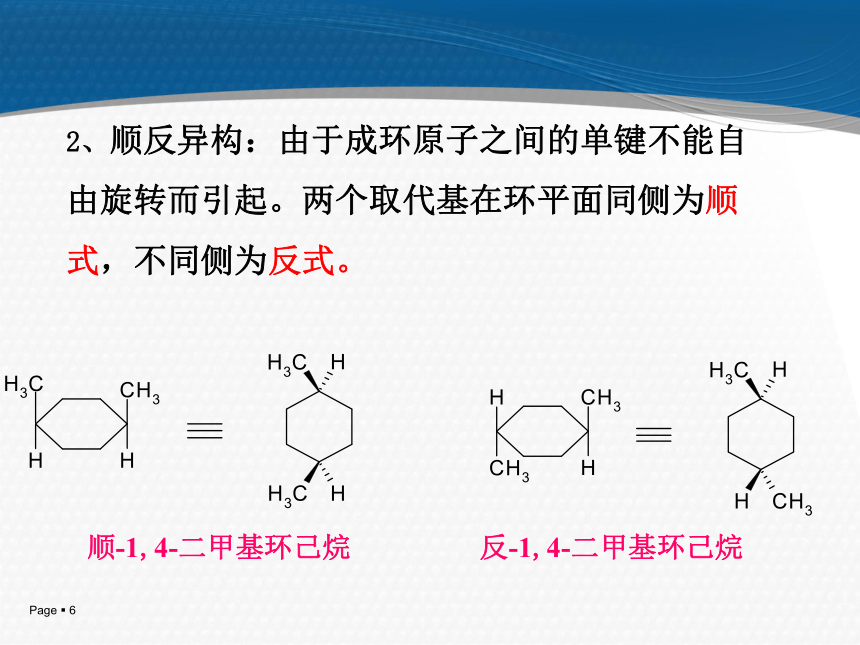
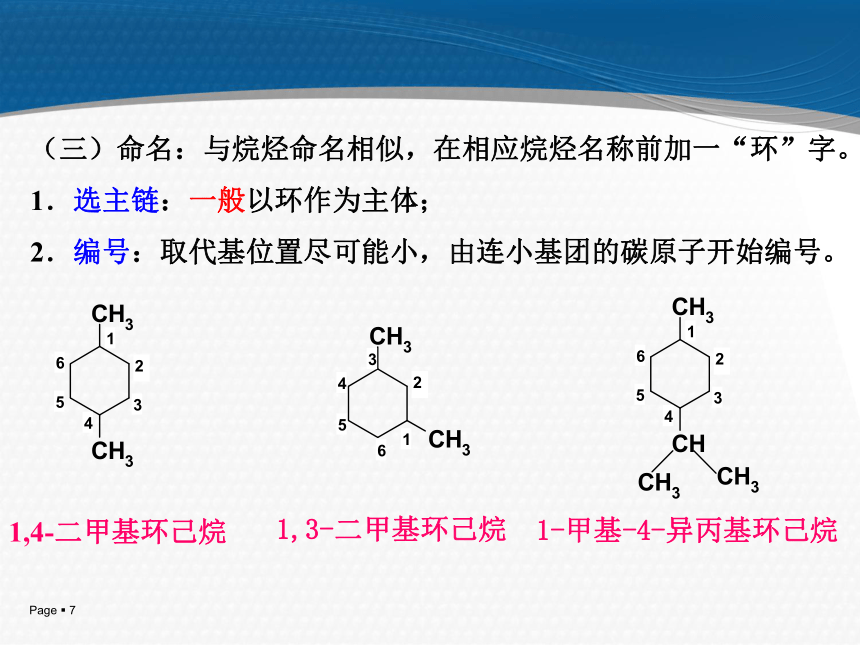
螺环(两个环共用一个C原子)。碳骨架异构和立体顺反异构: 1、碳骨架异构 如:C8H16 (二)同分异构2、顺反异构:由于成环原子之间的单键不能自由旋转而引起。两个取代基在环平面同侧为顺式,不同侧为反式。 顺-1,4-二甲基环己烷 反-1,4-二甲基环己烷 (三)命名:与烷烃命名相似,在相应烷烃名称前加一“环”字。
1.选主链:一般以环作为主体;
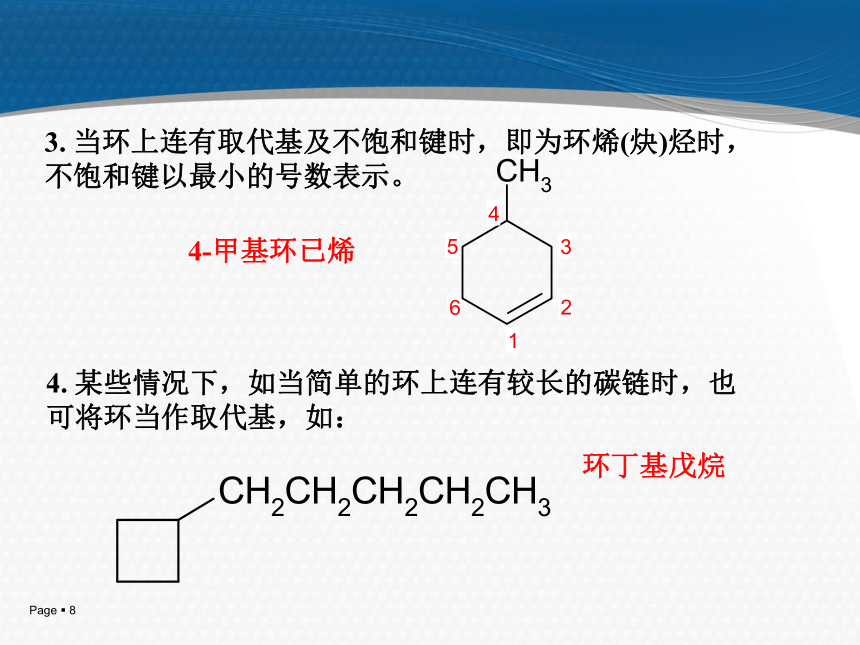
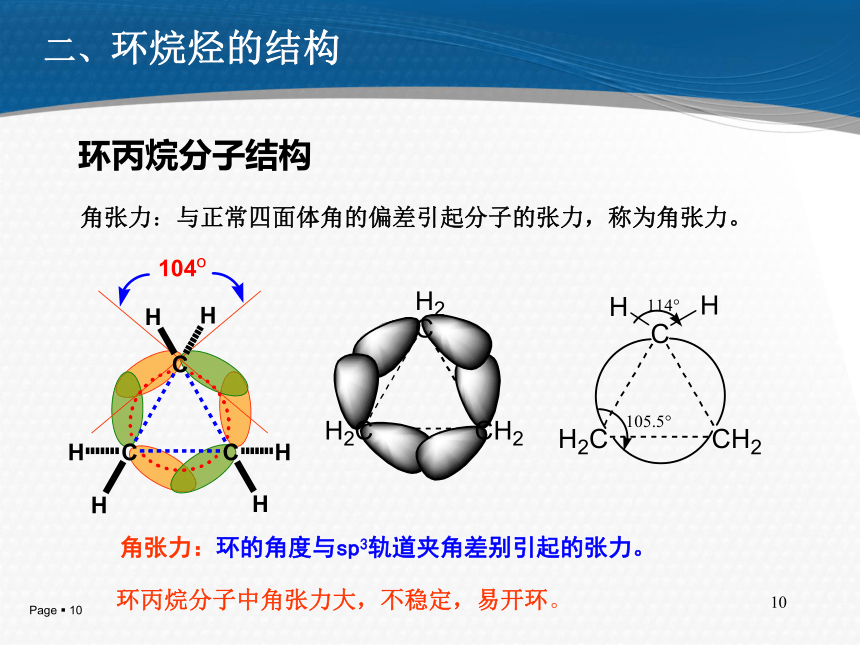
2.编号:取代基位置尽可能小,由连小基团的碳原子开始编号。 1,4-二甲基环己烷 1,3-二甲基环己烷 1-甲基-4-异丙基环己烷 4. 某些情况下,如当简单的环上连有较长的碳链时,也可将环当作取代基,如:环丁基戊烷3. 当环上连有取代基及不饱和键时,即为环烯(炔)烃时,不饱和键以最小的号数表示。4-甲基环已烯十氢化萘 螺[5,5]十一烷 降菠烷5. 螺环烃和桥环烃10环丙烷分子结构环丙烷分子中角张力大,不稳定,易开环。 角张力:与正常四面体角的偏差引起分子的张力,称为角张力。二、环烷烃的结构角张力:环的角度与sp3轨道夹角差别引起的张力。11(1)环的稳定性:环戊烷> 环丁烷 >环丙烷
(2)环戊烷、环己烷分子中的碳原子不在一个平面上,碳碳σ键
的夹角 接近或保持109.5°,分子中既无角张力,又无扭转
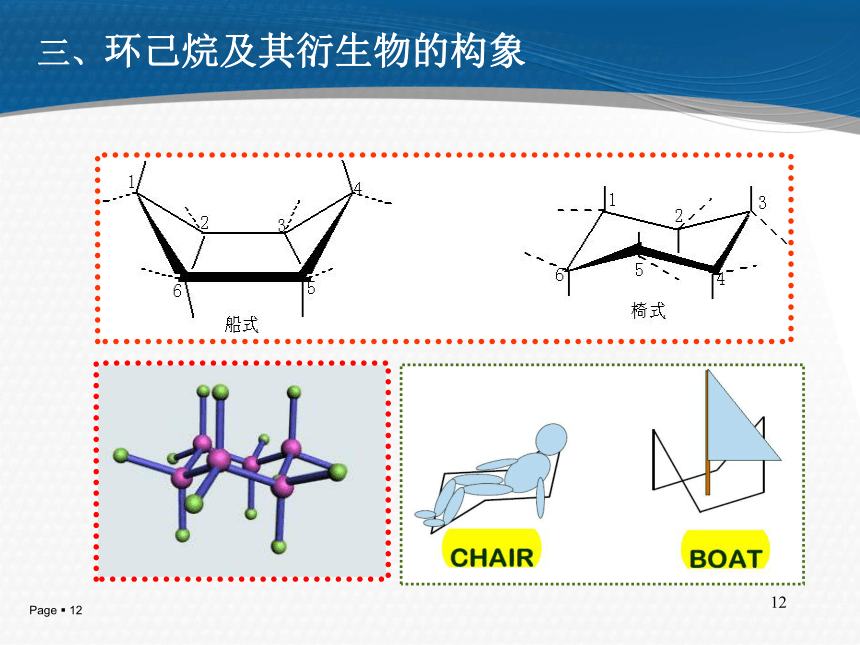
张力,所以都比较稳定。结论:环丁烷与环戊烷分子结构12三、环己烷及其衍生物的构象如何画环己烷优势构象六条线两两相平行;
六个碳原子交替分布
在两个平面上;
每个碳上的两个C-H
键,一a键,一e键,
必须一上,一向下;
相邻碳上的a键和e键
为顺式,相同碳上a
键(或e键)为反式。俩俩平行且等长141.环已烷的构象①椅式构象投影式 透视式 ②船式构象 透视式 投影式 ④a 键和e 键 在椅式构象中的两种类型。 ③椅式与船式 椅式是稳定的构象162.取代环已烷的构象 ①取代基在e 键上的是稳定构象。②二取代环已烷:e 键取代基多的构象是稳定的。 ③取代环已烷:e键取代基越多的构象越稳定。④环有不同取代基时,大的取代基在e键的构象最稳定。17四、化学性质 1.开环反应①催化加氢②加卤素“大环似烷,小环似烯”18 2.氧化反应①? (了解) 环烯烃可被KMnO4,O3等氧化,和烯烃相似。 ② 环烷烃在一般条件下与KMnO4,O3不起反应。
环丙烷虽然易起开环加成反应,但对氧化剂是稳定的。19五、金刚烷204.2 芳香烃芳香烃的分类单环芳烃的构造异构和命名 1.? 烃基取代芳烃 ①一烃基苯只有一种,没有异构体。
▲ 以苯环作为母体,把烷基作为取代基。
▲ 以不饱和烃当作母体,把苯环作为取代基。22 ②二烃基苯有三种异构体,是由于取代基在苯环的相对位置而产生的。 ③ 三烃基苯,也有三种异构体。23 ⑤ 芳基 ④?复杂烃基苯的衍生物,可把苯环当作取代基命名。苄基 2.? 其它取代的芳烃衍生物 ① 作为取代基的有:R,NO2,X。 ② 作为母体的取代基有:-NH2,-OH,-CHO,-COOH,-SO3H。 25多环芳香烃命名(1)联苯类:苯环之间以一单键相连 二联苯 1,4-联三苯(2)多苯代脂肪烃:看作脂肪烃分子中的氢原子被苯环取代的产物二苯甲烷(3)稠环芳烃:指分子中含两个或两个以上苯环,且苯环之间
共用两个相邻的碳原子结合的芳烃。萘 蒽 菲26一、单环芳烃1、苯的分子式为C6H6,碳氢数目比为1:1,应具有高度
不饱和性。
2、但事实上,苯在一般条件下,不能被高锰酸钾等氧化剂
氧化,也不能与卤素、卤化氢等进行加成反应,
3、但它却容易发生取代发应。
4、并且苯环具有较高的热稳定性。
5、像苯环表现出的对热较稳定,不易发生加成、氧化,而
易进行取代的特性,被称之为芳香性。(一)苯的结构271865年,凯库勒提出苯的环状对称结构式。 1、苯的凯库勒式可以说明苯分子的组成及原子相互连接次
序,并表明碳原子是四价的,六个氢原子的位置等同,
因而可以解释苯的一元取代产物只有一种的事实。
2、但不能解释苯的邻位二元取代产物只有一种的实验事实。
按凯库勒式推测苯的邻位二元取代产物,应有以下两种:凯库勒式不能表明苯的真实结构 说明杂化理论:碳原子都是sp2杂化,每个碳原子都以三个sp2杂化轨道分别与碳和氢形成三个σ键,平面结构。每个碳余下的未参加杂化的p轨道垂直于平面且相互平行、重叠,形成了环闭的共轭体系。
p轨道重叠程度完全相等,形成一个环状的离域的π电子云,如两个轮胎,分布在分子平面的上下两侧。29近代物理方法测定,分子中六个碳和六个氢都在同一平面,碳-碳键长均相等(0.1396nm),六个碳组成一正六边形,所有键角均120° σ键形成30六个碳原子完全等同,所以大键电子云在六个碳原子之间均匀分布,即电子云分布完全平均化,因此碳-碳键长完全相等,不存在单双键之分。由于苯环共轭大π键高度离域,使分子能量大大降低,因此苯环具有高度的稳定性。 π 键的形成非苯芳香烃(补充)Hückel规则:
芳香性:环稳定,易取代,难加成。Hückel规则:环多烯化合物中,具有共平面的离域体系,其π电子数等于4n+2(n=0,1,2,3…)
,此化合物具有芳香性。2个p电子,具有芳香性 6个p电子,具有芳香性 32(二)性质 1.物理性质 ①苯系芳烃具有一定的毒性。和苯长期接触会导致
慢性中毒。
②一般为无色有芳香气味的液体。不溶于水。
密度小于1,在0.86-0.93之间。
③燃烧时火焰带有较浓的黑烟。
④是良好的有机溶剂。
2 .化学性质 ①?取代反应 卤代 条件:催化加热卤代 F2 > Cl2 > Br2 > I2注意反应条件对产物的影响34硝化 磺化 35傅氏反应 (1)傅氏烷基化反应 a.催化剂:无水三氯化铝等
b.烷基化试剂:常用的有R-X、醇、烯c.烷基超过两个C原子时,烷基碳链经常发生重排得到的产物不纯。 d.当苯环上连有强的吸电子基时,一般不发生烷基化反应。36(2)傅氏酰基化反应: a.酰基化试剂:一般用酰氯或酸酐。
b.催化剂:常用三氯化铝
c. 不发生重排。37 ②加成反应 加H2 加Cl2 ③氧化反应 苯环氧化 顺丁烯二酸酐38侧链氧化 注意:可鉴别烷基苯和苯39(三)苯环亲电取代反应历程40 1.? 卤代反应历程 2 .? 硝化反应历程42 3. 磺化反应历程43 4.傅氏反应历程44(四)苯环上取代基的定位规律甲苯进行硝化反应时,硝基主要进入甲基的邻位和对位,并且该硝化反应比苯容易。硝基苯再进行硝化反应时,硝基主要进入原硝基的间位,并且该硝化反应比苯困难。45苯环上已有的取代基不仅影响第二个取代基进入苯环的难易,而且还影响其进入苯环的位置。我们把苯环上原有取代基的这种作用,称为苯环上亲电取代反应的定位效应,苯环上原有的取代基称为定位基。 结论46第一类:邻、对位定位基(邻 + 对 > 60% ) 特点:与苯环相连的原子一般只连有单键,有的具有孤对电子或带负电荷第一类定位基能使苯环活化,即第二个取代基的进入比苯容易(卤素除外);第二个取代基主要进入它的邻位和对位。 ①?定位基的分类第二类:间位定位基(间> 40%)。特点:与苯环直接相连的原子带正电荷,或以重键与电负性较强的原子相连接。这类定位基能使苯环钝化,即第二个取代基的进入比苯困难,同时使第二个取代基主要进入它的间位。 48[注意] a.定位规则仅能指出反应的主要产物,还有少量进入它位置的产物生成。 b.同一个一元取代苯在不同的反应中,得到的二元取代产物异构体的比例不同
c.同一个一元取代苯,进行同样的取代反应,当反应条件不同时,二元取代产
物异构体的比例也不相同。d. 反应温度和催化剂不同,对异构体分布的影响。49 ② 第三个取代基的引入位置是依据原二个定位基性质而定。 a.两个定位基属于同类,第三个取代基主要进入的位置决定于受强的定位基影响。 b.两个定位基属于不同类,第三个取代基主要进入的位置决定于邻、对位基。因为邻、对位基定位能力强于间位基。(五)定位规律与电子效应1.诱导效应诱导效应:由于分子中电负性不同的原子或基团的影响,共用电子对偏向于电负性较大的原子,使之带有部分负电荷,另一原子则带有部分正电荷。在静电引力作用下,这种影响能沿着分子链诱导传递,使整个分子中成键的电子云向着一个方向偏移,使分子发生极化的效应,叫诱导效应 。 诱导效应的特点:
由电负性不同而引起
不存在极性交替现象
沿原子链传递,随传递距离增加而迅速减弱 +I效应:烷基、带负电荷的基团O-等
-I效应:-X、-NO2、-OH、-COOH、-CH=CH2等、带正电荷的基团-+NHR3 由原子或基团的电负性决定。
比氢原子电负性大的原子或基团表现出吸电性,称为吸电子基,具有亲电诱导效应,一般用–I表示;比氢原子电负性小的原子或基团表现出供电性,称为供电子基,具有给电子诱导效应,一般用+I表示。2. 共轭效应53甲基通过给电子作用,可分散正电荷,使碳正离子比较稳定。 ①? 取代基对苯环致活、致钝的解释 硝基吸电子作用,使中间体碳正离子的正电荷增加,导致碳正离子更不稳定,反应较慢。 ②?邻、对位定位基 除卤素外,其它邻、对位基都使邻、对位电荷密度增加,亲电试剂必然进攻电子云密度大的邻、对位,而且比苯容易进行取代。 a. 甲基 b. 氨基和羟基 ⅰ.诱导效应使苯环电子云密度降低(-I)。
ⅱ.p-π共轭,O原子上孤对电子与苯环的π电子发生p-π共轭,氧原子上电子云向苯环转移,使苯环电子云密度增加(+C)。由于+C>-I,总的结果电荷密度增加。55 c. 卤素原子 ⅰ.-I; ⅱ.+C
结果:-I>+C 使苯环的电子云密度降低,亲电反应比苯难。 ③? 间位定位基56选择适当的合成路线 3 、 定位规则的应用二、稠环芳烃 (一)萘 1. 结构 分子式:C10H858 ① 取代反应 卤代 硝化 磺化 2 . 性质59 萘环上的定位规则 如萘环上的α位上已有一个第一定位基,第二个取代基进入萘环的4位(多)和2位(少)。 如萘环上β位有第一类定位基,第二个取代基主要进入1位。 如萘环上α或β位上有第二类定位基,第二个取代基主要进入另一个苯环的5、8位。60 ②?加成反应 ③ 氧化反应 比苯容易。61 (二) 蒽和菲9、10位相同称γ-位;
1、4、5、8位称α-位;
2、3、6、7位称β-位。 1和8相同;2和7相同;
3和6相同;4和5相同;
9和10相同。 1. 主要存于煤焦油中,分子式C14H10,是同分异构体。2. 结构 氧化还原反应发生在9.10位 (三) 致癌芳烃(自学)(四)石墨和C60 (自学) 1.石墨:层状,由一层层无数的苯环并联而成的碳的另一种同素异形体。 2.C60:1985年合成,由60个C以20个元环及12五元环连接成的似足球状空心对称分子。三、煤焦油和石油(自学) (一) 煤焦油将煤焦油进行分馏,可得到下列馏分: 1. 轻油:170℃以下的馏分。比水轻,主要组分是苯、甲苯、二甲苯等。
2.中油:170-230℃间的馏分。比重近于1,主要组分是萘、苯酚、甲苯酚、吡啶等。
3. 重油:230-270℃间的馏分。比水重,主要组分是萘、甲苯酚、喹啉等。
4. 蒽油(绿油):270-360℃间的馏分。比水重,主要组分是蒽、菲、咔唑等。64 (二)石油 1.石油的形成: 2. 石油的化学组成很复杂。有机物的富集是生成石油的内在根据,适当的成油环境是生成石油的外部条件。 主要元素:C和H,C约占83-87%,H约占11-14%,其它元素含量在1%以下。 3.分类? 按结构可分为 :烷烃石油(大庆油)、环烷烃石油(胜利油)等。 按化学组成可分为 :石蜡基石油、沥青基石油、混合基石油。 4.资源丰富 例:将1吨石油裂解,可得二百多公斤乙烯。
将1吨煤炼焦,从焦炉气中只能提取五公斤乙烯 基本有机化工原料: 三烯:乙烯、丙烯、丁二烯。
三苯:苯、甲苯、二甲苯。 一炔:乙炔。 一萘:萘。 5.石油与生物。作业P76 4.3a,f,g;P77 4.4; P78 4.10; P78 4.11;P78 4.14
一、环烷烃命名、结构
二、环己烷及其衍生物构象
三、脂环烃性质
四、金刚烷 4.2 芳香烃
一、芳香烃分类及命名
二、单环芳烃
三、稠环芳烃
4.3 煤焦油和石油31、掌握环烃的命名,分子结构,环烷烃取代与开环反应;苯
的结构及芳香性,闭合共轭体系及大π键,苯环亲电取代
反应及其定位法则与电子效应,苯同系物侧链卤代与氧 化。
2、熟悉环己烷及其衍生物的优势构象,环烷烃的稳定性,萘,
蒽,菲及环戊烷多氢菲的结构,萘的取代反应与加氢反应。
3、了解十氢化萘的构象,苯及其主要同系物,萘,蒽,菲的
物理性质;萘,蒽,菲的氧化反应;致癌烃,煤焦油和石
油的基本知识。 教学目的要求 4.1 脂环烃一、脂环烃的分类、同分异构和命名(一)分类 1. 按饱和程度可分为:环烷烃、环烯烃、环炔烃 2. 按环大小可分为:大环(12个以上C原子的环);
中环(8-11个C原子的环);
一般环(5-7个C原子的环);
小环(3-4个C原子的环)。 3. 按碳环的数目可分为:
单环;
桥环(两个环共用两个C原子);
螺环(两个环共用一个C原子)。碳骨架异构和立体顺反异构: 1、碳骨架异构 如:C8H16 (二)同分异构2、顺反异构:由于成环原子之间的单键不能自由旋转而引起。两个取代基在环平面同侧为顺式,不同侧为反式。 顺-1,4-二甲基环己烷 反-1,4-二甲基环己烷 (三)命名:与烷烃命名相似,在相应烷烃名称前加一“环”字。
1.选主链:一般以环作为主体;
2.编号:取代基位置尽可能小,由连小基团的碳原子开始编号。 1,4-二甲基环己烷 1,3-二甲基环己烷 1-甲基-4-异丙基环己烷 4. 某些情况下,如当简单的环上连有较长的碳链时,也可将环当作取代基,如:环丁基戊烷3. 当环上连有取代基及不饱和键时,即为环烯(炔)烃时,不饱和键以最小的号数表示。4-甲基环已烯十氢化萘 螺[5,5]十一烷 降菠烷5. 螺环烃和桥环烃10环丙烷分子结构环丙烷分子中角张力大,不稳定,易开环。 角张力:与正常四面体角的偏差引起分子的张力,称为角张力。二、环烷烃的结构角张力:环的角度与sp3轨道夹角差别引起的张力。11(1)环的稳定性:环戊烷> 环丁烷 >环丙烷
(2)环戊烷、环己烷分子中的碳原子不在一个平面上,碳碳σ键
的夹角 接近或保持109.5°,分子中既无角张力,又无扭转
张力,所以都比较稳定。结论:环丁烷与环戊烷分子结构12三、环己烷及其衍生物的构象如何画环己烷优势构象六条线两两相平行;
六个碳原子交替分布
在两个平面上;
每个碳上的两个C-H
键,一a键,一e键,
必须一上,一向下;
相邻碳上的a键和e键
为顺式,相同碳上a
键(或e键)为反式。俩俩平行且等长141.环已烷的构象①椅式构象投影式 透视式 ②船式构象 透视式 投影式 ④a 键和e 键 在椅式构象中的两种类型。 ③椅式与船式 椅式是稳定的构象162.取代环已烷的构象 ①取代基在e 键上的是稳定构象。②二取代环已烷:e 键取代基多的构象是稳定的。 ③取代环已烷:e键取代基越多的构象越稳定。④环有不同取代基时,大的取代基在e键的构象最稳定。17四、化学性质 1.开环反应①催化加氢②加卤素“大环似烷,小环似烯”18 2.氧化反应①? (了解) 环烯烃可被KMnO4,O3等氧化,和烯烃相似。 ② 环烷烃在一般条件下与KMnO4,O3不起反应。
环丙烷虽然易起开环加成反应,但对氧化剂是稳定的。19五、金刚烷204.2 芳香烃芳香烃的分类单环芳烃的构造异构和命名 1.? 烃基取代芳烃 ①一烃基苯只有一种,没有异构体。
▲ 以苯环作为母体,把烷基作为取代基。
▲ 以不饱和烃当作母体,把苯环作为取代基。22 ②二烃基苯有三种异构体,是由于取代基在苯环的相对位置而产生的。 ③ 三烃基苯,也有三种异构体。23 ⑤ 芳基 ④?复杂烃基苯的衍生物,可把苯环当作取代基命名。苄基 2.? 其它取代的芳烃衍生物 ① 作为取代基的有:R,NO2,X。 ② 作为母体的取代基有:-NH2,-OH,-CHO,-COOH,-SO3H。 25多环芳香烃命名(1)联苯类:苯环之间以一单键相连 二联苯 1,4-联三苯(2)多苯代脂肪烃:看作脂肪烃分子中的氢原子被苯环取代的产物二苯甲烷(3)稠环芳烃:指分子中含两个或两个以上苯环,且苯环之间
共用两个相邻的碳原子结合的芳烃。萘 蒽 菲26一、单环芳烃1、苯的分子式为C6H6,碳氢数目比为1:1,应具有高度
不饱和性。
2、但事实上,苯在一般条件下,不能被高锰酸钾等氧化剂
氧化,也不能与卤素、卤化氢等进行加成反应,
3、但它却容易发生取代发应。
4、并且苯环具有较高的热稳定性。
5、像苯环表现出的对热较稳定,不易发生加成、氧化,而
易进行取代的特性,被称之为芳香性。(一)苯的结构271865年,凯库勒提出苯的环状对称结构式。 1、苯的凯库勒式可以说明苯分子的组成及原子相互连接次
序,并表明碳原子是四价的,六个氢原子的位置等同,
因而可以解释苯的一元取代产物只有一种的事实。
2、但不能解释苯的邻位二元取代产物只有一种的实验事实。
按凯库勒式推测苯的邻位二元取代产物,应有以下两种:凯库勒式不能表明苯的真实结构 说明杂化理论:碳原子都是sp2杂化,每个碳原子都以三个sp2杂化轨道分别与碳和氢形成三个σ键,平面结构。每个碳余下的未参加杂化的p轨道垂直于平面且相互平行、重叠,形成了环闭的共轭体系。
p轨道重叠程度完全相等,形成一个环状的离域的π电子云,如两个轮胎,分布在分子平面的上下两侧。29近代物理方法测定,分子中六个碳和六个氢都在同一平面,碳-碳键长均相等(0.1396nm),六个碳组成一正六边形,所有键角均120° σ键形成30六个碳原子完全等同,所以大键电子云在六个碳原子之间均匀分布,即电子云分布完全平均化,因此碳-碳键长完全相等,不存在单双键之分。由于苯环共轭大π键高度离域,使分子能量大大降低,因此苯环具有高度的稳定性。 π 键的形成非苯芳香烃(补充)Hückel规则:
芳香性:环稳定,易取代,难加成。Hückel规则:环多烯化合物中,具有共平面的离域体系,其π电子数等于4n+2(n=0,1,2,3…)
,此化合物具有芳香性。2个p电子,具有芳香性 6个p电子,具有芳香性 32(二)性质 1.物理性质 ①苯系芳烃具有一定的毒性。和苯长期接触会导致
慢性中毒。
②一般为无色有芳香气味的液体。不溶于水。
密度小于1,在0.86-0.93之间。
③燃烧时火焰带有较浓的黑烟。
④是良好的有机溶剂。
2 .化学性质 ①?取代反应 卤代 条件:催化加热卤代 F2 > Cl2 > Br2 > I2注意反应条件对产物的影响34硝化 磺化 35傅氏反应 (1)傅氏烷基化反应 a.催化剂:无水三氯化铝等
b.烷基化试剂:常用的有R-X、醇、烯c.烷基超过两个C原子时,烷基碳链经常发生重排得到的产物不纯。 d.当苯环上连有强的吸电子基时,一般不发生烷基化反应。36(2)傅氏酰基化反应: a.酰基化试剂:一般用酰氯或酸酐。
b.催化剂:常用三氯化铝
c. 不发生重排。37 ②加成反应 加H2 加Cl2 ③氧化反应 苯环氧化 顺丁烯二酸酐38侧链氧化 注意:可鉴别烷基苯和苯39(三)苯环亲电取代反应历程40 1.? 卤代反应历程 2 .? 硝化反应历程42 3. 磺化反应历程43 4.傅氏反应历程44(四)苯环上取代基的定位规律甲苯进行硝化反应时,硝基主要进入甲基的邻位和对位,并且该硝化反应比苯容易。硝基苯再进行硝化反应时,硝基主要进入原硝基的间位,并且该硝化反应比苯困难。45苯环上已有的取代基不仅影响第二个取代基进入苯环的难易,而且还影响其进入苯环的位置。我们把苯环上原有取代基的这种作用,称为苯环上亲电取代反应的定位效应,苯环上原有的取代基称为定位基。 结论46第一类:邻、对位定位基(邻 + 对 > 60% ) 特点:与苯环相连的原子一般只连有单键,有的具有孤对电子或带负电荷第一类定位基能使苯环活化,即第二个取代基的进入比苯容易(卤素除外);第二个取代基主要进入它的邻位和对位。 ①?定位基的分类第二类:间位定位基(间> 40%)。特点:与苯环直接相连的原子带正电荷,或以重键与电负性较强的原子相连接。这类定位基能使苯环钝化,即第二个取代基的进入比苯困难,同时使第二个取代基主要进入它的间位。 48[注意] a.定位规则仅能指出反应的主要产物,还有少量进入它位置的产物生成。 b.同一个一元取代苯在不同的反应中,得到的二元取代产物异构体的比例不同
c.同一个一元取代苯,进行同样的取代反应,当反应条件不同时,二元取代产
物异构体的比例也不相同。d. 反应温度和催化剂不同,对异构体分布的影响。49 ② 第三个取代基的引入位置是依据原二个定位基性质而定。 a.两个定位基属于同类,第三个取代基主要进入的位置决定于受强的定位基影响。 b.两个定位基属于不同类,第三个取代基主要进入的位置决定于邻、对位基。因为邻、对位基定位能力强于间位基。(五)定位规律与电子效应1.诱导效应诱导效应:由于分子中电负性不同的原子或基团的影响,共用电子对偏向于电负性较大的原子,使之带有部分负电荷,另一原子则带有部分正电荷。在静电引力作用下,这种影响能沿着分子链诱导传递,使整个分子中成键的电子云向着一个方向偏移,使分子发生极化的效应,叫诱导效应 。 诱导效应的特点:
由电负性不同而引起
不存在极性交替现象
沿原子链传递,随传递距离增加而迅速减弱 +I效应:烷基、带负电荷的基团O-等
-I效应:-X、-NO2、-OH、-COOH、-CH=CH2等、带正电荷的基团-+NHR3 由原子或基团的电负性决定。
比氢原子电负性大的原子或基团表现出吸电性,称为吸电子基,具有亲电诱导效应,一般用–I表示;比氢原子电负性小的原子或基团表现出供电性,称为供电子基,具有给电子诱导效应,一般用+I表示。2. 共轭效应53甲基通过给电子作用,可分散正电荷,使碳正离子比较稳定。 ①? 取代基对苯环致活、致钝的解释 硝基吸电子作用,使中间体碳正离子的正电荷增加,导致碳正离子更不稳定,反应较慢。 ②?邻、对位定位基 除卤素外,其它邻、对位基都使邻、对位电荷密度增加,亲电试剂必然进攻电子云密度大的邻、对位,而且比苯容易进行取代。 a. 甲基 b. 氨基和羟基 ⅰ.诱导效应使苯环电子云密度降低(-I)。
ⅱ.p-π共轭,O原子上孤对电子与苯环的π电子发生p-π共轭,氧原子上电子云向苯环转移,使苯环电子云密度增加(+C)。由于+C>-I,总的结果电荷密度增加。55 c. 卤素原子 ⅰ.-I; ⅱ.+C
结果:-I>+C 使苯环的电子云密度降低,亲电反应比苯难。 ③? 间位定位基56选择适当的合成路线 3 、 定位规则的应用二、稠环芳烃 (一)萘 1. 结构 分子式:C10H858 ① 取代反应 卤代 硝化 磺化 2 . 性质59 萘环上的定位规则 如萘环上的α位上已有一个第一定位基,第二个取代基进入萘环的4位(多)和2位(少)。 如萘环上β位有第一类定位基,第二个取代基主要进入1位。 如萘环上α或β位上有第二类定位基,第二个取代基主要进入另一个苯环的5、8位。60 ②?加成反应 ③ 氧化反应 比苯容易。61 (二) 蒽和菲9、10位相同称γ-位;
1、4、5、8位称α-位;
2、3、6、7位称β-位。 1和8相同;2和7相同;
3和6相同;4和5相同;
9和10相同。 1. 主要存于煤焦油中,分子式C14H10,是同分异构体。2. 结构 氧化还原反应发生在9.10位 (三) 致癌芳烃(自学)(四)石墨和C60 (自学) 1.石墨:层状,由一层层无数的苯环并联而成的碳的另一种同素异形体。 2.C60:1985年合成,由60个C以20个元环及12五元环连接成的似足球状空心对称分子。三、煤焦油和石油(自学) (一) 煤焦油将煤焦油进行分馏,可得到下列馏分: 1. 轻油:170℃以下的馏分。比水轻,主要组分是苯、甲苯、二甲苯等。
2.中油:170-230℃间的馏分。比重近于1,主要组分是萘、苯酚、甲苯酚、吡啶等。
3. 重油:230-270℃间的馏分。比水重,主要组分是萘、甲苯酚、喹啉等。
4. 蒽油(绿油):270-360℃间的馏分。比水重,主要组分是蒽、菲、咔唑等。64 (二)石油 1.石油的形成: 2. 石油的化学组成很复杂。有机物的富集是生成石油的内在根据,适当的成油环境是生成石油的外部条件。 主要元素:C和H,C约占83-87%,H约占11-14%,其它元素含量在1%以下。 3.分类? 按结构可分为 :烷烃石油(大庆油)、环烷烃石油(胜利油)等。 按化学组成可分为 :石蜡基石油、沥青基石油、混合基石油。 4.资源丰富 例:将1吨石油裂解,可得二百多公斤乙烯。
将1吨煤炼焦,从焦炉气中只能提取五公斤乙烯 基本有机化工原料: 三烯:乙烯、丙烯、丁二烯。
三苯:苯、甲苯、二甲苯。 一炔:乙炔。 一萘:萘。 5.石油与生物。作业P76 4.3a,f,g;P77 4.4; P78 4.10; P78 4.11;P78 4.14
