河南省名校联盟2022-2023学年高二上学期9月开学考试化学试题(Word版含答案)
文档属性
| 名称 | 河南省名校联盟2022-2023学年高二上学期9月开学考试化学试题(Word版含答案) |

|
|
| 格式 | docx | ||
| 文件大小 | 520.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-09-04 00:00:00 | ||
图片预览



文档简介
河南省名校联盟2022-2023学年高二上学期9月开学考试
化学
考生注意:
1.本试卷分选择题和非选择题两部分。满分100分,考试时间90分钟。
2.答题前,考生务必用直径0.5毫米黑色墨水签字笔将密封线内项目填写清楚。
3.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑;非选择题请用直径0.5毫米黑色墨水签字笔在答题卡上各题的答题区域内作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
4.本卷命题范围:人教版必修第一册、第二册,选择性必修1第一章。
5.可能用到的相对原子质量:H 1 C 12 O 16 Na 23
一、选择题(本大题共16小题,每小题3分,共计48分。在每小题列出的四个选项中,只有一项是符合题目要求的)
1.下列金属的冶炼原理中,主要涉及的反应属于置换反应的是( )
A.热分解法冶炼银 B.湿法炼铜 C.高炉炼铁 D.电解法冶炼镁
2.下列操作一定能加快相应化学反应速率的是( )
A.延长反应时间 B.增大容积 C.升高体系温度 D.增大浓度
3.如图表示物质或概念间的从属关系,下列物质不符合的是( )
选项 X Y Z
A 置换反应 氧化还原反应 离子反应
B 胶体 分散系 混合物
C 碱性氧化物 金属氧化物 氧化物
D 酸 电解质 化合物
A.A B.B C.C D.D
4.下列说法错误的是( )
A.用丁达尔效应可鉴别溶液和胶体
B.与在灼烧时火焰颜色相同
C.相同条件下比更稳定
D.用氨水可鉴别溶液和溶液
5.设为阿伏加德罗常数的数值,下列说法正确的是( )
A.常温常压下,所含的电子数为
B.氨水中所含的时数为
C.标准状况下,盐酸中所含的分子数为
D.被完全氧化生成,失去的电子数为
6.用钯的化合物可检测有毒气体,该反应为。下列有关该反应的说法错误的是( )
A.反应中氧化剂是 B.都是非电解质
C.中均含极性键 D.反应涉及的均为短周期主族元素
7.下列说法错误的是( )
A.化学反应一定伴随着能量变化
B.放热反应的速率可能小于吸热反应的
C.化学键的断裂过程放出热量,形成过程吸收热量
D.应用盖斯定律,可计算某些难以直接测量的反应焓变
8.有一白色粉末由等质量的两种物质混合而成,分别取适量该白色粉末置于三支试管中进行实验:
实验1:逐滴加入的盐酸,振荡,有气泡产生,反应结束后得到无色溶液。
实验2:加热试管中的白色粉末,试管口有水滴凝结。
实验3:逐滴加入的硫酸,振荡,有气泡产生,反应结束后试管中有白色不溶物。
下列混合物中符合以上实验现象的是( )
A. B.
C. D.
9.常温常压下,充分燃烧一定量的乙醇放出的热量为,用溶液吸收生成的,恰好完全转变成正盐,则充分燃烧所放出的热量为( )
A. B. C. D.
10.已知下列热化学方程式:
则反应的约为( )
A. B. C. D.
11.能正确表示下列反应的离子方程式的是( )
A.溶液与溶液反应:
B.铜粉与浓硫酸共热:
C.向溶液中加入过量氢碘酸:
D.溶液中加入少量:
12.下列物质间的转化在给定条件下不能实现的是( )
A.
B.
C.
D.
13.下列由实验及现象能推出相应结论的是( )
选项 实验 现象 结论
A 向溶液中通入,再滴加溶液 产生白色沉淀 氧化性:
B 将粉末用脱脂棉包裹,向其中吹入 粉末变白,脱脂棉燃烧 与反应放热
C 用铂丝蘸取某待测液在酒精灯上灼烧 观察到焰色试验呈黄色 待测液中一定含钠盐
D 向碳酸钠溶液中滴加足量浓盐酸 产生无色无味的气体 非金属性:
A.A B.B C.C D.D
14.某同学为研究原电池原理,设计如图所示装置,下列说法正确的是( )
A.当a和b之间连接灵敏电流计时,电流计指针发生偏转,为正极
B.不论a和b是否连接,铁发生的反应均为
C.不论a和b是否连接,均得到电子,发生还原反应
D.a和b之间连接灵敏电流计时,向电极区迁移
15.W、X、Y、Z均为原子序数依次增大的短周期元素且分据三个周期。元素W和Y同主族,元素X的非金属性是元素周期表中最强的,Z的氧化物可制作光导纤维。下列说法正确的是( )
A.原子半径大小为
B.元素X的最高正价等于其原子最外层电子数
C.与均含有极性共价键
D.标准状况下,W的单质状态与X的相同
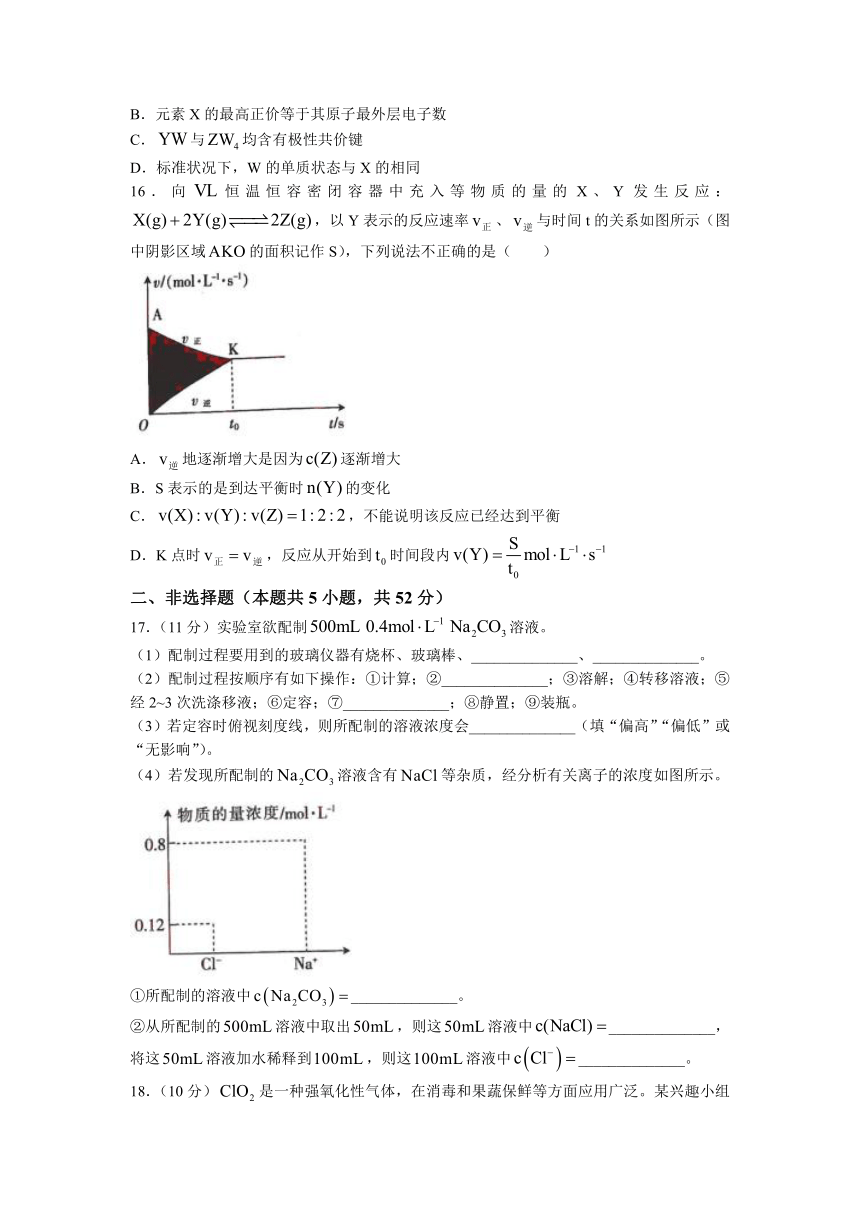
16.向恒温恒容密闭容器中充入等物质的量的X、Y发生反应:,以Y表示的反应速率、与时间t的关系如图所示(图中阴影区域的面积记作S),下列说法不正确的是( )
A.地逐渐增大是因为逐渐增大
B.S表示的是到达平衡时的变化
C.,不能说明该反应已经达到平衡
D.K点时,反应从开始到时间段内
二、非选择题(本题共5小题,共52分)
17.(11分)实验室欲配制溶液。
(1)配制过程要用到的玻璃仪器有烧杯、玻璃棒、______________、______________。
(2)配制过程按顺序有如下操作:①计算;②______________;③溶解;④转移溶液;⑤经2~3次洗涤移液;⑥定容;⑦______________;⑧静置;⑨装瓶。
(3)若定容时俯视刻度线,则所配制的溶液浓度会______________(填“偏高”“偏低”或“无影响”)。
(4)若发现所配制的溶液含有等杂质,经分析有关离子的浓度如图所示。
①所配制的溶液中______________。
②从所配制的溶液中取出,则这溶液中______________,将这溶液加水稀释到,则这溶液中______________。
18.(10分)是一种强氧化性气体,在消毒和果蔬保鲜等方面应用广泛。某兴趣小组通过如图所示装置(夹持装置略)对其进行制备、收集、吸收并制取。
(1)仪器A的名称是______________。
(2)图中装置有一明显错误,请指出:______________。
(3)打开B的活塞,A中有生成,D中吸收后生成和,写出D中所发生反应的离子方程式:____________________________。
(4)E中溶液出现黄色能否说明未被和的混合溶液充分吸收,判断并说明理由:____________________________。
(5)写出一种提高吸收率的方法:____________________________。
(6)已知在酸性条件下可发生反应生成并释放出,向溶液中滴加盐酸,反应剧烈,若将盐酸换成等的硫酸,开始反应缓慢,稍后一段时间产生气体迅速加快,产生这种现象可能的原因是____________________________。
(7)已知饱和溶液在温度低于时析出的晶体是,在温度高于时析出的晶体是,设计从溶液中制取晶体的操作:____________________________。
19.(10分)研究化学反应时,既要考虑物质变化与能量变化,又要关注反应的快慢与限度。回答下列问题:
Ⅰ.能源是现代生产生活、科学研究和社会发展的重要支柱。化学反应中的能量变化,主要表现为化学能、热能、电能等的变化。
(1)下列反应中,既属于放热反应,在一定条件下又能设计成原电池反应的是______________(填字母)。
A.与混合 B.
C. D.溶液与溶液中和
(2)原电池的装置如图所示。
①铁作______________(填“正极”或“负极”),溶液中向______________(填“铁”或“铜”)电极方向移动。
②正极的现象是______________,负极的电极反应式为____________________________。
③若反应过程中有电子发生转移,则生成的氢气在标准状况下的体积为______________L。
Ⅱ.恒容密闭容器中发生反应,生成物氨气的浓度随反应时间的变化情况如下表所示。
时间/s 0 8 16 24 32 400
0 1.3 1.8 2.1 2.2 2.2
(3)在内,以表示的平均反应速率______________,对于该反应,下列说法一定正确的是______________(填字母)。
A.加入合适的催化剂可加快该反应的速率,但并不改变其限度
B.时不再改变,说明此时该反应恰好到达平衡状态
C.将研成粉末,可以缩短反应达到平衡的时间
D.当氨气的体积分数不再改变时,说明该反应已达到化学平衡
20.(10分)有机物C可以用来衡量一个国家的石油化工发展水平,以A为原料合成F的流程如图。
请回答下列问题:
(1)有机物C的结构简式为:______________.
(2)已知A为烷烃,其分子式可表示为,则______________.
(3)B与A互为同系物,最多可与发生取代反应,则B的分子式为____________________________.
(4)D分子中只含有一个甲基(),则反应的化学方程式为______________.
(5)F的结构简式为____________________________,F的同分异构体有多种,其中能与溶液反应放出的有______________种(不含立体异构)。
21.(11分)化学能与热能的转化是当今化学研究的热点。回答下列问题:
(1)卤化镁高温分解的相对能量变化如图所示。
①写出该温度下分解的热化学方程式:____________________________.
②比较热稳定性:______________(填“>”或“<”)。
③反应______________
(2)氢氟酸是一种弱酸,已知时:
;
H。
则表示稀溶液与稀溶液的热化学方程式为____________________________,氢氟酸的中和反应反应热的绝对值大于的原因可能是____________________________。
(3)与在黑暗中混合也会发生剧烈反应,反应的热化学方程式为,查阅文献,断裂下列化学键所需能量数据如下:
化学键
436 565
则。
河南省名校联盟2022-2023学年高二上学期9月开学考试
化学
参考答案、提示及评分细则
1.B 2.C 3.A 4.D 5.A 6.D 7.C 8.A 9.B 10.B 11.A 12.D 13.B 14.C 15.D 16.B
17.(1)容量瓶;胶头滴管(各1分)
(2)称量:摇匀(各1分)
(3)偏高(1分)
(4)①(2分)
②;(各2分)
18.(1)锥形瓶(1分)
(2)C装置中导气管应该长进短出(1分)
(3)(2分)
(4)不能,因为D装置中有氧气产生,氧气也可能将氧化为(2分)
(5)减缓稀硫酸的滴加速率,长导管口加装多孔球泡(其他合理答案都给分,2分)
(6)生成的氯离子对反应起催化作用(1分)
(7)将溶液蒸发结品,温度高于趁热过滤(1分)
19.(1)B(1分)
(2)①负极;铜(各1分)
②有气泡产生:(各1分)
③2.24(2分)
(3)1.875(1分);AC(2分)
20.(1)(1分)
(2)6(1分)
(3)(2分)
(4)(2分)
(5);2(各2分)
21.(1)①(或其他合理形式)(2分)
②<(2分)
③(2分)
(2)(2分);氢氟酸电离过程中放热(1分)
(3)(2分)
化学
考生注意:
1.本试卷分选择题和非选择题两部分。满分100分,考试时间90分钟。
2.答题前,考生务必用直径0.5毫米黑色墨水签字笔将密封线内项目填写清楚。
3.考生作答时,请将答案答在答题卡上。选择题每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑;非选择题请用直径0.5毫米黑色墨水签字笔在答题卡上各题的答题区域内作答,超出答题区域书写的答案无效,在试题卷、草稿纸上作答无效。
4.本卷命题范围:人教版必修第一册、第二册,选择性必修1第一章。
5.可能用到的相对原子质量:H 1 C 12 O 16 Na 23
一、选择题(本大题共16小题,每小题3分,共计48分。在每小题列出的四个选项中,只有一项是符合题目要求的)
1.下列金属的冶炼原理中,主要涉及的反应属于置换反应的是( )
A.热分解法冶炼银 B.湿法炼铜 C.高炉炼铁 D.电解法冶炼镁
2.下列操作一定能加快相应化学反应速率的是( )
A.延长反应时间 B.增大容积 C.升高体系温度 D.增大浓度
3.如图表示物质或概念间的从属关系,下列物质不符合的是( )
选项 X Y Z
A 置换反应 氧化还原反应 离子反应
B 胶体 分散系 混合物
C 碱性氧化物 金属氧化物 氧化物
D 酸 电解质 化合物
A.A B.B C.C D.D
4.下列说法错误的是( )
A.用丁达尔效应可鉴别溶液和胶体
B.与在灼烧时火焰颜色相同
C.相同条件下比更稳定
D.用氨水可鉴别溶液和溶液
5.设为阿伏加德罗常数的数值,下列说法正确的是( )
A.常温常压下,所含的电子数为
B.氨水中所含的时数为
C.标准状况下,盐酸中所含的分子数为
D.被完全氧化生成,失去的电子数为
6.用钯的化合物可检测有毒气体,该反应为。下列有关该反应的说法错误的是( )
A.反应中氧化剂是 B.都是非电解质
C.中均含极性键 D.反应涉及的均为短周期主族元素
7.下列说法错误的是( )
A.化学反应一定伴随着能量变化
B.放热反应的速率可能小于吸热反应的
C.化学键的断裂过程放出热量,形成过程吸收热量
D.应用盖斯定律,可计算某些难以直接测量的反应焓变
8.有一白色粉末由等质量的两种物质混合而成,分别取适量该白色粉末置于三支试管中进行实验:
实验1:逐滴加入的盐酸,振荡,有气泡产生,反应结束后得到无色溶液。
实验2:加热试管中的白色粉末,试管口有水滴凝结。
实验3:逐滴加入的硫酸,振荡,有气泡产生,反应结束后试管中有白色不溶物。
下列混合物中符合以上实验现象的是( )
A. B.
C. D.
9.常温常压下,充分燃烧一定量的乙醇放出的热量为,用溶液吸收生成的,恰好完全转变成正盐,则充分燃烧所放出的热量为( )
A. B. C. D.
10.已知下列热化学方程式:
则反应的约为( )
A. B. C. D.
11.能正确表示下列反应的离子方程式的是( )
A.溶液与溶液反应:
B.铜粉与浓硫酸共热:
C.向溶液中加入过量氢碘酸:
D.溶液中加入少量:
12.下列物质间的转化在给定条件下不能实现的是( )
A.
B.
C.
D.
13.下列由实验及现象能推出相应结论的是( )
选项 实验 现象 结论
A 向溶液中通入,再滴加溶液 产生白色沉淀 氧化性:
B 将粉末用脱脂棉包裹,向其中吹入 粉末变白,脱脂棉燃烧 与反应放热
C 用铂丝蘸取某待测液在酒精灯上灼烧 观察到焰色试验呈黄色 待测液中一定含钠盐
D 向碳酸钠溶液中滴加足量浓盐酸 产生无色无味的气体 非金属性:
A.A B.B C.C D.D
14.某同学为研究原电池原理,设计如图所示装置,下列说法正确的是( )
A.当a和b之间连接灵敏电流计时,电流计指针发生偏转,为正极
B.不论a和b是否连接,铁发生的反应均为
C.不论a和b是否连接,均得到电子,发生还原反应
D.a和b之间连接灵敏电流计时,向电极区迁移
15.W、X、Y、Z均为原子序数依次增大的短周期元素且分据三个周期。元素W和Y同主族,元素X的非金属性是元素周期表中最强的,Z的氧化物可制作光导纤维。下列说法正确的是( )
A.原子半径大小为
B.元素X的最高正价等于其原子最外层电子数
C.与均含有极性共价键
D.标准状况下,W的单质状态与X的相同
16.向恒温恒容密闭容器中充入等物质的量的X、Y发生反应:,以Y表示的反应速率、与时间t的关系如图所示(图中阴影区域的面积记作S),下列说法不正确的是( )
A.地逐渐增大是因为逐渐增大
B.S表示的是到达平衡时的变化
C.,不能说明该反应已经达到平衡
D.K点时,反应从开始到时间段内
二、非选择题(本题共5小题,共52分)
17.(11分)实验室欲配制溶液。
(1)配制过程要用到的玻璃仪器有烧杯、玻璃棒、______________、______________。
(2)配制过程按顺序有如下操作:①计算;②______________;③溶解;④转移溶液;⑤经2~3次洗涤移液;⑥定容;⑦______________;⑧静置;⑨装瓶。
(3)若定容时俯视刻度线,则所配制的溶液浓度会______________(填“偏高”“偏低”或“无影响”)。
(4)若发现所配制的溶液含有等杂质,经分析有关离子的浓度如图所示。
①所配制的溶液中______________。
②从所配制的溶液中取出,则这溶液中______________,将这溶液加水稀释到,则这溶液中______________。
18.(10分)是一种强氧化性气体,在消毒和果蔬保鲜等方面应用广泛。某兴趣小组通过如图所示装置(夹持装置略)对其进行制备、收集、吸收并制取。
(1)仪器A的名称是______________。
(2)图中装置有一明显错误,请指出:______________。
(3)打开B的活塞,A中有生成,D中吸收后生成和,写出D中所发生反应的离子方程式:____________________________。
(4)E中溶液出现黄色能否说明未被和的混合溶液充分吸收,判断并说明理由:____________________________。
(5)写出一种提高吸收率的方法:____________________________。
(6)已知在酸性条件下可发生反应生成并释放出,向溶液中滴加盐酸,反应剧烈,若将盐酸换成等的硫酸,开始反应缓慢,稍后一段时间产生气体迅速加快,产生这种现象可能的原因是____________________________。
(7)已知饱和溶液在温度低于时析出的晶体是,在温度高于时析出的晶体是,设计从溶液中制取晶体的操作:____________________________。
19.(10分)研究化学反应时,既要考虑物质变化与能量变化,又要关注反应的快慢与限度。回答下列问题:
Ⅰ.能源是现代生产生活、科学研究和社会发展的重要支柱。化学反应中的能量变化,主要表现为化学能、热能、电能等的变化。
(1)下列反应中,既属于放热反应,在一定条件下又能设计成原电池反应的是______________(填字母)。
A.与混合 B.
C. D.溶液与溶液中和
(2)原电池的装置如图所示。
①铁作______________(填“正极”或“负极”),溶液中向______________(填“铁”或“铜”)电极方向移动。
②正极的现象是______________,负极的电极反应式为____________________________。
③若反应过程中有电子发生转移,则生成的氢气在标准状况下的体积为______________L。
Ⅱ.恒容密闭容器中发生反应,生成物氨气的浓度随反应时间的变化情况如下表所示。
时间/s 0 8 16 24 32 400
0 1.3 1.8 2.1 2.2 2.2
(3)在内,以表示的平均反应速率______________,对于该反应,下列说法一定正确的是______________(填字母)。
A.加入合适的催化剂可加快该反应的速率,但并不改变其限度
B.时不再改变,说明此时该反应恰好到达平衡状态
C.将研成粉末,可以缩短反应达到平衡的时间
D.当氨气的体积分数不再改变时,说明该反应已达到化学平衡
20.(10分)有机物C可以用来衡量一个国家的石油化工发展水平,以A为原料合成F的流程如图。
请回答下列问题:
(1)有机物C的结构简式为:______________.
(2)已知A为烷烃,其分子式可表示为,则______________.
(3)B与A互为同系物,最多可与发生取代反应,则B的分子式为____________________________.
(4)D分子中只含有一个甲基(),则反应的化学方程式为______________.
(5)F的结构简式为____________________________,F的同分异构体有多种,其中能与溶液反应放出的有______________种(不含立体异构)。
21.(11分)化学能与热能的转化是当今化学研究的热点。回答下列问题:
(1)卤化镁高温分解的相对能量变化如图所示。
①写出该温度下分解的热化学方程式:____________________________.
②比较热稳定性:______________(填“>”或“<”)。
③反应______________
(2)氢氟酸是一种弱酸,已知时:
;
H。
则表示稀溶液与稀溶液的热化学方程式为____________________________,氢氟酸的中和反应反应热的绝对值大于的原因可能是____________________________。
(3)与在黑暗中混合也会发生剧烈反应,反应的热化学方程式为,查阅文献,断裂下列化学键所需能量数据如下:
化学键
436 565
则。
河南省名校联盟2022-2023学年高二上学期9月开学考试
化学
参考答案、提示及评分细则
1.B 2.C 3.A 4.D 5.A 6.D 7.C 8.A 9.B 10.B 11.A 12.D 13.B 14.C 15.D 16.B
17.(1)容量瓶;胶头滴管(各1分)
(2)称量:摇匀(各1分)
(3)偏高(1分)
(4)①(2分)
②;(各2分)
18.(1)锥形瓶(1分)
(2)C装置中导气管应该长进短出(1分)
(3)(2分)
(4)不能,因为D装置中有氧气产生,氧气也可能将氧化为(2分)
(5)减缓稀硫酸的滴加速率,长导管口加装多孔球泡(其他合理答案都给分,2分)
(6)生成的氯离子对反应起催化作用(1分)
(7)将溶液蒸发结品,温度高于趁热过滤(1分)
19.(1)B(1分)
(2)①负极;铜(各1分)
②有气泡产生:(各1分)
③2.24(2分)
(3)1.875(1分);AC(2分)
20.(1)(1分)
(2)6(1分)
(3)(2分)
(4)(2分)
(5);2(各2分)
21.(1)①(或其他合理形式)(2分)
②<(2分)
③(2分)
(2)(2分);氢氟酸电离过程中放热(1分)
(3)(2分)
同课章节目录
