2.3构成物质的微粒——原子课件—2022-2023学年九年级化学科粤版上册(共25张PPT)
文档属性
| 名称 | 2.3构成物质的微粒——原子课件—2022-2023学年九年级化学科粤版上册(共25张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 粤教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-09-05 00:00:00 | ||
图片预览






文档简介
(共25张PPT)
分子的特性:
1.分子总是————,且温度越高,分子——越快。
2.分子之间有————。
3.分子的质量和体积都————。
4.同种分子的物质化学性质——,
不同种分子的物质化学性质——。
不断的运动着
运动
间隔
极小
相同
不相同
5.由同一种分子构成的物质为——
6.由不同种分子构成的物质为——
纯净物
混合物
7.由分子构成的物质,在物理变化中,分子本身 ;在化学变化中,分子本身 ,生成新的分子。
不发生改变
发生改变
2.3 构成物质的微粒(II)
-----原子
原子是化学变化中的最小的微粒
在化学变化中不可再分
ATOM
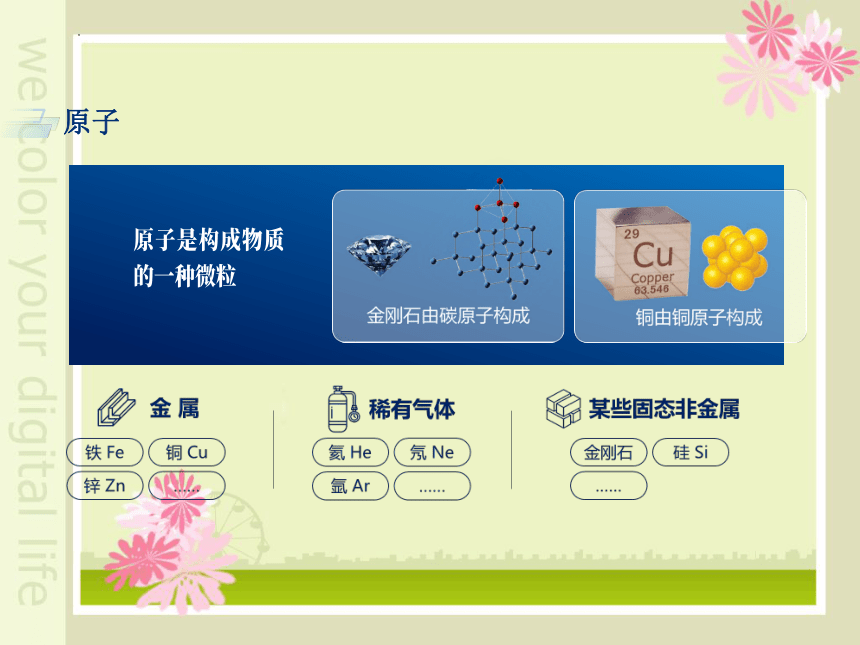
原子
二、原子的概念P47
1、原子是构成物质的另一种微粒。(原子构成分子,原子也可直接构成物质)
例如:金属单质(汞、镁、铜等);稀有气体和固态非金属单质(碳、磷等)
2、原子是化学变化中的最小微粒。
“化学变化”是前提条件。脱离“化学变化”这前提,原子仍可分成更小的粒子(质子、中子、电子)。
重新组合
O
H
H
O
H
H
1个水分子
(H2O)
氧分子
(O2)
氢分子
(H2)
O
O
H
H
H
H
O
O
H
H
通电
H
H
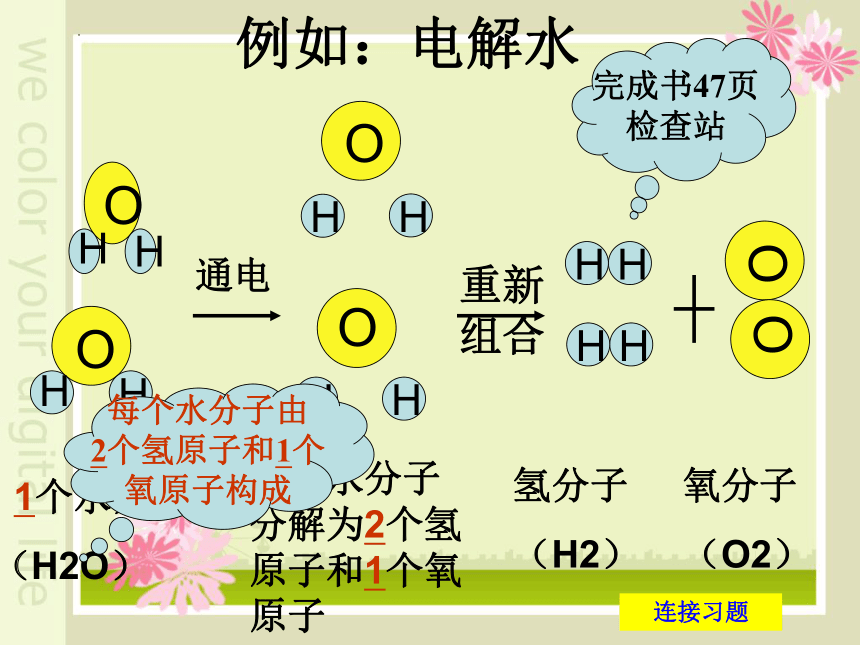
每个水分子分解为2个氢原子和1个氧原子
例如:电解水
每个水分子由
2个氢原子和1个
氧原子构成
完成书47页
检查站
连接习题
原子的特性:(与 分子一样)
1、原子是在不断地运动。
2、原子间存在间隙。
3、原子的质量和体积很小。
4、同种原子性质相同,不同种原子性质不同。
5、原子在化学变化中不能再分。
分子、原子的区别与联系 P63
分子 原子
相同点
不同点
联系
都是构成物质的微粒;质量、体积小;彼此间存在间隙;不断运动;同种分子(原子)性质相同,反之亦然。
①分子是保持物质的化学
性质的一种微粒。
①原子是化学变化中的最
小粒子。
②在化学变化中,分子本身发生改变
②在化学变化中,原子本
身不发生根本改变。
③分子可以直接构成物质。
③原子可以构成分子,也
可以直接构成物质
构成
构成
构成
分成
原子
分子
物质
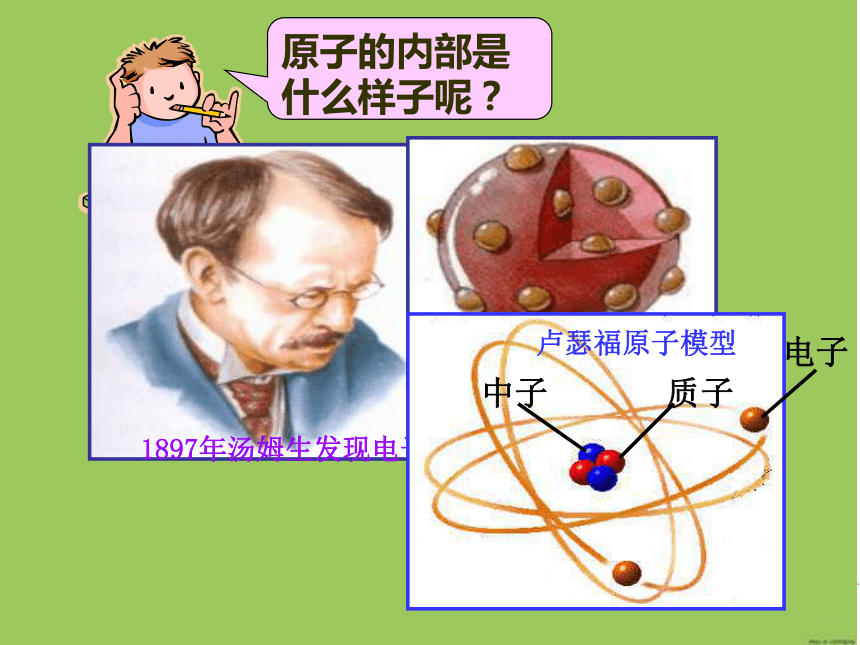
原子的内部是什么样子呢?
1897年汤姆生发现电子
卢瑟福原子模型
中子
质子
电子
讨论与交流(P49)
原子为什么呈电中性?
所有原子的原子核都是由质子、中子构成的吗?不同原子之间有什么区别?
在原子中质子数=中子数吗?
质子数=电子数,所以原子核与核外电子所带电量相等,电性相反,所以整个原子不显电性。
不是,例如:氢原子
不同原子的核电荷数各不相同
不是,例如:钠原子
结论:
1.原子核由质子和中子构成(氢原子除外);
2.每种原子中:质子数=电子数,但不一定等于中子数;
3.每种原子都含有质子和电子,但不一定有中子。
4.不同原子核电荷数不同
三.原子的构成:
原子
(中性)
原 子 核
(带正电)
核外电子
(1个电子带1个单位负电荷)
质子
(1个质子带1
个单位正电荷)
中子
(不带电)
所带正电荷数称为核电荷数
核电荷数=质子数
=核外电子数
+11
2. 原子结构示意图:
电子层
原子核
质子数
各电子层上的电子数
圆圈表示
圈内数字表示
弧线表示
原子核带正电
“+”表示
最外层电子数
数字1也可以表示
2 8 1
弧线上的数字表示
第一层
第二层
第三层(最外层)
核外电子的排布规律
自学指导
P50 知识之窗
请试着画出1-20号元素的原子结构示意图
质子数(核电荷数)决定元素或原子的种类
稀有气体元素,最外层电子数
横看,同一行原子 相同
电子层数
纵看,同一列原子, 相同,化学性质相似
最外层电子数
稀有气体元素,最外层电子数
等于8,为稳定结构
这些原子结构示意图告诉了我们哪些信息?
金属元素,最外层电子数 ,通常容易 .
<4
稀
有
气
体
元
素
非金属元素,最外层电子数 ,通常容易 .
失电子
>4
得电子
金属元素
非金属元素
根据下列原子的结构示意图,回答下列问题:
A
B
C
D
(2)易失电子的原子的是 ;易得电子的原子的是 ;
(1)具有相对稳定结构的是 (填序号,下同);
(3)化学性质相似的是 .
B
C和D
C和D
A
下列结构中表示同种元素的是:
A
B
C
D
E
F
B和D
C和E
相对原子质量
相对原子质量是一个比值不是实际质量
实际质量越大,相对原子质量越大
原子的真实质量之比等于其相对原子质量之比
定义式
Ar(某原子)=
m某原子
m碳原子×
是一个比值,没有单位
相对原子质量
定义式
Ar(某原子)=
m某原子
m碳原子×
注:单位“1”,省略不写
近似式
Ar(某原子)=质子数 + 中子数
原子的主要质量集中在原子核上
质子、中子的相对质量为1
电子的质量忽略不计
2. 氧化汞分解的反应中,发生变化的是( )
A.分子个数 B.原子个数
C. 原子种类 D.物质的总质量
1. 关于原子的说法不正确的是( )
A.是构成物质的一种粒子
B.是化学变化中的最小粒子
C.在化学反应中可以再分
D.是由原子核和核外电子构成
1.电解水过程中的最小微粒是 ,
保持水化学性质的最小微粒是 。
4、保持CO2和铁的化学性质的最小微粒分
A、CO2分子,铁分子
B、C原子和O原子,铁分子
C、CO2分子,铁原子
D、C原子和O原子,铁原子
5、氩气是一种惰性气体,若以●表示氩原子,则氩气是以下列何种形式存在?( )
A
B
C
D
1. 关于原子的叙述正确的是( )
2. 构成原子核的粒子一定有 ( )
A
质子
B
中 子
C
电 子
D
质子和中子
D
A
3. 原子的质量主要集中在 ( )
A
质子
B
中 子
C
电 子
D
原子核
D
A
原子是微粒中最小的
B
原子是不能再分的微粒
C
原子中不存在带电微粒
D
原子是化学变化中的最小微粒
4.下列关于原子核的说法错误的是( )
C
A
原子核在原子中所占的体积很小
B
原子核居于原子中心带正电荷
C
原子核居于原子中心带负电荷
D
原子的质量主要集中在原子核上
5. 铈(Ce)是一种常见的稀土元素,已知铈原子的原子核内有58个质子和
82个中子,该原子的核外电子数是( )
A
24
B
58
C
82
D
140
B
6.在分子、原子、质子、中子、电子这些粒子中,选择合适的答案
随堂练习
(1)能直接构成物质的粒子有: .
(2)在化学变化中最小的粒子有: .
(3)不显电性的粒子有: .
(4)带正电的粒子有: .
(5)带负电的粒子有: .
(6)构成原子的微粒有: .
(7)构成原子核的微粒有: .
分子、原子
原子
分子、原子、中子
质子
电子
质子、中子、电子
质子、中子
分子的特性:
1.分子总是————,且温度越高,分子——越快。
2.分子之间有————。
3.分子的质量和体积都————。
4.同种分子的物质化学性质——,
不同种分子的物质化学性质——。
不断的运动着
运动
间隔
极小
相同
不相同
5.由同一种分子构成的物质为——
6.由不同种分子构成的物质为——
纯净物
混合物
7.由分子构成的物质,在物理变化中,分子本身 ;在化学变化中,分子本身 ,生成新的分子。
不发生改变
发生改变
2.3 构成物质的微粒(II)
-----原子
原子是化学变化中的最小的微粒
在化学变化中不可再分
ATOM
原子
二、原子的概念P47
1、原子是构成物质的另一种微粒。(原子构成分子,原子也可直接构成物质)
例如:金属单质(汞、镁、铜等);稀有气体和固态非金属单质(碳、磷等)
2、原子是化学变化中的最小微粒。
“化学变化”是前提条件。脱离“化学变化”这前提,原子仍可分成更小的粒子(质子、中子、电子)。
重新组合
O
H
H
O
H
H
1个水分子
(H2O)
氧分子
(O2)
氢分子
(H2)
O
O
H
H
H
H
O
O
H
H
通电
H
H
每个水分子分解为2个氢原子和1个氧原子
例如:电解水
每个水分子由
2个氢原子和1个
氧原子构成
完成书47页
检查站
连接习题
原子的特性:(与 分子一样)
1、原子是在不断地运动。
2、原子间存在间隙。
3、原子的质量和体积很小。
4、同种原子性质相同,不同种原子性质不同。
5、原子在化学变化中不能再分。
分子、原子的区别与联系 P63
分子 原子
相同点
不同点
联系
都是构成物质的微粒;质量、体积小;彼此间存在间隙;不断运动;同种分子(原子)性质相同,反之亦然。
①分子是保持物质的化学
性质的一种微粒。
①原子是化学变化中的最
小粒子。
②在化学变化中,分子本身发生改变
②在化学变化中,原子本
身不发生根本改变。
③分子可以直接构成物质。
③原子可以构成分子,也
可以直接构成物质
构成
构成
构成
分成
原子
分子
物质
原子的内部是什么样子呢?
1897年汤姆生发现电子
卢瑟福原子模型
中子
质子
电子
讨论与交流(P49)
原子为什么呈电中性?
所有原子的原子核都是由质子、中子构成的吗?不同原子之间有什么区别?
在原子中质子数=中子数吗?
质子数=电子数,所以原子核与核外电子所带电量相等,电性相反,所以整个原子不显电性。
不是,例如:氢原子
不同原子的核电荷数各不相同
不是,例如:钠原子
结论:
1.原子核由质子和中子构成(氢原子除外);
2.每种原子中:质子数=电子数,但不一定等于中子数;
3.每种原子都含有质子和电子,但不一定有中子。
4.不同原子核电荷数不同
三.原子的构成:
原子
(中性)
原 子 核
(带正电)
核外电子
(1个电子带1个单位负电荷)
质子
(1个质子带1
个单位正电荷)
中子
(不带电)
所带正电荷数称为核电荷数
核电荷数=质子数
=核外电子数
+11
2. 原子结构示意图:
电子层
原子核
质子数
各电子层上的电子数
圆圈表示
圈内数字表示
弧线表示
原子核带正电
“+”表示
最外层电子数
数字1也可以表示
2 8 1
弧线上的数字表示
第一层
第二层
第三层(最外层)
核外电子的排布规律
自学指导
P50 知识之窗
请试着画出1-20号元素的原子结构示意图
质子数(核电荷数)决定元素或原子的种类
稀有气体元素,最外层电子数
横看,同一行原子 相同
电子层数
纵看,同一列原子, 相同,化学性质相似
最外层电子数
稀有气体元素,最外层电子数
等于8,为稳定结构
这些原子结构示意图告诉了我们哪些信息?
金属元素,最外层电子数 ,通常容易 .
<4
稀
有
气
体
元
素
非金属元素,最外层电子数 ,通常容易 .
失电子
>4
得电子
金属元素
非金属元素
根据下列原子的结构示意图,回答下列问题:
A
B
C
D
(2)易失电子的原子的是 ;易得电子的原子的是 ;
(1)具有相对稳定结构的是 (填序号,下同);
(3)化学性质相似的是 .
B
C和D
C和D
A
下列结构中表示同种元素的是:
A
B
C
D
E
F
B和D
C和E
相对原子质量
相对原子质量是一个比值不是实际质量
实际质量越大,相对原子质量越大
原子的真实质量之比等于其相对原子质量之比
定义式
Ar(某原子)=
m某原子
m碳原子×
是一个比值,没有单位
相对原子质量
定义式
Ar(某原子)=
m某原子
m碳原子×
注:单位“1”,省略不写
近似式
Ar(某原子)=质子数 + 中子数
原子的主要质量集中在原子核上
质子、中子的相对质量为1
电子的质量忽略不计
2. 氧化汞分解的反应中,发生变化的是( )
A.分子个数 B.原子个数
C. 原子种类 D.物质的总质量
1. 关于原子的说法不正确的是( )
A.是构成物质的一种粒子
B.是化学变化中的最小粒子
C.在化学反应中可以再分
D.是由原子核和核外电子构成
1.电解水过程中的最小微粒是 ,
保持水化学性质的最小微粒是 。
4、保持CO2和铁的化学性质的最小微粒分
A、CO2分子,铁分子
B、C原子和O原子,铁分子
C、CO2分子,铁原子
D、C原子和O原子,铁原子
5、氩气是一种惰性气体,若以●表示氩原子,则氩气是以下列何种形式存在?( )
A
B
C
D
1. 关于原子的叙述正确的是( )
2. 构成原子核的粒子一定有 ( )
A
质子
B
中 子
C
电 子
D
质子和中子
D
A
3. 原子的质量主要集中在 ( )
A
质子
B
中 子
C
电 子
D
原子核
D
A
原子是微粒中最小的
B
原子是不能再分的微粒
C
原子中不存在带电微粒
D
原子是化学变化中的最小微粒
4.下列关于原子核的说法错误的是( )
C
A
原子核在原子中所占的体积很小
B
原子核居于原子中心带正电荷
C
原子核居于原子中心带负电荷
D
原子的质量主要集中在原子核上
5. 铈(Ce)是一种常见的稀土元素,已知铈原子的原子核内有58个质子和
82个中子,该原子的核外电子数是( )
A
24
B
58
C
82
D
140
B
6.在分子、原子、质子、中子、电子这些粒子中,选择合适的答案
随堂练习
(1)能直接构成物质的粒子有: .
(2)在化学变化中最小的粒子有: .
(3)不显电性的粒子有: .
(4)带正电的粒子有: .
(5)带负电的粒子有: .
(6)构成原子的微粒有: .
(7)构成原子核的微粒有: .
分子、原子
原子
分子、原子、中子
质子
电子
质子、中子、电子
质子、中子
同课章节目录
- 第一章 大家都来学化学
- 1.1 身边的化学
- 1.2 化学实验室之旅
- 1.3 物质的变化
- 1.4 物质性质的探究
- 第二章 空气、物质的构成
- 2.1 空气的成分
- 2.2 构成物质的微粒(Ⅰ)——分子
- 2.3 构成物质的微粒(Ⅱ)——原子和离子
- 2.4 辨别物质的元素组成
- 第三章 维持生命之气——氧气
- 3.1 氧气的性质和用途
- 3.2 制取氧气
- 3.3 燃烧条件与灭火原理
- 3.4 物质构成的表示式
- 第四章 生命之源——水
- 4.1 我们的水资源
- 4.2 水的组成
- 4.3 质量守恒定律
- 4.4 化学方程式
- 第五章 燃料
- 5.1 洁净的燃料——氢气
- 5.2 组成燃料的主要元素——碳
- 5.3 二氧化碳的性质和制法
- 5.4 古生物的“遗产”——化石燃料
