【高效备课】人教版(2019)化学必修一 同步课件 2.3.1 物质的量和摩尔质量(34张ppt)
文档属性
| 名称 | 【高效备课】人教版(2019)化学必修一 同步课件 2.3.1 物质的量和摩尔质量(34张ppt) |  | |
| 格式 | pptx | ||
| 文件大小 | 3.7MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-09-15 17:22:51 | ||
图片预览







文档简介
(共33张PPT)
2.3.1物质的量和摩尔质量
人教版(2019)必修第一册
高一上学期
第二章
海水中的重要元素——钠和氯
第一节
钠及其化合物
第三节
物质的量
第二节
氯及其化合物
目录/
DIRECTORY
1
3
物质的量
摩尔质量
2
阿伏伽德罗常数
新知导入
我们怎样测量一张纸的厚度?我们怎样称量一粒米的质量?
mm
g
Q:你知道一滴水中有多少个水分子吗?
A:一滴水中大约含有1.7万亿亿个水分子。
新知导入
我一口气能喝下6000万亿亿个水分子,厉害吧!
我一口气能喝36克水,我才厉害!
宏 观
(质量)
微 观
(微粒数目)
新知导入
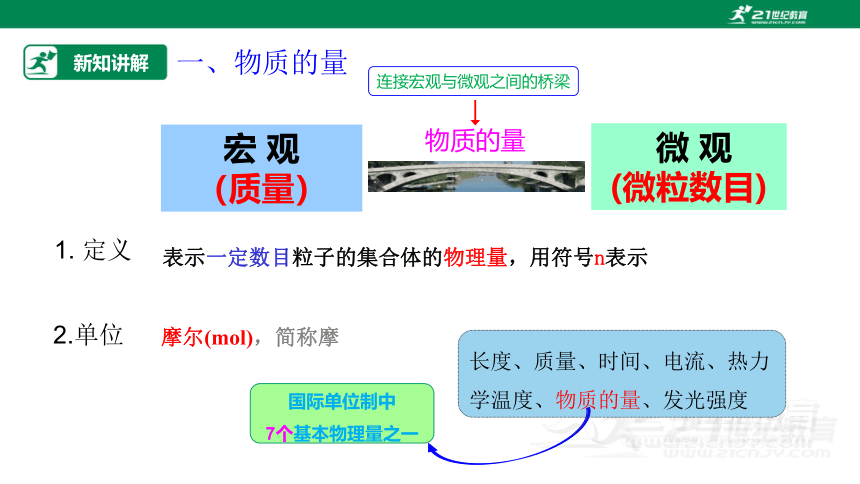
新知讲解
1. 定义
一、物质的量
表示一定数目粒子的集合体的物理量,用符号n表示
2.单位
摩尔(mol),简称摩
国际单位制中
7个基本物理量之一
长度、质量、时间、电流、热力学温度、物质的量、发光强度
宏 观
(质量)
微 观
(微粒数目)
物质的量
连接宏观与微观之间的桥梁
3.计量标准
国际上规定,1mol粒子集合体所含的粒子数约为6.02×1023
微观粒子,如分子、原子、离子、质子、中子、电子
4. 适用范围
新知讲解
新知讲解
5.表示方法
“数值+单位+粒子化学式/名称”
如: 1 mol 氧分子
1 mol H2 O
课堂练习
【例1】下列与物质的量有关的说法中正确的是
A.物质的量是物质所含粒子数量的简称
B.物质的量适用于计量分子、原子、离子等粒子
C.摩尔是表示物质所含微粒个数的物理量
D.物质的量就是指物质的质量
B
课堂练习
【例2】摩尔作为一种计量单位,在第26届国际计量大会上,以全新的面貌呈现。下列叙述错误的是
A.1摩尔任何分子所含的原子数均相等 B.1mol CO的质量为28g
C.摩尔是微观粒子的计量单位 D.1mol H可表示1摩尔氢原子
A
课堂练习
【例3】
B
课堂练习
【例4】下列关于“物质的量”“摩尔”和“摩尔质量”的叙述中正确的是
A.物质的摩尔质量等于其相对分子(原子)质量
B.“物质的量”是国际单位制中的一个基本单位
C.1 mol氦气中所含原子数目为NA
D.1 mol任何物质都约含有6.02×1023个原子
C
课堂练习
【例5】下列哪种物质所含氧原子数与0.4 mol H2O2所含的氧原子数相等( )
A.0.5mol水 B.0.3mol硝酸
C.0.1mol磷酸 D.0.2mol硫酸
D
1.定义
二、阿伏加德罗常数
1mol任何粒子的粒子数,符号为 NA
2.单位
每摩尔(mol-1)
0.012 kg 12C中所含碳原子数相同,约为6.02×1023
3.数值
新知讲解
如果把6.02×1023个硬币
排成一行,可以来回于地球与太阳之间多少次?
如果有 6.02×1023 粒米让全球60亿人吃,每人每天吃10斤,可吃多久?
240亿次
1万4千年!
新知讲解
6.02×1023 究竟是一个多大的数字呢?
1mol CO2中含_____个CO2分子
2mol CO2中含_____个CO2分子
n mol CO2中含_____个CO2分子
微思考
粒子数=
n
NA
·
NA
2NA
nNA
N
新知讲解
4.相关计算
n
=
N
NA
粒子数,单位“个”,省略
阿伏加德罗常数,单位:mol-1
物质的量,单位:mol
【思考2】1.806×1024个CO2分子的物质的量是______
3mol
新知讲解
求原子、离子的物质的量或粒子数时,需注意______
下标
4
2
4
7
2
9NA
课堂练习
课堂练习
【例6】根据所学知识填空。
(1)0.5 mol O3中氧原子数为__________。
(2)3.01×1024个OH-的物质的量为____ mol。
(3)含有3.01×1023个氧原子的H2SO4的物质的量是________。
(4)0.3 mol NH3分子中所含质子数与__________个H2O分子中所含电子数相等。
9.03×1023
5
0.125mol
1.806×1023
课堂练习
【例7】下列叙述错误的是
①摩尔是国际单位制中七个基本物理量之一;
②1 mol任何物质都含有约6.02×1023个原子;
③6.02×1023就是阿伏加德罗常数;
④氢原子的摩尔质量是1 g;
⑤HCl的摩尔质量等于1 mol HCl分子的质量;
⑥1 mol CO2中含有1 mol碳和2 mol氧。
A.①②③ B.②③④
C.②③④⑥ D.全部
D
课堂练习
【例8】酸奶中含有乳酸(C3H6O3),2 mol乳酸分子中含有( )
A.3 mol氧原子 B.12 mol氢原子
C.6.02×1023个O3分子 D.6.02×1023个乳酸分子
B
【例9】
A
宏观角度:
微观角度:
12g 32g 44g
1个碳原子 1个氧分子 1个二氧化碳分子
C + O2 CO2
扩大6.02×1023倍
扩大6.02×1023倍
扩大6.02×1023倍
NA个碳原子 NA氧分子 NA二氧化碳分子
微思考
1mol碳原子 1mol氧分子 1mol二氧化碳分子
1mol 粒子的数目约为6.02×1023个
新知讲解
C的相对原子质量为____,1mol C原子的质量为_____
O2的相对分子质量为____,1mol O2分子的质量为____
CO2的相对分子质量为____,1mol CO2分子的质量为_____
12
12g
32
44
44g
32g
1mol物质的质量与其相对原子或相对分子质量之间的关系
【结论】1mol任何物质的质量,以g为单位时,在数值上_____其相对原子或相对分子质量
等于
新知讲解
1.定义
三、摩尔质量
单位物质的量的物质所具有的质量,符号为 M
2.单位
克每摩尔(g·mol-1)
以g/mol为单位时,摩尔质量在数值上等于该物质的相对原子质量或相对分子质量
3.数值
新知讲解
1mol H2O的质量是_____ 水的摩尔质量是_______
2mol H2O的质量是_____ n mol H2O的质量是_______
36g水的物质的量是____ m g水的物质的量是_____mol
微思考
18g
18g/mol
36g
2mol
18n g
新知讲解
4.相关计算
n
=
m
M
质量,单位g
摩尔质量,单位g·mol-1
物质的量,单位mol
128g Cu的物质的量是多少?
2mol
新知讲解
课堂练习
【例10】下列叙述中正确的是
A.硫酸的摩尔质量是98g
B.1molMg的质量在数值上等于镁的摩尔质量
C.Fe2+与Fe3+的摩尔质量不相同
D.铁的摩尔质量就是铁原子的相对原子质量
B
课堂练习
【例11】
A
课堂练习
【例12】等质量的下列气体中,所含分子数最多的是( )
A.甲烷 B.二氧化碳 C.硫化氢 D.氮气
A
【例13】若氖原子的质量是a g,12C的原子质量是b g,下列说法错误的是( )
A.氖元素的相对原子质量是12a/b
B.则氖气的摩尔质量是aNA g/ mol
C.W g该氖原子的物质的量是W/a NA
D.W g该氖原子所含质子数是10W/a
C
课堂练习
【例14】
(1)1molCO(NH2)2中含_______mol碳原子,_______mol氮原子,_______个氢原子,约有_______个氧原子。
(2)与0.2molH3PO4具有相同氢原子数的HNO3的物质的量是_______mol,具有相同氧原子数的硫酸分子有_______个,具有相同的分子数的HCl的物质的量是_______mol,具有相同原子总数的NH3的物质的量是_______mol。
1
2
2.408×1024
6.02×1023
0.6
1.204×1023
0.2
0.4
谢谢
21世纪教育网(www.21cnjy.com)
中小学教育资源网站
兼职招聘:
https://www.21cnjy.com/recruitment/home/admin
2.3.1物质的量和摩尔质量
人教版(2019)必修第一册
高一上学期
第二章
海水中的重要元素——钠和氯
第一节
钠及其化合物
第三节
物质的量
第二节
氯及其化合物
目录/
DIRECTORY
1
3
物质的量
摩尔质量
2
阿伏伽德罗常数
新知导入
我们怎样测量一张纸的厚度?我们怎样称量一粒米的质量?
mm
g
Q:你知道一滴水中有多少个水分子吗?
A:一滴水中大约含有1.7万亿亿个水分子。
新知导入
我一口气能喝下6000万亿亿个水分子,厉害吧!
我一口气能喝36克水,我才厉害!
宏 观
(质量)
微 观
(微粒数目)
新知导入
新知讲解
1. 定义
一、物质的量
表示一定数目粒子的集合体的物理量,用符号n表示
2.单位
摩尔(mol),简称摩
国际单位制中
7个基本物理量之一
长度、质量、时间、电流、热力学温度、物质的量、发光强度
宏 观
(质量)
微 观
(微粒数目)
物质的量
连接宏观与微观之间的桥梁
3.计量标准
国际上规定,1mol粒子集合体所含的粒子数约为6.02×1023
微观粒子,如分子、原子、离子、质子、中子、电子
4. 适用范围
新知讲解
新知讲解
5.表示方法
“数值+单位+粒子化学式/名称”
如: 1 mol 氧分子
1 mol H2 O
课堂练习
【例1】下列与物质的量有关的说法中正确的是
A.物质的量是物质所含粒子数量的简称
B.物质的量适用于计量分子、原子、离子等粒子
C.摩尔是表示物质所含微粒个数的物理量
D.物质的量就是指物质的质量
B
课堂练习
【例2】摩尔作为一种计量单位,在第26届国际计量大会上,以全新的面貌呈现。下列叙述错误的是
A.1摩尔任何分子所含的原子数均相等 B.1mol CO的质量为28g
C.摩尔是微观粒子的计量单位 D.1mol H可表示1摩尔氢原子
A
课堂练习
【例3】
B
课堂练习
【例4】下列关于“物质的量”“摩尔”和“摩尔质量”的叙述中正确的是
A.物质的摩尔质量等于其相对分子(原子)质量
B.“物质的量”是国际单位制中的一个基本单位
C.1 mol氦气中所含原子数目为NA
D.1 mol任何物质都约含有6.02×1023个原子
C
课堂练习
【例5】下列哪种物质所含氧原子数与0.4 mol H2O2所含的氧原子数相等( )
A.0.5mol水 B.0.3mol硝酸
C.0.1mol磷酸 D.0.2mol硫酸
D
1.定义
二、阿伏加德罗常数
1mol任何粒子的粒子数,符号为 NA
2.单位
每摩尔(mol-1)
0.012 kg 12C中所含碳原子数相同,约为6.02×1023
3.数值
新知讲解
如果把6.02×1023个硬币
排成一行,可以来回于地球与太阳之间多少次?
如果有 6.02×1023 粒米让全球60亿人吃,每人每天吃10斤,可吃多久?
240亿次
1万4千年!
新知讲解
6.02×1023 究竟是一个多大的数字呢?
1mol CO2中含_____个CO2分子
2mol CO2中含_____个CO2分子
n mol CO2中含_____个CO2分子
微思考
粒子数=
n
NA
·
NA
2NA
nNA
N
新知讲解
4.相关计算
n
=
N
NA
粒子数,单位“个”,省略
阿伏加德罗常数,单位:mol-1
物质的量,单位:mol
【思考2】1.806×1024个CO2分子的物质的量是______
3mol
新知讲解
求原子、离子的物质的量或粒子数时,需注意______
下标
4
2
4
7
2
9NA
课堂练习
课堂练习
【例6】根据所学知识填空。
(1)0.5 mol O3中氧原子数为__________。
(2)3.01×1024个OH-的物质的量为____ mol。
(3)含有3.01×1023个氧原子的H2SO4的物质的量是________。
(4)0.3 mol NH3分子中所含质子数与__________个H2O分子中所含电子数相等。
9.03×1023
5
0.125mol
1.806×1023
课堂练习
【例7】下列叙述错误的是
①摩尔是国际单位制中七个基本物理量之一;
②1 mol任何物质都含有约6.02×1023个原子;
③6.02×1023就是阿伏加德罗常数;
④氢原子的摩尔质量是1 g;
⑤HCl的摩尔质量等于1 mol HCl分子的质量;
⑥1 mol CO2中含有1 mol碳和2 mol氧。
A.①②③ B.②③④
C.②③④⑥ D.全部
D
课堂练习
【例8】酸奶中含有乳酸(C3H6O3),2 mol乳酸分子中含有( )
A.3 mol氧原子 B.12 mol氢原子
C.6.02×1023个O3分子 D.6.02×1023个乳酸分子
B
【例9】
A
宏观角度:
微观角度:
12g 32g 44g
1个碳原子 1个氧分子 1个二氧化碳分子
C + O2 CO2
扩大6.02×1023倍
扩大6.02×1023倍
扩大6.02×1023倍
NA个碳原子 NA氧分子 NA二氧化碳分子
微思考
1mol碳原子 1mol氧分子 1mol二氧化碳分子
1mol 粒子的数目约为6.02×1023个
新知讲解
C的相对原子质量为____,1mol C原子的质量为_____
O2的相对分子质量为____,1mol O2分子的质量为____
CO2的相对分子质量为____,1mol CO2分子的质量为_____
12
12g
32
44
44g
32g
1mol物质的质量与其相对原子或相对分子质量之间的关系
【结论】1mol任何物质的质量,以g为单位时,在数值上_____其相对原子或相对分子质量
等于
新知讲解
1.定义
三、摩尔质量
单位物质的量的物质所具有的质量,符号为 M
2.单位
克每摩尔(g·mol-1)
以g/mol为单位时,摩尔质量在数值上等于该物质的相对原子质量或相对分子质量
3.数值
新知讲解
1mol H2O的质量是_____ 水的摩尔质量是_______
2mol H2O的质量是_____ n mol H2O的质量是_______
36g水的物质的量是____ m g水的物质的量是_____mol
微思考
18g
18g/mol
36g
2mol
18n g
新知讲解
4.相关计算
n
=
m
M
质量,单位g
摩尔质量,单位g·mol-1
物质的量,单位mol
128g Cu的物质的量是多少?
2mol
新知讲解
课堂练习
【例10】下列叙述中正确的是
A.硫酸的摩尔质量是98g
B.1molMg的质量在数值上等于镁的摩尔质量
C.Fe2+与Fe3+的摩尔质量不相同
D.铁的摩尔质量就是铁原子的相对原子质量
B
课堂练习
【例11】
A
课堂练习
【例12】等质量的下列气体中,所含分子数最多的是( )
A.甲烷 B.二氧化碳 C.硫化氢 D.氮气
A
【例13】若氖原子的质量是a g,12C的原子质量是b g,下列说法错误的是( )
A.氖元素的相对原子质量是12a/b
B.则氖气的摩尔质量是aNA g/ mol
C.W g该氖原子的物质的量是W/a NA
D.W g该氖原子所含质子数是10W/a
C
课堂练习
【例14】
(1)1molCO(NH2)2中含_______mol碳原子,_______mol氮原子,_______个氢原子,约有_______个氧原子。
(2)与0.2molH3PO4具有相同氢原子数的HNO3的物质的量是_______mol,具有相同氧原子数的硫酸分子有_______个,具有相同的分子数的HCl的物质的量是_______mol,具有相同原子总数的NH3的物质的量是_______mol。
1
2
2.408×1024
6.02×1023
0.6
1.204×1023
0.2
0.4
谢谢
21世纪教育网(www.21cnjy.com)
中小学教育资源网站
兼职招聘:
https://www.21cnjy.com/recruitment/home/admin
