2022-2023学年人教版九年级化学下册 第十单元 课题1 常见的酸和碱第1-3课时 课时作业(word版有答案)
文档属性
| 名称 | 2022-2023学年人教版九年级化学下册 第十单元 课题1 常见的酸和碱第1-3课时 课时作业(word版有答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 631.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-09-07 00:00:00 | ||
图片预览


文档简介
第十单元 酸和碱
课题1 常见的酸和碱
第1课时 什么是酸和碱 酸碱指示剂
1.实验室常用的紫色石蕊溶液是由以下哪位科学家发现的( )
A.拉瓦锡 B.阿伏加德罗
C.波义耳 D.道尔顿
2.实验室有一瓶保管不当使标签残缺的试剂(如图),其溶质可能是( )
A.单质 B.氧化物
C.碱 D.酸
3.下列试剂能使紫色石蕊溶液和无色酚酞溶液都变色的是( )
A.石灰水 B.氯化钠溶液
C.盐酸 D.乙醇溶液
4.下列说法正确的是( )
A.能使石蕊变蓝的溶液一定是碱溶液
B.显酸性的溶液不一定是酸溶液
C.不能使酚酞变红的溶液一定显酸性
D.酸和碱中一定都含有氢、氧元素
5.分类是化学学习和研究常用的方法之一。下列物质的分类正确的是( )
A.金属:镁、铁、金刚石
B.氧化物:H2O、CH2O、Al2O3
C.酸:盐酸、硝酸、氯酸钾
D.碱:氢氧化钠、氢氧化钙、氢氧化钾
6.取下列三种植物的花瓣分别在研钵中捣烂,加入酒精浸泡,过滤得到花汁。三种花汁在水和酸、碱溶液中的颜色如下表。下列说法错误的是( )
花的种类 花汁在水中的颜色 花汁在酸溶液中的颜色 花汁在碱溶液中的颜色
玫瑰 粉红色 粉红色 绿色
万寿菊 黄色 黄色 黄色
雏菊 无色 无色 黄色
A.花瓣捣烂后,加入酒精是为了溶解色素
B.玫瑰花汁、雏菊花汁都可用作酸碱指示剂
C.使玫瑰花汁呈粉红色的溶液一定显酸性
D.可用雏菊花汁区分食盐水和澄清石灰水
7.在点滴板的孔穴里分别滴入几滴白醋、澄清石灰水、蔗糖水、苹果汁、食盐水、氨水,再分别滴入1滴紫色石蕊溶液,观察颜色的变化(如图)。
(1)使紫色石蕊溶液变红的有 。
(2)使紫色石蕊溶液变蓝的有 。
(3)不能使紫色石蕊溶液变色的有 。
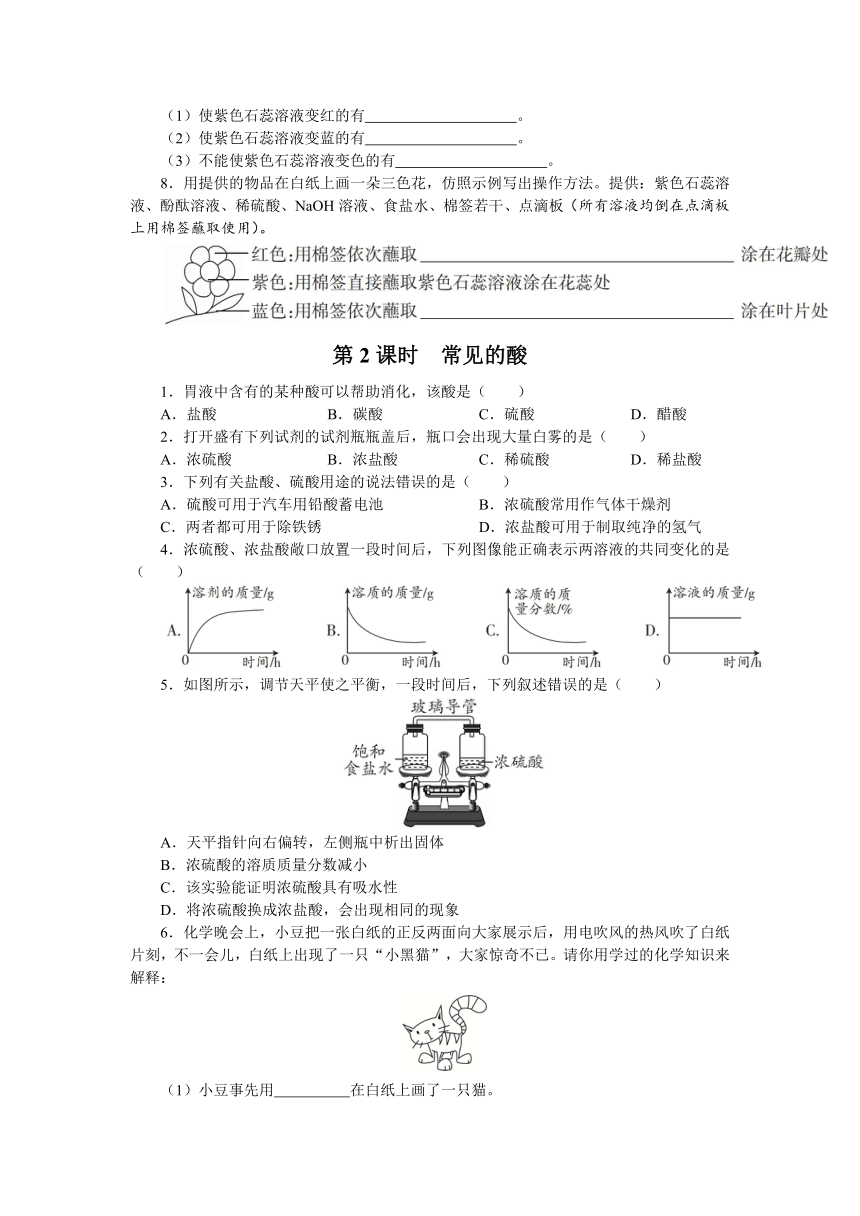
8.用提供的物品在白纸上画一朵三色花,仿照示例写出操作方法。提供:紫色石蕊溶液、酚酞溶液、稀硫酸、NaOH溶液、食盐水、棉签若干、点滴板(所有溶液均倒在点滴板上用棉签蘸取使用)。
第2课时 常见的酸
1.胃液中含有的某种酸可以帮助消化,该酸是( )
A.盐酸 B.碳酸 C.硫酸 D.醋酸
2.打开盛有下列试剂的试剂瓶瓶盖后,瓶口会出现大量白雾的是( )
A.浓硫酸 B.浓盐酸 C.稀硫酸 D.稀盐酸
3.下列有关盐酸、硫酸用途的说法错误的是( )
A.硫酸可用于汽车用铅酸蓄电池 B.浓硫酸常用作气体干燥剂
C.两者都可用于除铁锈 D.浓盐酸可用于制取纯净的氢气
4.浓硫酸、浓盐酸敞口放置一段时间后,下列图像能正确表示两溶液的共同变化的是( )
5.如图所示,调节天平使之平衡,一段时间后,下列叙述错误的是( )
A.天平指针向右偏转,左侧瓶中析出固体
B.浓硫酸的溶质质量分数减小
C.该实验能证明浓硫酸具有吸水性
D.将浓硫酸换成浓盐酸,会出现相同的现象
6.化学晚会上,小豆把一张白纸的正反两面向大家展示后,用电吹风的热风吹了白纸片刻,不一会儿,白纸上出现了一只“小黑猫”,大家惊奇不已。请你用学过的化学知识来解释:
(1)小豆事先用 在白纸上画了一只猫。
(2)使白纸上出现“小黑猫”的物质是 ,说明该物质具有 性,该性质属于物质的 (填“物理”或“化学”)性质。
7.将滤纸折成蝴蝶并喷洒A溶液后,悬挂于铁架台上。另取一个盛有B溶液的烧杯,放在纸蝴蝶的下方(如图)。一段时间后,纸蝴蝶的颜色发生变化,请回答:
(1)若A溶液是酚酞溶液,纸蝴蝶变红,则B溶液是 。
(2)若A溶液是紫色石蕊溶液,纸蝴蝶变红,则B溶液是 ;若纸蝴蝶变蓝,则B溶液是 。
(3)产生上述现象的原因是 。
8.实验室中常需要使用硫酸,请回答下列问题:
(1)用小木棍蘸取少量浓硫酸,放置一段时间后,可观察到 。
(2)用温度计的液泡端蘸取少量浓硫酸,放置在空气中一段时间,可观察到温度计示数增大,原因是 。
(3)如果不慎将浓硫酸沾到皮肤上,应立即 ,然后涂上3%~5%的 。
(4)浓硫酸稀释过程如图所示,b中盛放的物质是 ,a的作用是 。
第3课时 酸的化学性质
基础强化
1.白蚁分泌出的蚁酸能腐蚀多种建筑材料。下列建筑材料中最不容易被白蚁破坏的是( )
A.大理石 B.铜锌合金板 C.钢筋 D.铜板
2.食醋中含有醋酸,在生活中有许多妙用。下列使用食醋肯定不能达到目的的是( )
A.除去水壶内壁上的水垢 B.检验黄金中是否含有铜
C.除去菜刀上的铁锈 D.检验鸡蛋壳中是否含有碳酸钙
3.下列四种物质中有一种在适当条件下能跟其他三种物质反应,该物质是( )
A.稀盐酸 B.碳酸钙 C.铁 D.氧化铜
4.(2021秋邢台期末)如图所示,试管中盛有某种液体,将气球中的某种固体小心地倒入试管中,不能使气球逐渐变大的一组物质是( )
A.过氧化氢溶液和二氧化锰
B.水和硝酸铵固体
C.稀硫酸和锌粒
D.稀盐酸和碳酸钠固体
5.(2022春金昌月考)下列实验现象不能证明某无色溶液显酸性的是( )
A.滴入紫色石蕊溶液,溶液变红 B.加入Mg粉,有气泡产生
C.滴入酚酞溶液,溶液保持无色 D.加入CaCO3固体,有气泡产生
6.除去下列物质中的少量杂质(括号内为杂质),所选试剂不能达到实验目的的是( )
A.Fe粉(Zn):稀硫酸 B.Cu粉(Fe):稀盐酸
C.CaCl2溶液(HCl):CaCO3 D.MgSO4溶液(H2SO4):MgO
7.如图,X表示稀盐酸或稀硫酸。下列叙述错误的是( )
A.a不可能是无色酚酞溶液
B.b可能是氧化物
C.c参与的两个反应的基本类型相同
D.d可能是单质
8.实验小组将表面被氧化的铝片和稀盐酸放入密闭容器中,用传感器测得反应过程中压强和温度的变化曲线如图。下列说法错误的是( )
A.0~50 s内,稀盐酸与Al2O3反应 B.50 s 时,溶液中的溶质为AlCl3
C.100 s后,压强减小是因为温度降低 D.铝与稀盐酸反应过程中放出热量
9.某同学对硫酸的化学性质进行了总结(如图)。
(1)硫酸能使紫色石蕊溶液变成 色。
(2)写出一个符合性质②的反应的化学方程式: 。
(3)硫酸常用于清洗钢材表面的锈迹,这是利用了性质 (填序号),写出该反应的化学方程式: 。
(4)实验室不用稀硫酸与大理石反应制取二氧化碳的原因是
。用稀盐酸与大理石反应制取二氧化碳的化学方程式为 。
10.(2021黄石中考)取一氧化碳还原氧化铜实验的固体残留物20 g,向其中加入稀硫酸,剩余固体质量与加入稀硫酸质量的关系如图所示,请回答下列问题。
(1)所取固体残留物中铜的质量为 g。
(2)求a点溶液中溶质的质量分数。(相对原子质量:O-16 S-32 Cu-64)
能力提升
11.※※(2022杭州模拟)小金完成了如图所示实验,下列判断正确的是( )
A.实验①中最终一定有锌剩余
B.实验②中最终可能有氧化铜剩余
C.实验③所得溶液一定为无色
D.实验③所得溶液一定含有硫酸锌和硫酸铜
12.如图是某雪碧汽水标签中的部分内容。化学小组想利用此雪碧汽水验证柠檬酸的酸性。
已知:①柠檬酸是一种有机酸,具有酸的通性,且受热不分解。②白砂糖、香料、苯甲酸钠等不显酸性。
(1)小明将一定量的雪碧汽水倒入试管中,然后滴加紫色石蕊溶液,发现溶液变红。据此,他断定柠檬酸具有酸性。他作出判断的依据是 。
(2)小红认为小明的实验不够严谨,她的理由是 ;她建议在原来实验的基础上再进行一步操作,即把小明实验中已经变红的混合液体加热,若观察到 ,就能证明柠檬酸确实具有酸性。
(3)该实验还可以用 (填化学式)代替紫色石蕊溶液。
参考答案
第1课时 什么是酸和碱 酸碱指示剂
1.C 2.D 3.A 4.B 5.D 6.C
7.(1)白醋、苹果汁 (2)澄清石灰水、氨水 (3)蔗糖水、食盐水
8.酚酞溶液和NaOH溶液(或紫色石蕊溶液和稀硫酸) 紫色石蕊溶液和NaOH溶液
第2课时 常见的酸
1.A 2.B 3.D 4.C 5.D
6.(1)稀硫酸 (2)浓硫酸 腐蚀(或脱水) 化学
7.(1)浓氨水 (2)浓盐酸 浓氨水
(3)浓氨水显碱性、浓盐酸显酸性,且它们都具有挥发性
8.(1)木棍变黑 (2)浓硫酸具有吸水性,吸收空气中的水蒸气,浓硫酸溶于水放热
(3)用大量的水冲洗 碳酸氢钠溶液 (4)浓硫酸 搅拌,加快热量散失
第3课时 酸的化学性质
1.D 2.B 3.A 4.B 5.C 6.A 7.D 8.B
9.(1)红 (2)Zn+H2SO4=== ZnSO4+H2↑(合理即可)
(3)③ Fe2O3+3H2SO4=== Fe2(SO4)3+3H2O
(4)稀硫酸与大理石反应生成微溶于水的硫酸钙,附着在大理石表面,使反应停止
2HCl+CaCO3=== CaCl2+CO2↑+H2O
10.(1)17.5
(2)解:a点表示氧化铜和稀硫酸恰好反应。设生成硫酸铜的质量为x。
CuO+H2SO4=== CuSO4+H2O
80 160
2.5 g x
=,x=5 g
a点溶液中溶质的质量分数=×100%=12.5%
答:a点溶液中溶质的质量分数为12.5%。
11.A 【解析】A.实验③中最终烧杯内有红色固体,说明烧杯中发生了锌与硫酸铜的置换反应,故实验①中最终一定有锌剩余,正确。B.实验①中最终有锌剩余,说明稀硫酸完全反应,若实验②中有氧化铜剩余,则混合后氧化铜不发生反应,实验③的烧杯中一定有黑色固体剩余,错误;C.若实验①中剩余的锌不能将实验②中产生的硫酸铜完全消耗,则实验③所得溶液中含有硫酸铜,显蓝色,错误;D.若锌恰好与硫酸铜完全反应,则实验③所得溶液中不含硫酸铜,错误。故选A。
12.(1)酸能使紫色石蕊溶液变红
(2)雪碧汽水中含有的碳酸也能使紫色石蕊溶液变红 红色不褪去 (3)Mg(或CuO等)
课题1 常见的酸和碱
第1课时 什么是酸和碱 酸碱指示剂
1.实验室常用的紫色石蕊溶液是由以下哪位科学家发现的( )
A.拉瓦锡 B.阿伏加德罗
C.波义耳 D.道尔顿
2.实验室有一瓶保管不当使标签残缺的试剂(如图),其溶质可能是( )
A.单质 B.氧化物
C.碱 D.酸
3.下列试剂能使紫色石蕊溶液和无色酚酞溶液都变色的是( )
A.石灰水 B.氯化钠溶液
C.盐酸 D.乙醇溶液
4.下列说法正确的是( )
A.能使石蕊变蓝的溶液一定是碱溶液
B.显酸性的溶液不一定是酸溶液
C.不能使酚酞变红的溶液一定显酸性
D.酸和碱中一定都含有氢、氧元素
5.分类是化学学习和研究常用的方法之一。下列物质的分类正确的是( )
A.金属:镁、铁、金刚石
B.氧化物:H2O、CH2O、Al2O3
C.酸:盐酸、硝酸、氯酸钾
D.碱:氢氧化钠、氢氧化钙、氢氧化钾
6.取下列三种植物的花瓣分别在研钵中捣烂,加入酒精浸泡,过滤得到花汁。三种花汁在水和酸、碱溶液中的颜色如下表。下列说法错误的是( )
花的种类 花汁在水中的颜色 花汁在酸溶液中的颜色 花汁在碱溶液中的颜色
玫瑰 粉红色 粉红色 绿色
万寿菊 黄色 黄色 黄色
雏菊 无色 无色 黄色
A.花瓣捣烂后,加入酒精是为了溶解色素
B.玫瑰花汁、雏菊花汁都可用作酸碱指示剂
C.使玫瑰花汁呈粉红色的溶液一定显酸性
D.可用雏菊花汁区分食盐水和澄清石灰水
7.在点滴板的孔穴里分别滴入几滴白醋、澄清石灰水、蔗糖水、苹果汁、食盐水、氨水,再分别滴入1滴紫色石蕊溶液,观察颜色的变化(如图)。
(1)使紫色石蕊溶液变红的有 。
(2)使紫色石蕊溶液变蓝的有 。
(3)不能使紫色石蕊溶液变色的有 。
8.用提供的物品在白纸上画一朵三色花,仿照示例写出操作方法。提供:紫色石蕊溶液、酚酞溶液、稀硫酸、NaOH溶液、食盐水、棉签若干、点滴板(所有溶液均倒在点滴板上用棉签蘸取使用)。
第2课时 常见的酸
1.胃液中含有的某种酸可以帮助消化,该酸是( )
A.盐酸 B.碳酸 C.硫酸 D.醋酸
2.打开盛有下列试剂的试剂瓶瓶盖后,瓶口会出现大量白雾的是( )
A.浓硫酸 B.浓盐酸 C.稀硫酸 D.稀盐酸
3.下列有关盐酸、硫酸用途的说法错误的是( )
A.硫酸可用于汽车用铅酸蓄电池 B.浓硫酸常用作气体干燥剂
C.两者都可用于除铁锈 D.浓盐酸可用于制取纯净的氢气
4.浓硫酸、浓盐酸敞口放置一段时间后,下列图像能正确表示两溶液的共同变化的是( )
5.如图所示,调节天平使之平衡,一段时间后,下列叙述错误的是( )
A.天平指针向右偏转,左侧瓶中析出固体
B.浓硫酸的溶质质量分数减小
C.该实验能证明浓硫酸具有吸水性
D.将浓硫酸换成浓盐酸,会出现相同的现象
6.化学晚会上,小豆把一张白纸的正反两面向大家展示后,用电吹风的热风吹了白纸片刻,不一会儿,白纸上出现了一只“小黑猫”,大家惊奇不已。请你用学过的化学知识来解释:
(1)小豆事先用 在白纸上画了一只猫。
(2)使白纸上出现“小黑猫”的物质是 ,说明该物质具有 性,该性质属于物质的 (填“物理”或“化学”)性质。
7.将滤纸折成蝴蝶并喷洒A溶液后,悬挂于铁架台上。另取一个盛有B溶液的烧杯,放在纸蝴蝶的下方(如图)。一段时间后,纸蝴蝶的颜色发生变化,请回答:
(1)若A溶液是酚酞溶液,纸蝴蝶变红,则B溶液是 。
(2)若A溶液是紫色石蕊溶液,纸蝴蝶变红,则B溶液是 ;若纸蝴蝶变蓝,则B溶液是 。
(3)产生上述现象的原因是 。
8.实验室中常需要使用硫酸,请回答下列问题:
(1)用小木棍蘸取少量浓硫酸,放置一段时间后,可观察到 。
(2)用温度计的液泡端蘸取少量浓硫酸,放置在空气中一段时间,可观察到温度计示数增大,原因是 。
(3)如果不慎将浓硫酸沾到皮肤上,应立即 ,然后涂上3%~5%的 。
(4)浓硫酸稀释过程如图所示,b中盛放的物质是 ,a的作用是 。
第3课时 酸的化学性质
基础强化
1.白蚁分泌出的蚁酸能腐蚀多种建筑材料。下列建筑材料中最不容易被白蚁破坏的是( )
A.大理石 B.铜锌合金板 C.钢筋 D.铜板
2.食醋中含有醋酸,在生活中有许多妙用。下列使用食醋肯定不能达到目的的是( )
A.除去水壶内壁上的水垢 B.检验黄金中是否含有铜
C.除去菜刀上的铁锈 D.检验鸡蛋壳中是否含有碳酸钙
3.下列四种物质中有一种在适当条件下能跟其他三种物质反应,该物质是( )
A.稀盐酸 B.碳酸钙 C.铁 D.氧化铜
4.(2021秋邢台期末)如图所示,试管中盛有某种液体,将气球中的某种固体小心地倒入试管中,不能使气球逐渐变大的一组物质是( )
A.过氧化氢溶液和二氧化锰
B.水和硝酸铵固体
C.稀硫酸和锌粒
D.稀盐酸和碳酸钠固体
5.(2022春金昌月考)下列实验现象不能证明某无色溶液显酸性的是( )
A.滴入紫色石蕊溶液,溶液变红 B.加入Mg粉,有气泡产生
C.滴入酚酞溶液,溶液保持无色 D.加入CaCO3固体,有气泡产生
6.除去下列物质中的少量杂质(括号内为杂质),所选试剂不能达到实验目的的是( )
A.Fe粉(Zn):稀硫酸 B.Cu粉(Fe):稀盐酸
C.CaCl2溶液(HCl):CaCO3 D.MgSO4溶液(H2SO4):MgO
7.如图,X表示稀盐酸或稀硫酸。下列叙述错误的是( )
A.a不可能是无色酚酞溶液
B.b可能是氧化物
C.c参与的两个反应的基本类型相同
D.d可能是单质
8.实验小组将表面被氧化的铝片和稀盐酸放入密闭容器中,用传感器测得反应过程中压强和温度的变化曲线如图。下列说法错误的是( )
A.0~50 s内,稀盐酸与Al2O3反应 B.50 s 时,溶液中的溶质为AlCl3
C.100 s后,压强减小是因为温度降低 D.铝与稀盐酸反应过程中放出热量
9.某同学对硫酸的化学性质进行了总结(如图)。
(1)硫酸能使紫色石蕊溶液变成 色。
(2)写出一个符合性质②的反应的化学方程式: 。
(3)硫酸常用于清洗钢材表面的锈迹,这是利用了性质 (填序号),写出该反应的化学方程式: 。
(4)实验室不用稀硫酸与大理石反应制取二氧化碳的原因是
。用稀盐酸与大理石反应制取二氧化碳的化学方程式为 。
10.(2021黄石中考)取一氧化碳还原氧化铜实验的固体残留物20 g,向其中加入稀硫酸,剩余固体质量与加入稀硫酸质量的关系如图所示,请回答下列问题。
(1)所取固体残留物中铜的质量为 g。
(2)求a点溶液中溶质的质量分数。(相对原子质量:O-16 S-32 Cu-64)
能力提升
11.※※(2022杭州模拟)小金完成了如图所示实验,下列判断正确的是( )
A.实验①中最终一定有锌剩余
B.实验②中最终可能有氧化铜剩余
C.实验③所得溶液一定为无色
D.实验③所得溶液一定含有硫酸锌和硫酸铜
12.如图是某雪碧汽水标签中的部分内容。化学小组想利用此雪碧汽水验证柠檬酸的酸性。
已知:①柠檬酸是一种有机酸,具有酸的通性,且受热不分解。②白砂糖、香料、苯甲酸钠等不显酸性。
(1)小明将一定量的雪碧汽水倒入试管中,然后滴加紫色石蕊溶液,发现溶液变红。据此,他断定柠檬酸具有酸性。他作出判断的依据是 。
(2)小红认为小明的实验不够严谨,她的理由是 ;她建议在原来实验的基础上再进行一步操作,即把小明实验中已经变红的混合液体加热,若观察到 ,就能证明柠檬酸确实具有酸性。
(3)该实验还可以用 (填化学式)代替紫色石蕊溶液。
参考答案
第1课时 什么是酸和碱 酸碱指示剂
1.C 2.D 3.A 4.B 5.D 6.C
7.(1)白醋、苹果汁 (2)澄清石灰水、氨水 (3)蔗糖水、食盐水
8.酚酞溶液和NaOH溶液(或紫色石蕊溶液和稀硫酸) 紫色石蕊溶液和NaOH溶液
第2课时 常见的酸
1.A 2.B 3.D 4.C 5.D
6.(1)稀硫酸 (2)浓硫酸 腐蚀(或脱水) 化学
7.(1)浓氨水 (2)浓盐酸 浓氨水
(3)浓氨水显碱性、浓盐酸显酸性,且它们都具有挥发性
8.(1)木棍变黑 (2)浓硫酸具有吸水性,吸收空气中的水蒸气,浓硫酸溶于水放热
(3)用大量的水冲洗 碳酸氢钠溶液 (4)浓硫酸 搅拌,加快热量散失
第3课时 酸的化学性质
1.D 2.B 3.A 4.B 5.C 6.A 7.D 8.B
9.(1)红 (2)Zn+H2SO4=== ZnSO4+H2↑(合理即可)
(3)③ Fe2O3+3H2SO4=== Fe2(SO4)3+3H2O
(4)稀硫酸与大理石反应生成微溶于水的硫酸钙,附着在大理石表面,使反应停止
2HCl+CaCO3=== CaCl2+CO2↑+H2O
10.(1)17.5
(2)解:a点表示氧化铜和稀硫酸恰好反应。设生成硫酸铜的质量为x。
CuO+H2SO4=== CuSO4+H2O
80 160
2.5 g x
=,x=5 g
a点溶液中溶质的质量分数=×100%=12.5%
答:a点溶液中溶质的质量分数为12.5%。
11.A 【解析】A.实验③中最终烧杯内有红色固体,说明烧杯中发生了锌与硫酸铜的置换反应,故实验①中最终一定有锌剩余,正确。B.实验①中最终有锌剩余,说明稀硫酸完全反应,若实验②中有氧化铜剩余,则混合后氧化铜不发生反应,实验③的烧杯中一定有黑色固体剩余,错误;C.若实验①中剩余的锌不能将实验②中产生的硫酸铜完全消耗,则实验③所得溶液中含有硫酸铜,显蓝色,错误;D.若锌恰好与硫酸铜完全反应,则实验③所得溶液中不含硫酸铜,错误。故选A。
12.(1)酸能使紫色石蕊溶液变红
(2)雪碧汽水中含有的碳酸也能使紫色石蕊溶液变红 红色不褪去 (3)Mg(或CuO等)
同课章节目录
