2022-2023学年人教版九年级化学下册 第十单元 课题2 酸和碱的中和反应 课时作业(word版有答案)
文档属性
| 名称 | 2022-2023学年人教版九年级化学下册 第十单元 课题2 酸和碱的中和反应 课时作业(word版有答案) |  | |
| 格式 | zip | ||
| 文件大小 | 282.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-09-07 21:33:50 | ||
图片预览


文档简介
课题2 酸和碱的中和反应
第1课时 中和反应及其在实际中的应用
基础强化
1.在探究中和反应的实验中,不需要用到的玻璃仪器是( )
A.烧杯 B.玻璃棒 C.滴管 D.酒精灯
2.(2020上海中考)下列有关中和反应的说法一定正确的是( )
A.有沉淀生成 B.有盐生成 C.有气体生成 D.反应物均需溶于水
3.(2021春南平月考)室温下,将稀盐酸慢慢滴入盛有氢氧化钠溶液的烧杯中,利用温度传感器测出烧杯中溶液温度变化的曲线如图所示,下列说法错误的是( )
A.在a处溶液中加入石蕊溶液,溶液呈蓝色
B.b处溶液中的溶质是氯化钠
C.a→b的过程中溶液由酸性变成中性
D.在c处溶液中加入碳酸钙,有气泡产生
4.要除去氯化钾溶液中含有的少量氢氧化钾,可选用的试剂是( )
A.稀盐酸 B.稀硫酸
C.二氧化碳 D.酚酞溶液
5.小东为探究氢氧化钠溶液与稀盐酸是否恰好中和,分别取少量反应后的溶液于试管中,选用不同试剂进行实验。下列实验操作和现象不能得出相应实验结论的是( )
选项 实验操作和现象 实验结论
A 加入铁粉,有气泡产生 稀盐酸过量
B 加入碳酸钙粉末,无气泡产生 稀盐酸不过量
C 滴入紫色石蕊溶液,溶液呈紫色 一定恰好中和
D 滴入无色酚酞溶液,溶液呈无色 一定恰好中和
6.写出下列物质的化学式并按要求分类(填序号):
①醋酸 ②碳酸钡 ③氢氧化钾 ④碳酸
⑤氢氧化铁 ⑥硝酸 ⑦氯化银 ⑧碳酸钾
其中属于酸的有 ,属于碱的有 ,属于盐的有 。
7.部分变质的氢氧化钠溶液中溶质的成分是 (填化学式),向其中滴加稀盐酸,若刚开始没有气泡产生,此时反应的化学方程式是 。
8.如图为某“胃酸完全抑制剂”的部分标签。
(1)该“胃酸完全抑制剂”的主要成分中属于盐的物质是 (填化学式)。
(2)服用该“胃酸完全抑制剂”后在胃内发生的中和反应的化学方程式是
。
9.结合图示回答下列问题:
(1)图1是稀硫酸与氢氧化钠溶液反应的微观示意图。
①C方框内甲、乙两种粒子分别为 (填粒子符号,下同)。
②该反应的实质是酸中的 与碱中的 结合生成 。
(2)图2是Ba(OH)2溶液与稀硫酸反应的微观示意图(硫酸钡不溶于水)。
①写出该反应的化学方程式: 。
②向反应后的混合物中滴加紫色石蕊溶液,溶液变为 色。
10.某化工厂用熟石灰处理废水中的残余盐酸。已知废水中盐酸的质量分数为0.003 65%,现中和池中有1.0×106 kg废水(废水中的其他物质均不与熟石灰反应),则需要多少千克熟石灰才能将该废水恰好完全中和?(相对原子质量:H-1 O-16 Cl-35.5 Ca-40)
能力提升
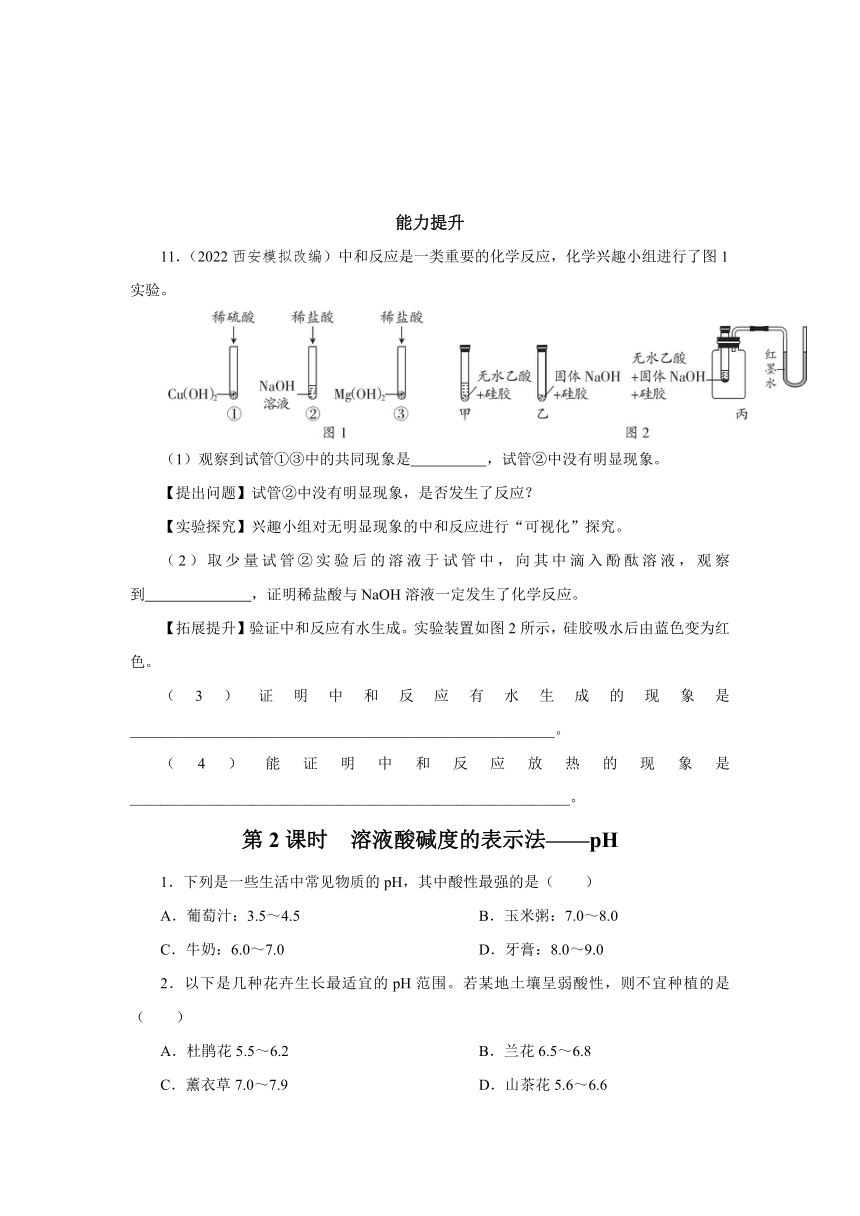
11.(2022西安模拟改编)中和反应是一类重要的化学反应,化学兴趣小组进行了图1实验。
(1)观察到试管①③中的共同现象是 ,试管②中没有明显现象。
【提出问题】试管②中没有明显现象,是否发生了反应?
【实验探究】兴趣小组对无明显现象的中和反应进行“可视化”探究。
(2)取少量试管②实验后的溶液于试管中,向其中滴入酚酞溶液,观察到 ,证明稀盐酸与NaOH溶液一定发生了化学反应。
【拓展提升】验证中和反应有水生成。实验装置如图2所示,硅胶吸水后由蓝色变为红色。
(3)证明中和反应有水生成的现象是________________________________________________________。
(4)能证明中和反应放热的现象是__________________________________________________________。
第2课时 溶液酸碱度的表示法——pH
1.下列是一些生活中常见物质的pH,其中酸性最强的是( )
A.葡萄汁:3.5~4.5 B.玉米粥:7.0~8.0
C.牛奶:6.0~7.0 D.牙膏:8.0~9.0
2.以下是几种花卉生长最适宜的pH范围。若某地土壤呈弱酸性,则不宜种植的是( )
A.杜鹃花5.5~6.2 B.兰花6.5~6.8
C.薰衣草7.0~7.9 D.山茶花5.6~6.6
3.(2022郑州模拟)欲使pH=3的盐酸的pH升高到7,可以加入( )
A.过量的水 B.过量的生石灰
C.过量的熟石灰 D.过量的石灰石
4.(2021秋泰安期中)下列有关溶液酸碱性的说法错误的是( )
A.pH=7的溶液呈中性 B.呈碱性的溶液一定是碱溶液
C.pH<7的溶液一定呈酸性 D.pH越小的酸溶液的酸性越强
5.(2022合肥模拟)某同学想用pH试纸测定一些物质的pH,下列说法正确的是( )
A.能用干燥的pH试纸测定98%的浓硫酸的pH
B.测出草木灰水的pH为6
C.用湿润的pH试纸测定白醋的pH,结果会偏大
D.测出0.4%的氢氧化钠溶液的pH为12.7
6.(2021苏州中考)如图是室温下稀盐酸与稀氢氧化钠溶液反应过程中溶液pH的变化曲线。下列说法错误的是( )
A.该实验是将稀盐酸逐滴滴入稀氢氧化钠溶液中
B.a点到b点pH变化的原因是H+和OH-发生反应
C.b点时,参加反应的HCl与NaOH的质量比为36.5∶40
D.c点时,溶液中的Na+数目大于Cl-数目
7.某小型造纸厂非法向河中排放了大量碱性废液,请你根据所学知识,设计两种检测碱性废液的方法,并提出合理的治理措施。
实验操作 实验现象
(1) 取少量废液样品于试管中,滴加2~3滴 溶液 溶液变红
(2) 在白瓷板上放一小片pH试纸, 读出溶液pH 7 (填“>”“=”或“<”)
(3)你提出的一条治理措施是 。
8.(教材习题改编)某校“酸雨”(pH<5.6)测量小组的同学取刚降到地面的雨水样品,用pH计每隔五分钟测一次pH,记录数据如下:
测定时刻 5:05 5:10 5:15 5:20 5:25 5:30 5:35
pH 4.95 4.94 4.94 4.88 4.86 4.85 4.85
(1)正常雨水的pH<7的原因是 。
(2)由表中数据可知,该雨水 (填“是”或“不是”)酸雨,降到地面的雨水的酸性逐渐 (填“减弱”或“增强”)。
(3)该雨水pH发生变化的主要原因是其中的亚硫酸(化学式为H2SO3)与空气中的氧气反应生成硫酸,该反应的化学方程式为 。
参考答案
第1课时 中和反应及其在实际中的应用
1.D 2.B 3.C 4.A 5.D
6.①CH3COOH ②BaCO3 ③KOH ④H2CO3 ⑤Fe(OH)3
⑥HNO3 ⑦AgCl ⑧K2CO3 ①④⑥ ③⑤ ②⑦⑧
7.Na2CO3、NaOH NaOH+HCl=== NaCl+H2O
8.(1)CaCO3 (2)Mg(OH)2+2HCl=== MgCl2+2H2O
9.(1)①Na+、SO ②H+ OH- H2O
(2)①Ba(OH)2+H2SO4=== BaSO4↓+2H2O ②红
10.解:设将该废水恰好完全中和需要熟石灰的质量为x。
Ca(OH)2+2HCl=== CaCl2+2H2O
74 73
x 1.0×106 kg×0.003 65%
=,x=37 kg
答:需要37 kg熟石灰才能将该废水恰好完全中和。
11.(1)固体溶解 (2)无明显现象
(3)甲、乙中硅胶不变色,丙中硅胶由蓝色变为红色
(4)丙中U形管左端液面降低,右端液面升高
第2课时 溶液酸碱度的表示法——pH
1.A 2.C 3.D 4.B 5.C 6.D
7.(1)酚酞
(2)用玻璃棒蘸取废液样品滴到pH试纸上,将试纸显示的颜色与标准比色卡比较 >
(3)加入稀硫酸,调节废液的pH至7后再排放(合理即可)
8.(1)二氧化碳与水反应生成碳酸
(2)是 增强 (3)2H2SO3+O2=== 2H2SO4
第1课时 中和反应及其在实际中的应用
基础强化
1.在探究中和反应的实验中,不需要用到的玻璃仪器是( )
A.烧杯 B.玻璃棒 C.滴管 D.酒精灯
2.(2020上海中考)下列有关中和反应的说法一定正确的是( )
A.有沉淀生成 B.有盐生成 C.有气体生成 D.反应物均需溶于水
3.(2021春南平月考)室温下,将稀盐酸慢慢滴入盛有氢氧化钠溶液的烧杯中,利用温度传感器测出烧杯中溶液温度变化的曲线如图所示,下列说法错误的是( )
A.在a处溶液中加入石蕊溶液,溶液呈蓝色
B.b处溶液中的溶质是氯化钠
C.a→b的过程中溶液由酸性变成中性
D.在c处溶液中加入碳酸钙,有气泡产生
4.要除去氯化钾溶液中含有的少量氢氧化钾,可选用的试剂是( )
A.稀盐酸 B.稀硫酸
C.二氧化碳 D.酚酞溶液
5.小东为探究氢氧化钠溶液与稀盐酸是否恰好中和,分别取少量反应后的溶液于试管中,选用不同试剂进行实验。下列实验操作和现象不能得出相应实验结论的是( )
选项 实验操作和现象 实验结论
A 加入铁粉,有气泡产生 稀盐酸过量
B 加入碳酸钙粉末,无气泡产生 稀盐酸不过量
C 滴入紫色石蕊溶液,溶液呈紫色 一定恰好中和
D 滴入无色酚酞溶液,溶液呈无色 一定恰好中和
6.写出下列物质的化学式并按要求分类(填序号):
①醋酸 ②碳酸钡 ③氢氧化钾 ④碳酸
⑤氢氧化铁 ⑥硝酸 ⑦氯化银 ⑧碳酸钾
其中属于酸的有 ,属于碱的有 ,属于盐的有 。
7.部分变质的氢氧化钠溶液中溶质的成分是 (填化学式),向其中滴加稀盐酸,若刚开始没有气泡产生,此时反应的化学方程式是 。
8.如图为某“胃酸完全抑制剂”的部分标签。
(1)该“胃酸完全抑制剂”的主要成分中属于盐的物质是 (填化学式)。
(2)服用该“胃酸完全抑制剂”后在胃内发生的中和反应的化学方程式是
。
9.结合图示回答下列问题:
(1)图1是稀硫酸与氢氧化钠溶液反应的微观示意图。
①C方框内甲、乙两种粒子分别为 (填粒子符号,下同)。
②该反应的实质是酸中的 与碱中的 结合生成 。
(2)图2是Ba(OH)2溶液与稀硫酸反应的微观示意图(硫酸钡不溶于水)。
①写出该反应的化学方程式: 。
②向反应后的混合物中滴加紫色石蕊溶液,溶液变为 色。
10.某化工厂用熟石灰处理废水中的残余盐酸。已知废水中盐酸的质量分数为0.003 65%,现中和池中有1.0×106 kg废水(废水中的其他物质均不与熟石灰反应),则需要多少千克熟石灰才能将该废水恰好完全中和?(相对原子质量:H-1 O-16 Cl-35.5 Ca-40)
能力提升
11.(2022西安模拟改编)中和反应是一类重要的化学反应,化学兴趣小组进行了图1实验。
(1)观察到试管①③中的共同现象是 ,试管②中没有明显现象。
【提出问题】试管②中没有明显现象,是否发生了反应?
【实验探究】兴趣小组对无明显现象的中和反应进行“可视化”探究。
(2)取少量试管②实验后的溶液于试管中,向其中滴入酚酞溶液,观察到 ,证明稀盐酸与NaOH溶液一定发生了化学反应。
【拓展提升】验证中和反应有水生成。实验装置如图2所示,硅胶吸水后由蓝色变为红色。
(3)证明中和反应有水生成的现象是________________________________________________________。
(4)能证明中和反应放热的现象是__________________________________________________________。
第2课时 溶液酸碱度的表示法——pH
1.下列是一些生活中常见物质的pH,其中酸性最强的是( )
A.葡萄汁:3.5~4.5 B.玉米粥:7.0~8.0
C.牛奶:6.0~7.0 D.牙膏:8.0~9.0
2.以下是几种花卉生长最适宜的pH范围。若某地土壤呈弱酸性,则不宜种植的是( )
A.杜鹃花5.5~6.2 B.兰花6.5~6.8
C.薰衣草7.0~7.9 D.山茶花5.6~6.6
3.(2022郑州模拟)欲使pH=3的盐酸的pH升高到7,可以加入( )
A.过量的水 B.过量的生石灰
C.过量的熟石灰 D.过量的石灰石
4.(2021秋泰安期中)下列有关溶液酸碱性的说法错误的是( )
A.pH=7的溶液呈中性 B.呈碱性的溶液一定是碱溶液
C.pH<7的溶液一定呈酸性 D.pH越小的酸溶液的酸性越强
5.(2022合肥模拟)某同学想用pH试纸测定一些物质的pH,下列说法正确的是( )
A.能用干燥的pH试纸测定98%的浓硫酸的pH
B.测出草木灰水的pH为6
C.用湿润的pH试纸测定白醋的pH,结果会偏大
D.测出0.4%的氢氧化钠溶液的pH为12.7
6.(2021苏州中考)如图是室温下稀盐酸与稀氢氧化钠溶液反应过程中溶液pH的变化曲线。下列说法错误的是( )
A.该实验是将稀盐酸逐滴滴入稀氢氧化钠溶液中
B.a点到b点pH变化的原因是H+和OH-发生反应
C.b点时,参加反应的HCl与NaOH的质量比为36.5∶40
D.c点时,溶液中的Na+数目大于Cl-数目
7.某小型造纸厂非法向河中排放了大量碱性废液,请你根据所学知识,设计两种检测碱性废液的方法,并提出合理的治理措施。
实验操作 实验现象
(1) 取少量废液样品于试管中,滴加2~3滴 溶液 溶液变红
(2) 在白瓷板上放一小片pH试纸, 读出溶液pH 7 (填“>”“=”或“<”)
(3)你提出的一条治理措施是 。
8.(教材习题改编)某校“酸雨”(pH<5.6)测量小组的同学取刚降到地面的雨水样品,用pH计每隔五分钟测一次pH,记录数据如下:
测定时刻 5:05 5:10 5:15 5:20 5:25 5:30 5:35
pH 4.95 4.94 4.94 4.88 4.86 4.85 4.85
(1)正常雨水的pH<7的原因是 。
(2)由表中数据可知,该雨水 (填“是”或“不是”)酸雨,降到地面的雨水的酸性逐渐 (填“减弱”或“增强”)。
(3)该雨水pH发生变化的主要原因是其中的亚硫酸(化学式为H2SO3)与空气中的氧气反应生成硫酸,该反应的化学方程式为 。
参考答案
第1课时 中和反应及其在实际中的应用
1.D 2.B 3.C 4.A 5.D
6.①CH3COOH ②BaCO3 ③KOH ④H2CO3 ⑤Fe(OH)3
⑥HNO3 ⑦AgCl ⑧K2CO3 ①④⑥ ③⑤ ②⑦⑧
7.Na2CO3、NaOH NaOH+HCl=== NaCl+H2O
8.(1)CaCO3 (2)Mg(OH)2+2HCl=== MgCl2+2H2O
9.(1)①Na+、SO ②H+ OH- H2O
(2)①Ba(OH)2+H2SO4=== BaSO4↓+2H2O ②红
10.解:设将该废水恰好完全中和需要熟石灰的质量为x。
Ca(OH)2+2HCl=== CaCl2+2H2O
74 73
x 1.0×106 kg×0.003 65%
=,x=37 kg
答:需要37 kg熟石灰才能将该废水恰好完全中和。
11.(1)固体溶解 (2)无明显现象
(3)甲、乙中硅胶不变色,丙中硅胶由蓝色变为红色
(4)丙中U形管左端液面降低,右端液面升高
第2课时 溶液酸碱度的表示法——pH
1.A 2.C 3.D 4.B 5.C 6.D
7.(1)酚酞
(2)用玻璃棒蘸取废液样品滴到pH试纸上,将试纸显示的颜色与标准比色卡比较 >
(3)加入稀硫酸,调节废液的pH至7后再排放(合理即可)
8.(1)二氧化碳与水反应生成碳酸
(2)是 增强 (3)2H2SO3+O2=== 2H2SO4
同课章节目录
