【高效备课】人教版(2019)化学必修一 同步课件 2.3.2气体摩尔体积(37张ppt)
文档属性
| 名称 | 【高效备课】人教版(2019)化学必修一 同步课件 2.3.2气体摩尔体积(37张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 3.1MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-09-15 00:00:00 | ||
图片预览




文档简介
(共38张PPT)
2.3.2 气体摩尔体积
人教版(2019)必修一
高一上学期
第二章
海水中的重要元素——钠和氯
第一节
钠及其化合物
第三节
物质的量
第二节
氯及其化合物
目录/
DIRECTORY
1
3
影响物质体积的因素
气体摩尔体积
2
阿伏伽德罗定律及其推论
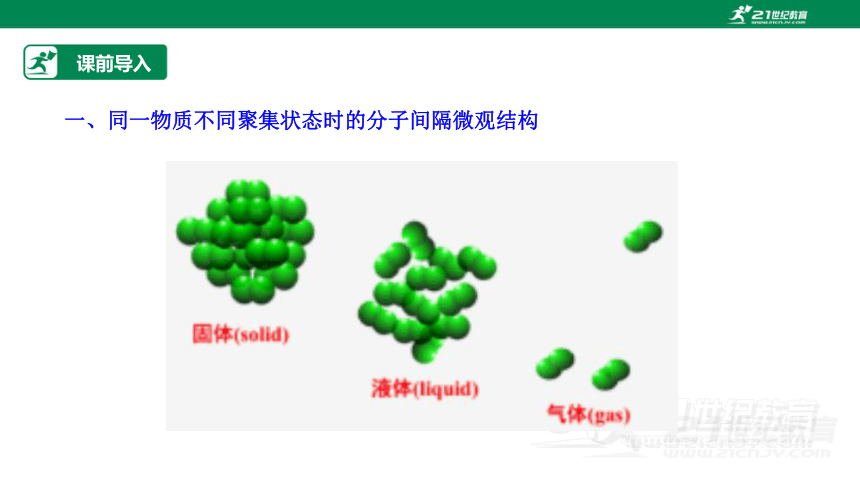
课前导入
一、同一物质不同聚集状态时的分子间隔微观结构
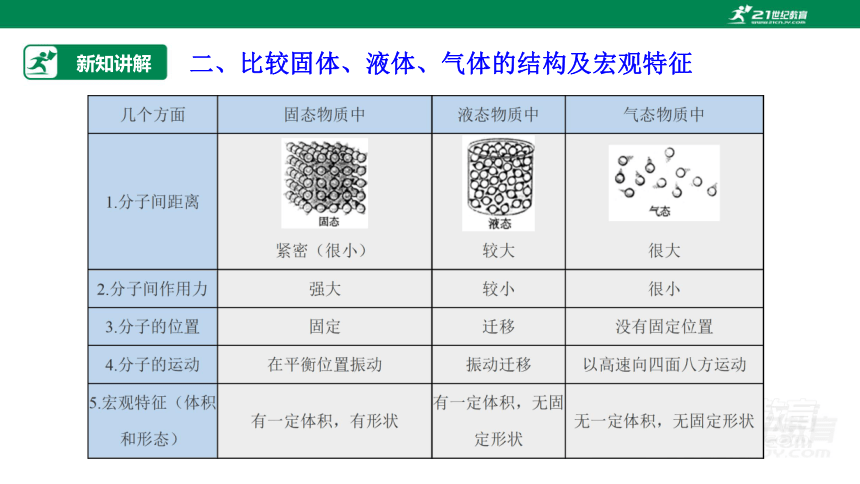
新知讲解
二、比较固体、液体、气体的结构及宏观特征
新知讲解
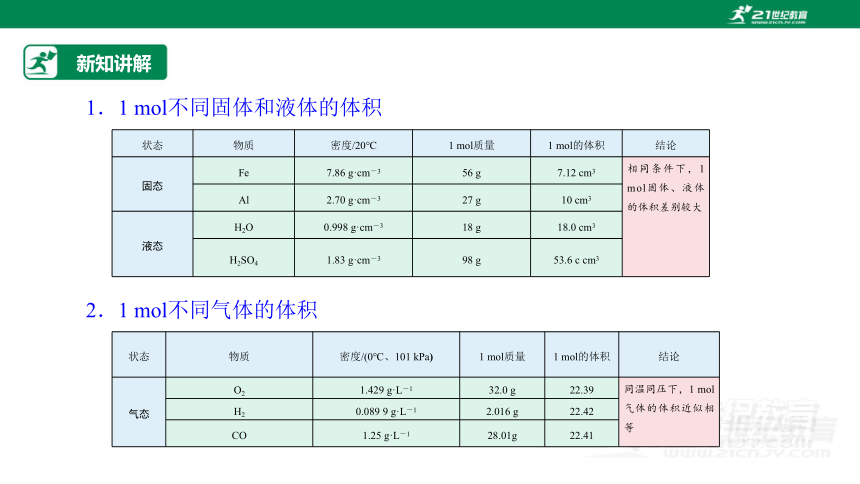
1.1 mol不同固体和液体的体积
状态 物质 密度/20℃ 1 mol质量 1 mol的体积 结论
固态 Fe 7.86 g·cm-3 56 g 7.12 cm3 相同条件下,1 mol固体、液体的体积差别较大
Al 2.70 g·cm-3 27 g 10 cm3
液态 H2O 0.998 g·cm-3 18 g 18.0 cm3
H2SO4 1.83 g·cm-3 98 g 53.6 c cm3
2.1 mol不同气体的体积
状态 物质 密度/(0℃、101 kPa) 1 mol质量 1 mol的体积 结论
气态 O2 1.429 g·L-1 32.0 g 22.39 同温同压下,1 mol气体的体积近似相等
H2 0.089 9 g·L-1 2.016 g 22.42
CO 1.25 g·L-1 28.01g 22.41
新知讲解
3.结论
相同条件下,等物质的量(如1mol )固体或液体的体积一般______,但气体的体积却_________相同。
且温度压强相同时,气体的物质的量之比等于_____之比
不同
几乎完全
体积
新知讲解
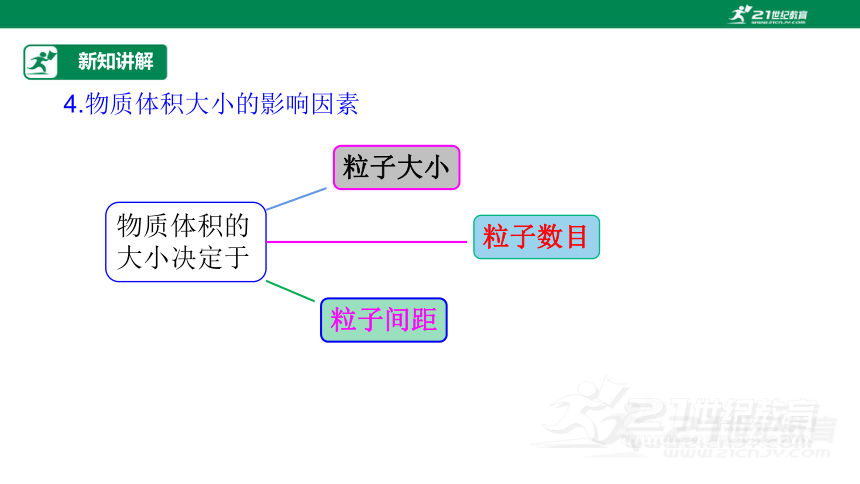
物质体积的大小决定于
粒子数目
粒子大小
粒子间距
4.物质体积大小的影响因素
新知讲解
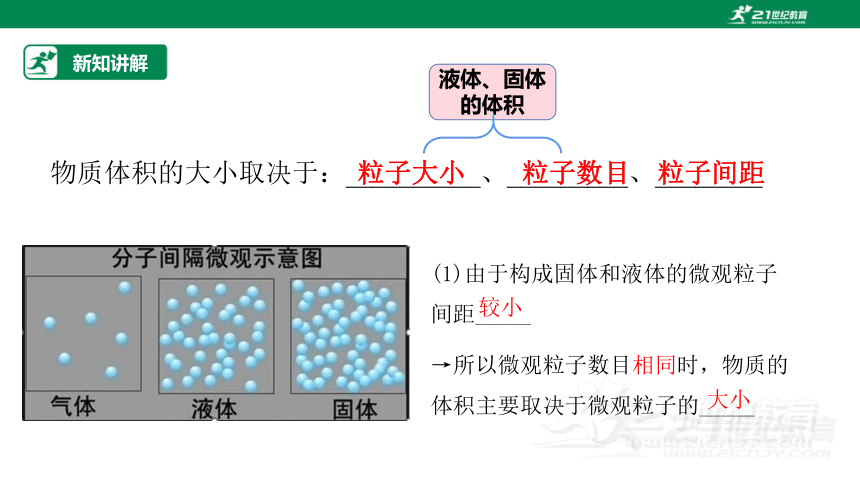
物质体积的大小取决于:__________、_________、________
粒子数目
粒子大小
粒子间距
液体、固体
的体积
(1)由于构成固体和液体的微观粒子间距_____
→所以微观粒子数目相同时,物质的体积主要取决于微观粒子的_____
较小
大小
新知讲解
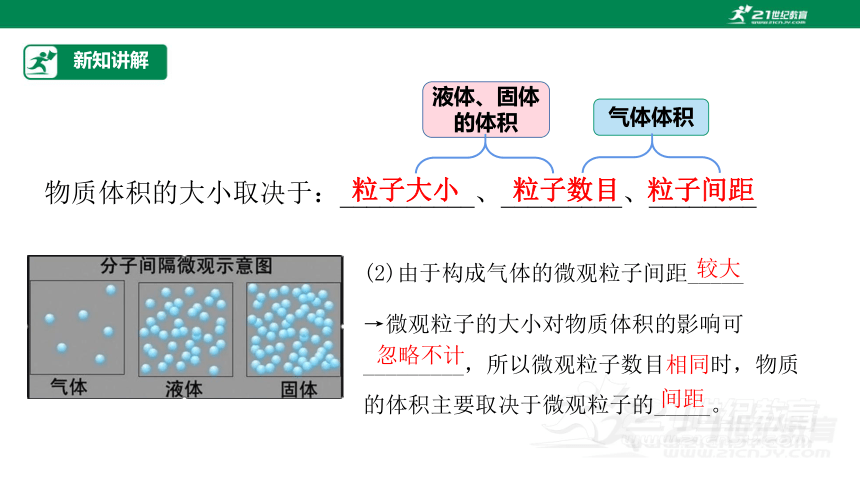
物质体积的大小取决于:__________、_________、________
粒子数目
粒子大小
粒子间距
气体体积
(2)由于构成气体的微观粒子间距_____
→微观粒子的大小对物质体积的影响可_________,所以微观粒子数目相同时,物质的体积主要取决于微观粒子的_____。
较大
忽略不计
间距
液体、固体
的体积
新知讲解
粒子数目
粒子间距
温度越高,气体的粒子间距______
压强越大,气体的粒子间距______
同温同压下,气体的粒子间距____
在相同的______和______下,等物质的量的任何气体的体积_______
温度
压强
都相同
越大
越小
相等
气体体积
结论:
课堂练习
【例1】关于决定物质体积的因素,说法错误的是
A.物质的体积取决于微粒数目、微粒大小和微粒间距
B.同温同压下,相同体积的任何气体具有相同数目的分子
C.同温同压下,1mol任何物质所占有的体积均相同
D.等质量的H2,压强越小、温度越高,气体所占体积越大
C
课堂练习
【例2】影响气体体积的微观因素主要有
A.微粒大小和数目 B.微粒数目和间距
C.微粒间距和大小 D.以上说法均错误
B
课堂练习
【例3】同温同压时,相同质量的下列气体中体积最大的是
A.N2 B.HCl C.H2 D.Cl2
C
课堂练习
【例4】
B
新知讲解
二、阿伏加德罗定律及其推论
__________下,相同_____的任何气体都含有相同的________
同温同压
体积
分子数
1.阿伏加德罗定律
三同定一同
同温同压下,气体的粒子间距相等
粒子数目
粒子间距
气体体积
阿伏加德罗定律及其推论都可由理想气体状态方程(______________)及其变形推出
PV=nRT
2.依据
压强
体积
物
质
的
量
常数
温度
新知讲解
新知讲解
(1)同温同压下,气体的体积之比=其_________之比 =其_______之比,即
(2)同温同压下,气体的密度之比=其_________之比,即
P V = n R T
3.推论
物质的量
分子数
摩尔质量
新知讲解
(3)同温同体积下,气体的压强之比=其_________之比,即
(4)同温、同体积、同质量下,气体的压强与其摩尔质量______
(5)同温时,等物质的量的气体的压强与体积________
PV=nRT
3. 推论
成反比
物质的量
成反比
【例5】常温常压下,相同体积的下列气体密度最大的是( )
A.O3 B.CH4 C.NH3 D.Ne
A
【例6】关于同温、同压下,相同体积的CO2与CO
A.物质的量不相等 B.所含分子数相等
C.密度相等 D.所含氧原子个数相等
B
课堂练习
【例7】在相同温度的和压强下,50ml气体A2和100ml气体B2化合生成100mlC,则C的化学为
A.AB2 B.A2B C.A2B4 D.AB
A
课堂练习
课堂练习
【例8】在标准状况下,一个密闭容器中盛有11g CO2。如果在相同温度下,把更多的CO2充入容器中,使容器内压压强增至5×105Pa,这时容器内气体的分子数约为( )
A.3.3×1025 B.3.3×1024
C.7.5×1023 D.7.5×1022
C
课堂练习
【例9】下列关于阿伏伽德罗定律说法中,正确的是
A.含有相同分子数的两种气体,占有相同的体积
B.同温同压下,相同质量的两种任何气体,含有相同的分子数
C.相同物质的量两种气体,占有相同的体积
D.同温同压下,2升O2与2升CO2含有相同的分子数
D
课堂练习
【例10】
D
新知讲解
1.定义
升每摩尔(L/mol)
三、气体摩尔体积
单位_________的气体所占的_____,符号为____
体积
物质的量
Vm
2.单位
3.相关公式
n
=
V
Vm
气体体积,单位:L
气体摩尔体积,单位:L/mol
物质的量,单位mol
新知讲解
4.注意事项
(1)Vm的数值与______和______有关
(2)温度压强一定时,Vm是 _____
标准状况( ℃, kPa)下Vm约为__________
(3)用“22.4L/mol”作为气体摩尔体积进行计算时,必须确保是
______,且在__________
温度
压强
定值
22.4L/mol
气体
标准状况下
0
101
标况下,1mol任何气体的体积约为22.4L
课堂练习
【例11】判断下列说法是否正确。
(1)常温常压下,NA个SO2分子的体积约为22.4L。 ( )
(2)标准状况下,1mol任何气体的体积都约为22.4升。 ( )
(3)常温常压下,32gSO2气体含有0.5NA个分子。 ( )
(4)标准状况下,NA个水分子的体积约为22.4L。 ( )
(5)25℃,101KPa下,NA个SO2分子构成的气体的体积大于22.4L。 ( )
(6)0℃,101kPa下,11.2L氦气含有的原子数为NA个。 ( )
×
√
×
√
√
×
课堂练习
【例12】下列有关气体摩尔体积的描述正确的是
A.单位物质的量的物质所占的体积就是气体摩尔体积
B.通常状况下,气体摩尔体积约为22.4 L·mol-1
C.标准状况下,气体摩尔体积约为22.4 L·mol-1
D.标准状况下,1摩尔水的体积约为22.4 L
C
课堂练习
【例13】下列说法不正确的是
A.标准状况下,气体摩尔体积约为22.4 L/mol
B.非标准状况下,任何气体1 mol不可能为22.4 L
C.标准状况下,1 mol任何气体都约含有6.02×1023个分子
D.标准状况下,1 mol H2和O2的混合气体的体积约为22.4 L
B
课堂练习
【例14】下列各物质中所含原子个数由多到少的顺序正确的是_______
①0.5mol的氯气 ②标准状况下22.4L氢气
③4℃时9mL的水 ④0.2mol的磷酸
②④③①
课堂练习
【例15】标准状况下有①6.72LCH4 ②3.01×1023个HCl分子 ③13.6gH2S,下列对这三种气体的关系从小到大的排列顺序是:
(1)物质的量___________; (2)体积___________;
(3)质量_______________; (4)氢原子数_________。
①③②
①③②
①③②
②③①
课堂练习
【例16】下列物质中,在标准状况下体积最大的是
A.28g N2 B.1mol N2 C.48g O2 D.2mol O2
D
课堂练习
【例17】同温同压下,A容器中充满O2,B容器中充满O3。
(1)若所含分子总数相等,则A容器和B容器的容积之比是_______。
(2)若两容器中所含气体原子总数相等,则A容器和B容器的容积之比是_______。
(3)若两容器的容积之比为3∶2,则O2和O3的物质的量之比为______,质量之比为_______,密度之比为______。
1:1
3:2
3:2
1:1
2:3
课堂练习
【例18】
0.2mol
88
111g/mol
40
11:7
③>①>②
课堂练习
【例19】同温同压下,500mL气体R的质量为1.2g,1.5LO2的质量为2.4g,则R的相对分子质量为_______。
48
课堂练习
【例20】回答下列问题:
(1)0.5 molNH3的质量是___________,在标准状况下的体积为___________。
(2)7.8 gNa2X中含有Na+0.2 mol,则Na2X的摩尔质量为___________,X的相对原子质量为___________。
(3)某气体在标准状况下的密度为1.25 g/L,则28g该气体所含有的分子数为___________。
(4)设NA表示阿伏加德罗常数的值,0.2 molCH4中含有的电子数是___________个。
8.5 g
11.2L
78 g/mol
32
NA
2NA
谢谢
21世纪教育网(www.21cnjy.com)
中小学教育资源网站
兼职招聘:
https://www.21cnjy.com/recruitment/home/admin
2.3.2 气体摩尔体积
人教版(2019)必修一
高一上学期
第二章
海水中的重要元素——钠和氯
第一节
钠及其化合物
第三节
物质的量
第二节
氯及其化合物
目录/
DIRECTORY
1
3
影响物质体积的因素
气体摩尔体积
2
阿伏伽德罗定律及其推论
课前导入
一、同一物质不同聚集状态时的分子间隔微观结构
新知讲解
二、比较固体、液体、气体的结构及宏观特征
新知讲解
1.1 mol不同固体和液体的体积
状态 物质 密度/20℃ 1 mol质量 1 mol的体积 结论
固态 Fe 7.86 g·cm-3 56 g 7.12 cm3 相同条件下,1 mol固体、液体的体积差别较大
Al 2.70 g·cm-3 27 g 10 cm3
液态 H2O 0.998 g·cm-3 18 g 18.0 cm3
H2SO4 1.83 g·cm-3 98 g 53.6 c cm3
2.1 mol不同气体的体积
状态 物质 密度/(0℃、101 kPa) 1 mol质量 1 mol的体积 结论
气态 O2 1.429 g·L-1 32.0 g 22.39 同温同压下,1 mol气体的体积近似相等
H2 0.089 9 g·L-1 2.016 g 22.42
CO 1.25 g·L-1 28.01g 22.41
新知讲解
3.结论
相同条件下,等物质的量(如1mol )固体或液体的体积一般______,但气体的体积却_________相同。
且温度压强相同时,气体的物质的量之比等于_____之比
不同
几乎完全
体积
新知讲解
物质体积的大小决定于
粒子数目
粒子大小
粒子间距
4.物质体积大小的影响因素
新知讲解
物质体积的大小取决于:__________、_________、________
粒子数目
粒子大小
粒子间距
液体、固体
的体积
(1)由于构成固体和液体的微观粒子间距_____
→所以微观粒子数目相同时,物质的体积主要取决于微观粒子的_____
较小
大小
新知讲解
物质体积的大小取决于:__________、_________、________
粒子数目
粒子大小
粒子间距
气体体积
(2)由于构成气体的微观粒子间距_____
→微观粒子的大小对物质体积的影响可_________,所以微观粒子数目相同时,物质的体积主要取决于微观粒子的_____。
较大
忽略不计
间距
液体、固体
的体积
新知讲解
粒子数目
粒子间距
温度越高,气体的粒子间距______
压强越大,气体的粒子间距______
同温同压下,气体的粒子间距____
在相同的______和______下,等物质的量的任何气体的体积_______
温度
压强
都相同
越大
越小
相等
气体体积
结论:
课堂练习
【例1】关于决定物质体积的因素,说法错误的是
A.物质的体积取决于微粒数目、微粒大小和微粒间距
B.同温同压下,相同体积的任何气体具有相同数目的分子
C.同温同压下,1mol任何物质所占有的体积均相同
D.等质量的H2,压强越小、温度越高,气体所占体积越大
C
课堂练习
【例2】影响气体体积的微观因素主要有
A.微粒大小和数目 B.微粒数目和间距
C.微粒间距和大小 D.以上说法均错误
B
课堂练习
【例3】同温同压时,相同质量的下列气体中体积最大的是
A.N2 B.HCl C.H2 D.Cl2
C
课堂练习
【例4】
B
新知讲解
二、阿伏加德罗定律及其推论
__________下,相同_____的任何气体都含有相同的________
同温同压
体积
分子数
1.阿伏加德罗定律
三同定一同
同温同压下,气体的粒子间距相等
粒子数目
粒子间距
气体体积
阿伏加德罗定律及其推论都可由理想气体状态方程(______________)及其变形推出
PV=nRT
2.依据
压强
体积
物
质
的
量
常数
温度
新知讲解
新知讲解
(1)同温同压下,气体的体积之比=其_________之比 =其_______之比,即
(2)同温同压下,气体的密度之比=其_________之比,即
P V = n R T
3.推论
物质的量
分子数
摩尔质量
新知讲解
(3)同温同体积下,气体的压强之比=其_________之比,即
(4)同温、同体积、同质量下,气体的压强与其摩尔质量______
(5)同温时,等物质的量的气体的压强与体积________
PV=nRT
3. 推论
成反比
物质的量
成反比
【例5】常温常压下,相同体积的下列气体密度最大的是( )
A.O3 B.CH4 C.NH3 D.Ne
A
【例6】关于同温、同压下,相同体积的CO2与CO
A.物质的量不相等 B.所含分子数相等
C.密度相等 D.所含氧原子个数相等
B
课堂练习
【例7】在相同温度的和压强下,50ml气体A2和100ml气体B2化合生成100mlC,则C的化学为
A.AB2 B.A2B C.A2B4 D.AB
A
课堂练习
课堂练习
【例8】在标准状况下,一个密闭容器中盛有11g CO2。如果在相同温度下,把更多的CO2充入容器中,使容器内压压强增至5×105Pa,这时容器内气体的分子数约为( )
A.3.3×1025 B.3.3×1024
C.7.5×1023 D.7.5×1022
C
课堂练习
【例9】下列关于阿伏伽德罗定律说法中,正确的是
A.含有相同分子数的两种气体,占有相同的体积
B.同温同压下,相同质量的两种任何气体,含有相同的分子数
C.相同物质的量两种气体,占有相同的体积
D.同温同压下,2升O2与2升CO2含有相同的分子数
D
课堂练习
【例10】
D
新知讲解
1.定义
升每摩尔(L/mol)
三、气体摩尔体积
单位_________的气体所占的_____,符号为____
体积
物质的量
Vm
2.单位
3.相关公式
n
=
V
Vm
气体体积,单位:L
气体摩尔体积,单位:L/mol
物质的量,单位mol
新知讲解
4.注意事项
(1)Vm的数值与______和______有关
(2)温度压强一定时,Vm是 _____
标准状况( ℃, kPa)下Vm约为__________
(3)用“22.4L/mol”作为气体摩尔体积进行计算时,必须确保是
______,且在__________
温度
压强
定值
22.4L/mol
气体
标准状况下
0
101
标况下,1mol任何气体的体积约为22.4L
课堂练习
【例11】判断下列说法是否正确。
(1)常温常压下,NA个SO2分子的体积约为22.4L。 ( )
(2)标准状况下,1mol任何气体的体积都约为22.4升。 ( )
(3)常温常压下,32gSO2气体含有0.5NA个分子。 ( )
(4)标准状况下,NA个水分子的体积约为22.4L。 ( )
(5)25℃,101KPa下,NA个SO2分子构成的气体的体积大于22.4L。 ( )
(6)0℃,101kPa下,11.2L氦气含有的原子数为NA个。 ( )
×
√
×
√
√
×
课堂练习
【例12】下列有关气体摩尔体积的描述正确的是
A.单位物质的量的物质所占的体积就是气体摩尔体积
B.通常状况下,气体摩尔体积约为22.4 L·mol-1
C.标准状况下,气体摩尔体积约为22.4 L·mol-1
D.标准状况下,1摩尔水的体积约为22.4 L
C
课堂练习
【例13】下列说法不正确的是
A.标准状况下,气体摩尔体积约为22.4 L/mol
B.非标准状况下,任何气体1 mol不可能为22.4 L
C.标准状况下,1 mol任何气体都约含有6.02×1023个分子
D.标准状况下,1 mol H2和O2的混合气体的体积约为22.4 L
B
课堂练习
【例14】下列各物质中所含原子个数由多到少的顺序正确的是_______
①0.5mol的氯气 ②标准状况下22.4L氢气
③4℃时9mL的水 ④0.2mol的磷酸
②④③①
课堂练习
【例15】标准状况下有①6.72LCH4 ②3.01×1023个HCl分子 ③13.6gH2S,下列对这三种气体的关系从小到大的排列顺序是:
(1)物质的量___________; (2)体积___________;
(3)质量_______________; (4)氢原子数_________。
①③②
①③②
①③②
②③①
课堂练习
【例16】下列物质中,在标准状况下体积最大的是
A.28g N2 B.1mol N2 C.48g O2 D.2mol O2
D
课堂练习
【例17】同温同压下,A容器中充满O2,B容器中充满O3。
(1)若所含分子总数相等,则A容器和B容器的容积之比是_______。
(2)若两容器中所含气体原子总数相等,则A容器和B容器的容积之比是_______。
(3)若两容器的容积之比为3∶2,则O2和O3的物质的量之比为______,质量之比为_______,密度之比为______。
1:1
3:2
3:2
1:1
2:3
课堂练习
【例18】
0.2mol
88
111g/mol
40
11:7
③>①>②
课堂练习
【例19】同温同压下,500mL气体R的质量为1.2g,1.5LO2的质量为2.4g,则R的相对分子质量为_______。
48
课堂练习
【例20】回答下列问题:
(1)0.5 molNH3的质量是___________,在标准状况下的体积为___________。
(2)7.8 gNa2X中含有Na+0.2 mol,则Na2X的摩尔质量为___________,X的相对原子质量为___________。
(3)某气体在标准状况下的密度为1.25 g/L,则28g该气体所含有的分子数为___________。
(4)设NA表示阿伏加德罗常数的值,0.2 molCH4中含有的电子数是___________个。
8.5 g
11.2L
78 g/mol
32
NA
2NA
谢谢
21世纪教育网(www.21cnjy.com)
中小学教育资源网站
兼职招聘:
https://www.21cnjy.com/recruitment/home/admin
