九年级化学上册课题3 制取氧气 讲义
图片预览

文档简介
课题6 制取氧气
1.反应原理及制取装置
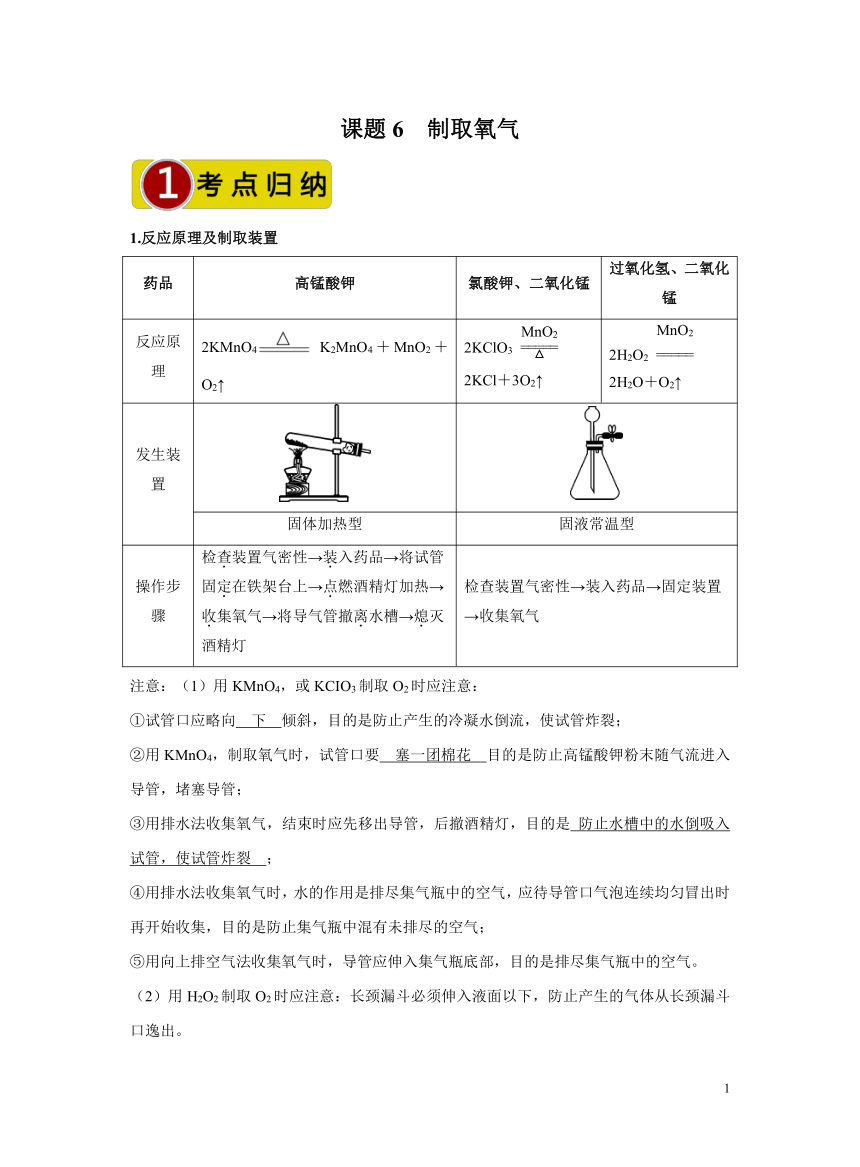
药品 高锰酸钾 氯酸钾、二氧化锰 过氧化氢、二氧化锰
反应原理 2KMnO4 K2MnO4+MnO2+O2↑ 2KClO3 2KCl+3O2↑ 2H2O2 2H2O+O2↑
发生装置
固体加热型 固液常温型
操作步骤 检查装置气密性→装入药品→将试管固定在铁架台上→点燃酒精灯加热→收集氧气→将导气管撤离水槽→熄灭酒精灯 检查装置气密性→装入药品→固定装置→收集氧气
注意:(1)用KMnO4,或KCIO3制取O2时应注意:
①试管口应略向 下 倾斜,目的是防止产生的冷凝水倒流,使试管炸裂;
②用KMnO4,制取氧气时,试管口要 塞一团棉花 目的是防止高锰酸钾粉末随气流进入导管,堵塞导管;
③用排水法收集氧气,结束时应先移出导管,后撤酒精灯,目的是 防止水槽中的水倒吸入试管,使试管炸裂 ;
④用排水法收集氧气时,水的作用是排尽集气瓶中的空气,应待导管口气泡连续均匀冒出时再开始收集,目的是防止集气瓶中混有未排尽的空气;
⑤用向上排空气法收集氧气时,导管应伸入集气瓶底部,目的是排尽集气瓶中的空气。
(2)用H2O2制取O2时应注意:长颈漏斗必须伸入液面以下,防止产生的气体从长颈漏斗口逸出。
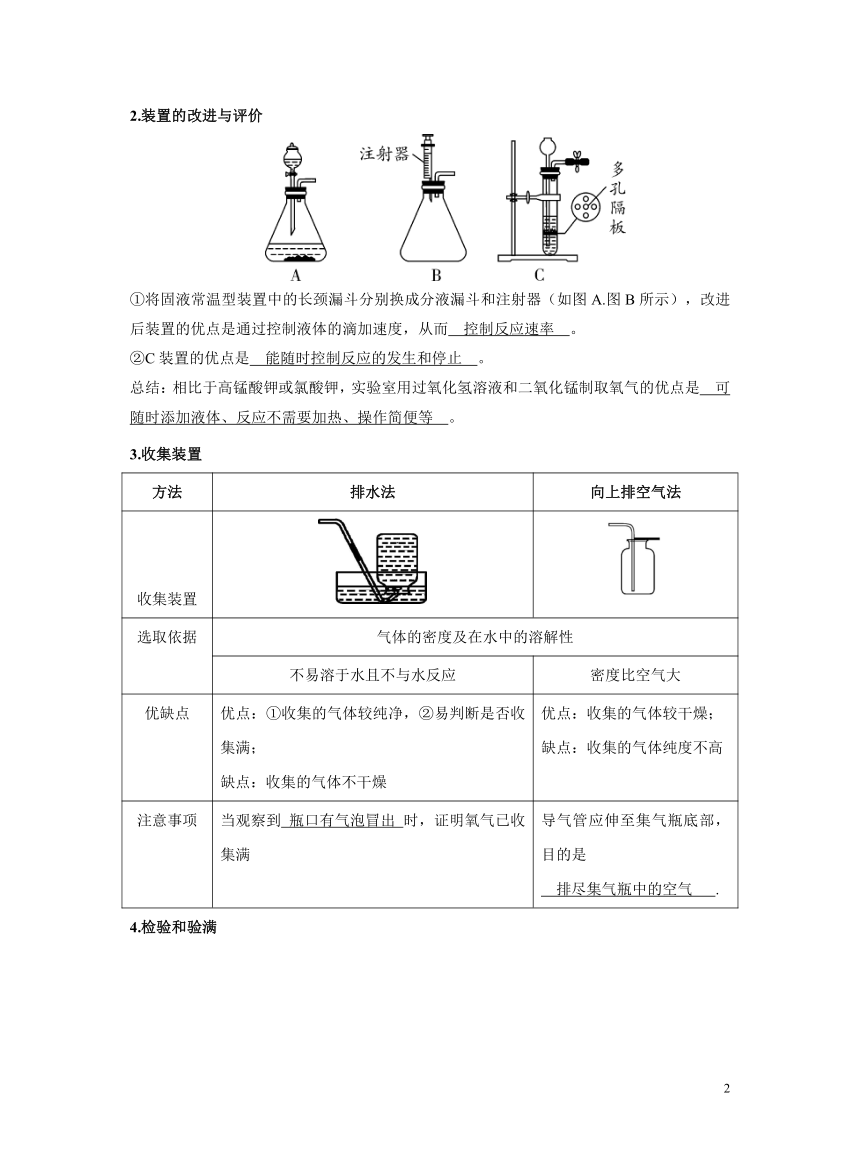
2.装置的改进与评价
①将固液常温型装置中的长颈漏斗分别换成分液漏斗和注射器(如图A.图B所示),改进后装置的优点是通过控制液体的滴加速度,从而 控制反应速率 。
②C装置的优点是 能随时控制反应的发生和停止 。
总结:相比于高锰酸钾或氯酸钾,实验室用过氧化氢溶液和二氧化锰制取氧气的优点是 可随时添加液体、反应不需要加热、操作简便等 。
3.收集装置
方法 排水法 向上排空气法
收集装置
选取依据 气体的密度及在水中的溶解性
不易溶于水且不与水反应 密度比空气大
优缺点 优点:①收集的气体较纯净,②易判断是否收集满;缺点:收集的气体不干燥 优点:收集的气体较干燥;缺点:收集的气体纯度不高
注意事项 当观察到 瓶口有气泡冒出 时,证明氧气已收集满 导气管应伸至集气瓶底部,目的是 排尽集气瓶中的空气 .
4.检验和验满
检验 将带火星的木条伸入集气瓶瓶内,如果木条复燃,证明收集的气体是氧气
验满 向上排空气法:将带火星的木条放在集气瓶瓶口,如果木条复燃,说明氧气已集满
排水法:当有大量气泡从集气瓶瓶口冒出时,说明氧气已集满
(4)操作步骤
以加热高锰酸钾制取氧气为例:查、装、定、点、收、离、熄。
①查:检查装置的气密性;
②装:把药品装入试管内,使之平铺在试管底部;
③定:把试管固定在铁架台上;
④点:点燃酒精灯加热;
⑤收:收集气体;
⑥离:将导管撤离水槽;
⑦熄:熄灭酒精灯。
拓展:无法收集到较纯净氧气的可能原因:
(1)装置气密性不好。
(2)用向上排空气法收集时导管未伸到集气瓶底部。
(3)用排水法收集时,未等导管口有连续、均匀地气泡冒出时就开始收集。
5.“多功能瓶”的应用
装置 功能 气体进出方向
排空气法收集气体 密度大于空气的气体 b进a出
密度小于空气的气体 a进b出
排水法收集气体 a进b出
检验、除杂、干燥气体 b进a出
6.干燥剂及干燥装置:
(1)常见气体的干燥剂及适用范围:
①浓硫酸——干燥酸性气体和中性气体,如氧气、二氧化碳、氮气等。
②氢氧化钠固体、碱石灰(CaO与NaOH的固体混合物)——干燥碱性气体和中性气体,如氨气、氮气等。
(2)干燥装置如图所示:
1.实验室用过氧化氢溶液和二氧化锰制取氧气,一定不需要用到的仪器是
A.酒精灯 B.水槽 C.集气瓶 D.分液漏斗
【答案】A
【解析】实验室用过氧化氢溶液和二氧化锰混合制取氧气,是固液常温型反应,不需要加热,故不需要酒精灯。故选A。
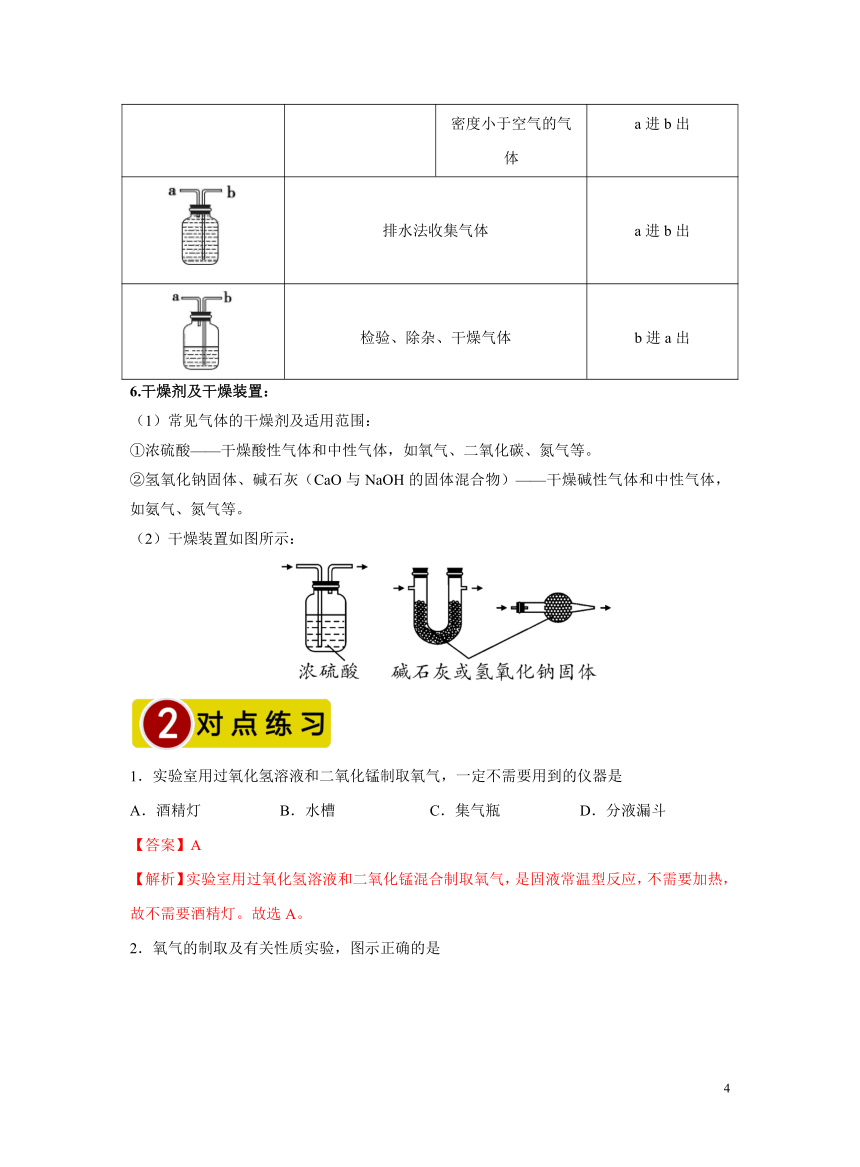
2.氧气的制取及有关性质实验,图示正确的是
A.制氧气 B.收集氧气
C.铁丝燃烧 D.测定空气中氧气的体积分数
【答案】C
【解析】A.为防止加热时产生的冷凝水倒流,加热固体制取气体时试管口应低于试管底部,图示操作错误;
B.利用向上排空气法收集氧气,试管口不能放塞子,应放玻璃片,便于排空气,图示操作错误;
C.铁丝在氧气中燃烧,集气瓶底要放一些水或沙子,防止燃烧后的高温熔融物溅落炸裂瓶底,图示操作正确;
D.木炭燃烧消耗氧气,但又生成二氧化碳,使瓶内气压变化不大,水不能倒流,无法测出氧气的体积分数,图示操作错误。故选C。
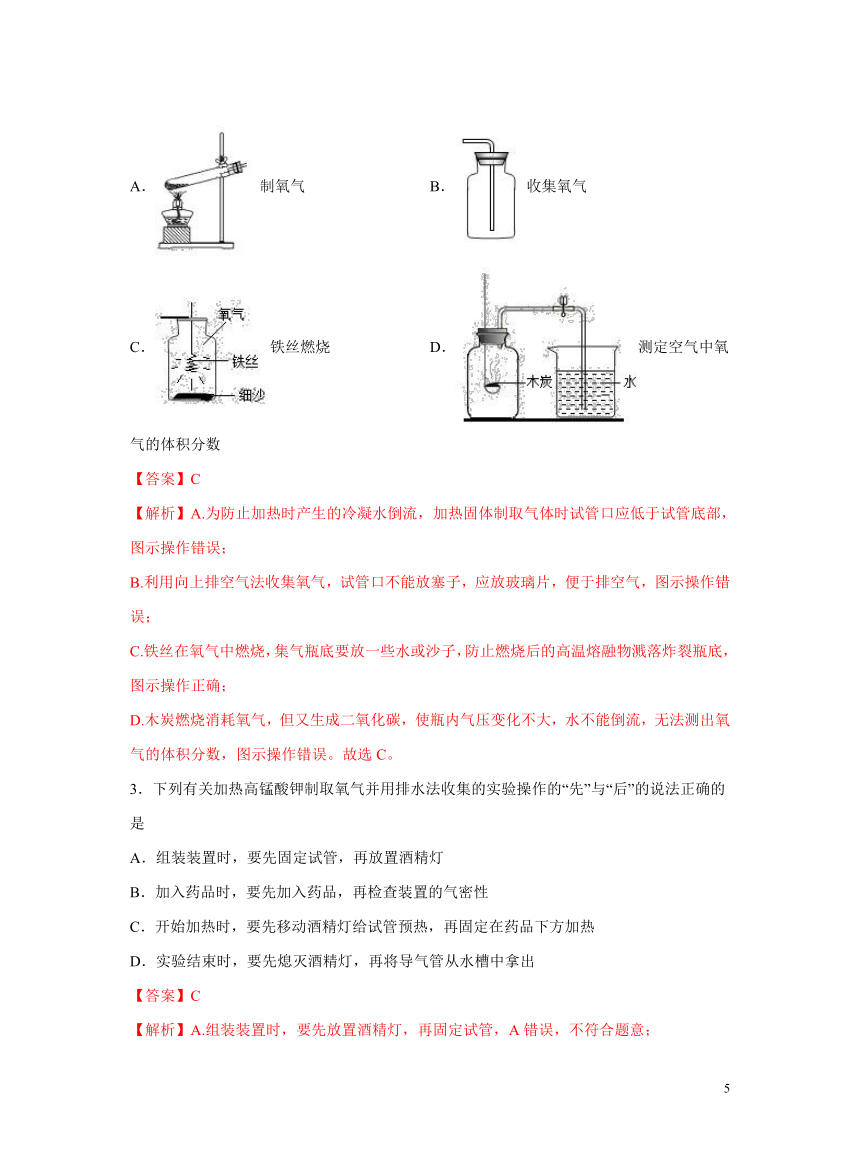
3.下列有关加热高锰酸钾制取氧气并用排水法收集的实验操作的“先”与“后”的说法正确的是
A.组装装置时,要先固定试管,再放置酒精灯
B.加入药品时,要先加入药品,再检查装置的气密性
C.开始加热时,要先移动酒精灯给试管预热,再固定在药品下方加热
D.实验结束时,要先熄灭酒精灯,再将导气管从水槽中拿出
【答案】C
【解析】A.组装装置时,要先放置酒精灯,再固定试管,A错误,不符合题意;
B.加入药品时,先检查装置的气密性再加入药品,B错误,不符合题意;
C.开始加热时,要先移动酒精灯给试管预热,再固定在药品下方加热,操作正确,符合题意;
D.实验结束时,要先将导气管从水槽中拿出,再熄灭酒精灯,D错误,不符合题意;
故选:C。
4.实验室用加热高锰酸钾制取氧气的主要操作有:①点燃酒精灯,加热;②检查装置的气密性;③装药品;④熄灭酒精灯;⑤收集气体;⑥把试管固定在铁架台上;⑦将导管撤离水槽。正确的顺序是
A.②③⑥①⑤⑦④ B.②③⑥①⑤④⑦
C.③②①⑥⑤⑦④ D.①②③⑤⑥④⑦
【答案】A
【解析】其操作顺序正确的是:检查装置的气密性,装入高锰酸钾,并在试管口放一团棉花,用带导管的胶塞塞紧,并将试管固定在铁架台上,点燃酒精灯给试管加热,用排水法收集氧气,从水槽中取出导管,熄灭酒精灯。
故填:A。
5.下列关于O2的实验室制法及性质实验的说法不正确的是
A制O2的药品 B发生装置 C收集装置 D验证O2的可燃性
【答案】D
【解析】A.实验室中用过氧化氢和二氧化锰制氧气,选项正确;
B.过氧化氢和二氧化锰制氧气属于固液常温型,可以采用B中装置制取,选项正确;
C.氧气密度比空气大,可以采用向上排空气法收集,选项正确;
D.氧气具有助燃性,不具可燃性,选项错误。
故选:D。
6.如图所示四种途径都可以得到O2(反应条件已省略),下列说法错误的是
A.根据绿色化学理念,甲途径是实验室制O2的最佳方案
B.为了使甲、乙两种途径更快地得到O2,还需要加入催化剂
C.甲、乙和丙途径中发生化学变化的基本反应类型都是分解反应
D.工业上采用途径丁制取大量O2,主要是利用了N2和O2的密度不同
【答案】D
【解析】A.乙途径和丙途径需要加热,丁途径需要让空气液化,需要外界提供能量,根据绿色化学理念,甲途径是实验室制O2的最佳方案,A选项说法正确,不符合题意;
B.为了使甲、乙两种途径更快地得到O2,还需要加入催化剂,B选项说法正确,不符合题意;
C.甲、乙和丙途径中发生化学变化的基本反应类型都是分解反应,C选项说法正确,不符合题意;
D.工业上采用途径丁制取大量O2,主要是利用了N2和O2的沸点不同,D选项说法错误,符合题意。故选D。
7.某同学误将少量KMnO4当成MnO2加入KClO3中进行加热制取氧气,部分物质质量随时间变化如图所示。下列关于该过程的说法正确的是:
A.c代表氧气
B.t1时刻,O2 开始产生
C.t2时刻,KMnO4 开始分解
D.KMnO4是催化剂
【答案】B
【解析】根据题干所给信息可知,b物质的质量少,b是高锰酸钾,a是氯酸钾,在t1时刻高锰酸钾开始分解,有氧气生成,随着高锰酸钾的分解,二氧化锰的质量也在不断的增加,故A.C.D错误,B正确。故选B。
8.分析下列实验中出现的异常现象,并从给定的选择项中把可能的原因用字母填入括号内。
(1)实验室用高锰酸钾制氧气时试管破裂_______________;
(2)用高锰酸钾制氧气时水槽中的水变为紫红色_______________;
(3)将细铁丝伸入氧气瓶中却未能看到细铁丝发生燃烧______________;
(4)制氧气时加热后却发现管口没有气泡产生________________。
A.试管口未放棉花 B.试管外壁有水 C.装置漏气 D.氧气不纯
【答案】B A D C
【解析】(1)实验室用高锰酸钾制氧气时试管破裂,可能是试管外壁有水,使试管受热不均匀发生破裂;(2)用高锰酸钾制氧气时水槽中的水变为紫红色,可能是试管口未放棉花,高锰酸钾颗粒通过导气管进入水中;(3)将细铁丝伸入氧气瓶中却未能看到细铁丝发生燃烧可能是氧气不纯;(4)制氧气时加热后却发现管口没有气泡产生可能是装置漏气。
9.氧气是空气的主要成分,是一种化学性质比较活泼的物质。如图是工业上利用分离液态空气的方法得到氧气的流程示意图:
① 分离液态空气制氧气的过程主要发生_____(填“物理”或“化学”)变化。
② 已知:液氮的沸点为﹣196℃,液氧的沸点为﹣183℃,液态空气在蒸发时,首先蒸发出来的是_____(填化学式)。
③ 这样制得的氧气属_____(填“纯净物”或“混合物”)。
【答案】物理 N2 混合物
【解析】① 分离液态空气制氧气,是利用液态氮和液态氧的沸点不同,没有新物质生成,属于物理变化。
② 液氮的沸点为﹣196℃,液氧的沸点为﹣183℃,液氮的沸点比液氧的低,故液态空气在蒸发时,首先蒸发出来的是氮气,其化学式为:N2。
③ 剩余的液体为液态氧和液态稀有气体等,这样制得的氧气属于混合物。
故答案为
① 物理;② N2;③ 混合物。
10.如图是实验室制取气体常用装置,请根据题意回答下列问题:
(1)写出图中仪器①的名称:_____。
(2)实验室选用高锰酸钾制取氧气的文字表达式为_____,若选用A作为其发生装置,还缺少棉花,加棉花的目的是_____。若选用F装置收集氧气,气体应从_____(填a或b)端通入,通入一段时间后,要证明氧气已经收集满的操作是:_____,若木条复燃,则氧气已集满。
(3)某同学用B装置制取氧气,该反应的文字表达式为_____。B装置中长颈漏斗下端要形成液封,目的是_____。实验过程中该同学观察到B中反应太快,不利于气体收集,他可选择下列措施中的_____(填序号)解决该问题。
A 将长颈漏斗换成注射器
B 向装置中加入适量蒸馏水
C 将锥形瓶换成试管
该同学要收集一瓶较纯净的氧气,他应选择上图中的_____(填装置序号)装置进行收集。收集时该同学看到B中液体里有大量气泡产生,但最终收集的氧气还不够纯净,原因可能是:
I、装置漏气;
II、_____。
(4)甲烷是一种无色无味密度小于空气的气体,它难溶于水,是一种常用的燃料。实验室中常加热醋酸钠固体和氢氧化钠固体混合物的方法制备甲烷,如果要制取并收集一瓶甲烷气体,可选择上图中的_____(填装置序号)装置。收集满甲烷气体的集气瓶盖上玻璃片后,要_____(填选“正放”或“倒放”)在试验台上。
【答案】锥形瓶 高锰酸钾锰酸钾+二氧化锰+氧气 防止高锰酸钾进入导管 b 将带火星的木条放在a导管口 过氧化氢水+氧气 防止生成的气体从长颈漏斗逸出 AB D 刚出现气泡就开始收集 AD或AE或AF 倒放
【解析】(1)图中仪器①的名称:锥形瓶;
(2)实验室选用高锰酸钾制取氧气的文字表达式为:高锰酸钾锰酸钾+二氧化锰+氧气;
若选用A作为其发生装置,还缺少棉花,加棉花的目的是防止高锰酸钾进入导管堵塞导管;
氧气的密度比空气大,用F装置收集氧气,气体应从b端通入;
通入一段时间后,要证明氧气已经收集满的操作是:将带火星的木条放在a导管口,若木条复燃,则氧气已集满;
(3) B装置属于固液常温型装置适用于双氧水和二氧化锰制氧气,文字表达式为:过氧化氢水+氧气。液封的目的是:防止生成的气体从长颈漏斗下端逸出;
实验过程中该同学观察到B中反应太快,不利于气体收集,可以选择减慢反应速度进行改进:
A.用注射器可以控制添加药品的速率故可以控制反应速率,正确;
B.加入蒸馏水以后过氧化氢浓度变低反应速率减慢,正确;
C.将锥形瓶换成试管不会影响反应速率,错误。故选AB;
题中要求收集的气体较纯净,排水法收集的氧气较纯净,故选D;
过早收集,没有等导管口有连续均匀的气泡冒出就开始收集,导致收集到了部分空气;
(4)制取甲烷时反应物为固体且需要加热,所以发生装置选择A装置;应为甲烷难溶于水,密度小于空气可选D.排水法收集、E向下排空气法收集。也可用F万用瓶进行收集。
因为甲烷密度比空气小所以放置时应该倒放。
1
1.反应原理及制取装置
药品 高锰酸钾 氯酸钾、二氧化锰 过氧化氢、二氧化锰
反应原理 2KMnO4 K2MnO4+MnO2+O2↑ 2KClO3 2KCl+3O2↑ 2H2O2 2H2O+O2↑
发生装置
固体加热型 固液常温型
操作步骤 检查装置气密性→装入药品→将试管固定在铁架台上→点燃酒精灯加热→收集氧气→将导气管撤离水槽→熄灭酒精灯 检查装置气密性→装入药品→固定装置→收集氧气
注意:(1)用KMnO4,或KCIO3制取O2时应注意:
①试管口应略向 下 倾斜,目的是防止产生的冷凝水倒流,使试管炸裂;
②用KMnO4,制取氧气时,试管口要 塞一团棉花 目的是防止高锰酸钾粉末随气流进入导管,堵塞导管;
③用排水法收集氧气,结束时应先移出导管,后撤酒精灯,目的是 防止水槽中的水倒吸入试管,使试管炸裂 ;
④用排水法收集氧气时,水的作用是排尽集气瓶中的空气,应待导管口气泡连续均匀冒出时再开始收集,目的是防止集气瓶中混有未排尽的空气;
⑤用向上排空气法收集氧气时,导管应伸入集气瓶底部,目的是排尽集气瓶中的空气。
(2)用H2O2制取O2时应注意:长颈漏斗必须伸入液面以下,防止产生的气体从长颈漏斗口逸出。
2.装置的改进与评价
①将固液常温型装置中的长颈漏斗分别换成分液漏斗和注射器(如图A.图B所示),改进后装置的优点是通过控制液体的滴加速度,从而 控制反应速率 。
②C装置的优点是 能随时控制反应的发生和停止 。
总结:相比于高锰酸钾或氯酸钾,实验室用过氧化氢溶液和二氧化锰制取氧气的优点是 可随时添加液体、反应不需要加热、操作简便等 。
3.收集装置
方法 排水法 向上排空气法
收集装置
选取依据 气体的密度及在水中的溶解性
不易溶于水且不与水反应 密度比空气大
优缺点 优点:①收集的气体较纯净,②易判断是否收集满;缺点:收集的气体不干燥 优点:收集的气体较干燥;缺点:收集的气体纯度不高
注意事项 当观察到 瓶口有气泡冒出 时,证明氧气已收集满 导气管应伸至集气瓶底部,目的是 排尽集气瓶中的空气 .
4.检验和验满
检验 将带火星的木条伸入集气瓶瓶内,如果木条复燃,证明收集的气体是氧气
验满 向上排空气法:将带火星的木条放在集气瓶瓶口,如果木条复燃,说明氧气已集满
排水法:当有大量气泡从集气瓶瓶口冒出时,说明氧气已集满
(4)操作步骤
以加热高锰酸钾制取氧气为例:查、装、定、点、收、离、熄。
①查:检查装置的气密性;
②装:把药品装入试管内,使之平铺在试管底部;
③定:把试管固定在铁架台上;
④点:点燃酒精灯加热;
⑤收:收集气体;
⑥离:将导管撤离水槽;
⑦熄:熄灭酒精灯。
拓展:无法收集到较纯净氧气的可能原因:
(1)装置气密性不好。
(2)用向上排空气法收集时导管未伸到集气瓶底部。
(3)用排水法收集时,未等导管口有连续、均匀地气泡冒出时就开始收集。
5.“多功能瓶”的应用
装置 功能 气体进出方向
排空气法收集气体 密度大于空气的气体 b进a出
密度小于空气的气体 a进b出
排水法收集气体 a进b出
检验、除杂、干燥气体 b进a出
6.干燥剂及干燥装置:
(1)常见气体的干燥剂及适用范围:
①浓硫酸——干燥酸性气体和中性气体,如氧气、二氧化碳、氮气等。
②氢氧化钠固体、碱石灰(CaO与NaOH的固体混合物)——干燥碱性气体和中性气体,如氨气、氮气等。
(2)干燥装置如图所示:
1.实验室用过氧化氢溶液和二氧化锰制取氧气,一定不需要用到的仪器是
A.酒精灯 B.水槽 C.集气瓶 D.分液漏斗
【答案】A
【解析】实验室用过氧化氢溶液和二氧化锰混合制取氧气,是固液常温型反应,不需要加热,故不需要酒精灯。故选A。
2.氧气的制取及有关性质实验,图示正确的是
A.制氧气 B.收集氧气
C.铁丝燃烧 D.测定空气中氧气的体积分数
【答案】C
【解析】A.为防止加热时产生的冷凝水倒流,加热固体制取气体时试管口应低于试管底部,图示操作错误;
B.利用向上排空气法收集氧气,试管口不能放塞子,应放玻璃片,便于排空气,图示操作错误;
C.铁丝在氧气中燃烧,集气瓶底要放一些水或沙子,防止燃烧后的高温熔融物溅落炸裂瓶底,图示操作正确;
D.木炭燃烧消耗氧气,但又生成二氧化碳,使瓶内气压变化不大,水不能倒流,无法测出氧气的体积分数,图示操作错误。故选C。
3.下列有关加热高锰酸钾制取氧气并用排水法收集的实验操作的“先”与“后”的说法正确的是
A.组装装置时,要先固定试管,再放置酒精灯
B.加入药品时,要先加入药品,再检查装置的气密性
C.开始加热时,要先移动酒精灯给试管预热,再固定在药品下方加热
D.实验结束时,要先熄灭酒精灯,再将导气管从水槽中拿出
【答案】C
【解析】A.组装装置时,要先放置酒精灯,再固定试管,A错误,不符合题意;
B.加入药品时,先检查装置的气密性再加入药品,B错误,不符合题意;
C.开始加热时,要先移动酒精灯给试管预热,再固定在药品下方加热,操作正确,符合题意;
D.实验结束时,要先将导气管从水槽中拿出,再熄灭酒精灯,D错误,不符合题意;
故选:C。
4.实验室用加热高锰酸钾制取氧气的主要操作有:①点燃酒精灯,加热;②检查装置的气密性;③装药品;④熄灭酒精灯;⑤收集气体;⑥把试管固定在铁架台上;⑦将导管撤离水槽。正确的顺序是
A.②③⑥①⑤⑦④ B.②③⑥①⑤④⑦
C.③②①⑥⑤⑦④ D.①②③⑤⑥④⑦
【答案】A
【解析】其操作顺序正确的是:检查装置的气密性,装入高锰酸钾,并在试管口放一团棉花,用带导管的胶塞塞紧,并将试管固定在铁架台上,点燃酒精灯给试管加热,用排水法收集氧气,从水槽中取出导管,熄灭酒精灯。
故填:A。
5.下列关于O2的实验室制法及性质实验的说法不正确的是
A制O2的药品 B发生装置 C收集装置 D验证O2的可燃性
【答案】D
【解析】A.实验室中用过氧化氢和二氧化锰制氧气,选项正确;
B.过氧化氢和二氧化锰制氧气属于固液常温型,可以采用B中装置制取,选项正确;
C.氧气密度比空气大,可以采用向上排空气法收集,选项正确;
D.氧气具有助燃性,不具可燃性,选项错误。
故选:D。
6.如图所示四种途径都可以得到O2(反应条件已省略),下列说法错误的是
A.根据绿色化学理念,甲途径是实验室制O2的最佳方案
B.为了使甲、乙两种途径更快地得到O2,还需要加入催化剂
C.甲、乙和丙途径中发生化学变化的基本反应类型都是分解反应
D.工业上采用途径丁制取大量O2,主要是利用了N2和O2的密度不同
【答案】D
【解析】A.乙途径和丙途径需要加热,丁途径需要让空气液化,需要外界提供能量,根据绿色化学理念,甲途径是实验室制O2的最佳方案,A选项说法正确,不符合题意;
B.为了使甲、乙两种途径更快地得到O2,还需要加入催化剂,B选项说法正确,不符合题意;
C.甲、乙和丙途径中发生化学变化的基本反应类型都是分解反应,C选项说法正确,不符合题意;
D.工业上采用途径丁制取大量O2,主要是利用了N2和O2的沸点不同,D选项说法错误,符合题意。故选D。
7.某同学误将少量KMnO4当成MnO2加入KClO3中进行加热制取氧气,部分物质质量随时间变化如图所示。下列关于该过程的说法正确的是:
A.c代表氧气
B.t1时刻,O2 开始产生
C.t2时刻,KMnO4 开始分解
D.KMnO4是催化剂
【答案】B
【解析】根据题干所给信息可知,b物质的质量少,b是高锰酸钾,a是氯酸钾,在t1时刻高锰酸钾开始分解,有氧气生成,随着高锰酸钾的分解,二氧化锰的质量也在不断的增加,故A.C.D错误,B正确。故选B。
8.分析下列实验中出现的异常现象,并从给定的选择项中把可能的原因用字母填入括号内。
(1)实验室用高锰酸钾制氧气时试管破裂_______________;
(2)用高锰酸钾制氧气时水槽中的水变为紫红色_______________;
(3)将细铁丝伸入氧气瓶中却未能看到细铁丝发生燃烧______________;
(4)制氧气时加热后却发现管口没有气泡产生________________。
A.试管口未放棉花 B.试管外壁有水 C.装置漏气 D.氧气不纯
【答案】B A D C
【解析】(1)实验室用高锰酸钾制氧气时试管破裂,可能是试管外壁有水,使试管受热不均匀发生破裂;(2)用高锰酸钾制氧气时水槽中的水变为紫红色,可能是试管口未放棉花,高锰酸钾颗粒通过导气管进入水中;(3)将细铁丝伸入氧气瓶中却未能看到细铁丝发生燃烧可能是氧气不纯;(4)制氧气时加热后却发现管口没有气泡产生可能是装置漏气。
9.氧气是空气的主要成分,是一种化学性质比较活泼的物质。如图是工业上利用分离液态空气的方法得到氧气的流程示意图:
① 分离液态空气制氧气的过程主要发生_____(填“物理”或“化学”)变化。
② 已知:液氮的沸点为﹣196℃,液氧的沸点为﹣183℃,液态空气在蒸发时,首先蒸发出来的是_____(填化学式)。
③ 这样制得的氧气属_____(填“纯净物”或“混合物”)。
【答案】物理 N2 混合物
【解析】① 分离液态空气制氧气,是利用液态氮和液态氧的沸点不同,没有新物质生成,属于物理变化。
② 液氮的沸点为﹣196℃,液氧的沸点为﹣183℃,液氮的沸点比液氧的低,故液态空气在蒸发时,首先蒸发出来的是氮气,其化学式为:N2。
③ 剩余的液体为液态氧和液态稀有气体等,这样制得的氧气属于混合物。
故答案为
① 物理;② N2;③ 混合物。
10.如图是实验室制取气体常用装置,请根据题意回答下列问题:
(1)写出图中仪器①的名称:_____。
(2)实验室选用高锰酸钾制取氧气的文字表达式为_____,若选用A作为其发生装置,还缺少棉花,加棉花的目的是_____。若选用F装置收集氧气,气体应从_____(填a或b)端通入,通入一段时间后,要证明氧气已经收集满的操作是:_____,若木条复燃,则氧气已集满。
(3)某同学用B装置制取氧气,该反应的文字表达式为_____。B装置中长颈漏斗下端要形成液封,目的是_____。实验过程中该同学观察到B中反应太快,不利于气体收集,他可选择下列措施中的_____(填序号)解决该问题。
A 将长颈漏斗换成注射器
B 向装置中加入适量蒸馏水
C 将锥形瓶换成试管
该同学要收集一瓶较纯净的氧气,他应选择上图中的_____(填装置序号)装置进行收集。收集时该同学看到B中液体里有大量气泡产生,但最终收集的氧气还不够纯净,原因可能是:
I、装置漏气;
II、_____。
(4)甲烷是一种无色无味密度小于空气的气体,它难溶于水,是一种常用的燃料。实验室中常加热醋酸钠固体和氢氧化钠固体混合物的方法制备甲烷,如果要制取并收集一瓶甲烷气体,可选择上图中的_____(填装置序号)装置。收集满甲烷气体的集气瓶盖上玻璃片后,要_____(填选“正放”或“倒放”)在试验台上。
【答案】锥形瓶 高锰酸钾锰酸钾+二氧化锰+氧气 防止高锰酸钾进入导管 b 将带火星的木条放在a导管口 过氧化氢水+氧气 防止生成的气体从长颈漏斗逸出 AB D 刚出现气泡就开始收集 AD或AE或AF 倒放
【解析】(1)图中仪器①的名称:锥形瓶;
(2)实验室选用高锰酸钾制取氧气的文字表达式为:高锰酸钾锰酸钾+二氧化锰+氧气;
若选用A作为其发生装置,还缺少棉花,加棉花的目的是防止高锰酸钾进入导管堵塞导管;
氧气的密度比空气大,用F装置收集氧气,气体应从b端通入;
通入一段时间后,要证明氧气已经收集满的操作是:将带火星的木条放在a导管口,若木条复燃,则氧气已集满;
(3) B装置属于固液常温型装置适用于双氧水和二氧化锰制氧气,文字表达式为:过氧化氢水+氧气。液封的目的是:防止生成的气体从长颈漏斗下端逸出;
实验过程中该同学观察到B中反应太快,不利于气体收集,可以选择减慢反应速度进行改进:
A.用注射器可以控制添加药品的速率故可以控制反应速率,正确;
B.加入蒸馏水以后过氧化氢浓度变低反应速率减慢,正确;
C.将锥形瓶换成试管不会影响反应速率,错误。故选AB;
题中要求收集的气体较纯净,排水法收集的氧气较纯净,故选D;
过早收集,没有等导管口有连续均匀的气泡冒出就开始收集,导致收集到了部分空气;
(4)制取甲烷时反应物为固体且需要加热,所以发生装置选择A装置;应为甲烷难溶于水,密度小于空气可选D.排水法收集、E向下排空气法收集。也可用F万用瓶进行收集。
因为甲烷密度比空气小所以放置时应该倒放。
1
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
