2022-2023学年九年级化学人教版上册 第二单元 课题1 空气 (第1课时)课件(25张PPT,内嵌音视频)
文档属性
| 名称 | 2022-2023学年九年级化学人教版上册 第二单元 课题1 空气 (第1课时)课件(25张PPT,内嵌音视频) |

|
|
| 格式 | zip | ||
| 文件大小 | 9.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-09-13 00:00:00 | ||
图片预览






文档简介
(共25张PPT)
课题一空气
第一课时
学习目标
了解空气的主要成分;
探究空气中氧气的含量;
初步认识纯净物和混合物的概念;
初步学习科学实验的方法,进行观察、记录,并初步学会分析实验现象。
【重点】探究空气中氧气的含量。
【难点】掌握纯净物和混合物的概念并能够准确区分。
人类、动植物的呼吸,每时每刻都离不开空气,没有空气就没有生命,你能看到空气吗?如何证明空气的存在吗?
你有办法证明空气的存在吗?
扁的密封袋开袋后抖动,然后封好
—双手挤压有压力
扇子朝脸扇、树叶在动
—有风
给车胎打气
—鼓起来
空烧杯在盛满水的水槽中向下压
—烧杯内的水无法上升到顶部
18世纪70年代,瑞典科学家舍勒和英国化学家普利斯特里分别制得了氧气,但他们并没有意识到自己发现了氧气。
1774年法国化学家拉瓦锡第一次用实验证明了空气中有氧气和氮气。
19世纪末英国物理学家瑞利发现了稀有气体氩气,之后各个稀有气体陆续被发现。
空气的发展史
18世纪70年代,瑞典科学家舍勒和英国化学家普利斯特里分别制得了氧气,但他们并没有意识到自己发现了氧气。
19世纪末英国物理学家瑞利发现了稀有气体氩气,之后各个稀有气体陆续被发现。
空气成分的探究
18世纪70年代,瑞典科学家舍勒和英国化学家普利斯特里分别制得了氧气,但他们并没有意识到自己发现了氧气。
最初人们以为空气是一种单一的物质。
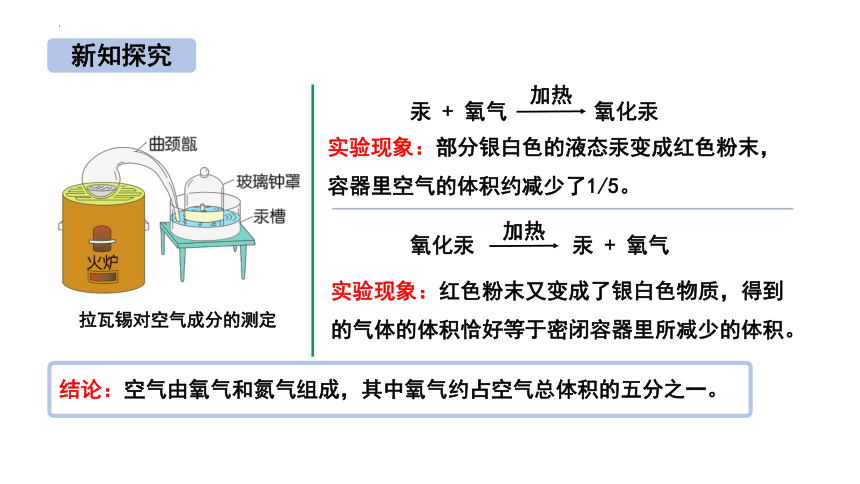
加热
氧化汞 汞 + 氧气
实验现象:红色粉末又变成了银白色物质,得到的气体的体积恰好等于密闭容器里所减少的体积。
汞 + 氧气 氧化汞
加热
拉瓦锡对空气成分的测定
实验现象:部分银白色的液态汞变成红色粉末,容器里空气的体积约减少了1/5。
结论:空气由氧气和氮气组成,其中氧气约占空气总体积的五分之一。
新知探究
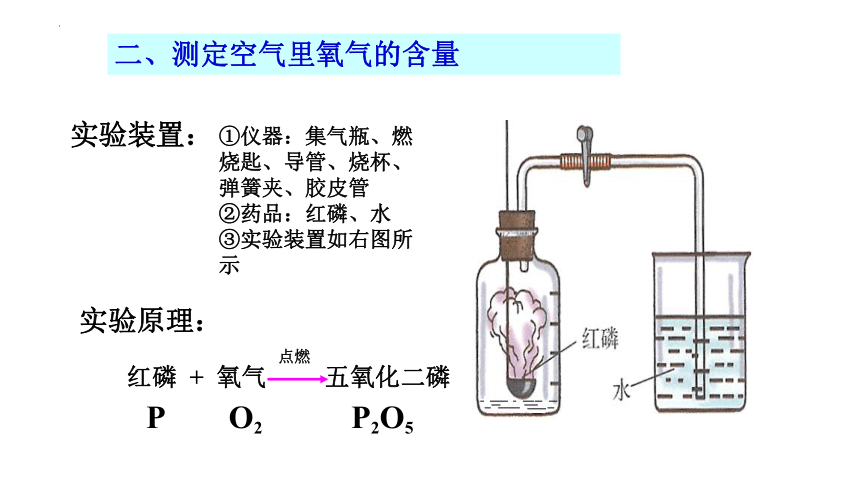
二、测定空气里氧气的含量
实验装置:
①仪器:集气瓶、燃烧匙、导管、烧杯、弹簧夹、胶皮管
②药品:红磷、水
③实验装置如右图所示
红磷 + 氧气
点燃
五氧化二磷
P O2 P2O5
实验原理:
空气中氧气含量的测定
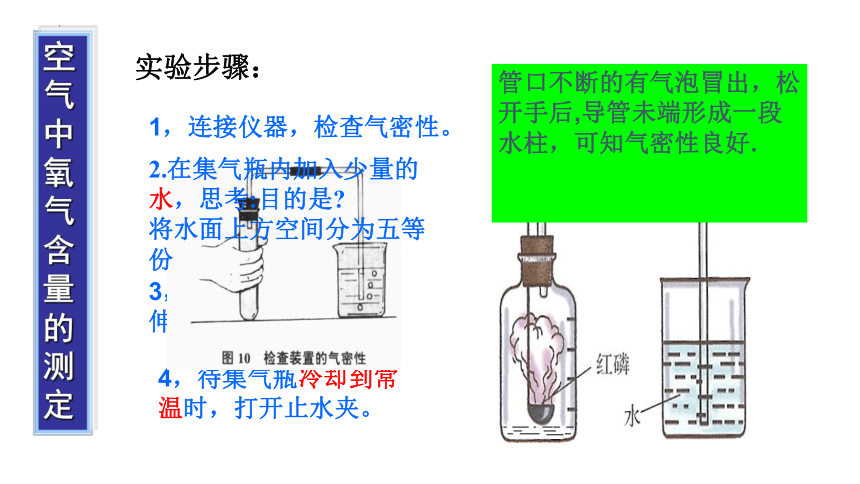
实验步骤:
1,连接仪器,检查气密性。
3,点燃红磷,迅速
伸入瓶中,塞紧瓶塞。
4,待集气瓶冷却到常温时,打开止水夹。
管口不断的有气泡冒出,松
开手后,导管未端形成一段
水柱,可知气密性良好.
2.在集气瓶内加入少量的水,思考:目的是
将水面上方空间分为五等份
实验现象
1.红磷燃烧,产生大量白烟,放热;
2.冷却后,打开弹簧夹,烧杯中的水沿导管进入集气瓶内,进入瓶内的水的体积约占瓶内原空气总体积的1/5。
实验结论
氧气约占空气总体积的五分之一。
【分析】 红磷在封闭的容器内充分燃烧,消耗了空气中的氧气,生成五氧化二磷固体,使容器内压强减小,在外界大气压的作用下水进入集气瓶。
【思考1】水为什么能够进入集气瓶中
想一想?
【分析】剩余气体不能燃烧也不支持燃烧。
【思考2】燃烧的红磷熄灭了,说明剩余气体有什么性质?
3.根据实验现象,分析瓶内剩余气体具有怎样的性质?
答:可得出剩余4/5 气体为N2的性质,①不支持燃烧,也不能燃烧,②难溶于水
想一想?
4、为什么要在集气瓶里放少量的水?
(1)防止燃着的红磷溅到集气瓶底,将集气瓶炸裂。(2)吸收五氧化二磷(3)降温
5、红磷燃烧后生成的“大量白烟”可以说“大量白雾”吗?
答:不能,烟是固体微粒;雾是小液滴。
6.能否用木炭、硫代替红磷做此实验?红磷代替品应满足什么条件?
答:木炭和硫燃烧生成二氧化碳和二氧化硫气体,生成气体的体积会弥补反应消耗氧气的体积,测量结果偏小。
代替品应满足以下条件:(1)在空气中能燃烧且只能与氧气反应;(2)该物质燃烧后生成物是固体。
讨 论
拉瓦锡通过实验得出的结论是氧气占空气总体积的1/5 ,而在我们的实验中,为什么气体减少的体积小于1/5 ?
1)红磷量不足
2)装置气密性不好
3)瓶内温度没有冷却到室温
4)导管中残留一些水
5)烧杯中的水不足
结果大于1/5的误差
弹簧夹未加紧
01
红磷点燃后没有立即插入集气瓶
02
测定空气中氧气含量的其他方法
常见装置
反应原理
点燃
红磷、白磷燃烧产物相同,文字表达式均为
磷+氧气 五氧化二磷
方法一:测量进入容器内水的体积或容器内水的体积变化
方法二:利用刻度测量密闭容器内气体体积的减少量
加热
铜+氧气 氧化铜
空气的组成
氮气(78%)
氧气(21%)
其他气体杂质(0.03%)
巧 学 妙 记
氮七八,氧二一,零点九四是稀气,还有两个点零三,二氧化碳和杂气,体积分数要记清,莫与质量混一起。
二氧化碳(0.03%)
稀有气体(0.94%)
注意
(1)上述比例是体积分数不是质量分数。
(2)空气中的成分和含量不是固定不变的,不同地区、不同时间都会有变化。
二、纯净物和混合物
纯净物:
由一种物质组成
如:氮气、氧气、水、二氧化碳等
混合物:
由多种物质组成
如:空气 海水 河水 矿泉水等
纯净物可以用专门的化学符号来表示如氮气、氧气、二氧化碳可分别表示为N2、 O2、CO2等。
物质
混合物中各物质各自保持着原来的性质。
练习:判断下列物质是混合物还是纯净物?
海水、自来水、蒸馏水、洁净的空气、氧气、河水、矿泉水、糖水、雪碧饮料、五氧化二磷、冰水混合物
拓 展
1.研究物质的性质应该用纯净物,事实上我们所见到的物质基本都是混合物,纯净物只是相对纯度较高的物质,绝对纯净的物质是不存在的。
2.不能根据“混合”“洁净”判断混合物和纯净物,如冰水混合物属于纯净物,洁净的空气属于混合物。
3.稀有气体包括多种气体,属于混合物,其中每一种气体是纯净物。
4.判断一种物质是纯净物还是混合物,不能被名称误导,如二氧化碳是一个物质的名称
1.请根据图示回答下列问题:
(1)现象:红磷在集气瓶内燃烧,产生_________;冷却后打开弹簧夹,烧杯内的水______________,瓶中的水面上升约占 体积。
(2)结论:_____________________。
大量白烟
倒流入集气瓶
1/5
氧气约占空气体积的1/5
课 堂 达 标
2、用如图装置进行实验。下列现象能证明空气中氧气(O2)的含量的是( )
A.红磷燃烧,产生白烟
B.瓶中液面先下降,后上升
C.水槽中液面下降
D.瓶中液面最终上升至1处
D
课堂练习
3、用如图装置测定空气中氧气的含量,下列说法正确的是( )
A.点燃白磷后缓慢将燃烧匙插入瓶中,塞紧瓶塞
B.用细铁丝代替白磷进行实验,不会影响实验结果
C.不打开瓶塞,聚焦太阳光引燃足量白磷,实验效果更好
D.若实验过程中,没有将弹簧夹夹紧,不会影响实验结果
C
课堂练习
4、下列物质中,属于纯净物的是( )
A.氧气
B.洁净的空气
C.无色食盐水
D.稀有气体
A
课堂练习
测定空气中
氧气的含量
空气的成分、
混合物和纯净物
原理:红磷+氧气 五氧化二磷
点燃
结论:氧气约占空气总体积的1/5
现象:红磷在空气中燃烧,产生大量白烟并放出热量;冷却至室温后,松开弹簧夹,烧杯中的水沿导管进入集气瓶中,进入的水约占集气瓶内原空气体积的1/5
空气是有
什么组成的
课堂小结
课题一空气
第一课时
学习目标
了解空气的主要成分;
探究空气中氧气的含量;
初步认识纯净物和混合物的概念;
初步学习科学实验的方法,进行观察、记录,并初步学会分析实验现象。
【重点】探究空气中氧气的含量。
【难点】掌握纯净物和混合物的概念并能够准确区分。
人类、动植物的呼吸,每时每刻都离不开空气,没有空气就没有生命,你能看到空气吗?如何证明空气的存在吗?
你有办法证明空气的存在吗?
扁的密封袋开袋后抖动,然后封好
—双手挤压有压力
扇子朝脸扇、树叶在动
—有风
给车胎打气
—鼓起来
空烧杯在盛满水的水槽中向下压
—烧杯内的水无法上升到顶部
18世纪70年代,瑞典科学家舍勒和英国化学家普利斯特里分别制得了氧气,但他们并没有意识到自己发现了氧气。
1774年法国化学家拉瓦锡第一次用实验证明了空气中有氧气和氮气。
19世纪末英国物理学家瑞利发现了稀有气体氩气,之后各个稀有气体陆续被发现。
空气的发展史
18世纪70年代,瑞典科学家舍勒和英国化学家普利斯特里分别制得了氧气,但他们并没有意识到自己发现了氧气。
19世纪末英国物理学家瑞利发现了稀有气体氩气,之后各个稀有气体陆续被发现。
空气成分的探究
18世纪70年代,瑞典科学家舍勒和英国化学家普利斯特里分别制得了氧气,但他们并没有意识到自己发现了氧气。
最初人们以为空气是一种单一的物质。
加热
氧化汞 汞 + 氧气
实验现象:红色粉末又变成了银白色物质,得到的气体的体积恰好等于密闭容器里所减少的体积。
汞 + 氧气 氧化汞
加热
拉瓦锡对空气成分的测定
实验现象:部分银白色的液态汞变成红色粉末,容器里空气的体积约减少了1/5。
结论:空气由氧气和氮气组成,其中氧气约占空气总体积的五分之一。
新知探究
二、测定空气里氧气的含量
实验装置:
①仪器:集气瓶、燃烧匙、导管、烧杯、弹簧夹、胶皮管
②药品:红磷、水
③实验装置如右图所示
红磷 + 氧气
点燃
五氧化二磷
P O2 P2O5
实验原理:
空气中氧气含量的测定
实验步骤:
1,连接仪器,检查气密性。
3,点燃红磷,迅速
伸入瓶中,塞紧瓶塞。
4,待集气瓶冷却到常温时,打开止水夹。
管口不断的有气泡冒出,松
开手后,导管未端形成一段
水柱,可知气密性良好.
2.在集气瓶内加入少量的水,思考:目的是
将水面上方空间分为五等份
实验现象
1.红磷燃烧,产生大量白烟,放热;
2.冷却后,打开弹簧夹,烧杯中的水沿导管进入集气瓶内,进入瓶内的水的体积约占瓶内原空气总体积的1/5。
实验结论
氧气约占空气总体积的五分之一。
【分析】 红磷在封闭的容器内充分燃烧,消耗了空气中的氧气,生成五氧化二磷固体,使容器内压强减小,在外界大气压的作用下水进入集气瓶。
【思考1】水为什么能够进入集气瓶中
想一想?
【分析】剩余气体不能燃烧也不支持燃烧。
【思考2】燃烧的红磷熄灭了,说明剩余气体有什么性质?
3.根据实验现象,分析瓶内剩余气体具有怎样的性质?
答:可得出剩余4/5 气体为N2的性质,①不支持燃烧,也不能燃烧,②难溶于水
想一想?
4、为什么要在集气瓶里放少量的水?
(1)防止燃着的红磷溅到集气瓶底,将集气瓶炸裂。(2)吸收五氧化二磷(3)降温
5、红磷燃烧后生成的“大量白烟”可以说“大量白雾”吗?
答:不能,烟是固体微粒;雾是小液滴。
6.能否用木炭、硫代替红磷做此实验?红磷代替品应满足什么条件?
答:木炭和硫燃烧生成二氧化碳和二氧化硫气体,生成气体的体积会弥补反应消耗氧气的体积,测量结果偏小。
代替品应满足以下条件:(1)在空气中能燃烧且只能与氧气反应;(2)该物质燃烧后生成物是固体。
讨 论
拉瓦锡通过实验得出的结论是氧气占空气总体积的1/5 ,而在我们的实验中,为什么气体减少的体积小于1/5 ?
1)红磷量不足
2)装置气密性不好
3)瓶内温度没有冷却到室温
4)导管中残留一些水
5)烧杯中的水不足
结果大于1/5的误差
弹簧夹未加紧
01
红磷点燃后没有立即插入集气瓶
02
测定空气中氧气含量的其他方法
常见装置
反应原理
点燃
红磷、白磷燃烧产物相同,文字表达式均为
磷+氧气 五氧化二磷
方法一:测量进入容器内水的体积或容器内水的体积变化
方法二:利用刻度测量密闭容器内气体体积的减少量
加热
铜+氧气 氧化铜
空气的组成
氮气(78%)
氧气(21%)
其他气体杂质(0.03%)
巧 学 妙 记
氮七八,氧二一,零点九四是稀气,还有两个点零三,二氧化碳和杂气,体积分数要记清,莫与质量混一起。
二氧化碳(0.03%)
稀有气体(0.94%)
注意
(1)上述比例是体积分数不是质量分数。
(2)空气中的成分和含量不是固定不变的,不同地区、不同时间都会有变化。
二、纯净物和混合物
纯净物:
由一种物质组成
如:氮气、氧气、水、二氧化碳等
混合物:
由多种物质组成
如:空气 海水 河水 矿泉水等
纯净物可以用专门的化学符号来表示如氮气、氧气、二氧化碳可分别表示为N2、 O2、CO2等。
物质
混合物中各物质各自保持着原来的性质。
练习:判断下列物质是混合物还是纯净物?
海水、自来水、蒸馏水、洁净的空气、氧气、河水、矿泉水、糖水、雪碧饮料、五氧化二磷、冰水混合物
拓 展
1.研究物质的性质应该用纯净物,事实上我们所见到的物质基本都是混合物,纯净物只是相对纯度较高的物质,绝对纯净的物质是不存在的。
2.不能根据“混合”“洁净”判断混合物和纯净物,如冰水混合物属于纯净物,洁净的空气属于混合物。
3.稀有气体包括多种气体,属于混合物,其中每一种气体是纯净物。
4.判断一种物质是纯净物还是混合物,不能被名称误导,如二氧化碳是一个物质的名称
1.请根据图示回答下列问题:
(1)现象:红磷在集气瓶内燃烧,产生_________;冷却后打开弹簧夹,烧杯内的水______________,瓶中的水面上升约占 体积。
(2)结论:_____________________。
大量白烟
倒流入集气瓶
1/5
氧气约占空气体积的1/5
课 堂 达 标
2、用如图装置进行实验。下列现象能证明空气中氧气(O2)的含量的是( )
A.红磷燃烧,产生白烟
B.瓶中液面先下降,后上升
C.水槽中液面下降
D.瓶中液面最终上升至1处
D
课堂练习
3、用如图装置测定空气中氧气的含量,下列说法正确的是( )
A.点燃白磷后缓慢将燃烧匙插入瓶中,塞紧瓶塞
B.用细铁丝代替白磷进行实验,不会影响实验结果
C.不打开瓶塞,聚焦太阳光引燃足量白磷,实验效果更好
D.若实验过程中,没有将弹簧夹夹紧,不会影响实验结果
C
课堂练习
4、下列物质中,属于纯净物的是( )
A.氧气
B.洁净的空气
C.无色食盐水
D.稀有气体
A
课堂练习
测定空气中
氧气的含量
空气的成分、
混合物和纯净物
原理:红磷+氧气 五氧化二磷
点燃
结论:氧气约占空气总体积的1/5
现象:红磷在空气中燃烧,产生大量白烟并放出热量;冷却至室温后,松开弹簧夹,烧杯中的水沿导管进入集气瓶中,进入的水约占集气瓶内原空气体积的1/5
空气是有
什么组成的
课堂小结
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
