浙教版八上第一章专题四 溶解度曲线图像题(含解析)
文档属性
| 名称 | 浙教版八上第一章专题四 溶解度曲线图像题(含解析) |

|
|
| 格式 | zip | ||
| 文件大小 | 966.3KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2022-09-16 00:00:00 | ||
图片预览


文档简介
中小学教育资源及组卷应用平台
专题四 溶解度曲线图像题
一、题型分析
题型一、某一点的含义
1、曲线上的一点:在t2℃时,A的溶解度是
2、两曲线焦点:在t1℃时,A和C的溶解度相等均为
注:①纵坐标若给出数值需指出
②若A、B、C的名称给出需标明名称
题型二、相同温度,溶解性大小的比较
3、t2℃时三种物质溶解度大小顺序为
题型三、结合图像的计算(注意有陷阱)
4、t2℃时把75gA物质放入100g水中,所得溶液质量为 ,溶质的质量分数为 。
溶质质量分数
题型四、不饱和与饱和溶液的转换方法
题型五、同一温度,不同溶质质量的饱和溶液降温(升温)所得溶液的溶质质量分数大小比较
解题技巧:找变化前后的最低点
5、t2℃时三个物质的饱和溶液的溶质质量分数大小 ,降温至t1℃时溶液溶质质量分数大小
题型六、等质量不同溶质的饱和溶液,降温(升温),所得析出固体质量的大小比较
解题技巧:溶解度减小快,析出多;溶解度增加,不析出。
6、t2℃时,同质量的ABC饱和溶液降温至t1℃后,A、B溶解度减小,有晶体析出,且A的溶解度受温度影响大,A析出的晶体 ,B析出的晶体 ,C溶解度增加,晶体 ,故析出晶体质量
题型七、利用溶解度曲线特点提纯某物质
7、溶解度随温度变化大,如A,常用
8、溶解度随温度变化小,如B,常用
9、物质提纯,以主角为中心,如除去A中少量B(留下A)采用 ,若除去B中的少量A(留下B)
题型八、会用气体溶解度的影响因素解释简单实际问题:
10、①喝汽水易打嗝:
②打开汽水瓶盖会冒出大量气泡:
③水沸腾前就会出现气泡:
二、题型训练
1.如图为a、b、c三种不含结晶水的固体物质的溶解度曲线,下列叙述中正确的是( )
A.t1℃ 时,a、b、c饱和溶液的溶质质量分数为20%
B.P点表示:t2℃时,a、b的溶液是饱和状态,c的溶液是不饱和状态
C.t2℃时,a、b、c三种物质溶液的溶质质量分数a>b>c
D.70g a的饱和溶液从t2℃降温到t1℃时,析出晶体15g
2.如图为A物质的溶解度曲线.M、N两点分别表示A物质的两种溶液.下列做法不能实现M、N间的相互转化的是(A从溶液中析出时不带结晶水)( )
A.从N→M:先向N中加入适量固体A,再降温至t1℃
B.从N→M:先将N降温至t1℃,再恒温蒸发至有晶体析出
C.从M→N:先将M升温至t2℃,再恒温加入适量水
D.从M→N:先将M升温至t2℃,再恒温将其蒸发掉部分水
3.甲、乙两种固体的溶解度曲线如图所示。将①②两支试管中的甲、乙饱和溶液(均有少量未溶解的固体)放进盛有热水的烧杯里,升高温度后,下列有关说法正确的是( )
A.①溶液质量增加,②溶液质量减少
B.①②两溶液均变为不饱和溶液
C.甲的溶解度大于乙的溶解度
D.①溶液中溶质的质量分数大于②溶液
4.如图为甲、乙、丙三种固体物质的溶解度曲线图,请回答下列问题。
(1)Q点的含义是 ;
(2)若使接近饱和的丙溶液转变成饱和溶液,可采取的方法是 (任写一种方法);
(3)甲中含少量乙时,可通过 的方法提纯甲;
(4)t2℃时,将35g甲加入到50g水中,充分搅拌后,所形成溶液的质量为 g;
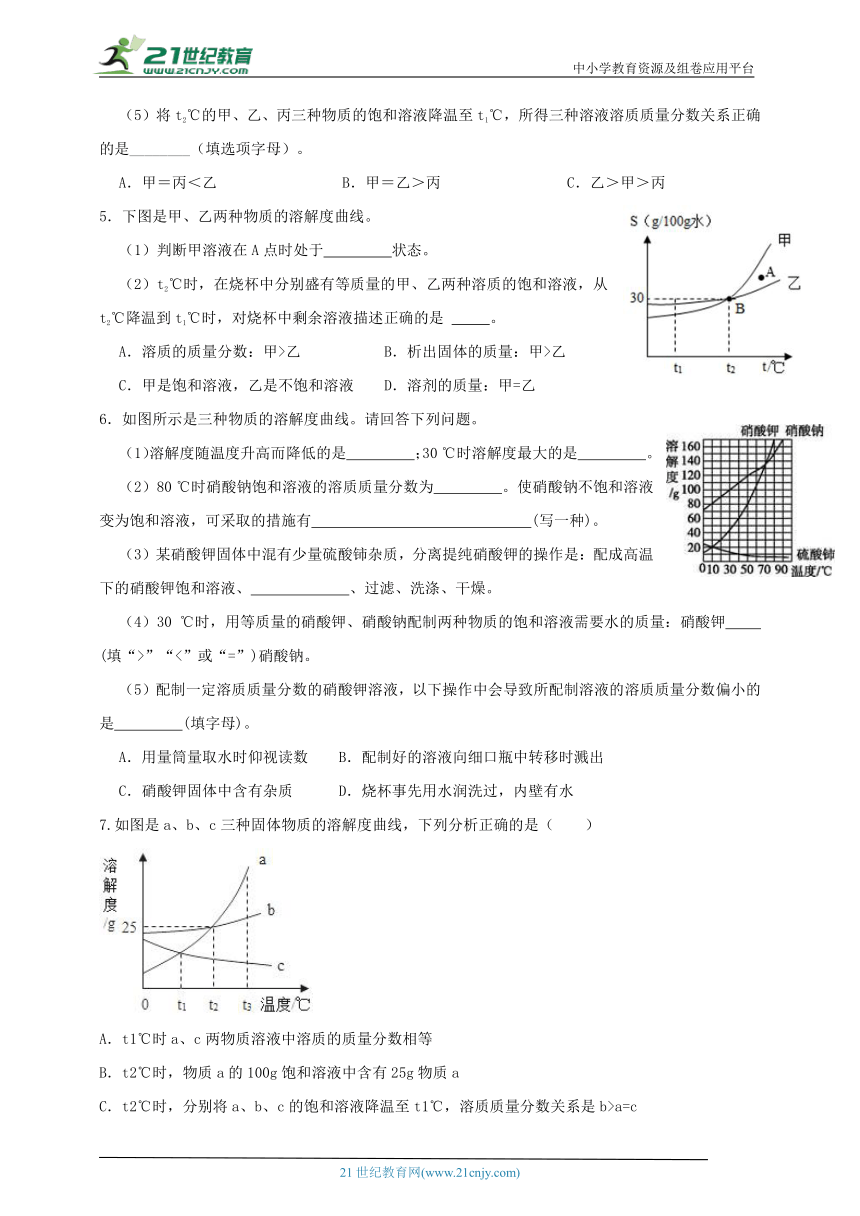
(5)将t2℃的甲、乙、丙三种物质的饱和溶液降温至t1℃,所得三种溶液溶质质量分数关系正确的是________(填选项字母)。
A.甲=丙<乙 B.甲=乙>丙 C.乙>甲>丙
5.下图是甲、乙两种物质的溶解度曲线。
(1)判断甲溶液在A点时处于 状态。
(2)t2℃时,在烧杯中分别盛有等质量的甲、乙两种溶质的饱和溶液,从t2℃降温到t1℃时,对烧杯中剩余溶液描述正确的是 。
A.溶质的质量分数:甲>乙 B.析出固体的质量:甲>乙
C.甲是饱和溶液,乙是不饱和溶液 D.溶剂的质量:甲=乙
6.如图所示是三种物质的溶解度曲线。请回答下列问题。
(1)溶解度随温度升高而降低的是 ;30 ℃时溶解度最大的是 。
(2)80 ℃时硝酸钠饱和溶液的溶质质量分数为 。使硝酸钠不饱和溶液变为饱和溶液,可采取的措施有 (写一种)。
(3)某硝酸钾固体中混有少量硫酸铈杂质,分离提纯硝酸钾的操作是:配成高温下的硝酸钾饱和溶液、 、过滤、洗涤、干燥。
(4)30 ℃时,用等质量的硝酸钾、硝酸钠配制两种物质的饱和溶液需要水的质量:硝酸钾 (填“>”“<”或“=”)硝酸钠。
(5)配制一定溶质质量分数的硝酸钾溶液,以下操作中会导致所配制溶液的溶质质量分数偏小的是 (填字母)。
A.用量筒量取水时仰视读数 B.配制好的溶液向细口瓶中转移时溅出
C.硝酸钾固体中含有杂质 D.烧杯事先用水润洗过,内壁有水
7.如图是a、b、c三种固体物质的溶解度曲线,下列分析正确的是( )
A.t1℃时a、c两物质溶液中溶质的质量分数相等
B.t2℃时,物质a的100g饱和溶液中含有25g物质a
C.t2℃时,分别将a、b、c的饱和溶液降温至t1℃,溶质质量分数关系是b>a=c
D.t2℃时向50g水中加入15g物质b充分搅拌,所得溶液质量一定小于65g
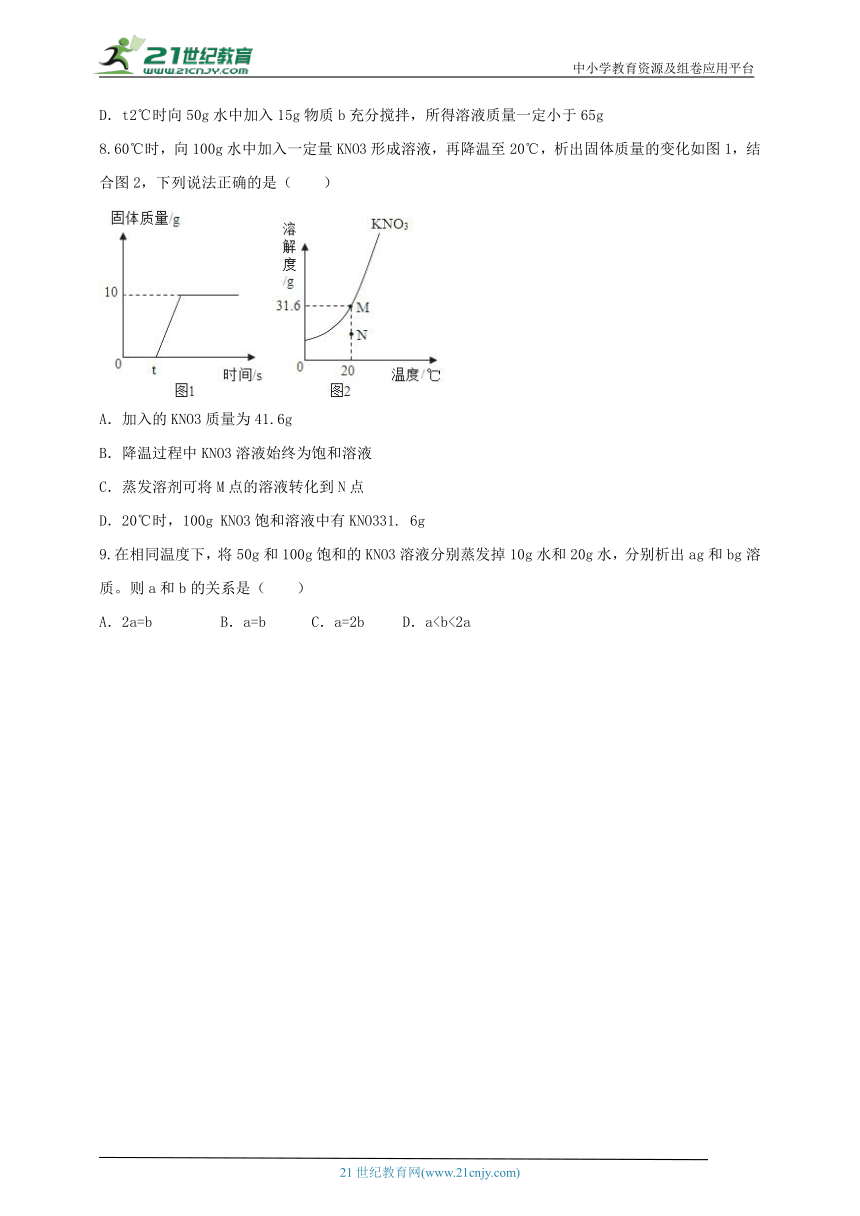
8.60℃时,向100g水中加入一定量KNO3形成溶液,再降温至20℃,析出固体质量的变化如图1,结合图2,下列说法正确的是( )
A.加入的KNO3质量为41.6g
B.降温过程中KNO3溶液始终为饱和溶液
C.蒸发溶剂可将M点的溶液转化到N点
D.20℃时,100g KNO3饱和溶液中有KNO331. 6g
9.在相同温度下,将50g和100g饱和的KNO3溶液分别蒸发掉10g水和20g水,分别析出ag和bg溶质。则a和b的关系是( )
A.2a=b B.a=b C.a=2b D.a答案解析
一、
题型一、 1、50g 2、15g
题型二、 3、A>B>C
题型三、 4、150g 33.3%
题型五、 5、A>B>C B>A>C
题型六、 6、多 少 没有析出 A>B>C
题型七、 7、冷却热饱和溶液(降温结晶) 8、蒸发结晶 9、冷却热饱和溶液 蒸发溶剂后趁热过滤
题型八、 10、①体内温度高,二氧化碳溶解度变小逸出
②打开瓶盖时瓶内压强变小,二氧化碳溶解度变小逸出
③温度升高,水中空气的溶解度变小逸出
二、
1.【答案】A
【解答】A.t1℃时,a、b、c的溶解度都是25g,
则它们的饱和溶液的溶质质量分数约为:,故A正确;
B.t2℃时,P点在a、b图像对应点的下方,即此时溶质质量小于溶解度,即a、b的溶液是不饱和状态。P点在图像c的上方,即溶质质量大于c的溶解度,因此c的溶液是饱和的,故B错误;
C.t2℃时,a、b、c三种物质的溶解度:a>b>c,则它们的饱和溶液的溶质质量分数a>b>c,因为没有指明是饱和溶液,故C错误;
D.t2℃时,70ga的饱和溶液中溶质质量为:。t1℃时,70ga的饱和溶液中溶质质量为:。则从t2℃降温到t1℃时,析出晶体:20g-14g=6g,故D错误。
故选A。
2.【答案】D
【解答】从N→M意思是单位溶剂溶解溶质的量增加,溶液由不饱和变饱和且溶液温度降低,可采取增加溶质和降低温度的方法,故A、B正确不合题意;
从M→N意思是单位溶剂溶解溶质的量减小,溶液由饱和变为不饱和且溶液温度升高,可采取减小溶质(如降温析出晶体或将溶质变成沉淀或气体反应掉)需将固体滤除和升温的方法,故C正确不合题意;
先将M升温溶质质量不会变小,此时溶液变为不饱和溶液(该物质的溶解度随温度的升高而增大),但然后将其蒸发掉部分水则溶液有可能又会变成饱和溶液,故D错误符合题意。
故选D。
3.【答案】A
【解答】①②试管中都存在少量为溶解的固体,则原来①②都是饱和溶液。
A.根据图像可知,甲的溶解度随温度的升高而增大,乙的溶解度随温度的升高而减小。当升高温度后,甲的溶解度增大,①中肯定会有甲继续溶解,即溶质质量增加。乙的溶解度减小,即②中肯定会有乙固体继续析出,则②中溶质质量减小,溶液质量减小,故A正确;
B.原来它们都是饱和溶液,甲的溶解度增大,则①变为不饱和溶液;乙的溶解度减小,则②仍然为饱和溶液,故B错误;
C.根据图像可知,溶解度甲可能大于乙,等于乙或小于乙,不指明温度,无法比较,故C错误;
D.无法确定甲和乙中溶质和溶液的质量大小,因为无法比较它们的溶质质量分数的大小,故D错误。
故选A。
4.【答案】(1)表示t1℃时,甲和丙的溶解度相等
(2)增加溶质;升高温度,恒温蒸发水分
(3)降温结晶(或冷却热饱和溶液)
(4)80
(5)C
【解答】(1)根据图像可知,Q点的含义为:t1℃时,甲和丙的溶解度相等。
(2)根据图像可知,丙的溶解度随温度的升高而减小,则将丙的不饱和溶液转换为饱和溶液的方法为:增加溶质;升高温度;恒温蒸发水分。
(3)根据图像可知,甲的溶解度随温度的升高而迅速增多,乙的溶解度受温度的影响较小,则:甲中含少量乙时,可通过降温结晶(或冷却热饱和溶液)的方法提纯甲。
(4)t2℃时,甲的溶解度为60g,即100g水中最多溶解60g甲,那么50g水中最多溶解30g。因为35g>30g,所用此时溶液饱和,即形成溶液的质量:30g+50g=80g。
(5)甲和乙的溶解度随温度的降低而减小,即它们的饱和溶液从t2℃降低到t1℃时,仍然为饱和溶液。因为此时的溶解度乙>甲,所以此时的溶质质量分数乙>甲。丙的溶解度随温度的降低而增大,因此丙由饱和溶液变成不饱和溶液。t1℃时,甲和丙的溶解度相等,即二者此时的饱和溶液的溶质质量分数相同,因此溶质质量分数甲>丙。
那么溶质质量分数乙>甲>丙。
5.【答案】(1)不饱和
(2)B;D
【解答】(1)根据图片可知,A点的溶质质量小于对应温度下甲的溶解度,因此处于不饱和状态。
(2)根据图像可知,二者的溶解度都随温度的降低而减小,因此温度降低后二者还是饱和溶液,故C错误;
t1℃时,甲的溶解度小于乙的溶解度,因此甲的溶质质量分数小于乙的溶质质量分数,故A错误;
t2℃时,甲和乙的溶解度相等,而t1℃时,甲的溶解度小于乙的溶解度,则析出固体的质量:甲>乙,故B正确;
在降温的过程中,变化的是溶质的质量,而溶剂的质量保持不变,故D正确。
故选BD。
6.【答案】(1)硫酸铈;硝酸钠
(2)60%;加入硝酸钠固体(合理即可)
(3)降温结晶
(4)>
(5)A;C;D
【解答】(1)根据图片可知,溶解度随温度升高而降低的是硫酸铈。30℃时,硝酸钠、硝酸钾和硫酸铈的溶解度分别为100g、40g和10g,则此时溶解度最大的是硝酸钠。
(2)80℃时硝酸钠的溶解度为150g,则溶质质量分数为:;
使硝酸钠的不饱和溶液变为饱和溶液,采取的措施为:加入硝酸钠固体,蒸发溶剂或降低温度从而减小溶解度。
(3)硝酸钾的溶解度随温度的升高而增大,而硫酸铈的溶解度随温度的升高而减小,那么某硝酸钾固体中混有少量硫酸铈杂质,分离提纯硝酸钾的操作是:配成高温下的硝酸钾饱和溶液、降温结晶、过滤、洗涤、干燥。
(4)30℃时,硝酸钾的溶解度为40g,设m克硝酸钾配制成饱和溶液需用水质量为x,
;
解得:x=;
30℃时,硝酸钠的溶解度为100g,设m克硝酸钾配制成饱和溶液需用水质量为y,
;
解得:z=;
则需要水的质量:硝酸钾>硝酸钠。
(5)A.用量筒量取水时仰视读数,读出的示数偏小,而实际的水的体积偏大,从而导致溶质质量分数偏小,故A符合题意;
B.配制好的溶液向细口瓶中转移时溅出,由于溶液的均一性,因此不会改变溶质质量分数,故B不会题意;
C.硝酸钾固体中含有杂质,会导致溶质质量减小,故C符合题意;
D.烧杯事先用水润洗过,内壁有水,会导致溶剂水的体积偏大,故D符合题意。
故选ACD。
7.【答案】D
【解答】A、t1℃时a、c两物质溶解度相同,二者饱和溶液中溶质的质量分数相等,题干中未注明“饱和”,溶质的质量分数不一定相等,故A错误;B、t2℃时,物质a的溶解度是25g,100g水中最多溶解物质a的质量为25g,所以100g饱和溶液中含有20g物质a,故B错误;C、t2℃降温至t1℃,由于c的溶解度随温度降低而增大,c的质量分数不变;a、b溶解度随温度降低而减小,故质量分数减小。故比较t1℃时a、b饱和溶液的质量分数与t2℃物质c饱和溶质质量分数即可。溶质质量分数关系是b>a>c,故C错误; D、t2℃时b的溶解度为25g,即该温度下100g水中最多溶解b12.5g,向50g水中加入15g物质b充分搅拌,所得溶液质量一定小于65g,故D正确。故选D。
8.【答案】A
【解答】A、20℃时,硝酸钾的溶解度为31.6g,即该温度下,100g水中最多能溶解31.6g硝酸钾,故60℃时,向100g水中加入一定量KNO3形成溶液,再降温至20℃,共析出10g硝酸钾,说明加入硝酸钾的质量为41.6g,符合题意;B、由图2可知,硝酸钾的溶解度随温度的升高而增加,由图1可知,降温过程中,一开始没有溶质析出,说明一开始是不饱和溶液,后有溶质析出,变为饱和溶液,不符合题意;C、M点为20℃时,硝酸钾的饱和溶液,N点为20℃时,硝酸钾的不饱和溶液,故增加溶剂或恒温蒸发可将M点的溶液转化到N点,不符合题意;D、20℃时,硝酸钾的溶解度为31.6g,131.6g硝酸钾饱和溶液中硝酸钾的质量31.6g,不符合题意。故选A。
9. 【答案】A
【解答】两KNO3溶液处于同一温度下,且都是饱和溶液,因此它们溶液的浓度是一样的,其中20g水中所含有溶质应是10g水中的两倍,故2a=b。故选A。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
专题四 溶解度曲线图像题
一、题型分析
题型一、某一点的含义
1、曲线上的一点:在t2℃时,A的溶解度是
2、两曲线焦点:在t1℃时,A和C的溶解度相等均为
注:①纵坐标若给出数值需指出
②若A、B、C的名称给出需标明名称
题型二、相同温度,溶解性大小的比较
3、t2℃时三种物质溶解度大小顺序为
题型三、结合图像的计算(注意有陷阱)
4、t2℃时把75gA物质放入100g水中,所得溶液质量为 ,溶质的质量分数为 。
溶质质量分数
题型四、不饱和与饱和溶液的转换方法
题型五、同一温度,不同溶质质量的饱和溶液降温(升温)所得溶液的溶质质量分数大小比较
解题技巧:找变化前后的最低点
5、t2℃时三个物质的饱和溶液的溶质质量分数大小 ,降温至t1℃时溶液溶质质量分数大小
题型六、等质量不同溶质的饱和溶液,降温(升温),所得析出固体质量的大小比较
解题技巧:溶解度减小快,析出多;溶解度增加,不析出。
6、t2℃时,同质量的ABC饱和溶液降温至t1℃后,A、B溶解度减小,有晶体析出,且A的溶解度受温度影响大,A析出的晶体 ,B析出的晶体 ,C溶解度增加,晶体 ,故析出晶体质量
题型七、利用溶解度曲线特点提纯某物质
7、溶解度随温度变化大,如A,常用
8、溶解度随温度变化小,如B,常用
9、物质提纯,以主角为中心,如除去A中少量B(留下A)采用 ,若除去B中的少量A(留下B)
题型八、会用气体溶解度的影响因素解释简单实际问题:
10、①喝汽水易打嗝:
②打开汽水瓶盖会冒出大量气泡:
③水沸腾前就会出现气泡:
二、题型训练
1.如图为a、b、c三种不含结晶水的固体物质的溶解度曲线,下列叙述中正确的是( )
A.t1℃ 时,a、b、c饱和溶液的溶质质量分数为20%
B.P点表示:t2℃时,a、b的溶液是饱和状态,c的溶液是不饱和状态
C.t2℃时,a、b、c三种物质溶液的溶质质量分数a>b>c
D.70g a的饱和溶液从t2℃降温到t1℃时,析出晶体15g
2.如图为A物质的溶解度曲线.M、N两点分别表示A物质的两种溶液.下列做法不能实现M、N间的相互转化的是(A从溶液中析出时不带结晶水)( )
A.从N→M:先向N中加入适量固体A,再降温至t1℃
B.从N→M:先将N降温至t1℃,再恒温蒸发至有晶体析出
C.从M→N:先将M升温至t2℃,再恒温加入适量水
D.从M→N:先将M升温至t2℃,再恒温将其蒸发掉部分水
3.甲、乙两种固体的溶解度曲线如图所示。将①②两支试管中的甲、乙饱和溶液(均有少量未溶解的固体)放进盛有热水的烧杯里,升高温度后,下列有关说法正确的是( )
A.①溶液质量增加,②溶液质量减少
B.①②两溶液均变为不饱和溶液
C.甲的溶解度大于乙的溶解度
D.①溶液中溶质的质量分数大于②溶液
4.如图为甲、乙、丙三种固体物质的溶解度曲线图,请回答下列问题。
(1)Q点的含义是 ;
(2)若使接近饱和的丙溶液转变成饱和溶液,可采取的方法是 (任写一种方法);
(3)甲中含少量乙时,可通过 的方法提纯甲;
(4)t2℃时,将35g甲加入到50g水中,充分搅拌后,所形成溶液的质量为 g;
(5)将t2℃的甲、乙、丙三种物质的饱和溶液降温至t1℃,所得三种溶液溶质质量分数关系正确的是________(填选项字母)。
A.甲=丙<乙 B.甲=乙>丙 C.乙>甲>丙
5.下图是甲、乙两种物质的溶解度曲线。
(1)判断甲溶液在A点时处于 状态。
(2)t2℃时,在烧杯中分别盛有等质量的甲、乙两种溶质的饱和溶液,从t2℃降温到t1℃时,对烧杯中剩余溶液描述正确的是 。
A.溶质的质量分数:甲>乙 B.析出固体的质量:甲>乙
C.甲是饱和溶液,乙是不饱和溶液 D.溶剂的质量:甲=乙
6.如图所示是三种物质的溶解度曲线。请回答下列问题。
(1)溶解度随温度升高而降低的是 ;30 ℃时溶解度最大的是 。
(2)80 ℃时硝酸钠饱和溶液的溶质质量分数为 。使硝酸钠不饱和溶液变为饱和溶液,可采取的措施有 (写一种)。
(3)某硝酸钾固体中混有少量硫酸铈杂质,分离提纯硝酸钾的操作是:配成高温下的硝酸钾饱和溶液、 、过滤、洗涤、干燥。
(4)30 ℃时,用等质量的硝酸钾、硝酸钠配制两种物质的饱和溶液需要水的质量:硝酸钾 (填“>”“<”或“=”)硝酸钠。
(5)配制一定溶质质量分数的硝酸钾溶液,以下操作中会导致所配制溶液的溶质质量分数偏小的是 (填字母)。
A.用量筒量取水时仰视读数 B.配制好的溶液向细口瓶中转移时溅出
C.硝酸钾固体中含有杂质 D.烧杯事先用水润洗过,内壁有水
7.如图是a、b、c三种固体物质的溶解度曲线,下列分析正确的是( )
A.t1℃时a、c两物质溶液中溶质的质量分数相等
B.t2℃时,物质a的100g饱和溶液中含有25g物质a
C.t2℃时,分别将a、b、c的饱和溶液降温至t1℃,溶质质量分数关系是b>a=c
D.t2℃时向50g水中加入15g物质b充分搅拌,所得溶液质量一定小于65g
8.60℃时,向100g水中加入一定量KNO3形成溶液,再降温至20℃,析出固体质量的变化如图1,结合图2,下列说法正确的是( )
A.加入的KNO3质量为41.6g
B.降温过程中KNO3溶液始终为饱和溶液
C.蒸发溶剂可将M点的溶液转化到N点
D.20℃时,100g KNO3饱和溶液中有KNO331. 6g
9.在相同温度下,将50g和100g饱和的KNO3溶液分别蒸发掉10g水和20g水,分别析出ag和bg溶质。则a和b的关系是( )
A.2a=b B.a=b C.a=2b D.a
一、
题型一、 1、50g 2、15g
题型二、 3、A>B>C
题型三、 4、150g 33.3%
题型五、 5、A>B>C B>A>C
题型六、 6、多 少 没有析出 A>B>C
题型七、 7、冷却热饱和溶液(降温结晶) 8、蒸发结晶 9、冷却热饱和溶液 蒸发溶剂后趁热过滤
题型八、 10、①体内温度高,二氧化碳溶解度变小逸出
②打开瓶盖时瓶内压强变小,二氧化碳溶解度变小逸出
③温度升高,水中空气的溶解度变小逸出
二、
1.【答案】A
【解答】A.t1℃时,a、b、c的溶解度都是25g,
则它们的饱和溶液的溶质质量分数约为:,故A正确;
B.t2℃时,P点在a、b图像对应点的下方,即此时溶质质量小于溶解度,即a、b的溶液是不饱和状态。P点在图像c的上方,即溶质质量大于c的溶解度,因此c的溶液是饱和的,故B错误;
C.t2℃时,a、b、c三种物质的溶解度:a>b>c,则它们的饱和溶液的溶质质量分数a>b>c,因为没有指明是饱和溶液,故C错误;
D.t2℃时,70ga的饱和溶液中溶质质量为:。t1℃时,70ga的饱和溶液中溶质质量为:。则从t2℃降温到t1℃时,析出晶体:20g-14g=6g,故D错误。
故选A。
2.【答案】D
【解答】从N→M意思是单位溶剂溶解溶质的量增加,溶液由不饱和变饱和且溶液温度降低,可采取增加溶质和降低温度的方法,故A、B正确不合题意;
从M→N意思是单位溶剂溶解溶质的量减小,溶液由饱和变为不饱和且溶液温度升高,可采取减小溶质(如降温析出晶体或将溶质变成沉淀或气体反应掉)需将固体滤除和升温的方法,故C正确不合题意;
先将M升温溶质质量不会变小,此时溶液变为不饱和溶液(该物质的溶解度随温度的升高而增大),但然后将其蒸发掉部分水则溶液有可能又会变成饱和溶液,故D错误符合题意。
故选D。
3.【答案】A
【解答】①②试管中都存在少量为溶解的固体,则原来①②都是饱和溶液。
A.根据图像可知,甲的溶解度随温度的升高而增大,乙的溶解度随温度的升高而减小。当升高温度后,甲的溶解度增大,①中肯定会有甲继续溶解,即溶质质量增加。乙的溶解度减小,即②中肯定会有乙固体继续析出,则②中溶质质量减小,溶液质量减小,故A正确;
B.原来它们都是饱和溶液,甲的溶解度增大,则①变为不饱和溶液;乙的溶解度减小,则②仍然为饱和溶液,故B错误;
C.根据图像可知,溶解度甲可能大于乙,等于乙或小于乙,不指明温度,无法比较,故C错误;
D.无法确定甲和乙中溶质和溶液的质量大小,因为无法比较它们的溶质质量分数的大小,故D错误。
故选A。
4.【答案】(1)表示t1℃时,甲和丙的溶解度相等
(2)增加溶质;升高温度,恒温蒸发水分
(3)降温结晶(或冷却热饱和溶液)
(4)80
(5)C
【解答】(1)根据图像可知,Q点的含义为:t1℃时,甲和丙的溶解度相等。
(2)根据图像可知,丙的溶解度随温度的升高而减小,则将丙的不饱和溶液转换为饱和溶液的方法为:增加溶质;升高温度;恒温蒸发水分。
(3)根据图像可知,甲的溶解度随温度的升高而迅速增多,乙的溶解度受温度的影响较小,则:甲中含少量乙时,可通过降温结晶(或冷却热饱和溶液)的方法提纯甲。
(4)t2℃时,甲的溶解度为60g,即100g水中最多溶解60g甲,那么50g水中最多溶解30g。因为35g>30g,所用此时溶液饱和,即形成溶液的质量:30g+50g=80g。
(5)甲和乙的溶解度随温度的降低而减小,即它们的饱和溶液从t2℃降低到t1℃时,仍然为饱和溶液。因为此时的溶解度乙>甲,所以此时的溶质质量分数乙>甲。丙的溶解度随温度的降低而增大,因此丙由饱和溶液变成不饱和溶液。t1℃时,甲和丙的溶解度相等,即二者此时的饱和溶液的溶质质量分数相同,因此溶质质量分数甲>丙。
那么溶质质量分数乙>甲>丙。
5.【答案】(1)不饱和
(2)B;D
【解答】(1)根据图片可知,A点的溶质质量小于对应温度下甲的溶解度,因此处于不饱和状态。
(2)根据图像可知,二者的溶解度都随温度的降低而减小,因此温度降低后二者还是饱和溶液,故C错误;
t1℃时,甲的溶解度小于乙的溶解度,因此甲的溶质质量分数小于乙的溶质质量分数,故A错误;
t2℃时,甲和乙的溶解度相等,而t1℃时,甲的溶解度小于乙的溶解度,则析出固体的质量:甲>乙,故B正确;
在降温的过程中,变化的是溶质的质量,而溶剂的质量保持不变,故D正确。
故选BD。
6.【答案】(1)硫酸铈;硝酸钠
(2)60%;加入硝酸钠固体(合理即可)
(3)降温结晶
(4)>
(5)A;C;D
【解答】(1)根据图片可知,溶解度随温度升高而降低的是硫酸铈。30℃时,硝酸钠、硝酸钾和硫酸铈的溶解度分别为100g、40g和10g,则此时溶解度最大的是硝酸钠。
(2)80℃时硝酸钠的溶解度为150g,则溶质质量分数为:;
使硝酸钠的不饱和溶液变为饱和溶液,采取的措施为:加入硝酸钠固体,蒸发溶剂或降低温度从而减小溶解度。
(3)硝酸钾的溶解度随温度的升高而增大,而硫酸铈的溶解度随温度的升高而减小,那么某硝酸钾固体中混有少量硫酸铈杂质,分离提纯硝酸钾的操作是:配成高温下的硝酸钾饱和溶液、降温结晶、过滤、洗涤、干燥。
(4)30℃时,硝酸钾的溶解度为40g,设m克硝酸钾配制成饱和溶液需用水质量为x,
;
解得:x=;
30℃时,硝酸钠的溶解度为100g,设m克硝酸钾配制成饱和溶液需用水质量为y,
;
解得:z=;
则需要水的质量:硝酸钾>硝酸钠。
(5)A.用量筒量取水时仰视读数,读出的示数偏小,而实际的水的体积偏大,从而导致溶质质量分数偏小,故A符合题意;
B.配制好的溶液向细口瓶中转移时溅出,由于溶液的均一性,因此不会改变溶质质量分数,故B不会题意;
C.硝酸钾固体中含有杂质,会导致溶质质量减小,故C符合题意;
D.烧杯事先用水润洗过,内壁有水,会导致溶剂水的体积偏大,故D符合题意。
故选ACD。
7.【答案】D
【解答】A、t1℃时a、c两物质溶解度相同,二者饱和溶液中溶质的质量分数相等,题干中未注明“饱和”,溶质的质量分数不一定相等,故A错误;B、t2℃时,物质a的溶解度是25g,100g水中最多溶解物质a的质量为25g,所以100g饱和溶液中含有20g物质a,故B错误;C、t2℃降温至t1℃,由于c的溶解度随温度降低而增大,c的质量分数不变;a、b溶解度随温度降低而减小,故质量分数减小。故比较t1℃时a、b饱和溶液的质量分数与t2℃物质c饱和溶质质量分数即可。溶质质量分数关系是b>a>c,故C错误; D、t2℃时b的溶解度为25g,即该温度下100g水中最多溶解b12.5g,向50g水中加入15g物质b充分搅拌,所得溶液质量一定小于65g,故D正确。故选D。
8.【答案】A
【解答】A、20℃时,硝酸钾的溶解度为31.6g,即该温度下,100g水中最多能溶解31.6g硝酸钾,故60℃时,向100g水中加入一定量KNO3形成溶液,再降温至20℃,共析出10g硝酸钾,说明加入硝酸钾的质量为41.6g,符合题意;B、由图2可知,硝酸钾的溶解度随温度的升高而增加,由图1可知,降温过程中,一开始没有溶质析出,说明一开始是不饱和溶液,后有溶质析出,变为饱和溶液,不符合题意;C、M点为20℃时,硝酸钾的饱和溶液,N点为20℃时,硝酸钾的不饱和溶液,故增加溶剂或恒温蒸发可将M点的溶液转化到N点,不符合题意;D、20℃时,硝酸钾的溶解度为31.6g,131.6g硝酸钾饱和溶液中硝酸钾的质量31.6g,不符合题意。故选A。
9. 【答案】A
【解答】两KNO3溶液处于同一温度下,且都是饱和溶液,因此它们溶液的浓度是一样的,其中20g水中所含有溶质应是10g水中的两倍,故2a=b。故选A。
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com)
同课章节目录
- 第1章 水和水的溶液
- 第1节 地球上的水
- 第2节 水的组成
- 第3节 水的浮力
- 第4节 物质在水中的分散状况
- 第5节 物质的溶解
- 第6节 物质的分离
- 第7节 水资源的利用、开发和保护
- 第2章 天气与气候
- 第1节 大气层
- 第2节 气温
- 第3节 大气的压强
- 第4节 风和降水
- 第5节 天气预报
- 第6节 气候和影响气候的因素
- 第7节 我国的气候特征与主要气象灾害
- 第3章 生命活动的调节
- 第1节 植物生命活动的调节
- 第2节 人体的激素调节
- 第3节 神经调节
- 第4节 动物的行为
- 第5节 体温的控制
- 第4章 电路探秘
- 第1节 电荷与电流
- 第2节 电流的测量
- 第3节 物质的导电性与电阻
- 第4节 变阻器
- 第5节 电压的测量
- 第6节 电流与电压、电阻的关系
- 第7节 电路分析与应用
- 研究性学习课题
- 一 测定本地区的“酸雨”情况及分析原因
- 二 太阳黑子活动与本地区降水的关系
- 三 训练小动物建立某种条件反射
- 四 调查在自然界或生命活动中的电现象
