2022华师大版九上科学 3.3常见的盐(4)教学设计
文档属性
| 名称 | 2022华师大版九上科学 3.3常见的盐(4)教学设计 |

|
|
| 格式 | doc | ||
| 文件大小 | 1.4MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 华东师大版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2022-09-20 00:00:00 | ||
图片预览

文档简介
中小学教育资源及组卷应用平台
HS版九上3.3常见的盐(4)教学设计
课题 3.3常见的盐(4) 单元 三 学科 科学 年级 九上
教材分析 本课时主要是实验指导:实验室制取二氧化碳。这是培养学生在实验室中制取某种气体,药品的选择、装置的设计、实验的方法等思路的最佳素材。从反应到实验装置到验证方法,把研究气体的一般思维和方法进行到底,升华为认识物质的一种能力。建议教学思路:(1)先通过稀盐酸和大理石反应、稀硫酸和大理石反应、稀盐酸和碳酸钠反应的对比来探究实验室制取二氧化碳的理想药品;(2)开放性探究实验室制取二氧化碳的装置。(切不可将教材中给出的装置作为唯一的标准的装置,要鼓励创新)(3)收集装置可与氧气进行对比确定。
学习目标 科学观念:了解实验室制取二氧化碳的原理和方法,知道二氧化碳的检验和验满方法;知道实验室制取气体的一般思路和方法科学思维:通过二氧化碳和氧气性质对比,了解制取二氧化碳和氧气的发生装置与收集方法的异同,初步确立实验室制取气体的一般思路和方法探究实践:通过小组讨论、设计实验装置的来制取气体过程中,提高实验创新能力和创新意识;掌握基本实验技能,树立多角度、多层次观察和分析问题的能力;态度责任:增强对实验的好奇和探究欲,激发学习的兴趣,发展乐于探究、勇于创新、大胆实践的科学精神
重点 实验室制取二氧化碳反应原理、实验装置的选择、检验和验满
难点 实验装置的改进以及实验室制取气体的一般思路和方法
教学环节 教师活动 设计意图
导入新课 说出能产生二氧化碳的有关反应;常见的有:木炭燃烧 、碳酸分解 、盐酸(硫酸)与碳酸钠反应 、盐酸与石灰石反应 、碳酸钡与盐酸(硫酸)反应 、碳酸钙分解、煅烧石灰石 …… 等。针对学生列举的众多反应, 指出酸与碳酸盐反应最简易、安全、节能;并就此提出问题:哪一种方法更适合实验室制取二氧化碳? 从复习讨论引入,自然而有效
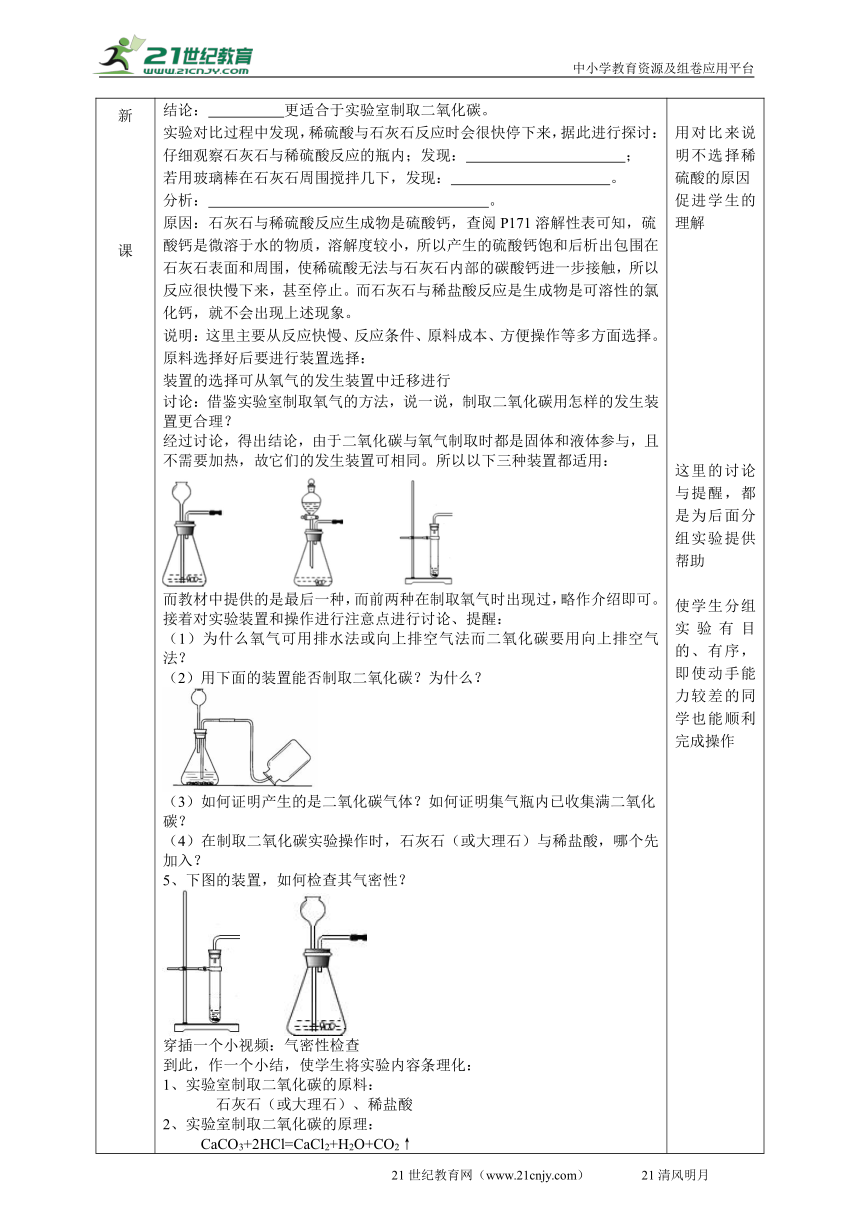
讲授新课 探究1:探究哪种碳酸盐更适用于实验室制取二氧化碳(1)取等量碳酸钠粉末、碳酸氢钠粉末、碳酸钙粉末、石灰石分别装入4个洁净的试管中; (2)向4个试管中分别加入等量的稀盐酸; 观察到的现象: 。 结论:石灰石更适合于实验室制取二氧化碳。同时指出大理石与石灰石类似,有效成分也是碳酸钙 ,两者都可用于制取二氧化碳接着要对酸进行选择:探究2、稀盐酸或稀硫酸中哪一种酸更适合与石灰石反应制取二氧化碳(1)取等量石灰石分别装入2个洁净的锥形瓶中; (2)向1个锥形瓶中加入适量的稀盐酸,另一锥形瓶中加入等量的稀硫酸; 观察到的现象: 。 结论: 更适合于实验室制取二氧化碳。 实验对比过程中发现,稀硫酸与石灰石反应时会很快停下来,据此进行探讨:仔细观察石灰石与稀硫酸反应的瓶内;发现: ; 若用玻璃棒在石灰石周围搅拌几下,发现: 。 分析: 。 原因:石灰石与稀硫酸反应生成物是硫酸钙,查阅P171溶解性表可知,硫酸钙是微溶于水的物质,溶解度较小,所以产生的硫酸钙饱和后析出包围在石灰石表面和周围,使稀硫酸无法与石灰石内部的碳酸钙进一步接触,所以反应很快慢下来,甚至停止。而石灰石与稀盐酸反应是生成物是可溶性的氯化钙,就不会出现上述现象。说明:这里主要从反应快慢、反应条件、原料成本、方便操作等多方面选择。原料选择好后要进行装置选择:装置的选择可从氧气的发生装置中迁移进行讨论:借鉴实验室制取氧气的方法,说一说,制取二氧化碳用怎样的发生装置更合理?经过讨论,得出结论,由于二氧化碳与氧气制取时都是固体和液体参与,且不需要加热,故它们的发生装置可相同。所以以下三种装置都适用:而教材中提供的是最后一种,而前两种在制取氧气时出现过,略作介绍即可。接着对实验装置和操作进行注意点进行讨论、提醒:(1)为什么氧气可用排水法或向上排空气法而二氧化碳要用向上排空气法?(2)用下面的装置能否制取二氧化碳?为什么? (3)如何证明产生的是二氧化碳气体?如何证明集气瓶内已收集满二氧化碳?(4)在制取二氧化碳实验操作时,石灰石(或大理石)与稀盐酸,哪个先加入? 5、下图的装置,如何检查其气密性? 穿插一个小视频:气密性检查到此,作一个小结,使学生将实验内容条理化:1、实验室制取二氧化碳的原料: 石灰石(或大理石)、稀盐酸 2、实验室制取二氧化碳的原理: CaCO3+2HCl=CaCl2+H2O+CO2↑3、实验室制取二氧化碳的装置图:下面进行分组实验(学生完成、教师巡视指导)1、按照图3.3.4装配仪器,并对装置进行气密性检查。在大试管里放入小块石灰石(或大理石),注入稀盐酸,塞上单孔塞。把导管伸到瓶口向上的集气瓶的底部,用向上排气法收集一瓶二氧化碳。在大试管里可以观察到的现象是: ,用燃着的火柴放在集气瓶口, 如果火焰立即熄灭,证明 。 2、再把导管伸入另一盛有澄清石灰水的试管中,通入气体,澄清石灰水会 ,说明 。 最后,进行必要的实验反馈、总结。学生观看视频“实验室制取二氧化碳”对照自己的操作,发现问题及时止损。 培养学生分析问题评价实验方案的能力初步形成实验室制取气体的反应原料的选择思路用对比来说明不选择稀硫酸的原因促进学生的理解这里的讨论与提醒,都是为后面分组实验提供帮助使学生分组实验有目的、有序,即使动手能力较差的同学也能顺利完成操作实验操作的过程、步骤、细节都了解了,学生再动手,有利于增强学生的信心起查漏补缺作用
课堂练习 1、下列反应常用于实验室制取二氧化碳的是( C )A.高温煅烧石灰石 B.石灰石与稀硫酸反应C.大理石与稀盐酸反应 D.木炭在氧气中燃烧2、下列是实验室制取二氧化碳的几个操作,下列的是( A) 3、实验表明,不能用块状大理石和稀硫酸制取大量的二氧化碳气体,但是可以用大理石粉末与稀硫酸制取,由此得出的结论是( B ) A.物质之间是否发生反应,与物质的形状有关 B.反应物之间的接触面积越大,越有利于反应的进行 C.块状大理石与大理石粉末的化学性质不同 D.块状大理石与大理石粉末中的元素种类不同4、实验室制取CO2有以下步骤:①连接好装置;②向试管中小心放入几小块石灰石;③向试管中小心注入适量稀盐酸;④检查装置的气密性;⑤收集产生的气体;⑥用燃着的木条检验集气瓶是否收集满CO2。以上操作按由先至后的顺序排列正确的是( B )A.①②③④⑤⑥ B.①④②③⑤⑥C.①③②④⑤⑥ D.③①②④⑤⑥5、下列有关实验室制取二氧化碳的叙述中,正确的是 ( C ) A.用稀硫酸和大理石反应来制取
B.反应中石灰石颗粒越小越好
C.反应前应先检查装置的气密性
D.用向下排空气法收集二氧化碳 6、在实验室中,同学们用如图所示装置制取纯净的CO2,下列说法不正确的是(A ) A.①中固体反应物也可用Na2CO3固体代替 B.③中没有白色沉淀产生,说明CO2气体中已经不混有HCl气体 C.④中浓H2SO4的作用是吸收CO2气体中混有的H2O D.将燃着的小木条放在⑤中的集气瓶口,可以检验集气瓶内是否收集满CO2 解题提示:饱和碳酸氢钠溶液可以吸收HCl而不吸收CO2 7、根据下列实验装置图,按要求回答下列问题: (1)写出标有序号的仪器名称:①_试管__;②__长颈漏斗___。 (2)实验室制取CO2的化学方程式为_CaCO3+2HCl=CaCl2+H2O+CO2↑__;其基本反应类型是__复分解反应_。制取并收集该气体应选择的装置是____BE_(填序号);若想控制反应速率,可以将仪器②用__分液漏斗__代替;检验该气体的方法是 将该气体通入澄清石灰水,若变浑浊则为二氧化碳 。 及时训练,有利于巩固刚刚学习的新知识。同时还有发现学生理解所学知识中存在的问题,便于及时纠正、修补。
课堂小结 1、实验室常用石灰石(或大理石)与稀盐酸反应制取二氧化碳;并用向上排空气法收集二氧化碳; 2、实验室制取二氧化碳的化学方程式: CaCO3+2HCl=CaCl2+H2O+CO2↑ 3、检验二氧化碳用澄清的石灰水;而二氧化碳验满要将燃着的木条放在集气瓶口。 帮助学生掌握重点,更加容易的学习。
板书
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com) 21清风明月
HS版九上3.3常见的盐(4)教学设计
课题 3.3常见的盐(4) 单元 三 学科 科学 年级 九上
教材分析 本课时主要是实验指导:实验室制取二氧化碳。这是培养学生在实验室中制取某种气体,药品的选择、装置的设计、实验的方法等思路的最佳素材。从反应到实验装置到验证方法,把研究气体的一般思维和方法进行到底,升华为认识物质的一种能力。建议教学思路:(1)先通过稀盐酸和大理石反应、稀硫酸和大理石反应、稀盐酸和碳酸钠反应的对比来探究实验室制取二氧化碳的理想药品;(2)开放性探究实验室制取二氧化碳的装置。(切不可将教材中给出的装置作为唯一的标准的装置,要鼓励创新)(3)收集装置可与氧气进行对比确定。
学习目标 科学观念:了解实验室制取二氧化碳的原理和方法,知道二氧化碳的检验和验满方法;知道实验室制取气体的一般思路和方法科学思维:通过二氧化碳和氧气性质对比,了解制取二氧化碳和氧气的发生装置与收集方法的异同,初步确立实验室制取气体的一般思路和方法探究实践:通过小组讨论、设计实验装置的来制取气体过程中,提高实验创新能力和创新意识;掌握基本实验技能,树立多角度、多层次观察和分析问题的能力;态度责任:增强对实验的好奇和探究欲,激发学习的兴趣,发展乐于探究、勇于创新、大胆实践的科学精神
重点 实验室制取二氧化碳反应原理、实验装置的选择、检验和验满
难点 实验装置的改进以及实验室制取气体的一般思路和方法
教学环节 教师活动 设计意图
导入新课 说出能产生二氧化碳的有关反应;常见的有:木炭燃烧 、碳酸分解 、盐酸(硫酸)与碳酸钠反应 、盐酸与石灰石反应 、碳酸钡与盐酸(硫酸)反应 、碳酸钙分解、煅烧石灰石 …… 等。针对学生列举的众多反应, 指出酸与碳酸盐反应最简易、安全、节能;并就此提出问题:哪一种方法更适合实验室制取二氧化碳? 从复习讨论引入,自然而有效
讲授新课 探究1:探究哪种碳酸盐更适用于实验室制取二氧化碳(1)取等量碳酸钠粉末、碳酸氢钠粉末、碳酸钙粉末、石灰石分别装入4个洁净的试管中; (2)向4个试管中分别加入等量的稀盐酸; 观察到的现象: 。 结论:石灰石更适合于实验室制取二氧化碳。同时指出大理石与石灰石类似,有效成分也是碳酸钙 ,两者都可用于制取二氧化碳接着要对酸进行选择:探究2、稀盐酸或稀硫酸中哪一种酸更适合与石灰石反应制取二氧化碳(1)取等量石灰石分别装入2个洁净的锥形瓶中; (2)向1个锥形瓶中加入适量的稀盐酸,另一锥形瓶中加入等量的稀硫酸; 观察到的现象: 。 结论: 更适合于实验室制取二氧化碳。 实验对比过程中发现,稀硫酸与石灰石反应时会很快停下来,据此进行探讨:仔细观察石灰石与稀硫酸反应的瓶内;发现: ; 若用玻璃棒在石灰石周围搅拌几下,发现: 。 分析: 。 原因:石灰石与稀硫酸反应生成物是硫酸钙,查阅P171溶解性表可知,硫酸钙是微溶于水的物质,溶解度较小,所以产生的硫酸钙饱和后析出包围在石灰石表面和周围,使稀硫酸无法与石灰石内部的碳酸钙进一步接触,所以反应很快慢下来,甚至停止。而石灰石与稀盐酸反应是生成物是可溶性的氯化钙,就不会出现上述现象。说明:这里主要从反应快慢、反应条件、原料成本、方便操作等多方面选择。原料选择好后要进行装置选择:装置的选择可从氧气的发生装置中迁移进行讨论:借鉴实验室制取氧气的方法,说一说,制取二氧化碳用怎样的发生装置更合理?经过讨论,得出结论,由于二氧化碳与氧气制取时都是固体和液体参与,且不需要加热,故它们的发生装置可相同。所以以下三种装置都适用:而教材中提供的是最后一种,而前两种在制取氧气时出现过,略作介绍即可。接着对实验装置和操作进行注意点进行讨论、提醒:(1)为什么氧气可用排水法或向上排空气法而二氧化碳要用向上排空气法?(2)用下面的装置能否制取二氧化碳?为什么? (3)如何证明产生的是二氧化碳气体?如何证明集气瓶内已收集满二氧化碳?(4)在制取二氧化碳实验操作时,石灰石(或大理石)与稀盐酸,哪个先加入? 5、下图的装置,如何检查其气密性? 穿插一个小视频:气密性检查到此,作一个小结,使学生将实验内容条理化:1、实验室制取二氧化碳的原料: 石灰石(或大理石)、稀盐酸 2、实验室制取二氧化碳的原理: CaCO3+2HCl=CaCl2+H2O+CO2↑3、实验室制取二氧化碳的装置图:下面进行分组实验(学生完成、教师巡视指导)1、按照图3.3.4装配仪器,并对装置进行气密性检查。在大试管里放入小块石灰石(或大理石),注入稀盐酸,塞上单孔塞。把导管伸到瓶口向上的集气瓶的底部,用向上排气法收集一瓶二氧化碳。在大试管里可以观察到的现象是: ,用燃着的火柴放在集气瓶口, 如果火焰立即熄灭,证明 。 2、再把导管伸入另一盛有澄清石灰水的试管中,通入气体,澄清石灰水会 ,说明 。 最后,进行必要的实验反馈、总结。学生观看视频“实验室制取二氧化碳”对照自己的操作,发现问题及时止损。 培养学生分析问题评价实验方案的能力初步形成实验室制取气体的反应原料的选择思路用对比来说明不选择稀硫酸的原因促进学生的理解这里的讨论与提醒,都是为后面分组实验提供帮助使学生分组实验有目的、有序,即使动手能力较差的同学也能顺利完成操作实验操作的过程、步骤、细节都了解了,学生再动手,有利于增强学生的信心起查漏补缺作用
课堂练习 1、下列反应常用于实验室制取二氧化碳的是( C )A.高温煅烧石灰石 B.石灰石与稀硫酸反应C.大理石与稀盐酸反应 D.木炭在氧气中燃烧2、下列是实验室制取二氧化碳的几个操作,下列的是( A) 3、实验表明,不能用块状大理石和稀硫酸制取大量的二氧化碳气体,但是可以用大理石粉末与稀硫酸制取,由此得出的结论是( B ) A.物质之间是否发生反应,与物质的形状有关 B.反应物之间的接触面积越大,越有利于反应的进行 C.块状大理石与大理石粉末的化学性质不同 D.块状大理石与大理石粉末中的元素种类不同4、实验室制取CO2有以下步骤:①连接好装置;②向试管中小心放入几小块石灰石;③向试管中小心注入适量稀盐酸;④检查装置的气密性;⑤收集产生的气体;⑥用燃着的木条检验集气瓶是否收集满CO2。以上操作按由先至后的顺序排列正确的是( B )A.①②③④⑤⑥ B.①④②③⑤⑥C.①③②④⑤⑥ D.③①②④⑤⑥5、下列有关实验室制取二氧化碳的叙述中,正确的是 ( C ) A.用稀硫酸和大理石反应来制取
B.反应中石灰石颗粒越小越好
C.反应前应先检查装置的气密性
D.用向下排空气法收集二氧化碳 6、在实验室中,同学们用如图所示装置制取纯净的CO2,下列说法不正确的是(A ) A.①中固体反应物也可用Na2CO3固体代替 B.③中没有白色沉淀产生,说明CO2气体中已经不混有HCl气体 C.④中浓H2SO4的作用是吸收CO2气体中混有的H2O D.将燃着的小木条放在⑤中的集气瓶口,可以检验集气瓶内是否收集满CO2 解题提示:饱和碳酸氢钠溶液可以吸收HCl而不吸收CO2 7、根据下列实验装置图,按要求回答下列问题: (1)写出标有序号的仪器名称:①_试管__;②__长颈漏斗___。 (2)实验室制取CO2的化学方程式为_CaCO3+2HCl=CaCl2+H2O+CO2↑__;其基本反应类型是__复分解反应_。制取并收集该气体应选择的装置是____BE_(填序号);若想控制反应速率,可以将仪器②用__分液漏斗__代替;检验该气体的方法是 将该气体通入澄清石灰水,若变浑浊则为二氧化碳 。 及时训练,有利于巩固刚刚学习的新知识。同时还有发现学生理解所学知识中存在的问题,便于及时纠正、修补。
课堂小结 1、实验室常用石灰石(或大理石)与稀盐酸反应制取二氧化碳;并用向上排空气法收集二氧化碳; 2、实验室制取二氧化碳的化学方程式: CaCO3+2HCl=CaCl2+H2O+CO2↑ 3、检验二氧化碳用澄清的石灰水;而二氧化碳验满要将燃着的木条放在集气瓶口。 帮助学生掌握重点,更加容易的学习。
板书
21世纪教育网 www.21cnjy.com 精品试卷·第 2 页 (共 2 页)
21世纪教育网(www.21cnjy.com) 21清风明月
