沪教版化学九年级上册2.1 性质活泼的氧气 课件(共28张PPT)
文档属性
| 名称 | 沪教版化学九年级上册2.1 性质活泼的氧气 课件(共28张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 3.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-09-20 00:00:00 | ||
图片预览








文档简介
(共28张PPT)
第二章 身边的化学物质
沪教版九年级上册化学课件
第一节
性质活泼的氧气
学习目标
学习目标
1.了解空气的组成;
2.了解什么是混合物和纯净物,并能进行区别;
3.了解排水集气法的基本原理;
4.简单了解氮气和稀有气体的特性和用途以及空气的污染和污染防治的有关知识。
新课讲解
新课讲解
知识点一
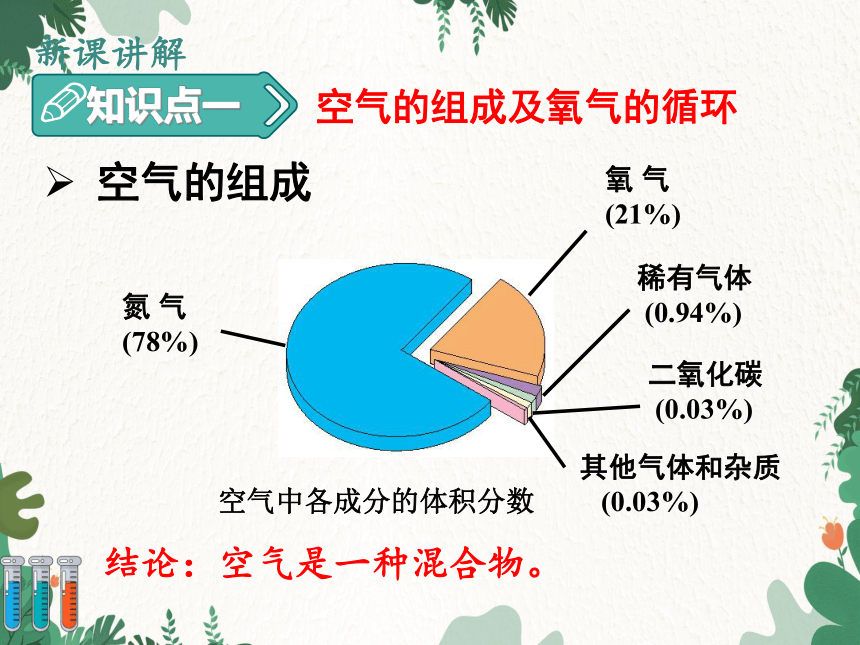
空气的组成及氧气的循环
氮 气
(78%)
氧 气
(21%)
稀有气体
(0.94%)
其他气体和杂质
(0.03%)
二氧化碳
(0.03%)
空气中各成分的体积分数
空气的组成
结论:空气是一种混合物。
新课讲解
氧气在自然界中的循环
自然界中氧气产生的途径主要是植物的光合作用,而消耗的途径主要有动植物呼吸、燃料的燃烧、金属的锈蚀、动植物的腐烂等。
由于绿色植物的光合作用所放出的氧气,弥补了自然界中氧气的消耗,正是这种持续、稳定的氧循环,维持了相对恒定的大气含氧量,不会使大气中氧气的含量越来越低。
新课讲解
知识点二
认识氧气的性质
颜色状态:
密度:
溶解性:
三态转化:101 kPa下,
无色、无气味的气体
比空气密度稍大
不易溶于水
无色气体
淡蓝色液体
淡蓝色固体
-183 ℃
-218.4 ℃
物理性质
贮存在钢瓶中的氧气
新课讲解
反应物的名称 反应物的色、态 在空气中燃烧现象 在氧气中燃烧现象 文字表达式
木炭
黑色固体
发出红光,
放出热量,
生成能使
澄清石灰
水变浑浊
的气体
碳+氧气
二氧化碳
点燃
化学性质
氧气和木炭反应
剧烈燃烧,发出白光,
放出大量的热量,生成能使澄清石灰水变浑浊
的气体
新课讲解
反应物的名称 反应物的色、态 在空气中燃烧现象 在氧气中燃烧现象 文字表达式
蜡烛
白色蜡状固体
石蜡+氧气
二氧化碳+水
点燃
氧气和石蜡反应
燃烧发出黄光,放热,瓶壁有雾珠出现,并生成能使澄清的石灰水变浑浊的气体
燃烧发出白光,放热,瓶壁有雾珠出现,并生成能使澄清的石灰水变浑浊的气体
化学性质
新课讲解
化学性质
氧气和铁丝反应
反应物的名称 反应物的色、态 在空气中燃烧现象 在氧气中燃烧现象 文字表达式
铁丝
银白色固体
铁丝红热,不能燃烧
铁+氧气
四氧化三铁
点燃
剧烈燃烧,火星四射,生成黑色固体,放出大量的热量
新课讲解
化学性质
①火柴的作用:引燃铁丝;
②将铁丝绕成螺旋状:增大与氧气的接触面积;
③待火柴即将燃尽时再将铁丝伸入氧气瓶中:
防止火柴燃烧消耗过多的氧气而使铁丝不能顺利燃烧;
④预先在集气瓶中装少量水或在瓶底铺一薄层细沙:
防止高温熔化物溅落下来炸裂瓶底;
⑤ 用砂纸磨掉铁丝表面的铁锈:使铁与氧气充分接触。
氧气和铁丝反应
新课讲解
氧化反应:
(非基本反应类型)
物质与氧气的反应称为氧化反应。
缓慢氧化:
物质与氧气只发生缓慢的氧化反应,甚至不易被察觉,这种氧化反应叫做缓慢氧化。例如:动植物呼吸、食物腐烂、酿酒等。
综上所述:氧气是一种化学性质比较活泼的气体,它在氧化反应中提供氧,具有氧化性,是一种常用的氧化剂。
供给呼吸
新课讲解
知识点三
氧气的用途
医疗、登山、潜水、航空等
新课讲解
支持燃烧
炼钢、气割、气焊、宇航、液氧炸药等
新课讲解
知识点四
氧气的制法
氧气的工业制法
新课讲解
氯酸钾
KClO3
氯化钾 + 氧气
二氧化锰
加热
KCl O2
(1)
(2)
高锰酸钾
锰酸钾+二氧化锰+氧气
加热
KMnO4
过氧化氢
二氧化锰
水 + 氧气
H2O2 H2O O2
(3)
K2MnO4 MnO2 O2
氧气的实验室制法
新课讲解
发生装置选择的依据:
固固加热型
反应物为固态
反应条件需加热
加热高锰酸钾制取氧气
发生装置
新课讲解
将带有导管的单孔胶塞塞紧试管,先将导管另一端放入水中,然后用手紧握试管,若导管口有气泡冒出,松开手后水倒流,导管内上升一段水柱,则说明装置的气密性好。
操作注意事项
加热高锰酸钾制取氧气
检查装置的气密性:
新课讲解
试管口应略低于试管底。防止加热时产生的水回流,使试管炸裂。
导管口应塞一团棉花。防止高锰酸钾粉末进入导气管。
铁夹应夹在试管的中上部。
药品应平铺于管底,用外焰加热。
酒精灯内的酒精不能超过2/3。防止引发火灾。
加热高锰酸钾制取氧气
操作注意事项
反应装置图
新课讲解
收(气泡连续、均匀冒出时开始收集)
点(酒精灯加热药品,利用外焰加热)
加热高锰酸钾制取氧气
操作注意事项
新课讲解
移(导管移出水槽)
熄(熄灭酒精灯)
防止水槽里的水倒流到试管底部,导致试管炸裂。
加热高锰酸钾制取氧气
操作注意事项
新课讲解
查(装置气密性)
装(装药品,塞紧单孔塞)
定(固定试管,先下后上、先左后右)
点(酒精灯加热药品)
收(气泡连续、均匀冒出时开始收集)
移(导管出水槽)
熄(灭酒精灯)
谐音:
茶
庄
定
点
收
利
息
加热高锰酸钾制取氧气
实验室制取氧气的步骤
新课讲解
发生装置
收集装置
分解双氧水制取氧气
装置图
新课讲解
固液常温型
发生装置
发生装置选择的依据:
反应物状态:
反应条件:
固态和液态
不需加热
分解双氧水制取氧气
新课讲解
收集装置选择的依据:
不易溶于水且不与水反应的气体
密度比空气大的气体且不与空气中气体反应
密度比空气小的气体且不与空气中气体反应
√
√
排水集气法
向上排空气法
向下排空气法
要考虑气体的
溶解性
是否与水反应
气体密度
与空气成分是否反应
(制得的氧气较纯)
(制得干燥的氧气)
收集装置
分解双氧水制取氧气
新课讲解
过氧化氢
二氧化锰
水 + 氧气
H2O2 H2O + O2
在化学反应中能增大化学反应速率,但本身的质量和化学性质在反应前后都没有发生变化的物质称为催化剂(又叫触媒)。
催化剂及其作用
新课讲解
(1)改变的只是化学反应速率,效果可加快或减慢。
(2)本身的化学性质在反应前后保持不变,但物理性质有可能改变。
(3)催化剂要针对某个具体反应而言。如不能单独说二氧化锰是催化剂;二氧化锰在氯酸钾分解实验中是催化剂,但不是所有化学反应的催化剂。
注意:
催化剂及其作用
谢谢聆听
第二章 身边的化学物质
沪教版九年级上册化学课件
第一节
性质活泼的氧气
学习目标
学习目标
1.了解空气的组成;
2.了解什么是混合物和纯净物,并能进行区别;
3.了解排水集气法的基本原理;
4.简单了解氮气和稀有气体的特性和用途以及空气的污染和污染防治的有关知识。
新课讲解
新课讲解
知识点一
空气的组成及氧气的循环
氮 气
(78%)
氧 气
(21%)
稀有气体
(0.94%)
其他气体和杂质
(0.03%)
二氧化碳
(0.03%)
空气中各成分的体积分数
空气的组成
结论:空气是一种混合物。
新课讲解
氧气在自然界中的循环
自然界中氧气产生的途径主要是植物的光合作用,而消耗的途径主要有动植物呼吸、燃料的燃烧、金属的锈蚀、动植物的腐烂等。
由于绿色植物的光合作用所放出的氧气,弥补了自然界中氧气的消耗,正是这种持续、稳定的氧循环,维持了相对恒定的大气含氧量,不会使大气中氧气的含量越来越低。
新课讲解
知识点二
认识氧气的性质
颜色状态:
密度:
溶解性:
三态转化:101 kPa下,
无色、无气味的气体
比空气密度稍大
不易溶于水
无色气体
淡蓝色液体
淡蓝色固体
-183 ℃
-218.4 ℃
物理性质
贮存在钢瓶中的氧气
新课讲解
反应物的名称 反应物的色、态 在空气中燃烧现象 在氧气中燃烧现象 文字表达式
木炭
黑色固体
发出红光,
放出热量,
生成能使
澄清石灰
水变浑浊
的气体
碳+氧气
二氧化碳
点燃
化学性质
氧气和木炭反应
剧烈燃烧,发出白光,
放出大量的热量,生成能使澄清石灰水变浑浊
的气体
新课讲解
反应物的名称 反应物的色、态 在空气中燃烧现象 在氧气中燃烧现象 文字表达式
蜡烛
白色蜡状固体
石蜡+氧气
二氧化碳+水
点燃
氧气和石蜡反应
燃烧发出黄光,放热,瓶壁有雾珠出现,并生成能使澄清的石灰水变浑浊的气体
燃烧发出白光,放热,瓶壁有雾珠出现,并生成能使澄清的石灰水变浑浊的气体
化学性质
新课讲解
化学性质
氧气和铁丝反应
反应物的名称 反应物的色、态 在空气中燃烧现象 在氧气中燃烧现象 文字表达式
铁丝
银白色固体
铁丝红热,不能燃烧
铁+氧气
四氧化三铁
点燃
剧烈燃烧,火星四射,生成黑色固体,放出大量的热量
新课讲解
化学性质
①火柴的作用:引燃铁丝;
②将铁丝绕成螺旋状:增大与氧气的接触面积;
③待火柴即将燃尽时再将铁丝伸入氧气瓶中:
防止火柴燃烧消耗过多的氧气而使铁丝不能顺利燃烧;
④预先在集气瓶中装少量水或在瓶底铺一薄层细沙:
防止高温熔化物溅落下来炸裂瓶底;
⑤ 用砂纸磨掉铁丝表面的铁锈:使铁与氧气充分接触。
氧气和铁丝反应
新课讲解
氧化反应:
(非基本反应类型)
物质与氧气的反应称为氧化反应。
缓慢氧化:
物质与氧气只发生缓慢的氧化反应,甚至不易被察觉,这种氧化反应叫做缓慢氧化。例如:动植物呼吸、食物腐烂、酿酒等。
综上所述:氧气是一种化学性质比较活泼的气体,它在氧化反应中提供氧,具有氧化性,是一种常用的氧化剂。
供给呼吸
新课讲解
知识点三
氧气的用途
医疗、登山、潜水、航空等
新课讲解
支持燃烧
炼钢、气割、气焊、宇航、液氧炸药等
新课讲解
知识点四
氧气的制法
氧气的工业制法
新课讲解
氯酸钾
KClO3
氯化钾 + 氧气
二氧化锰
加热
KCl O2
(1)
(2)
高锰酸钾
锰酸钾+二氧化锰+氧气
加热
KMnO4
过氧化氢
二氧化锰
水 + 氧气
H2O2 H2O O2
(3)
K2MnO4 MnO2 O2
氧气的实验室制法
新课讲解
发生装置选择的依据:
固固加热型
反应物为固态
反应条件需加热
加热高锰酸钾制取氧气
发生装置
新课讲解
将带有导管的单孔胶塞塞紧试管,先将导管另一端放入水中,然后用手紧握试管,若导管口有气泡冒出,松开手后水倒流,导管内上升一段水柱,则说明装置的气密性好。
操作注意事项
加热高锰酸钾制取氧气
检查装置的气密性:
新课讲解
试管口应略低于试管底。防止加热时产生的水回流,使试管炸裂。
导管口应塞一团棉花。防止高锰酸钾粉末进入导气管。
铁夹应夹在试管的中上部。
药品应平铺于管底,用外焰加热。
酒精灯内的酒精不能超过2/3。防止引发火灾。
加热高锰酸钾制取氧气
操作注意事项
反应装置图
新课讲解
收(气泡连续、均匀冒出时开始收集)
点(酒精灯加热药品,利用外焰加热)
加热高锰酸钾制取氧气
操作注意事项
新课讲解
移(导管移出水槽)
熄(熄灭酒精灯)
防止水槽里的水倒流到试管底部,导致试管炸裂。
加热高锰酸钾制取氧气
操作注意事项
新课讲解
查(装置气密性)
装(装药品,塞紧单孔塞)
定(固定试管,先下后上、先左后右)
点(酒精灯加热药品)
收(气泡连续、均匀冒出时开始收集)
移(导管出水槽)
熄(灭酒精灯)
谐音:
茶
庄
定
点
收
利
息
加热高锰酸钾制取氧气
实验室制取氧气的步骤
新课讲解
发生装置
收集装置
分解双氧水制取氧气
装置图
新课讲解
固液常温型
发生装置
发生装置选择的依据:
反应物状态:
反应条件:
固态和液态
不需加热
分解双氧水制取氧气
新课讲解
收集装置选择的依据:
不易溶于水且不与水反应的气体
密度比空气大的气体且不与空气中气体反应
密度比空气小的气体且不与空气中气体反应
√
√
排水集气法
向上排空气法
向下排空气法
要考虑气体的
溶解性
是否与水反应
气体密度
与空气成分是否反应
(制得的氧气较纯)
(制得干燥的氧气)
收集装置
分解双氧水制取氧气
新课讲解
过氧化氢
二氧化锰
水 + 氧气
H2O2 H2O + O2
在化学反应中能增大化学反应速率,但本身的质量和化学性质在反应前后都没有发生变化的物质称为催化剂(又叫触媒)。
催化剂及其作用
新课讲解
(1)改变的只是化学反应速率,效果可加快或减慢。
(2)本身的化学性质在反应前后保持不变,但物理性质有可能改变。
(3)催化剂要针对某个具体反应而言。如不能单独说二氧化锰是催化剂;二氧化锰在氯酸钾分解实验中是催化剂,但不是所有化学反应的催化剂。
注意:
催化剂及其作用
谢谢聆听
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
