2022年秋人教版九年级化学上册 3.2.2 离子 相对原子质量 同步练习(有解析)
文档属性
| 名称 | 2022年秋人教版九年级化学上册 3.2.2 离子 相对原子质量 同步练习(有解析) |

|
|
| 格式 | doc | ||
| 文件大小 | 118.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-09-20 00:00:00 | ||
图片预览



文档简介
3.2.2 离子 相对原子质量
一、单选题
1.下列结构示意图中表示阴离子的是
A. B. C. D.
2.某粒子最外层有8个电子,下列对该粒子的判断中正确的是
A.一定是阳离子 B.一定是阴离子
C.一定是稀有气体原子 D.无法确定
3.以下是四种微粒的结构示意图,下列有关各微粒的说法中,错误的是
A.①的化学性质比较稳定 B.③④属于同种元素
C.④是一种阴离子 D.②容易得到电子
4.下列结构示意图表示原子的是
A. B. C. D.
5.某原子的原子核内有161个中子,其相对原子质量为272,则下列说法错误的是
A.该原子的质子数是111
B.该原子的核电荷数为161
C.该原子的核外电子数是111
D.该原子的质量是一个碳12原子质量的倍
6.相对原子质量的说法有:①相对原子质量是一个原子的质量;②相对原子质量是一个原子质量的1/12;③相对原子质量是原子的相对质量,是一个比值;④相对原子质量的近似值为中子数和质子数之和;⑤相对原子质量是以碳的相对原子质量为标准的比值;⑥一般化学计算时采用相对原子质量的近似值。其中正确的是
A.③④⑤ B.③④⑥ C.②③④ D.①③⑤
7.A原子与B原子的质量之比为a∶b,而B原子与作为相对原子质量标准的碳原子的质量之比为m∶n,则A原子的相对原子质量为
A. B. C. D.
8.如图为某粒子结构示意图,下列说法错误的是
A.该粒子属于阳离子 B.该粒子核外电子数为18
C.该粒子具有3个电子层 D.该粒子的化学符号是
9.下列物质由离子构成的是( )
A.水 B.汞 C.氢气 D.氯化钠
10.我国“高分5号”卫星天线是用钛镍形状记忆合金制成的。如图为镍的原子结构示意图,关于该原子的叙述错误的一项是( )
A.它的核电荷数为28
B.它有4个电子层
C.它的质子数大于核外电子数
D.它易失电子
11.如图为氧原子的结构示意图,从图中可获得的信息是
A.氧原子核内质子数为8、中子数为0,核外电子数为8
B.氧原子核外第一层上有6个电子
C.氧原子的原子核在整个原子中所占体积极小
D.氧原子在化学反应中容易得到2个电子
二、填空题
12.下图是A、B、C、D四种粒子的结构示意图,据图请回答下列问题。
A B C D
(1)以上四种粒子的结构示意图中,属于同种元素的粒子是_____(填字母代号)。
(2)以上四种粒子中,能得到电子的是___________(填字母代号)。
(3)D元素的名称是__________;D中x =__________。
13.某粒子(原子或离子)的结构示意图为,请回答下列问题:
⑴若m=11,则该粒子所对应元素的符号为_________;
⑵若该粒子带两个单位负电荷,且n=8,则该粒子的符号为__________;
⑶若m-n<10,则该粒子是一个________(选填“原子”、“阳离子”或“阴离子”)。
14.氟的原子结构示意图为,氟离子的符号为______。
15.如图是A、B、C、D、E五种粒子的结构示意图,据图回答下列问题:
(1)属于相对稳定结构的粒子有______(填字母)。
(2)在化学反应中,易得到电子的原子有______(填字母)。
16.根据下列粒子结构示意图,回答下列问题:
(1)D粒子在化学反应中容易______电子。
(2)若E中,则该粒子属于______。
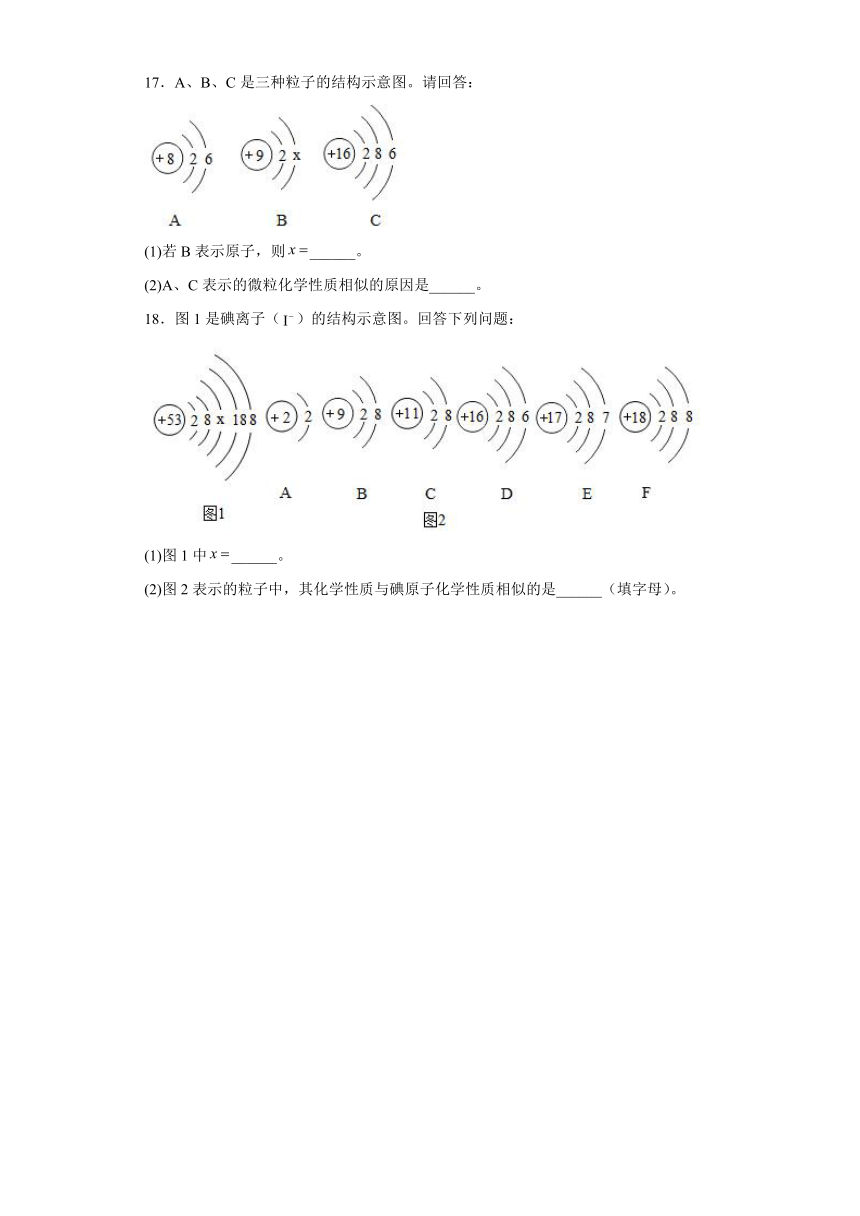
17.A、B、C是三种粒子的结构示意图。请回答:
(1)若B表示原子,则______。
(2)A、C表示的微粒化学性质相似的原因是______。
18.图1是碘离子()的结构示意图。回答下列问题:
(1)图1中______。
(2)图2表示的粒子中,其化学性质与碘原子化学性质相似的是______(填字母)。
参考答案:
1.D
【解析】
【详解】
A、质子数=核外电子数=11,为原子,故选项错误。
B、质子数=12,核外电子数=10,质子数>核外电子数,为阳离子,故选项错误。
C、质子数=核外电子数=10,为原子,故选项错误。
D、质子数=9,核外电子数=10,质子数<核外电子数,为阴离子,故选项正确。
故选D。
【点睛】
根据当质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子.
2.D
【解析】
【详解】
稀有气体原子和离子都是8电子的稳定结构,无法确定是稀有气体原子还是离子。
故选D。
考点:原子、离子的结构
3.C
【解析】
【详解】
A.①的最外层电子数为8,化学性质比较稳定,选项A正确;
B.元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质子数(即核电荷数),③④的质子数相同,属于同种元素,选项B正确;
C.④质子数=11,核外电子数=10,质子数>核外电子数,为阳离子,选项C错误;
D.②的最外层电子数是7,大于4,在化学反应中易得到1个电子而形成阴离子,选项D正确。故选C。
4.B
【解析】
【详解】
A、该粒子中,质子数=11,核外电子数=10,质子数>核外电子数,为阳离子,错误;
B、该粒子中,质子数=核外电子数=13,为原子,正确;
C、该粒子中,质子数=17,核外电子数=18,质子数<核外电子数,为阴离子,错误;
D、该粒子中,质子数=19,核外电子数=18,质子数>核外电子数,为阳离子,错误。
故选:B。
5.B
【解析】
【详解】
A、由它的相对原子质量为272,相对原子质量=质子数+中子数,该原子的质子数=272-161=111,故正确;
B、由质子数=核电荷数可知,核电荷数也为111,故错误;
C、由质子数=核电荷数=核外电子数,质子数为111,所以核外电子数为111,故正确;
D、碳的相对原子质量为12,相对原子质量之比等于实际质量之比,该元素的一个原子的质量是一个碳原子质量的倍,故正确。
点睛:
在原子中,核内质子数=核电荷数=核外电子数,相对原子质量=质子数+中子数。
6.B
【解析】
【详解】
国际上是以一种碳原子的质量的1/12作为标准,其他原子的质量跟它相比较所得到的比值,就是该原子的相对原子质量,不是一个原子的质量;不是一个原子质量的1/12;相对原子质量是以碳-12原子的原子质量的1/12 为标准的比值;
相对原子质量是原子的相对质量,是一个比值;原子的质量主要集中在原子核上,相对原子质量的近似值为中子数和质子数之和;原子的质量很小,一般化学计算时采用相对原子质量的近似值,故③④⑥说法正确。
7.A
【解析】
【详解】
B原子与作为相对原子质量标准的碳原子质量之比为m:n,则B原子的相对原子质量为 = ;
A原子与B原子的质量之比为a:b,它们的相对原子质量之比也为a:b,设A原子的相对原子质量为x,则x:=a:b ,x=。
8.A
【解析】
略
9.D
【解析】
【详解】
A、水是由非金属元素组成的化合物,是由水分子构成的,不符合题意,故选项错误;
B、汞属于金属单质,是由汞原子直接构成的,不符合题意,故选项错误;
C、氢气属于气态非金属单质,是由氢分子构成的,不符合题意,故选项错误;
D、氯化钠是含有金属元素和非金属元素的化合物,氯化钠是由钠离子和氯离子构成的,符合题意,故选项正确。
故选:D。
10.C
【解析】
【详解】
由原子结构示意图可判断:
A、它的核电荷数为28,故A说法正确;
B、该原子的电子层数为4,故B说法正确;
C、它的质子数等核外电子数,故C说法错误;
D、该原子的最外层电子数是2,小于4,它易失电子,故D说法正确。
故选C。
11.D
【解析】
【详解】
A、氧原子核内质子数为8、中子数为,质子数=核外电子数,核外电子数为8,故A不正确;
B、氧原子核外第一层上有2个电子,故B不正确;
C、原子是由原子核和核外电子构成的,原子核在原子中所占体积极小,则氧原子的原子核在整个原子中所占体积极小,但是原子结构示意图不能得到该信息,故C错误;
D、氧原子的最外层电子数为6,大于4,在化学反应中容易得到2个电子,故D正确。故选D。
故选D。
12. AB AC 氩元素 8
【解析】
【详解】
【详解】
(1)由元素的定义可知,A、B的质子数相同,属于同种元素的粒子;
(2)由四种粒子的结构示意图可知,在A、C结构中,最外层的电子数是7个,大于4个,在反应中能得到电子;
(3)由D粒子的结构示意图可知,核内的质子数是18,该元素的名称是氩元素;在原子中,由于核内的质子数等于核外的电子数,所以x的值是8.
13. Na S2- 阴离子
【解析】
【详解】
(1)若m=11,质子数为11的元素即为11号元素钠元素,符号为Na;
(2) 若该粒子带两个单位负电荷,且n=8,是核外有18个电子的带两个单位负电荷的阴离子,即16号元素的阴离子,离子符号为:S2- ;
(3)若m-n<10,即m<10+n,核外电子数大于质子数,为阴离子。
14.F-
【解析】
略
15.(1)BCD
(2)AE
【解析】
略
16.(1)得到一个
(2)氩原子
【解析】
略
17.(1)7
(2)原子的最外层电子数相同
【解析】
略
18.(1)18
(2)E
【解析】
略
一、单选题
1.下列结构示意图中表示阴离子的是
A. B. C. D.
2.某粒子最外层有8个电子,下列对该粒子的判断中正确的是
A.一定是阳离子 B.一定是阴离子
C.一定是稀有气体原子 D.无法确定
3.以下是四种微粒的结构示意图,下列有关各微粒的说法中,错误的是
A.①的化学性质比较稳定 B.③④属于同种元素
C.④是一种阴离子 D.②容易得到电子
4.下列结构示意图表示原子的是
A. B. C. D.
5.某原子的原子核内有161个中子,其相对原子质量为272,则下列说法错误的是
A.该原子的质子数是111
B.该原子的核电荷数为161
C.该原子的核外电子数是111
D.该原子的质量是一个碳12原子质量的倍
6.相对原子质量的说法有:①相对原子质量是一个原子的质量;②相对原子质量是一个原子质量的1/12;③相对原子质量是原子的相对质量,是一个比值;④相对原子质量的近似值为中子数和质子数之和;⑤相对原子质量是以碳的相对原子质量为标准的比值;⑥一般化学计算时采用相对原子质量的近似值。其中正确的是
A.③④⑤ B.③④⑥ C.②③④ D.①③⑤
7.A原子与B原子的质量之比为a∶b,而B原子与作为相对原子质量标准的碳原子的质量之比为m∶n,则A原子的相对原子质量为
A. B. C. D.
8.如图为某粒子结构示意图,下列说法错误的是
A.该粒子属于阳离子 B.该粒子核外电子数为18
C.该粒子具有3个电子层 D.该粒子的化学符号是
9.下列物质由离子构成的是( )
A.水 B.汞 C.氢气 D.氯化钠
10.我国“高分5号”卫星天线是用钛镍形状记忆合金制成的。如图为镍的原子结构示意图,关于该原子的叙述错误的一项是( )
A.它的核电荷数为28
B.它有4个电子层
C.它的质子数大于核外电子数
D.它易失电子
11.如图为氧原子的结构示意图,从图中可获得的信息是
A.氧原子核内质子数为8、中子数为0,核外电子数为8
B.氧原子核外第一层上有6个电子
C.氧原子的原子核在整个原子中所占体积极小
D.氧原子在化学反应中容易得到2个电子
二、填空题
12.下图是A、B、C、D四种粒子的结构示意图,据图请回答下列问题。
A B C D
(1)以上四种粒子的结构示意图中,属于同种元素的粒子是_____(填字母代号)。
(2)以上四种粒子中,能得到电子的是___________(填字母代号)。
(3)D元素的名称是__________;D中x =__________。
13.某粒子(原子或离子)的结构示意图为,请回答下列问题:
⑴若m=11,则该粒子所对应元素的符号为_________;
⑵若该粒子带两个单位负电荷,且n=8,则该粒子的符号为__________;
⑶若m-n<10,则该粒子是一个________(选填“原子”、“阳离子”或“阴离子”)。
14.氟的原子结构示意图为,氟离子的符号为______。
15.如图是A、B、C、D、E五种粒子的结构示意图,据图回答下列问题:
(1)属于相对稳定结构的粒子有______(填字母)。
(2)在化学反应中,易得到电子的原子有______(填字母)。
16.根据下列粒子结构示意图,回答下列问题:
(1)D粒子在化学反应中容易______电子。
(2)若E中,则该粒子属于______。
17.A、B、C是三种粒子的结构示意图。请回答:
(1)若B表示原子,则______。
(2)A、C表示的微粒化学性质相似的原因是______。
18.图1是碘离子()的结构示意图。回答下列问题:
(1)图1中______。
(2)图2表示的粒子中,其化学性质与碘原子化学性质相似的是______(填字母)。
参考答案:
1.D
【解析】
【详解】
A、质子数=核外电子数=11,为原子,故选项错误。
B、质子数=12,核外电子数=10,质子数>核外电子数,为阳离子,故选项错误。
C、质子数=核外电子数=10,为原子,故选项错误。
D、质子数=9,核外电子数=10,质子数<核外电子数,为阴离子,故选项正确。
故选D。
【点睛】
根据当质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子.
2.D
【解析】
【详解】
稀有气体原子和离子都是8电子的稳定结构,无法确定是稀有气体原子还是离子。
故选D。
考点:原子、离子的结构
3.C
【解析】
【详解】
A.①的最外层电子数为8,化学性质比较稳定,选项A正确;
B.元素是质子数(即核电荷数)相同的一类原子的总称,决定元素种类的是质子数(即核电荷数),③④的质子数相同,属于同种元素,选项B正确;
C.④质子数=11,核外电子数=10,质子数>核外电子数,为阳离子,选项C错误;
D.②的最外层电子数是7,大于4,在化学反应中易得到1个电子而形成阴离子,选项D正确。故选C。
4.B
【解析】
【详解】
A、该粒子中,质子数=11,核外电子数=10,质子数>核外电子数,为阳离子,错误;
B、该粒子中,质子数=核外电子数=13,为原子,正确;
C、该粒子中,质子数=17,核外电子数=18,质子数<核外电子数,为阴离子,错误;
D、该粒子中,质子数=19,核外电子数=18,质子数>核外电子数,为阳离子,错误。
故选:B。
5.B
【解析】
【详解】
A、由它的相对原子质量为272,相对原子质量=质子数+中子数,该原子的质子数=272-161=111,故正确;
B、由质子数=核电荷数可知,核电荷数也为111,故错误;
C、由质子数=核电荷数=核外电子数,质子数为111,所以核外电子数为111,故正确;
D、碳的相对原子质量为12,相对原子质量之比等于实际质量之比,该元素的一个原子的质量是一个碳原子质量的倍,故正确。
点睛:
在原子中,核内质子数=核电荷数=核外电子数,相对原子质量=质子数+中子数。
6.B
【解析】
【详解】
国际上是以一种碳原子的质量的1/12作为标准,其他原子的质量跟它相比较所得到的比值,就是该原子的相对原子质量,不是一个原子的质量;不是一个原子质量的1/12;相对原子质量是以碳-12原子的原子质量的1/12 为标准的比值;
相对原子质量是原子的相对质量,是一个比值;原子的质量主要集中在原子核上,相对原子质量的近似值为中子数和质子数之和;原子的质量很小,一般化学计算时采用相对原子质量的近似值,故③④⑥说法正确。
7.A
【解析】
【详解】
B原子与作为相对原子质量标准的碳原子质量之比为m:n,则B原子的相对原子质量为 = ;
A原子与B原子的质量之比为a:b,它们的相对原子质量之比也为a:b,设A原子的相对原子质量为x,则x:=a:b ,x=。
8.A
【解析】
略
9.D
【解析】
【详解】
A、水是由非金属元素组成的化合物,是由水分子构成的,不符合题意,故选项错误;
B、汞属于金属单质,是由汞原子直接构成的,不符合题意,故选项错误;
C、氢气属于气态非金属单质,是由氢分子构成的,不符合题意,故选项错误;
D、氯化钠是含有金属元素和非金属元素的化合物,氯化钠是由钠离子和氯离子构成的,符合题意,故选项正确。
故选:D。
10.C
【解析】
【详解】
由原子结构示意图可判断:
A、它的核电荷数为28,故A说法正确;
B、该原子的电子层数为4,故B说法正确;
C、它的质子数等核外电子数,故C说法错误;
D、该原子的最外层电子数是2,小于4,它易失电子,故D说法正确。
故选C。
11.D
【解析】
【详解】
A、氧原子核内质子数为8、中子数为,质子数=核外电子数,核外电子数为8,故A不正确;
B、氧原子核外第一层上有2个电子,故B不正确;
C、原子是由原子核和核外电子构成的,原子核在原子中所占体积极小,则氧原子的原子核在整个原子中所占体积极小,但是原子结构示意图不能得到该信息,故C错误;
D、氧原子的最外层电子数为6,大于4,在化学反应中容易得到2个电子,故D正确。故选D。
故选D。
12. AB AC 氩元素 8
【解析】
【详解】
【详解】
(1)由元素的定义可知,A、B的质子数相同,属于同种元素的粒子;
(2)由四种粒子的结构示意图可知,在A、C结构中,最外层的电子数是7个,大于4个,在反应中能得到电子;
(3)由D粒子的结构示意图可知,核内的质子数是18,该元素的名称是氩元素;在原子中,由于核内的质子数等于核外的电子数,所以x的值是8.
13. Na S2- 阴离子
【解析】
【详解】
(1)若m=11,质子数为11的元素即为11号元素钠元素,符号为Na;
(2) 若该粒子带两个单位负电荷,且n=8,是核外有18个电子的带两个单位负电荷的阴离子,即16号元素的阴离子,离子符号为:S2- ;
(3)若m-n<10,即m<10+n,核外电子数大于质子数,为阴离子。
14.F-
【解析】
略
15.(1)BCD
(2)AE
【解析】
略
16.(1)得到一个
(2)氩原子
【解析】
略
17.(1)7
(2)原子的最外层电子数相同
【解析】
略
18.(1)18
(2)E
【解析】
略
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
