第八单元 金属和金属材料 综合素质评价 人教版九年级化学 (有答案)
文档属性
| 名称 | 第八单元 金属和金属材料 综合素质评价 人教版九年级化学 (有答案) |

|
|
| 格式 | doc | ||
| 文件大小 | 240.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-09-20 00:00:00 | ||
图片预览



文档简介
第八单元综合素质评价
九年级化学下册 (R版)
时间:60分钟 满分:50分
可能用到的相对原子质量:H:1 O:16 Mg:24 Al:27 Cl:35. 5
Fe:56 Cu:64 Zn:65 Ag:108
一、选择题(本题包括12小题,1~10小题每题1分,11~12小题每题2分,共14分)
1. 铁是目前人类使用最广泛的金属。下列过程中没有发生化学变化的是( )
A. 铁丝织网 B. 矿石炼铁
C. 钢铁生锈 D. 湿法炼铜
2. 日常生活中,用得较多的材料是金属材料。下列不属于金属材料的是( )
A. 氧化铜 B. 铁钉 C. 黄铜 D. 金戒指
3. 下列金属能与硝酸银溶液反应,但不能与稀硫酸反应的是( )
A. Cu B. Zn C. Mg D. Fe
4. 下列有关金属及合金的说法错误的是( )
A. 金属在常温下大多数都是固体
B. 铝合金的硬度比铝的硬度小
C. 铁制品在潮湿的空气中易生锈
D. 钢铁是目前使用最多的金属材料
5. 甲、乙、丙、丁四种金属,只有丙在自然界中主要以单质形式存在,用甲制的容器不能盛放丁的化合物溶液,用乙制的容器却可以盛放丁的化合物溶液。由此推断四种金属的活动性由强到弱的顺序是( )
A. 丙>乙>甲>丁 B. 甲>丁>乙>丙
C. 丁>甲>乙>丙 D. 甲>乙>丁>丙
6. 取一段镁条放入盛有少量稀盐酸的试管中,用手摸试管外壁,会感觉发烫,反应的化学方程式为Mg+2HCl===MgCl2+H2↑。下列有关说法正确的是( )
A. 反应中无明显现象 B. 反应是一个吸热反应
C. 反应后溶液质量减少 D. 反应说明镁能置换出酸中的氢
7. 铁、铝、铜都具有的性质是( )
①有银白色的光泽 ②良好的导热性 ③能与稀硫酸反应
④能与氧气反应 ⑤能与硝酸银溶液反应
A. ②④⑤ B. ①③ C. ①②④ D. ①②③④⑤
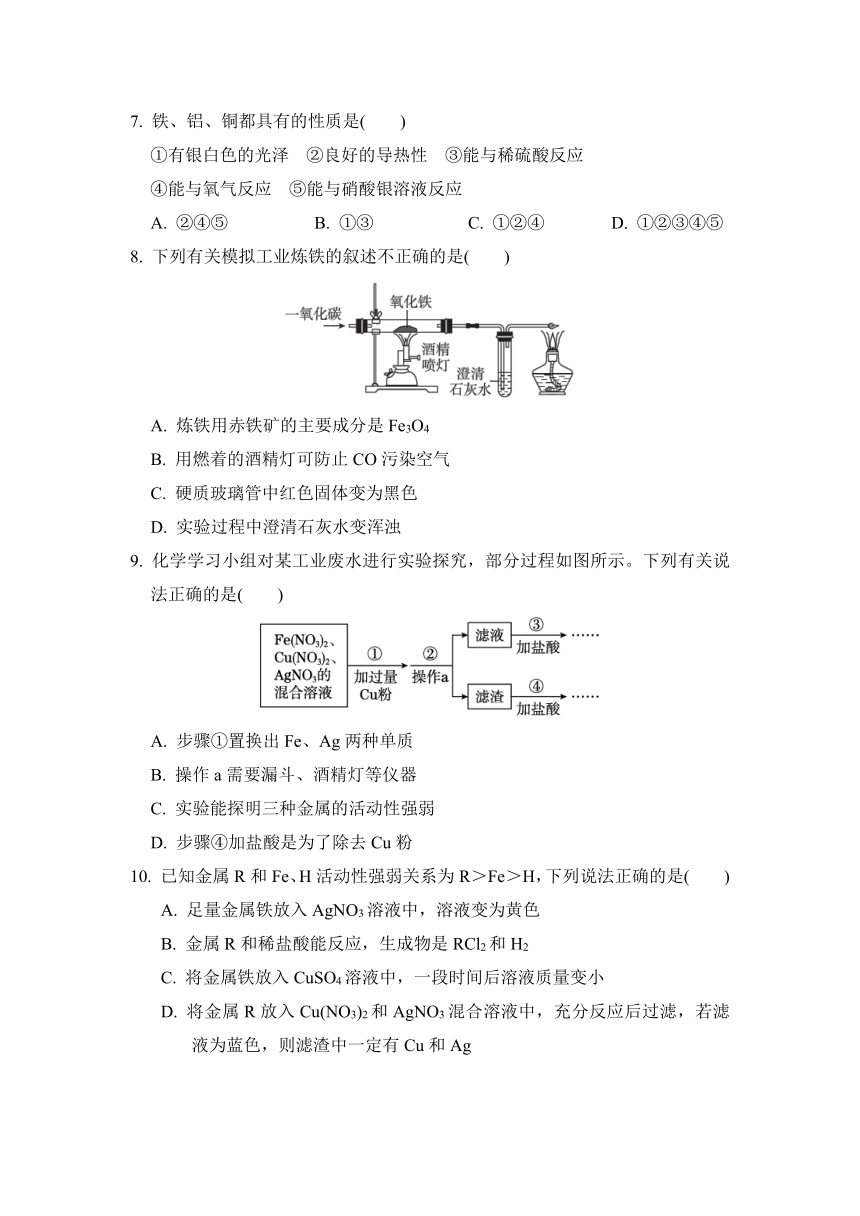
8. 下列有关模拟工业炼铁的叙述不正确的是( )
A. 炼铁用赤铁矿的主要成分是Fe3O4
B. 用燃着的酒精灯可防止CO污染空气
C. 硬质玻璃管中红色固体变为黑色
D. 实验过程中澄清石灰水变浑浊
9. 化学学习小组对某工业废水进行实验探究,部分过程如图所示。下列有关说法正确的是( )
INCLUDEPICTURE"WJ21.tif" INCLUDEPICTURE "F:\\英语\\23春\\化学\\人教\\文件\\word\\WJ21.tif" \* MERGEFORMATINET
A. 步骤①置换出Fe、Ag两种单质
B. 操作a需要漏斗、酒精灯等仪器
C. 实验能探明三种金属的活动性强弱
D. 步骤④加盐酸是为了除去Cu粉
10. 已知金属R和Fe、H活动性强弱关系为R>Fe>H,下列说法正确的是( )
A. 足量金属铁放入AgNO3溶液中,溶液变为黄色
B. 金属R和稀盐酸能反应,生成物是RCl2和H2
C. 将金属铁放入CuSO4溶液中,一段时间后溶液质量变小
D. 将金属R放入Cu(NO3)2和AgNO3混合溶液中,充分反应后过滤,若滤液为蓝色,则滤渣中一定有Cu和Ag
11. 【双选】把200 g一定溶质质量分数的稀盐酸平均分成两份,分别加入两个相同的烧杯中,放在已调平的天平左右两盘上,此时天平平衡,然后在左盘烧杯中加入5. 6 g铁粉。下列有关说法正确的是( )
A. 若在右盘烧杯中加入5. 6 g锌粉,反应停止后,天平可能平衡
B. 若在右盘烧杯中加入5. 6 g黄铜粉,反应停止后,天平不可能平衡
C. 在右盘烧杯中加入5. 6 g镁粉,反应停止后,若天平平衡,则100 g稀盐酸中所含HCl的质量不大于7. 3 g
D. 在右盘烧杯中加入5. 6 g铝粉,反应停止后,若天平不平衡,则左、右两盘烧杯中金属一定都无剩余
12. 向一定质量的Cu(NO3)2和AgNO3的混合溶液中逐渐加入锌粉。反应过程中Cu(NO3)2的质量随加入锌粉质量的变化关系如图所示。下列说法错误的是( )
INCLUDEPICTURE"WJ22.tif" INCLUDEPICTURE "F:\\英语\\23春\\化学\\人教\\文件\\word\\WJ22.tif" \* MERGEFORMATINET
A. a点时,溶液的总质量比反应前小
B. b点时,溶液为Zn(NO3)2和Cu(NO3)2的混合溶液
C. c点时,溶液呈无色
D. d点时,过滤所得滤渣为Cu和Ag的混合物
二、填空题(本题包括4小题,共19分)
13. (5分)我国第三艘国产航母“福建舰”已经下水,制造航母使用了大量的金属材料。
(1)金属材料包括纯金属以及它们的________。
(2)航母的航电系统使用铜作导线,利用了铜的延展性和________性。
(3)制造航母使用锰钢而不用纯铁,是因为锰钢比纯铁_________________。
(4)航母外壳用涂料覆盖是为了防止其与______________接触而锈蚀。
(5)为了探究航母材料中锌、铁、铜三种金属的活动性顺序,除Fe和ZnSO4溶液外,还需选用的试剂是______________。
14. (5分)人类文明进步与材料发展关系十分密切。
(1)铁锅用于炒菜,主要利用铁具有________的性质。
(2)铝合金被广泛用于航天工业。铝合金的硬度比纯铝的硬度________。
(3)一种新型材料氮化铝(AlN)应用于新能源汽车。工业上用氧化铝、焦炭和氮气在高温条件下制得氮化铝,并生成一氧化碳,该反应的化学方程式是__________________________________________________。
(4)世界最大跨径拱桥——广西天峨龙滩特大桥在建造过程中使用了大量钢材。在钢材表面刷漆可防锈,其原因是;建造过程中产生的废钢材可回收利用,其意义是__________________(写一条即可)。
15. (5分)金属及金属材料在生产、生活中应用广泛。
(1)铝具有很好的抗腐蚀性,是因为其表面生成一层致密的薄膜,该薄膜是_______________(填化学式)。
(2)向一定质量的氧化铜中加入一定量稀硫酸使其完全溶解,得到蓝色溶液。再加入铁粉充分反应,过滤,得到滤渣和滤液。向滤渣中加入稀硫酸,有气泡冒出,则滤液中除水外,所含化合物是________(填化学式)。
(3)生铁和钢都是铁的合金,性能不同是因为____________。现将某铁合金(只含铁和碳)8. 7 g放入盛有100 g稀盐酸的烧杯中,恰好完全反应,得到108. 1 g溶液,则该样品中碳的质量分数为________(结果精确到0. 1%)。该铁合金属于________(填“钢”或“生铁”)。
16. (4分)A~F是初中化学常见的物质,它们之间的相互转化关系如图所示(部分产物已略去)。已知A是一种黑色的氧化物,B、C、D均为单质,B是目前世界上年产量最高的金属,C是密度最小的气体,F的水溶液在农业上常用来配制波尔多液。
INCLUDEPICTURE"WJ23.tif" INCLUDEPICTURE "F:\\英语\\23春\\化学\\人教\\文件\\word\\WJ23.tif" \* MERGEFORMATINET
(1)A物质的化学式为________,E溶液中一定存在的阳离子为________(填离子符号)。
(2)列举D物质的一种用途________。
(3)写出反应③的化学方程式________________________,其基本反应类型为____________。
三、实验探究题(本题包括2小题,共13分)
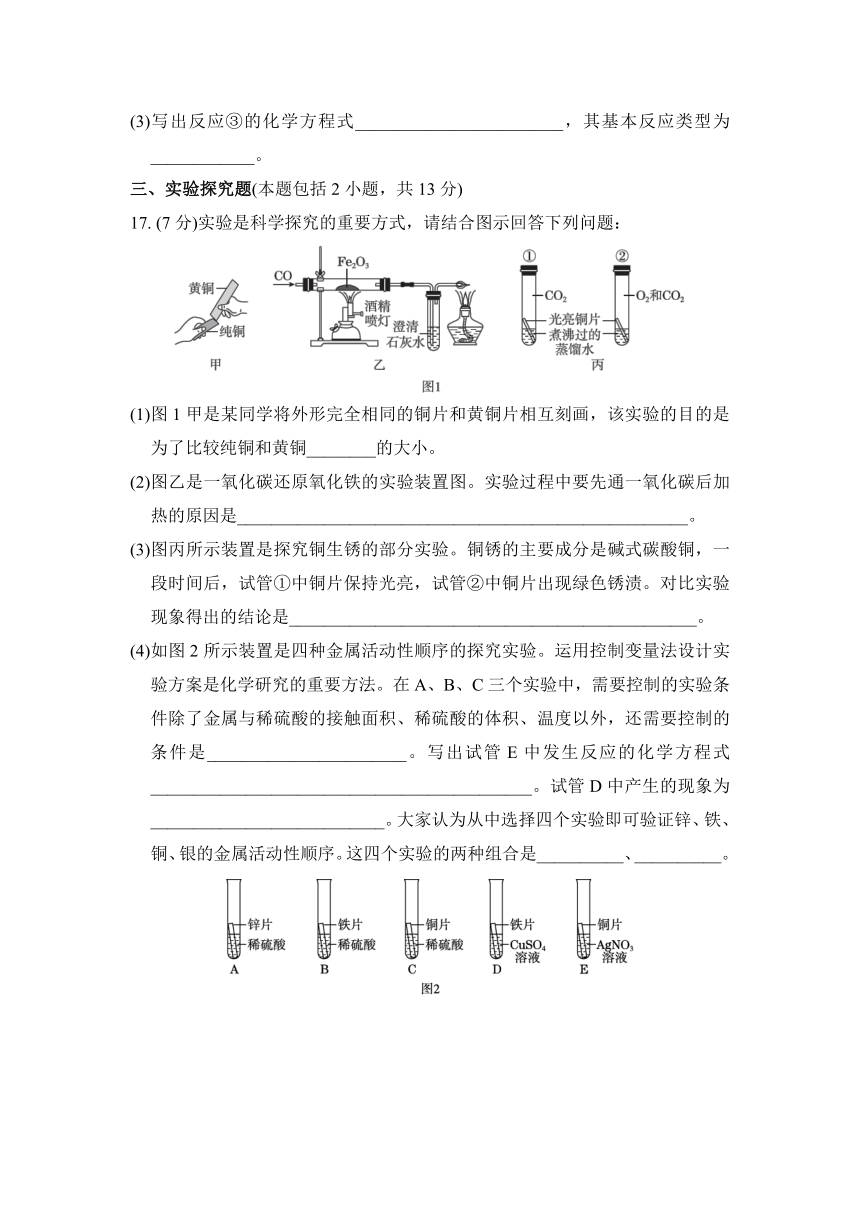
17. (7分)实验是科学探究的重要方式,请结合图示回答下列问题:
(1)图1甲是某同学将外形完全相同的铜片和黄铜片相互刻画,该实验的目的是为了比较纯铜和黄铜________的大小。
(2)图乙是一氧化碳还原氧化铁的实验装置图。实验过程中要先通一氧化碳后加热的原因是____________________________________________________。
(3)图丙所示装置是探究铜生锈的部分实验。铜锈的主要成分是碱式碳酸铜,一段时间后,试管①中铜片保持光亮,试管②中铜片出现绿色锈渍。对比实验现象得出的结论是_______________________________________________。
(4)如图2所示装置是四种金属活动性顺序的探究实验。运用控制变量法设计实验方案是化学研究的重要方法。在A、B、C三个实验中,需要控制的实验条件除了金属与稀硫酸的接触面积、稀硫酸的体积、温度以外,还需要控制的条件是_______________________。写出试管E中发生反应的化学方程式____________________________________________。试管D中产生的现象为___________________________。大家认为从中选择四个实验即可验证锌、铁、铜、银的金属活动性顺序。这四个实验的两种组合是__________、__________。
INCLUDEPICTURE"WJ25.tif" INCLUDEPICTURE "F:\\英语\\23春\\化学\\人教\\文件\\word\\WJ25.tif" \* MERGEFORMATINET
18. (6分)已知某金属材料中含有镁、锌、铁、铜中的两种。小明在老师的指导下对该金属材料的成分进行探究。
INCLUDEPICTURE"WJ26.tif" INCLUDEPICTURE "F:\\英语\\23春\\化学\\人教\\文件\\word\\WJ26.tif" \* MERGEFORMATINET
【查阅资料】金属与盐酸反应的比较,如图1所示。得出这四种金属的活动性由强到弱的顺序是__________________________________________。
【进行实验】实验一:
实验步骤 实验现象 实验结论
取少量金属材料样品于试管中,加入过量的稀硫酸,观察现象 固体全部溶解,_________________ 金属材料中一定有铁,一定没有______________
实验完成后,将废液倒入废液缸中 / /
实验二:步骤1:另取金属材料,用砂纸打磨,称量其质量为20 g;
步骤2:将打磨过的金属材料浸入过量的硫酸锌溶液中,过一会儿取出,洗净,在一定条件下烘干,称量其质量大于20 g;
步骤3:实验完成后,将废液倒入废液缸中。
INCLUDEPICTURE"WJ27.tif" INCLUDEPICTURE "F:\\英语\\23春\\化学\\人教\\文件\\word\\WJ27.tif" \* MERGEFORMATINET
【得出结论】该金属材料中除铁外,还含有________。
【实验反思】步骤2中,“一定条件”指的是。
【拓展提升】小红想对废液缸中的废液进行回收利用。请你帮她分析废液成分,废液中除水外,所含物质是________________________(填化学式)。
四、计算题(本题包括1小题,共4分)
19. (4分)赤铁矿的主要成分是Fe2O3,可用于冶炼铁。某地出产一种赤铁矿,其中Fe2O3的质量分数为64%,试计算:
(1)Fe2O3中铁元素的质量分数为________。
(2)用100 t该赤铁矿经过充分冶炼,最多可以生产出含铁96%的生铁多少吨?(计算结果保留两位小数)
答案
一、1. A 2. A 3. A 4. B 5. B
6. D 点拨:取一段镁条放入盛有少量稀盐酸的试管中,反应的化学方程式为Mg+2HCl===MgCl2+H2↑,有气泡产生,故A选项说法错误;用手摸试管外壁,会感觉发烫,说明放出了热量,故B选项说法错误;由反应的化学方程式知,每24份质量的镁可置换出2份质量的氢气,反应后溶液的质量会增加,故C选项说法错误;反应说明镁能置换出酸中的氢,故D选项说法正确。
7. A
8. A 点拨:赤铁矿的主要成分是Fe2O3,故A选项错误;一氧化碳有毒,直接排放到空气中会污染环境,故B选项正确;一氧化碳具有还原性,能与氧化铁反应生成铁和二氧化碳,硬质玻璃管中红色固体变为黑色,故C选项正确;一氧化碳与氧化铁反应有二氧化碳生成,二氧化碳能使澄清石灰水变浑浊,故D选项正确。
9. C 点拨:铜的金属活动性比银强,比铁弱,铜粉能与硝酸银溶液反应生成硝酸铜溶液和银,不能与硝酸亚铁溶液反应,步骤①不能置换出Fe单质,故A选项说法错误;操作a能将滤液和滤渣分离,是过滤操作,需要漏斗、烧杯、玻璃棒、铁架台等仪器,无需使用酒精灯,故B选项说法错误;由实验知,过量的铜粉能与硝酸银溶液反应生成硝酸铜溶液和银,不能与硝酸亚铁溶液反应,说明金属活动性铁>铜>银,实验能探明三种金属的活动性强弱,故C选项说法正确;铜不能与稀盐酸反应,步骤④加盐酸不是为了除去Cu粉,是为了验证是否含有铁,故D选项说法错误。
10. C 点拨:铁与硝酸银溶液反应生成硝酸亚铁溶液和银,足量金属铁放入AgNO3溶液中,溶液变为浅绿色,故A选项错误;金属R和稀盐酸反应,生成物不一定是RCl2,故B选项错误;铁与硫酸铜反应生成硫酸亚铁和铜,反应的化学方程式为Fe+CuSO4===FeSO4+Cu,每56份质量的铁可置换出64份质量的铜,溶液的质量会减少,故C选项正确;将金属R放入Cu(NO3)2和AgNO3混合溶液中,充分反应后过滤,若滤液为蓝色,则滤液中含有硝酸铜,滤渣中一定有Ag,可能有Cu,故D选项错误。
11. A、C 点拨:若在右盘烧杯中加入5. 6 g锌粉,如果金属过量,酸不足,酸完全反应,生成氢气的质量相等,则反应停止后,天平平衡,A选项符合题意;若在右盘烧杯中加入5. 6 g黄铜粉,黄铜粉是铜锌合金,如果金属过量,酸不足,酸完全反应,生成氢气的质量相等,则反应停止后,天平平衡,B选项不符合题意;在右盘烧杯中加入5. 6 g镁粉,反应停止后,若天平平衡,说明生成氢气的质量相等,镁和稀盐酸反应:Mg+2HCl===MgCl2+H2↑;铁和稀盐酸反应:Fe+2HCl===FeCl2+H2↑;镁的相对原子质量比铁小,生成相同质量的氢气,消耗铁的质量大,当铁恰好与稀盐酸完全反应时,盐酸的溶质质量分数最大,故反应停止后,若天平平衡,则稀盐酸的溶质质量分数不大于7. 3%,C选项符合题意;在右盘烧杯中加入5. 6 g铝粉,反应停止后,若天平不平衡,说明生成氢气的质量不相等,则两种金属可能完全反应,也可能铁完全反应,铝过量,D选项不符合题意。
12. C 点拨:a点时,发生锌与硝酸银的反应,由Zn+2AgNO3===Zn(NO3)2+2Ag可知,每65份质量的锌可置换出216份质量的银,溶液的总质量比反应前小,故A选项说法正确;b点时,硝酸银恰好完全反应,溶液为Zn(NO3)2和Cu(NO3)2的混合溶液,故B选项说法正确;c点时,硝酸铜有剩余,溶液显蓝色,故C选项说法错误;d点时,锌与硝酸铜溶液恰好完全反应,过滤所得滤渣为Cu和Ag的混合物,故D选项说法正确。
二、13. (1)合金 (2)导电 (3)硬度大 (4)水和氧气
(5)硫酸铜溶液(合理即可)
14. (1)导热 (2)大
(3)Al2O3+3C+N22AlN+3CO
(4)漆能隔绝氧气和水;节约金属资源(合理即可)
15. (1)Al2O3 (2)FeSO4 (3)含碳量不同;3. 4%;生铁
16. (1)Fe3O4;H+ (2)制导线(合理即可)
(3)Fe+CuSO4===FeSO4+Cu;置换反应
三、17. (1)硬度
(2)排尽装置内的空气,避免一氧化碳与空气混合加热发生爆炸
(3)铜生锈需要氧气
(4)稀硫酸的浓度;Cu+2AgNO3===2Ag+Cu(NO3)2;铁片表面覆盖一层红色固体,溶液由蓝色逐渐变为浅绿色;A、B、C、E;A、B、D、E
18. 【查阅资料】Mg>Zn>Fe>Cu
【进行实验】溶液变成浅绿色;铜
【得出结论】镁
【实验反思】在氮气或氦气气氛中(合理即可)
【拓展提升】一定有FeSO4、MgSO4、ZnSO4,可能有H2SO4
四、19. 解:(1)70%
(2)设最多可以炼出含铁96%的生铁质量为x。
3CO + Fe2O3===== 2Fe + 3CO2
160 112
100 t×64% x×96%
=
x≈46. 67 t
答:最多可以炼出含铁96%的生铁46. 67 t。
高温
九年级化学下册 (R版)
时间:60分钟 满分:50分
可能用到的相对原子质量:H:1 O:16 Mg:24 Al:27 Cl:35. 5
Fe:56 Cu:64 Zn:65 Ag:108
一、选择题(本题包括12小题,1~10小题每题1分,11~12小题每题2分,共14分)
1. 铁是目前人类使用最广泛的金属。下列过程中没有发生化学变化的是( )
A. 铁丝织网 B. 矿石炼铁
C. 钢铁生锈 D. 湿法炼铜
2. 日常生活中,用得较多的材料是金属材料。下列不属于金属材料的是( )
A. 氧化铜 B. 铁钉 C. 黄铜 D. 金戒指
3. 下列金属能与硝酸银溶液反应,但不能与稀硫酸反应的是( )
A. Cu B. Zn C. Mg D. Fe
4. 下列有关金属及合金的说法错误的是( )
A. 金属在常温下大多数都是固体
B. 铝合金的硬度比铝的硬度小
C. 铁制品在潮湿的空气中易生锈
D. 钢铁是目前使用最多的金属材料
5. 甲、乙、丙、丁四种金属,只有丙在自然界中主要以单质形式存在,用甲制的容器不能盛放丁的化合物溶液,用乙制的容器却可以盛放丁的化合物溶液。由此推断四种金属的活动性由强到弱的顺序是( )
A. 丙>乙>甲>丁 B. 甲>丁>乙>丙
C. 丁>甲>乙>丙 D. 甲>乙>丁>丙
6. 取一段镁条放入盛有少量稀盐酸的试管中,用手摸试管外壁,会感觉发烫,反应的化学方程式为Mg+2HCl===MgCl2+H2↑。下列有关说法正确的是( )
A. 反应中无明显现象 B. 反应是一个吸热反应
C. 反应后溶液质量减少 D. 反应说明镁能置换出酸中的氢
7. 铁、铝、铜都具有的性质是( )
①有银白色的光泽 ②良好的导热性 ③能与稀硫酸反应
④能与氧气反应 ⑤能与硝酸银溶液反应
A. ②④⑤ B. ①③ C. ①②④ D. ①②③④⑤
8. 下列有关模拟工业炼铁的叙述不正确的是( )
A. 炼铁用赤铁矿的主要成分是Fe3O4
B. 用燃着的酒精灯可防止CO污染空气
C. 硬质玻璃管中红色固体变为黑色
D. 实验过程中澄清石灰水变浑浊
9. 化学学习小组对某工业废水进行实验探究,部分过程如图所示。下列有关说法正确的是( )
INCLUDEPICTURE"WJ21.tif" INCLUDEPICTURE "F:\\英语\\23春\\化学\\人教\\文件\\word\\WJ21.tif" \* MERGEFORMATINET
A. 步骤①置换出Fe、Ag两种单质
B. 操作a需要漏斗、酒精灯等仪器
C. 实验能探明三种金属的活动性强弱
D. 步骤④加盐酸是为了除去Cu粉
10. 已知金属R和Fe、H活动性强弱关系为R>Fe>H,下列说法正确的是( )
A. 足量金属铁放入AgNO3溶液中,溶液变为黄色
B. 金属R和稀盐酸能反应,生成物是RCl2和H2
C. 将金属铁放入CuSO4溶液中,一段时间后溶液质量变小
D. 将金属R放入Cu(NO3)2和AgNO3混合溶液中,充分反应后过滤,若滤液为蓝色,则滤渣中一定有Cu和Ag
11. 【双选】把200 g一定溶质质量分数的稀盐酸平均分成两份,分别加入两个相同的烧杯中,放在已调平的天平左右两盘上,此时天平平衡,然后在左盘烧杯中加入5. 6 g铁粉。下列有关说法正确的是( )
A. 若在右盘烧杯中加入5. 6 g锌粉,反应停止后,天平可能平衡
B. 若在右盘烧杯中加入5. 6 g黄铜粉,反应停止后,天平不可能平衡
C. 在右盘烧杯中加入5. 6 g镁粉,反应停止后,若天平平衡,则100 g稀盐酸中所含HCl的质量不大于7. 3 g
D. 在右盘烧杯中加入5. 6 g铝粉,反应停止后,若天平不平衡,则左、右两盘烧杯中金属一定都无剩余
12. 向一定质量的Cu(NO3)2和AgNO3的混合溶液中逐渐加入锌粉。反应过程中Cu(NO3)2的质量随加入锌粉质量的变化关系如图所示。下列说法错误的是( )
INCLUDEPICTURE"WJ22.tif" INCLUDEPICTURE "F:\\英语\\23春\\化学\\人教\\文件\\word\\WJ22.tif" \* MERGEFORMATINET
A. a点时,溶液的总质量比反应前小
B. b点时,溶液为Zn(NO3)2和Cu(NO3)2的混合溶液
C. c点时,溶液呈无色
D. d点时,过滤所得滤渣为Cu和Ag的混合物
二、填空题(本题包括4小题,共19分)
13. (5分)我国第三艘国产航母“福建舰”已经下水,制造航母使用了大量的金属材料。
(1)金属材料包括纯金属以及它们的________。
(2)航母的航电系统使用铜作导线,利用了铜的延展性和________性。
(3)制造航母使用锰钢而不用纯铁,是因为锰钢比纯铁_________________。
(4)航母外壳用涂料覆盖是为了防止其与______________接触而锈蚀。
(5)为了探究航母材料中锌、铁、铜三种金属的活动性顺序,除Fe和ZnSO4溶液外,还需选用的试剂是______________。
14. (5分)人类文明进步与材料发展关系十分密切。
(1)铁锅用于炒菜,主要利用铁具有________的性质。
(2)铝合金被广泛用于航天工业。铝合金的硬度比纯铝的硬度________。
(3)一种新型材料氮化铝(AlN)应用于新能源汽车。工业上用氧化铝、焦炭和氮气在高温条件下制得氮化铝,并生成一氧化碳,该反应的化学方程式是__________________________________________________。
(4)世界最大跨径拱桥——广西天峨龙滩特大桥在建造过程中使用了大量钢材。在钢材表面刷漆可防锈,其原因是;建造过程中产生的废钢材可回收利用,其意义是__________________(写一条即可)。
15. (5分)金属及金属材料在生产、生活中应用广泛。
(1)铝具有很好的抗腐蚀性,是因为其表面生成一层致密的薄膜,该薄膜是_______________(填化学式)。
(2)向一定质量的氧化铜中加入一定量稀硫酸使其完全溶解,得到蓝色溶液。再加入铁粉充分反应,过滤,得到滤渣和滤液。向滤渣中加入稀硫酸,有气泡冒出,则滤液中除水外,所含化合物是________(填化学式)。
(3)生铁和钢都是铁的合金,性能不同是因为____________。现将某铁合金(只含铁和碳)8. 7 g放入盛有100 g稀盐酸的烧杯中,恰好完全反应,得到108. 1 g溶液,则该样品中碳的质量分数为________(结果精确到0. 1%)。该铁合金属于________(填“钢”或“生铁”)。
16. (4分)A~F是初中化学常见的物质,它们之间的相互转化关系如图所示(部分产物已略去)。已知A是一种黑色的氧化物,B、C、D均为单质,B是目前世界上年产量最高的金属,C是密度最小的气体,F的水溶液在农业上常用来配制波尔多液。
INCLUDEPICTURE"WJ23.tif" INCLUDEPICTURE "F:\\英语\\23春\\化学\\人教\\文件\\word\\WJ23.tif" \* MERGEFORMATINET
(1)A物质的化学式为________,E溶液中一定存在的阳离子为________(填离子符号)。
(2)列举D物质的一种用途________。
(3)写出反应③的化学方程式________________________,其基本反应类型为____________。
三、实验探究题(本题包括2小题,共13分)
17. (7分)实验是科学探究的重要方式,请结合图示回答下列问题:
(1)图1甲是某同学将外形完全相同的铜片和黄铜片相互刻画,该实验的目的是为了比较纯铜和黄铜________的大小。
(2)图乙是一氧化碳还原氧化铁的实验装置图。实验过程中要先通一氧化碳后加热的原因是____________________________________________________。
(3)图丙所示装置是探究铜生锈的部分实验。铜锈的主要成分是碱式碳酸铜,一段时间后,试管①中铜片保持光亮,试管②中铜片出现绿色锈渍。对比实验现象得出的结论是_______________________________________________。
(4)如图2所示装置是四种金属活动性顺序的探究实验。运用控制变量法设计实验方案是化学研究的重要方法。在A、B、C三个实验中,需要控制的实验条件除了金属与稀硫酸的接触面积、稀硫酸的体积、温度以外,还需要控制的条件是_______________________。写出试管E中发生反应的化学方程式____________________________________________。试管D中产生的现象为___________________________。大家认为从中选择四个实验即可验证锌、铁、铜、银的金属活动性顺序。这四个实验的两种组合是__________、__________。
INCLUDEPICTURE"WJ25.tif" INCLUDEPICTURE "F:\\英语\\23春\\化学\\人教\\文件\\word\\WJ25.tif" \* MERGEFORMATINET
18. (6分)已知某金属材料中含有镁、锌、铁、铜中的两种。小明在老师的指导下对该金属材料的成分进行探究。
INCLUDEPICTURE"WJ26.tif" INCLUDEPICTURE "F:\\英语\\23春\\化学\\人教\\文件\\word\\WJ26.tif" \* MERGEFORMATINET
【查阅资料】金属与盐酸反应的比较,如图1所示。得出这四种金属的活动性由强到弱的顺序是__________________________________________。
【进行实验】实验一:
实验步骤 实验现象 实验结论
取少量金属材料样品于试管中,加入过量的稀硫酸,观察现象 固体全部溶解,_________________ 金属材料中一定有铁,一定没有______________
实验完成后,将废液倒入废液缸中 / /
实验二:步骤1:另取金属材料,用砂纸打磨,称量其质量为20 g;
步骤2:将打磨过的金属材料浸入过量的硫酸锌溶液中,过一会儿取出,洗净,在一定条件下烘干,称量其质量大于20 g;
步骤3:实验完成后,将废液倒入废液缸中。
INCLUDEPICTURE"WJ27.tif" INCLUDEPICTURE "F:\\英语\\23春\\化学\\人教\\文件\\word\\WJ27.tif" \* MERGEFORMATINET
【得出结论】该金属材料中除铁外,还含有________。
【实验反思】步骤2中,“一定条件”指的是。
【拓展提升】小红想对废液缸中的废液进行回收利用。请你帮她分析废液成分,废液中除水外,所含物质是________________________(填化学式)。
四、计算题(本题包括1小题,共4分)
19. (4分)赤铁矿的主要成分是Fe2O3,可用于冶炼铁。某地出产一种赤铁矿,其中Fe2O3的质量分数为64%,试计算:
(1)Fe2O3中铁元素的质量分数为________。
(2)用100 t该赤铁矿经过充分冶炼,最多可以生产出含铁96%的生铁多少吨?(计算结果保留两位小数)
答案
一、1. A 2. A 3. A 4. B 5. B
6. D 点拨:取一段镁条放入盛有少量稀盐酸的试管中,反应的化学方程式为Mg+2HCl===MgCl2+H2↑,有气泡产生,故A选项说法错误;用手摸试管外壁,会感觉发烫,说明放出了热量,故B选项说法错误;由反应的化学方程式知,每24份质量的镁可置换出2份质量的氢气,反应后溶液的质量会增加,故C选项说法错误;反应说明镁能置换出酸中的氢,故D选项说法正确。
7. A
8. A 点拨:赤铁矿的主要成分是Fe2O3,故A选项错误;一氧化碳有毒,直接排放到空气中会污染环境,故B选项正确;一氧化碳具有还原性,能与氧化铁反应生成铁和二氧化碳,硬质玻璃管中红色固体变为黑色,故C选项正确;一氧化碳与氧化铁反应有二氧化碳生成,二氧化碳能使澄清石灰水变浑浊,故D选项正确。
9. C 点拨:铜的金属活动性比银强,比铁弱,铜粉能与硝酸银溶液反应生成硝酸铜溶液和银,不能与硝酸亚铁溶液反应,步骤①不能置换出Fe单质,故A选项说法错误;操作a能将滤液和滤渣分离,是过滤操作,需要漏斗、烧杯、玻璃棒、铁架台等仪器,无需使用酒精灯,故B选项说法错误;由实验知,过量的铜粉能与硝酸银溶液反应生成硝酸铜溶液和银,不能与硝酸亚铁溶液反应,说明金属活动性铁>铜>银,实验能探明三种金属的活动性强弱,故C选项说法正确;铜不能与稀盐酸反应,步骤④加盐酸不是为了除去Cu粉,是为了验证是否含有铁,故D选项说法错误。
10. C 点拨:铁与硝酸银溶液反应生成硝酸亚铁溶液和银,足量金属铁放入AgNO3溶液中,溶液变为浅绿色,故A选项错误;金属R和稀盐酸反应,生成物不一定是RCl2,故B选项错误;铁与硫酸铜反应生成硫酸亚铁和铜,反应的化学方程式为Fe+CuSO4===FeSO4+Cu,每56份质量的铁可置换出64份质量的铜,溶液的质量会减少,故C选项正确;将金属R放入Cu(NO3)2和AgNO3混合溶液中,充分反应后过滤,若滤液为蓝色,则滤液中含有硝酸铜,滤渣中一定有Ag,可能有Cu,故D选项错误。
11. A、C 点拨:若在右盘烧杯中加入5. 6 g锌粉,如果金属过量,酸不足,酸完全反应,生成氢气的质量相等,则反应停止后,天平平衡,A选项符合题意;若在右盘烧杯中加入5. 6 g黄铜粉,黄铜粉是铜锌合金,如果金属过量,酸不足,酸完全反应,生成氢气的质量相等,则反应停止后,天平平衡,B选项不符合题意;在右盘烧杯中加入5. 6 g镁粉,反应停止后,若天平平衡,说明生成氢气的质量相等,镁和稀盐酸反应:Mg+2HCl===MgCl2+H2↑;铁和稀盐酸反应:Fe+2HCl===FeCl2+H2↑;镁的相对原子质量比铁小,生成相同质量的氢气,消耗铁的质量大,当铁恰好与稀盐酸完全反应时,盐酸的溶质质量分数最大,故反应停止后,若天平平衡,则稀盐酸的溶质质量分数不大于7. 3%,C选项符合题意;在右盘烧杯中加入5. 6 g铝粉,反应停止后,若天平不平衡,说明生成氢气的质量不相等,则两种金属可能完全反应,也可能铁完全反应,铝过量,D选项不符合题意。
12. C 点拨:a点时,发生锌与硝酸银的反应,由Zn+2AgNO3===Zn(NO3)2+2Ag可知,每65份质量的锌可置换出216份质量的银,溶液的总质量比反应前小,故A选项说法正确;b点时,硝酸银恰好完全反应,溶液为Zn(NO3)2和Cu(NO3)2的混合溶液,故B选项说法正确;c点时,硝酸铜有剩余,溶液显蓝色,故C选项说法错误;d点时,锌与硝酸铜溶液恰好完全反应,过滤所得滤渣为Cu和Ag的混合物,故D选项说法正确。
二、13. (1)合金 (2)导电 (3)硬度大 (4)水和氧气
(5)硫酸铜溶液(合理即可)
14. (1)导热 (2)大
(3)Al2O3+3C+N22AlN+3CO
(4)漆能隔绝氧气和水;节约金属资源(合理即可)
15. (1)Al2O3 (2)FeSO4 (3)含碳量不同;3. 4%;生铁
16. (1)Fe3O4;H+ (2)制导线(合理即可)
(3)Fe+CuSO4===FeSO4+Cu;置换反应
三、17. (1)硬度
(2)排尽装置内的空气,避免一氧化碳与空气混合加热发生爆炸
(3)铜生锈需要氧气
(4)稀硫酸的浓度;Cu+2AgNO3===2Ag+Cu(NO3)2;铁片表面覆盖一层红色固体,溶液由蓝色逐渐变为浅绿色;A、B、C、E;A、B、D、E
18. 【查阅资料】Mg>Zn>Fe>Cu
【进行实验】溶液变成浅绿色;铜
【得出结论】镁
【实验反思】在氮气或氦气气氛中(合理即可)
【拓展提升】一定有FeSO4、MgSO4、ZnSO4,可能有H2SO4
四、19. 解:(1)70%
(2)设最多可以炼出含铁96%的生铁质量为x。
3CO + Fe2O3===== 2Fe + 3CO2
160 112
100 t×64% x×96%
=
x≈46. 67 t
答:最多可以炼出含铁96%的生铁46. 67 t。
高温
同课章节目录
