浙教版2022-2023学年上学期九年级科学分类题型训练:第一章《物质及其变化》填空题(10)【word,含答案】
文档属性
| 名称 | 浙教版2022-2023学年上学期九年级科学分类题型训练:第一章《物质及其变化》填空题(10)【word,含答案】 |  | |
| 格式 | doc | ||
| 文件大小 | 374.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2022-09-24 12:15:16 | ||
图片预览


文档简介
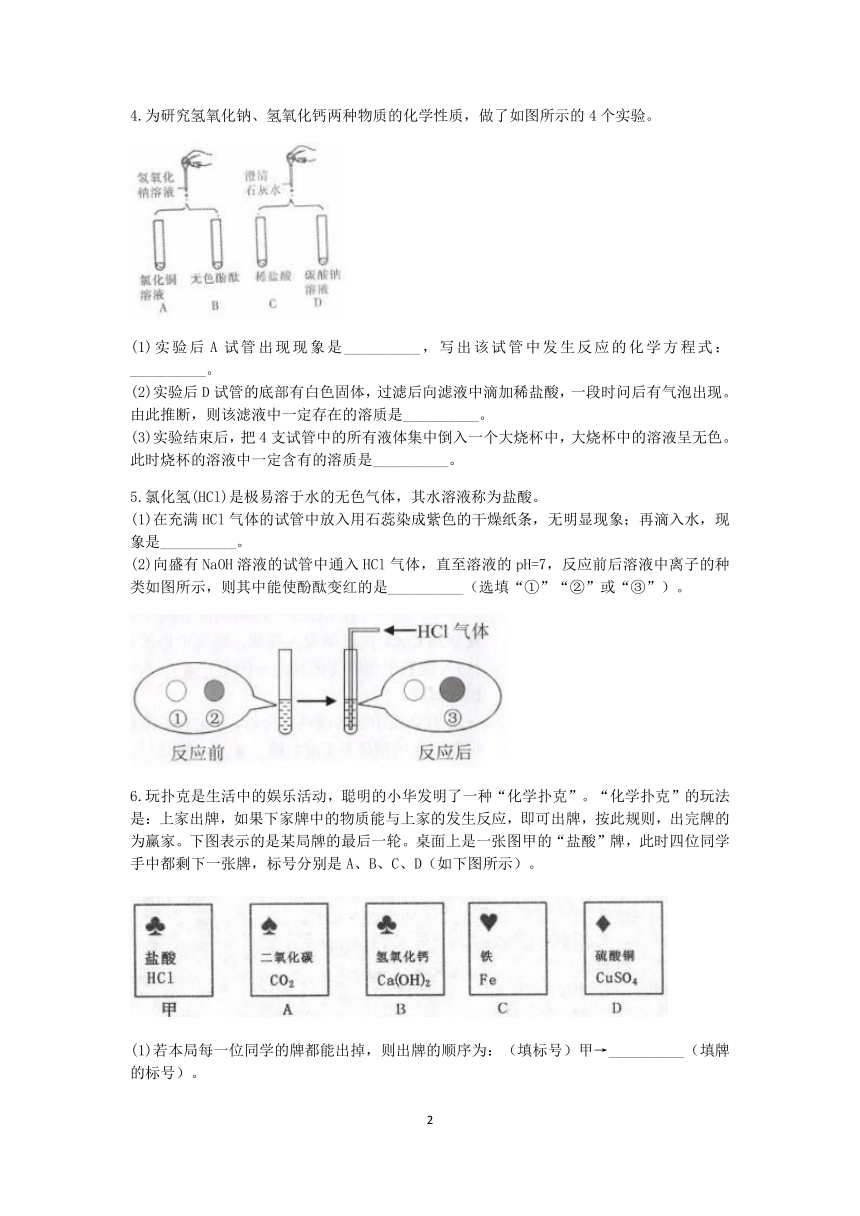
1.小金同学取了适量实验室制二氧化碳发生装置中的剩余溶液。逐滴滴加纯碱溶液,绘制产生沉淀的图象如甲图所示。
(1)请写出B点对应溶液的溶质是__________(写化学式)。
(2)乙图是甲图中O点到A点的反应微观实质模型图。则“”表示__________(写化学符号)。
2.有一包固体粉末,可能含有氯化钠、碳酸钠、硫酸钠中的一种或几种。为确定其组成,小杨设计出实验方案,实验步骤及现象如下。请回答:
(1)步骤②中产生的白色沉淀可能是___________。(用化学式表示)
(2)有同学认为该实验不能确定固体粉末的组成。为确定固体粉末的组成,应将上述步骤中_____________试剂改为__________________。
3.在探究稀盐酸性质时,小乐先在试管中注入少量稀盐酸,然后再加入足量氧化铜粉末与之反应。反应前后试管中溶液的离子种类及个数比变化如图所示。由图判断,“●”表示的是__________(填离子符号);下列能与盐酸发生反应,且符合图示离子种类和个数比变化的是__________(选填序号)。
①铜片;②铝片;③氢氧化钠溶液;④碳酸钙粉末
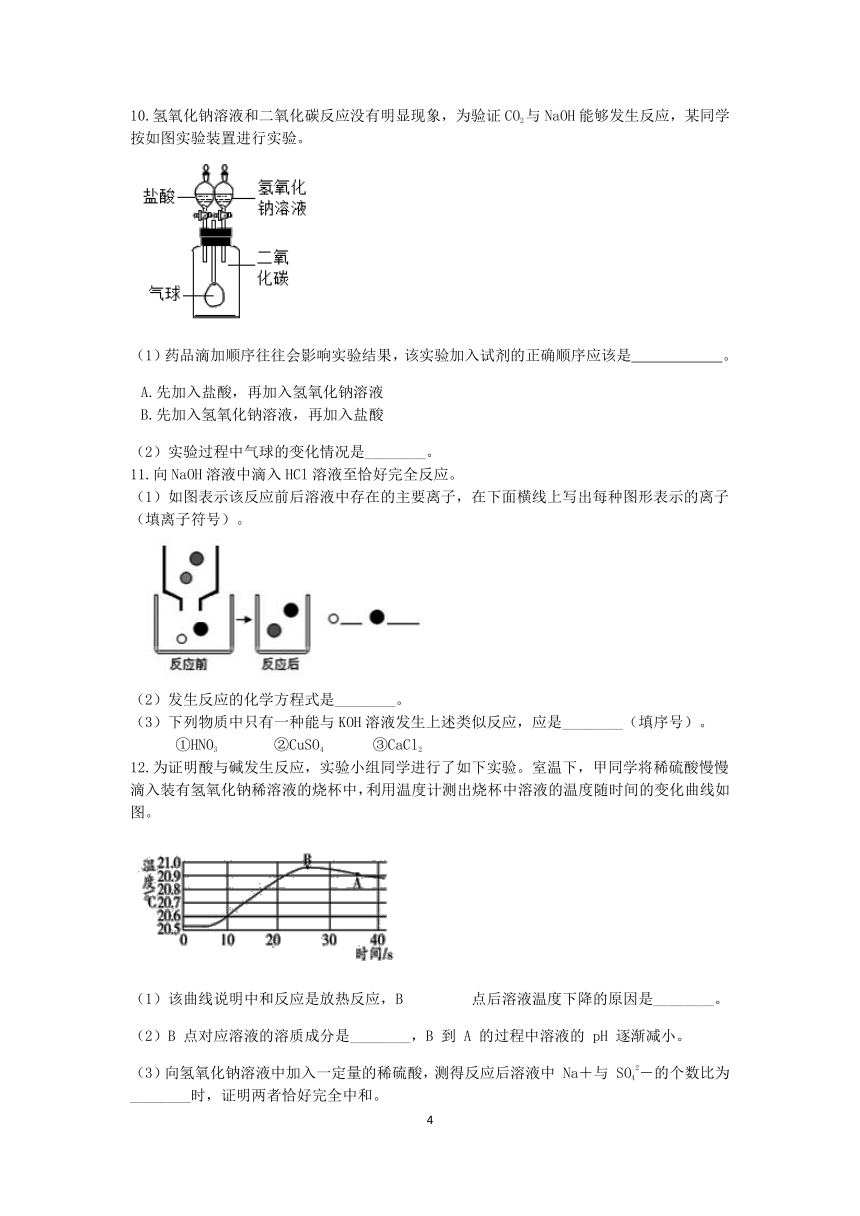
4.为研究氢氧化钠、氢氧化钙两种物质的化学性质,做了如图所示的4个实验。
(1)实验后A试管出现现象是__________,写出该试管中发生反应的化学方程式:__________。
(2)实验后D试管的底部有白色固体,过滤后向滤液中滴加稀盐酸,一段时问后有气泡出现。由此推断,则该滤液中一定存在的溶质是__________。
(3)实验结束后,把4支试管中的所有液体集中倒入一个大烧杯中,大烧杯中的溶液呈无色。此时烧杯的溶液中一定含有的溶质是__________。
5.氯化氢(HCl)是极易溶于水的无色气体,其水溶液称为盐酸。
(1)在充满HCl气体的试管中放入用石蕊染成紫色的干燥纸条,无明显现象;再滴入水,现象是__________。
(2)向盛有NaOH溶液的试管中通入HCl气体,直至溶液的pH=7,反应前后溶液中离子的种类如图所示,则其中能使酚酞变红的是__________(选填“①”“②”或“③”)。
6.玩扑克是生活中的娱乐活动,聪明的小华发明了一种“化学扑克”。“化学扑克”的玩法是:上家出牌,如果下家牌中的物质能与上家的发生反应,即可出牌,按此规则,出完牌的为赢家。下图表示的是某局牌的最后一轮。桌面上是一张图甲的“盐酸”牌,此时四位同学手中都剩下一张牌,标号分别是A、B、C、D(如下图所示)。
(1)若本局每一位同学的牌都能出掉,则出牌的顺序为:(填标号)甲→__________(填牌的标号)。
(2)若本局只有一位同学的牌出不掉,则出牌的顺序为:(填标号)甲→__________(填牌的标号)。
7.“84消毒液”的主要成分是NaClO,可通过氯气和氢氧化钠溶液反应制备,产物中还含有氯化钠和水。
(1)请写出上述反应的化学方程式__________。
(2)如图所示,小金利用试管②制取“84消毒液”,夹子开始处于关闭状态,将液体滴入试管②充分反应后,打开夹子,可发现试管①内的水立刻沸腾。请解释“打开夹子,水立刻沸腾”的原因是:__________。
8.向盛有10mLNaOH溶液(其中滴有少量无色酚酞溶液)的烧杯中逐滴加入稀盐酸,用pH计(用来精确测定溶液pH的仪器)测定溶液的pH,所得数据如下:
(1)当加入稀盐酸的体积为__________mL时,NaOH溶液和稀盐酸恰好完全反应。
(2)当加入稀盐酸的体积为3mL时,溶液显__________色;当加入稀盐酸的体积为14mL时,溶液显__________色。
(3)当烧杯中溶液的pH=2.1时,溶液中的溶质有:__________。(不考虑酚酞溶液)
9.实验室有一瓶标签残缺(如图)的试剂。实验员告诉小应,这瓶试剂可能是氢氧化钠、氯化钠、硫酸钠、碳酸钠溶液中的一种。为确定试剂成分,小应进行如下实验:
(1)根据步骤①,小应得出了该试剂可能为氯化钠溶液或硫酸钠溶液。小应作出该判断的依据是步骤①的实验现象是“无色酚酞__________”
(2)由步骤②最终确定该试剂为硫酸钠溶液,请你将步骤②的实验操作补充完整。
10.氢氧化钠溶液和二氧化碳反应没有明显现象,为验证CO2与NaOH能够发生反应,某同学按如图实验装置进行实验。
(1)药品滴加顺序往往会影响实验结果,该实验加入试剂的正确顺序应该是 。
A.先加入盐酸,再加入氢氧化钠溶液
B.先加入氢氧化钠溶液,再加入盐酸
(2)实验过程中气球的变化情况是________。
11.向NaOH溶液中滴入HCl溶液至恰好完全反应。
(1)如图表示该反应前后溶液中存在的主要离子,在下面横线上写出每种图形表示的离子(填离子符号)。
(2)发生反应的化学方程式是________。
(3)下列物质中只有一种能与KOH溶液发生上述类似反应,应是________(填序号)。
①HNO3 ②CuSO4 ③CaCl2
12.为证明酸与碱发生反应,实验小组同学进行了如下实验。室温下,甲同学将稀硫酸慢慢滴入装有氢氧化钠稀溶液的烧杯中,利用温度计测出烧杯中溶液的温度随时间的变化曲线如图。
(1)该曲线说明中和反应是放热反应,B 点后溶液温度下降的原因是________。
(2)B 点对应溶液的溶质成分是________,B 到 A 的过程中溶液的 pH 逐渐减小。
(3)向氢氧化钠溶液中加入一定量的稀硫酸,测得反应后溶液中 Na+与 SO42-的个数比为________时,证明两者恰好完全中和。
13.有一包白色固体,可能由 BaCl2、NaOH、Na2CO3、Na2SO4 中的一种或几种组成。为确定其成分,实验小组进行实验。实验过程中所加试剂均足量,实验过程及现象如图所示。
(1).写出沉淀A与稀盐酸反应的化学方程式 ,该反应属于基本反应类型中的 。
(2).白色沉淀C 的化学式为 。
(3).这包白色固体是由 (填化学式)组成的。
14.某种粗盐水中有少量含SO42-、K+的杂质,小金用这种粗盐水经过下列实验流程制取纯净氯化钠晶体。
(1)固体A是________。(填化学式)
(2)加碳酸钠溶液时发生反应的化学方程式________。
(3)若将溶液C蒸发至出现大量固体时停止加热,利用余热将溶液蒸干得到晶体,所得体仍不是纯净的氯化钠,理由是________。
15.有一包固体粉末,可能含有氯化钠、碳酸钠、硫酸钠中的一种或几种。为确定其组成,小杨设计出实验方案,实验步骤及现象如下。请回答:
(1)步骤②中产生的白色沉淀一定有________(用化学式表示)。
(2)有同学认为该实验不能确定固体粉末的组成。为确定固体粉末的组成,应将上述步骤中________试剂改为________(用化学式表示)。
16.根据碱的四条化学性质回答下列问题:
(1)图中的X代表一类物质,则X为酸,请写出符合性质③的一个化学反应方程式________.
(2)碱溶液有相似化学性质的原因是都含有________.
17.鉴别澄清石灰水和氢氧化钠溶液。
【提出问题】如何鉴别这两种无色溶液?
【实验方案】小琪等几位同学进行了如图所示的实验。
请你回答下列问题:
(1)C组实验中反应的化学方程式为 。
(2)其中不能达到实验目的的是 (填字母)。
(3)D组实验中变浑浊的原溶液是
18.“探险队员”——盐酸,不小心走进了科学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质或水溶液),盐酸必须避开它们,否则就无法通过.
(1)请你帮助他走出迷宫(请用图中物质前的序号依次连接起来表示他所走的路线)入口→________→出口.
(2)在能“吃掉”盐酸的化学反应中,属于酸和碱中和反应的有________个,其中能“吃掉”盐酸的盐是________.
(3)在不能与盐酸反应的物质中,写出一个能与硝酸银溶液反应的化学方程式________
19.已知铜在加热条件下与稀硝酸发生如下反应:3Cu+8HNO3(稀) 3Cu(NO3)2+2X↑+4H2O其中生成的气体X是一种难溶于水的无色气体,常温时易与空气中的氧气迅速化合生成红棕色的气体Y。
(1)则X的化学式为________ 。
(2)若用如图的装置来收集X气体,下列操作步骤中正确的是 。
A.先在集气瓶中装满空气 B.先在集气瓶中装满水 C.直接将气体从a管通入
20.硫酸、盐酸是重要的化工原料。
(1).浓硫酸在实验室常用作干燥剂,是因为浓硫酸有 性。
(2).98%的浓硫酸稀释为稀硫酸时,一定要将 沿烧杯壁缓慢地注入盛有水的烧杯里,并用 不断搅拌。
(3).盐酸在下列用途中,不能用硫酸代替盐酸的是 (填编号)。
①金属表面除锈 ②制造药物氯化锌 ③除去NaCl中的少量NaOH
参考答案
1.(1)CaCl2、NaCl; (2)Na+
2.BaCO3、BaSO4或BaCO3(只写BaSO4不给分);稀H2SO4;稀HCl(或稀HNO3)
3.Cu2+;④。
4.(1)观察到蓝色沉淀,2NaOH+CuCl2=Cu(OH)2↓+2NaCl (2)Na2CO3、NaOH (3)NaCl
5.(1)用石蕊染成紫色的干燥纸条变红色。(2)②。
6.(1)C→D→B→A (2)B→D→C
7.(1)Cl2+2NaOH═NaCl+NaClO+H2O。 (2)氢氧化钠和氯气反应后导致试管内气压减小,打开夹子后①中的气体进入②中导致气压减小,从而导致水的沸点降低。
8.(1)10;(2)红;无;(3)NaCl和HCl
9.(1)不变色(2)取5毫升试剂于B试管中,滴入几滴氯化钡(硝酸钡也可以)溶液
10.(1)B (2)先膨胀,后恢复原状
11.(1)OH-;Na+(2)NaOH + HCl = NaCl + H2O(3)①
12.(1)反应停止,不再有热量放出,同时过量稀硫酸起冷却降温作用
(2)Na2SO4(3)2:1
13.(1)BaCO3+2HCl═BaCl2+H2O+CO↑;复分解反应(2)CaCO3
(3)BaCl2、Na2CO3
14.(1)BaSO4(2)BaCl2 +Na2CO3=BaCO3↓ +2NaCI(3)钾离子未除去
15.(1)BaCO3(2)H2SO4;HNO3
16.(1)NaOH+HCl=NaCl+H2O (2)OH-
17.Ca(OH)2+Na2CO3===CaCO3↓+2NaOH AB Ca(OH)2溶液
18.(1)③⑥⑩⑦ (2)2;碳酸钠(3)NaCl+AgNO3=AgCl↓+NaNO3
19.(1)NO(2)B
20.(1)吸水(2)浓硫酸;玻璃棒(3)②③
《物质及其变化》填空训练(10)
(1)请写出B点对应溶液的溶质是__________(写化学式)。
(2)乙图是甲图中O点到A点的反应微观实质模型图。则“”表示__________(写化学符号)。
2.有一包固体粉末,可能含有氯化钠、碳酸钠、硫酸钠中的一种或几种。为确定其组成,小杨设计出实验方案,实验步骤及现象如下。请回答:
(1)步骤②中产生的白色沉淀可能是___________。(用化学式表示)
(2)有同学认为该实验不能确定固体粉末的组成。为确定固体粉末的组成,应将上述步骤中_____________试剂改为__________________。
3.在探究稀盐酸性质时,小乐先在试管中注入少量稀盐酸,然后再加入足量氧化铜粉末与之反应。反应前后试管中溶液的离子种类及个数比变化如图所示。由图判断,“●”表示的是__________(填离子符号);下列能与盐酸发生反应,且符合图示离子种类和个数比变化的是__________(选填序号)。
①铜片;②铝片;③氢氧化钠溶液;④碳酸钙粉末
4.为研究氢氧化钠、氢氧化钙两种物质的化学性质,做了如图所示的4个实验。
(1)实验后A试管出现现象是__________,写出该试管中发生反应的化学方程式:__________。
(2)实验后D试管的底部有白色固体,过滤后向滤液中滴加稀盐酸,一段时问后有气泡出现。由此推断,则该滤液中一定存在的溶质是__________。
(3)实验结束后,把4支试管中的所有液体集中倒入一个大烧杯中,大烧杯中的溶液呈无色。此时烧杯的溶液中一定含有的溶质是__________。
5.氯化氢(HCl)是极易溶于水的无色气体,其水溶液称为盐酸。
(1)在充满HCl气体的试管中放入用石蕊染成紫色的干燥纸条,无明显现象;再滴入水,现象是__________。
(2)向盛有NaOH溶液的试管中通入HCl气体,直至溶液的pH=7,反应前后溶液中离子的种类如图所示,则其中能使酚酞变红的是__________(选填“①”“②”或“③”)。
6.玩扑克是生活中的娱乐活动,聪明的小华发明了一种“化学扑克”。“化学扑克”的玩法是:上家出牌,如果下家牌中的物质能与上家的发生反应,即可出牌,按此规则,出完牌的为赢家。下图表示的是某局牌的最后一轮。桌面上是一张图甲的“盐酸”牌,此时四位同学手中都剩下一张牌,标号分别是A、B、C、D(如下图所示)。
(1)若本局每一位同学的牌都能出掉,则出牌的顺序为:(填标号)甲→__________(填牌的标号)。
(2)若本局只有一位同学的牌出不掉,则出牌的顺序为:(填标号)甲→__________(填牌的标号)。
7.“84消毒液”的主要成分是NaClO,可通过氯气和氢氧化钠溶液反应制备,产物中还含有氯化钠和水。
(1)请写出上述反应的化学方程式__________。
(2)如图所示,小金利用试管②制取“84消毒液”,夹子开始处于关闭状态,将液体滴入试管②充分反应后,打开夹子,可发现试管①内的水立刻沸腾。请解释“打开夹子,水立刻沸腾”的原因是:__________。
8.向盛有10mLNaOH溶液(其中滴有少量无色酚酞溶液)的烧杯中逐滴加入稀盐酸,用pH计(用来精确测定溶液pH的仪器)测定溶液的pH,所得数据如下:
(1)当加入稀盐酸的体积为__________mL时,NaOH溶液和稀盐酸恰好完全反应。
(2)当加入稀盐酸的体积为3mL时,溶液显__________色;当加入稀盐酸的体积为14mL时,溶液显__________色。
(3)当烧杯中溶液的pH=2.1时,溶液中的溶质有:__________。(不考虑酚酞溶液)
9.实验室有一瓶标签残缺(如图)的试剂。实验员告诉小应,这瓶试剂可能是氢氧化钠、氯化钠、硫酸钠、碳酸钠溶液中的一种。为确定试剂成分,小应进行如下实验:
(1)根据步骤①,小应得出了该试剂可能为氯化钠溶液或硫酸钠溶液。小应作出该判断的依据是步骤①的实验现象是“无色酚酞__________”
(2)由步骤②最终确定该试剂为硫酸钠溶液,请你将步骤②的实验操作补充完整。
10.氢氧化钠溶液和二氧化碳反应没有明显现象,为验证CO2与NaOH能够发生反应,某同学按如图实验装置进行实验。
(1)药品滴加顺序往往会影响实验结果,该实验加入试剂的正确顺序应该是 。
A.先加入盐酸,再加入氢氧化钠溶液
B.先加入氢氧化钠溶液,再加入盐酸
(2)实验过程中气球的变化情况是________。
11.向NaOH溶液中滴入HCl溶液至恰好完全反应。
(1)如图表示该反应前后溶液中存在的主要离子,在下面横线上写出每种图形表示的离子(填离子符号)。
(2)发生反应的化学方程式是________。
(3)下列物质中只有一种能与KOH溶液发生上述类似反应,应是________(填序号)。
①HNO3 ②CuSO4 ③CaCl2
12.为证明酸与碱发生反应,实验小组同学进行了如下实验。室温下,甲同学将稀硫酸慢慢滴入装有氢氧化钠稀溶液的烧杯中,利用温度计测出烧杯中溶液的温度随时间的变化曲线如图。
(1)该曲线说明中和反应是放热反应,B 点后溶液温度下降的原因是________。
(2)B 点对应溶液的溶质成分是________,B 到 A 的过程中溶液的 pH 逐渐减小。
(3)向氢氧化钠溶液中加入一定量的稀硫酸,测得反应后溶液中 Na+与 SO42-的个数比为________时,证明两者恰好完全中和。
13.有一包白色固体,可能由 BaCl2、NaOH、Na2CO3、Na2SO4 中的一种或几种组成。为确定其成分,实验小组进行实验。实验过程中所加试剂均足量,实验过程及现象如图所示。
(1).写出沉淀A与稀盐酸反应的化学方程式 ,该反应属于基本反应类型中的 。
(2).白色沉淀C 的化学式为 。
(3).这包白色固体是由 (填化学式)组成的。
14.某种粗盐水中有少量含SO42-、K+的杂质,小金用这种粗盐水经过下列实验流程制取纯净氯化钠晶体。
(1)固体A是________。(填化学式)
(2)加碳酸钠溶液时发生反应的化学方程式________。
(3)若将溶液C蒸发至出现大量固体时停止加热,利用余热将溶液蒸干得到晶体,所得体仍不是纯净的氯化钠,理由是________。
15.有一包固体粉末,可能含有氯化钠、碳酸钠、硫酸钠中的一种或几种。为确定其组成,小杨设计出实验方案,实验步骤及现象如下。请回答:
(1)步骤②中产生的白色沉淀一定有________(用化学式表示)。
(2)有同学认为该实验不能确定固体粉末的组成。为确定固体粉末的组成,应将上述步骤中________试剂改为________(用化学式表示)。
16.根据碱的四条化学性质回答下列问题:
(1)图中的X代表一类物质,则X为酸,请写出符合性质③的一个化学反应方程式________.
(2)碱溶液有相似化学性质的原因是都含有________.
17.鉴别澄清石灰水和氢氧化钠溶液。
【提出问题】如何鉴别这两种无色溶液?
【实验方案】小琪等几位同学进行了如图所示的实验。
请你回答下列问题:
(1)C组实验中反应的化学方程式为 。
(2)其中不能达到实验目的的是 (填字母)。
(3)D组实验中变浑浊的原溶液是
18.“探险队员”——盐酸,不小心走进了科学迷宫,不知怎样走出来,因为迷宫有许多“吃人的野兽”(即能与盐酸反应的物质或水溶液),盐酸必须避开它们,否则就无法通过.
(1)请你帮助他走出迷宫(请用图中物质前的序号依次连接起来表示他所走的路线)入口→________→出口.
(2)在能“吃掉”盐酸的化学反应中,属于酸和碱中和反应的有________个,其中能“吃掉”盐酸的盐是________.
(3)在不能与盐酸反应的物质中,写出一个能与硝酸银溶液反应的化学方程式________
19.已知铜在加热条件下与稀硝酸发生如下反应:3Cu+8HNO3(稀) 3Cu(NO3)2+2X↑+4H2O其中生成的气体X是一种难溶于水的无色气体,常温时易与空气中的氧气迅速化合生成红棕色的气体Y。
(1)则X的化学式为________ 。
(2)若用如图的装置来收集X气体,下列操作步骤中正确的是 。
A.先在集气瓶中装满空气 B.先在集气瓶中装满水 C.直接将气体从a管通入
20.硫酸、盐酸是重要的化工原料。
(1).浓硫酸在实验室常用作干燥剂,是因为浓硫酸有 性。
(2).98%的浓硫酸稀释为稀硫酸时,一定要将 沿烧杯壁缓慢地注入盛有水的烧杯里,并用 不断搅拌。
(3).盐酸在下列用途中,不能用硫酸代替盐酸的是 (填编号)。
①金属表面除锈 ②制造药物氯化锌 ③除去NaCl中的少量NaOH
参考答案
1.(1)CaCl2、NaCl; (2)Na+
2.BaCO3、BaSO4或BaCO3(只写BaSO4不给分);稀H2SO4;稀HCl(或稀HNO3)
3.Cu2+;④。
4.(1)观察到蓝色沉淀,2NaOH+CuCl2=Cu(OH)2↓+2NaCl (2)Na2CO3、NaOH (3)NaCl
5.(1)用石蕊染成紫色的干燥纸条变红色。(2)②。
6.(1)C→D→B→A (2)B→D→C
7.(1)Cl2+2NaOH═NaCl+NaClO+H2O。 (2)氢氧化钠和氯气反应后导致试管内气压减小,打开夹子后①中的气体进入②中导致气压减小,从而导致水的沸点降低。
8.(1)10;(2)红;无;(3)NaCl和HCl
9.(1)不变色(2)取5毫升试剂于B试管中,滴入几滴氯化钡(硝酸钡也可以)溶液
10.(1)B (2)先膨胀,后恢复原状
11.(1)OH-;Na+(2)NaOH + HCl = NaCl + H2O(3)①
12.(1)反应停止,不再有热量放出,同时过量稀硫酸起冷却降温作用
(2)Na2SO4(3)2:1
13.(1)BaCO3+2HCl═BaCl2+H2O+CO↑;复分解反应(2)CaCO3
(3)BaCl2、Na2CO3
14.(1)BaSO4(2)BaCl2 +Na2CO3=BaCO3↓ +2NaCI(3)钾离子未除去
15.(1)BaCO3(2)H2SO4;HNO3
16.(1)NaOH+HCl=NaCl+H2O (2)OH-
17.Ca(OH)2+Na2CO3===CaCO3↓+2NaOH AB Ca(OH)2溶液
18.(1)③⑥⑩⑦ (2)2;碳酸钠(3)NaCl+AgNO3=AgCl↓+NaNO3
19.(1)NO(2)B
20.(1)吸水(2)浓硫酸;玻璃棒(3)②③
《物质及其变化》填空训练(10)
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
