人教版化学九年级上册 3.2原子的结构(第1课时课件 17页)
文档属性
| 名称 | 人教版化学九年级上册 3.2原子的结构(第1课时课件 17页) |

|
|
| 格式 | zip | ||
| 文件大小 | 3.3MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-09-24 00:00:00 | ||
图片预览



文档简介
(共17张PPT)
课题2 原子的结构
第三单元
第1课时
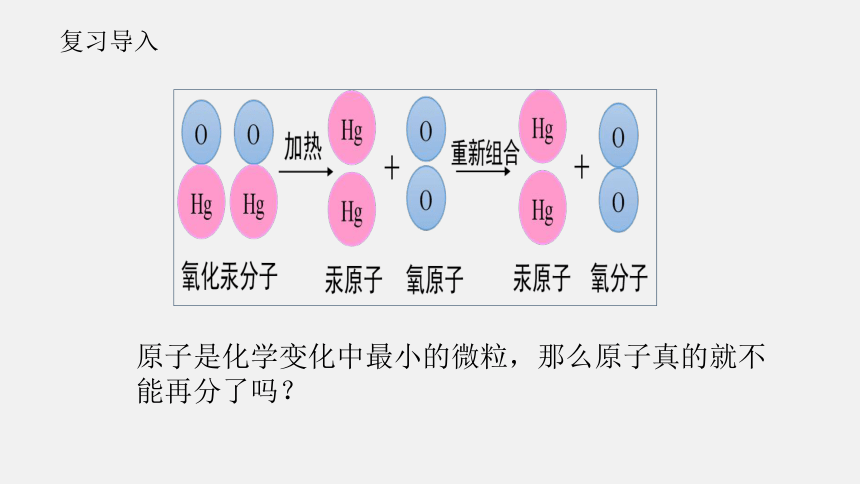
复习导入
原子是化学变化中最小的微粒,那么原子真的就不能再分了吗?
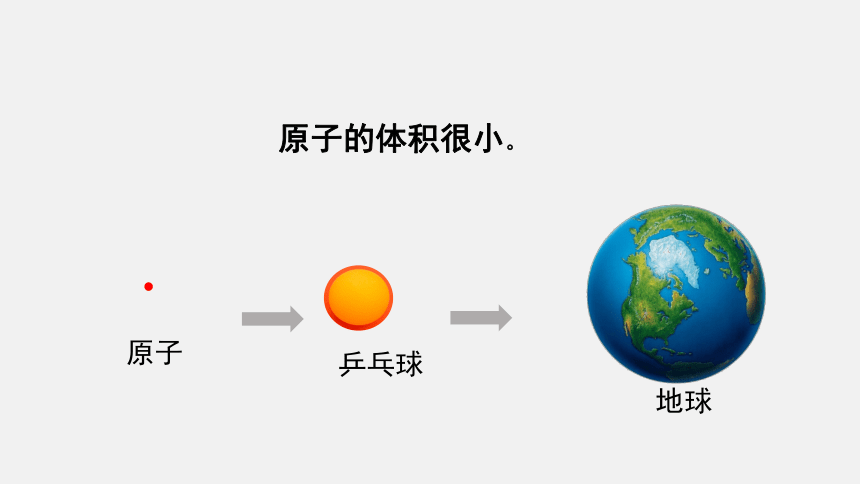
原子的体积很小。
.
原子
乒乓球
地球
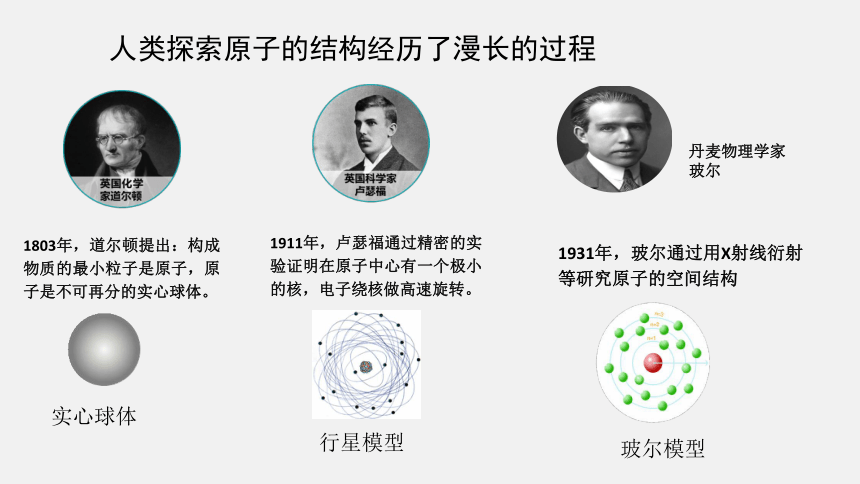
人类探索原子的结构经历了漫长的过程
1803年,道尔顿提出:构成物质的最小粒子是原子,原子是不可再分的实心球体。
1911年,卢瑟福通过精密的实验证明在原子中心有一个极小的核,电子绕核做高速旋转。
丹麦物理学家 玻尔
1931年,玻尔通过用X射线衍射等研究原子的空间结构
实心球体
行星模型
玻尔模型
原 子
原子核(+)
中子(不带电)
(带1个单位正电荷)
(带1个单位负电荷)
核外电子(-)
质子(+)
原子核所带的电荷叫做核电荷,它是由质子提供的,一个质子带一个单位的正电荷,所以核电荷数=质子数。
原子的构成
注意:原子的质量主要集中在原子核上。
在原子的构成中,一定不带电的粒子是
A.质子 B.中子 C.原子核 D.核外电子
原子是构成物质的一种微粒,某同学对其“心目中的原子”进行了如下阐述,你认为其中不正确的是
A.原子是化学变化中的最小粒子
B.原子是微小的实心球体,可以再分
C.原子可以结合成分子
D.原子由居于中心的原子核和核外电子构成
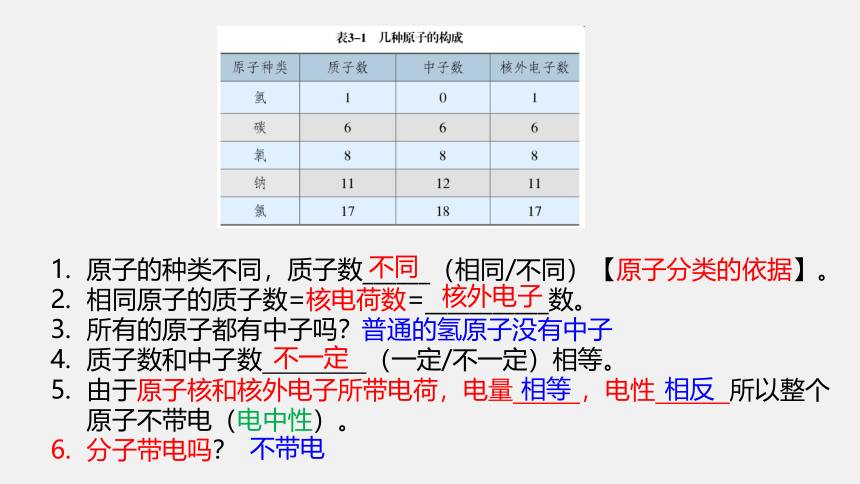
原子的种类不同,质子数______(相同/不同)【原子分类的依据】。
相同原子的质子数=核电荷数=___________数。
所有的原子都有中子吗?
质子数和中子数 (一定/不一定)相等。
由于原子核和核外电子所带电荷,电量 ,电性 所以整个原子不带电(电中性)。
分子带电吗?
普通的氢原子没有中子
不同
核外电子
不一定
相等
相反
不带电
原子不带电的原因?
由于原子里质子数=电子数,一个质子和一个电子所带的电量相等,电性相反,所以整个原子不显电性。
质子数
核外电子数
核电荷数
铈(Ce)是一种常见的稀土元素,已知铈原子的原子核内有58个质子和82个中子,该原子的核外电子数是( )
A.24
B .58
C.82
D.140
一个碳原子的质量是:1.993×10-26千克
一个氧原子的质量是:2.657×10-26千克
0.00000000000000000000000002657千克
0.00000000000000000000000001993千克
原子的质量很小,记忆、计算都很不方便,怎么办?
1.相对原子质量:以一种碳原子质量的 为标准,其他原子的质量与它相比较得到的____。(用Ar表示)
Ar=
比
1/12
一种原子的实际质量
一种碳原子质量的1/12
“相对原子质量”是一个比值,没有“克、千克……这种质量单位.其国际单位为一,一般不写出来.
已知1个碳原子的质量是1.993×10-26Kg,一个铁原子的质量是9.288×10-26Kg, 求出铁原子的相对原子质量.(结果取整数)
铁原子的相对原子质量=
9.288×10-26Kg
56
1.993×10-26Kg ×1/12
=
Ar(Fe)
有没有其他求相对原子质量的比较
简单的方法呢?
原子 质子数 中子数 相对原子质量
氢 1 0 1
氧 8 8 16
钠 11 12 23
镁 12 12 24
你能发现什么规律
规律:相对原子质量≈质子数+中子数
我国科学家张青莲主持测定了铟、铱、锑等10种元素相对原子质量的新值,被国际纯粹与应用化学联合会确定为新的国际标准数据。
下列有关分子、原子的说法中,正确的是
A.分子比原子大
B.分子可以再分,原子不能再分
C.保持水化学性质的最小粒子是水分子
D.原子都是由质子、中子、核外电子构成的
课堂小结
Thank You For Watching
课题2 原子的结构
第三单元
第1课时
复习导入
原子是化学变化中最小的微粒,那么原子真的就不能再分了吗?
原子的体积很小。
.
原子
乒乓球
地球
人类探索原子的结构经历了漫长的过程
1803年,道尔顿提出:构成物质的最小粒子是原子,原子是不可再分的实心球体。
1911年,卢瑟福通过精密的实验证明在原子中心有一个极小的核,电子绕核做高速旋转。
丹麦物理学家 玻尔
1931年,玻尔通过用X射线衍射等研究原子的空间结构
实心球体
行星模型
玻尔模型
原 子
原子核(+)
中子(不带电)
(带1个单位正电荷)
(带1个单位负电荷)
核外电子(-)
质子(+)
原子核所带的电荷叫做核电荷,它是由质子提供的,一个质子带一个单位的正电荷,所以核电荷数=质子数。
原子的构成
注意:原子的质量主要集中在原子核上。
在原子的构成中,一定不带电的粒子是
A.质子 B.中子 C.原子核 D.核外电子
原子是构成物质的一种微粒,某同学对其“心目中的原子”进行了如下阐述,你认为其中不正确的是
A.原子是化学变化中的最小粒子
B.原子是微小的实心球体,可以再分
C.原子可以结合成分子
D.原子由居于中心的原子核和核外电子构成
原子的种类不同,质子数______(相同/不同)【原子分类的依据】。
相同原子的质子数=核电荷数=___________数。
所有的原子都有中子吗?
质子数和中子数 (一定/不一定)相等。
由于原子核和核外电子所带电荷,电量 ,电性 所以整个原子不带电(电中性)。
分子带电吗?
普通的氢原子没有中子
不同
核外电子
不一定
相等
相反
不带电
原子不带电的原因?
由于原子里质子数=电子数,一个质子和一个电子所带的电量相等,电性相反,所以整个原子不显电性。
质子数
核外电子数
核电荷数
铈(Ce)是一种常见的稀土元素,已知铈原子的原子核内有58个质子和82个中子,该原子的核外电子数是( )
A.24
B .58
C.82
D.140
一个碳原子的质量是:1.993×10-26千克
一个氧原子的质量是:2.657×10-26千克
0.00000000000000000000000002657千克
0.00000000000000000000000001993千克
原子的质量很小,记忆、计算都很不方便,怎么办?
1.相对原子质量:以一种碳原子质量的 为标准,其他原子的质量与它相比较得到的____。(用Ar表示)
Ar=
比
1/12
一种原子的实际质量
一种碳原子质量的1/12
“相对原子质量”是一个比值,没有“克、千克……这种质量单位.其国际单位为一,一般不写出来.
已知1个碳原子的质量是1.993×10-26Kg,一个铁原子的质量是9.288×10-26Kg, 求出铁原子的相对原子质量.(结果取整数)
铁原子的相对原子质量=
9.288×10-26Kg
56
1.993×10-26Kg ×1/12
=
Ar(Fe)
有没有其他求相对原子质量的比较
简单的方法呢?
原子 质子数 中子数 相对原子质量
氢 1 0 1
氧 8 8 16
钠 11 12 23
镁 12 12 24
你能发现什么规律
规律:相对原子质量≈质子数+中子数
我国科学家张青莲主持测定了铟、铱、锑等10种元素相对原子质量的新值,被国际纯粹与应用化学联合会确定为新的国际标准数据。
下列有关分子、原子的说法中,正确的是
A.分子比原子大
B.分子可以再分,原子不能再分
C.保持水化学性质的最小粒子是水分子
D.原子都是由质子、中子、核外电子构成的
课堂小结
Thank You For Watching
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
