浙教版2022-2023学年上学期九年级科学分类题型训练:第一章《物质及其变化》实验题(2)【word,含答案】
文档属性
| 名称 | 浙教版2022-2023学年上学期九年级科学分类题型训练:第一章《物质及其变化》实验题(2)【word,含答案】 |

|
|
| 格式 | doc | ||
| 文件大小 | 889.0KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2022-09-24 00:00:00 | ||
图片预览


文档简介
1.将一定量的碳酸钠溶液与氯化钡溶液混合后,过滤反应的混合物.某研究小组的同学们欲探究滤液中溶质的组成.请你一同参与探究并回答有关问题:
【查阅资料】碳酸钠溶液显碱性;氯化钠、氯化钡溶液显中性。
请你写出碳酸钠溶液与氯化钡溶液反应的化学方程式__________________。
【提出猜想】
猜想1:滤液中溶质是NaCl;
猜想2:滤液中溶质是NaCl和__________(填化学式)的混合物;
猜想3:滤液中溶质是NaCl和Na2CO3的混合物。
【实验探究】
(1)取少量滤液于试管中,滴加2~3滴无色酚酞试液,振荡,无明显现象.同学们认为猜想__________不成立。
(2)另取少量滤液于另一支试管中,滴加碳酸钠溶液,若有__________(填实验现象)证明猜想2成立。
【问题讨论】
(1)甲同学认为要证明猜想2成立也可以改用硫酸钠溶液.你认为可行吗?______________
(2)乙同学认为要证明猜想2成立也可以改用硝酸银溶液.你认为可行吗?______________
2.小鹏与小明做完酸、碱、盐相关性质实验后,很感兴趣地把稀硫酸、氢氧化钠溶液和碳酸钠溶液混合在一起,看到有大量气泡生成。他们对反应后溶液中溶质的成分很好奇,请你与他们一起进行探究。
【提出问题】反应后溶液中溶质的成分是什么?
【猜想假设】猜想①:Na2SO4、Na2CO3;
猜想②:Na2SO4、Na2CO3、NaOH;
猜想③:Na2SO4、H2SO4、Na2CO3;
猜想④:Na2SO4、H2SO4;
猜想⑤:Na2SO4。
上述猜想中,不合理的是猜想___________(填序号)。
【实验探究】
(1)小鹏取少量该溶液于试管中,向其中滴加无色酚酞试液,发现溶液颜色无变化。据此,他认为猜想⑤是正确的。你认为他的结论是(填“合理”或“不合理”)的,理由是_______________。
(2)小明向盛有少量氧化铜粉末的试管中加入适量该溶液,振荡,溶液变蓝。该反应的化学方程式是______________________________________。
【实验结论】根据上述实验探究,你认为猜想______(填序号)是正确的。
【拓展应用】工厂与实验室的酸性废水必须处理至中性再排放,这样做的意义是___________(一点即可)。
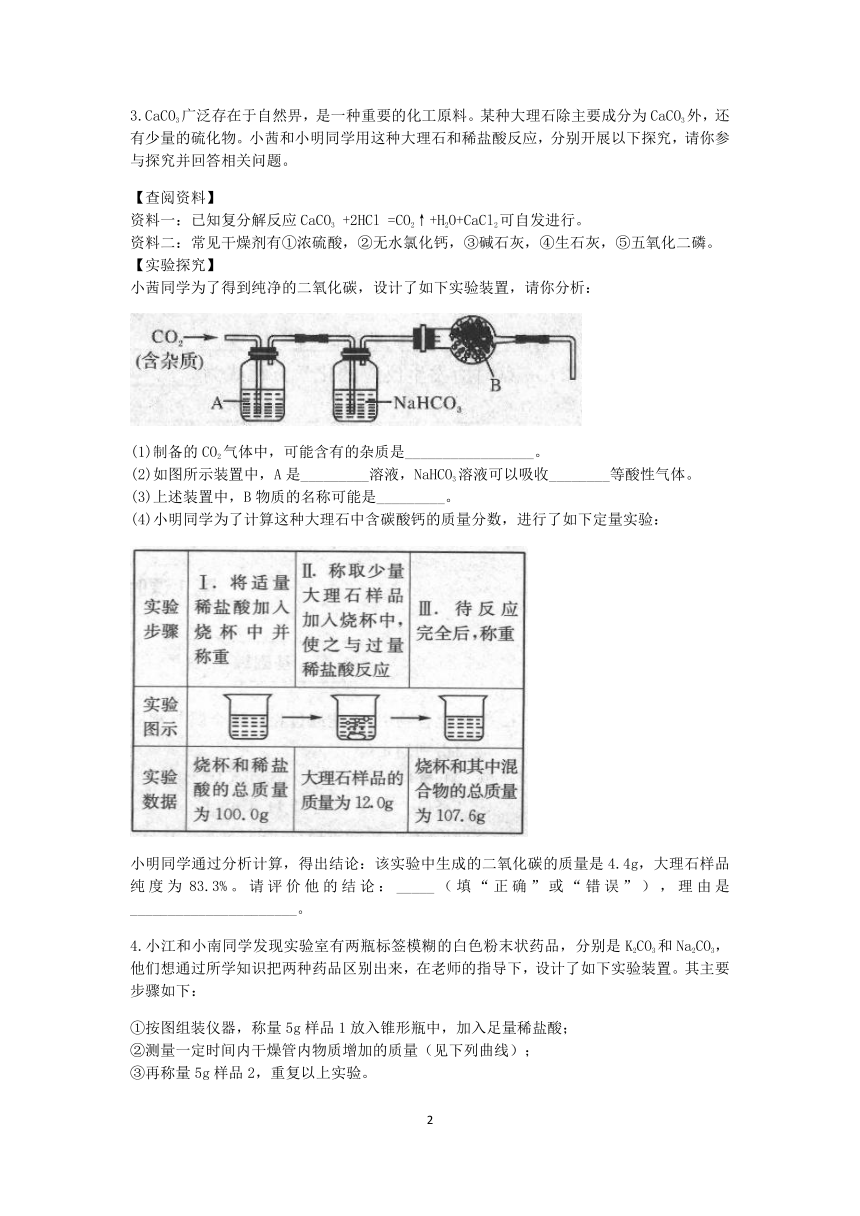
3.CaCO3广泛存在于自然畀,是一种重要的化工原料。某种大理石除主要成分为CaCO3外,还有少量的硫化物。小茜和小明同学用这种大理石和稀盐酸反应,分别开展以下探究,请你参与探究并回答相关问题。
【查阅资料】
资料一:已知复分解反应CaCO3 +2HCl =CO2↑+H2O+CaCl2可自发进行。
资料二:常见干燥剂有①浓硫酸,②无水氯化钙,③碱石灰,④生石灰,⑤五氧化二磷。
【实验探究】
小茜同学为了得到纯净的二氧化碳,设计了如下实验装置,请你分析:
(1)制备的CO2气体中,可能含有的杂质是_________________。
(2)如图所示装置中,A是_________溶液,NaHCO3溶液可以吸收________等酸性气体。
(3)上述装置中,B物质的名称可能是_________。
(4)小明同学为了计算这种大理石中含碳酸钙的质量分数,进行了如下定量实验:
小明同学通过分析计算,得出结论:该实验中生成的二氧化碳的质量是4.4g,大理石样品纯度为83.3%。请评价他的结论:_____(填“正确”或“错误”),理由是______________________。
4.小江和小南同学发现实验室有两瓶标签模糊的白色粉末状药品,分别是K2CO3和Na2CO3,他们想通过所学知识把两种药品区别出来,在老师的指导下,设计了如下实验装置。其主要步骤如下:
①按图组装仪器,称量5g样品1放入锥形瓶中,加入足量稀盐酸;
②测量一定时间内干燥管内物质增加的质量(见下列曲线);
③再称量5g样品2,重复以上实验。
【实验结果】以曲线图呈现,如图
【实骏结论】两位同学通过简单计算,认为样品1是_________。理由是_____________________。
【反思与拓展】两位同学的称量无误,但在两次实验中,干燥管内物质的增重均____(填“大于”或“小于”)理论值,请你帮助他们找出一个可能的原因:___________________________。
5.小华在吃黄花鱼时,看到其头骨上有两块白色的小石头。
【提出问题】这白色小石头中含有什么物质?
【查阅资料】小石头被称为“鱼脑石”,用来控制鱼在水中的沉浮。
【猜想与假设】“鱼脑石”中可能含有碳酸钙。
【供选试剂】10%稀盐酸,澄清石灰水,紫色石蕊试液,无色酚酞试液。
【进行实验】验证小华的猜想。
【反思】根据上述实验______(填“能”或“不能”)说明“鱼脑石”中一定含碳酸钙。
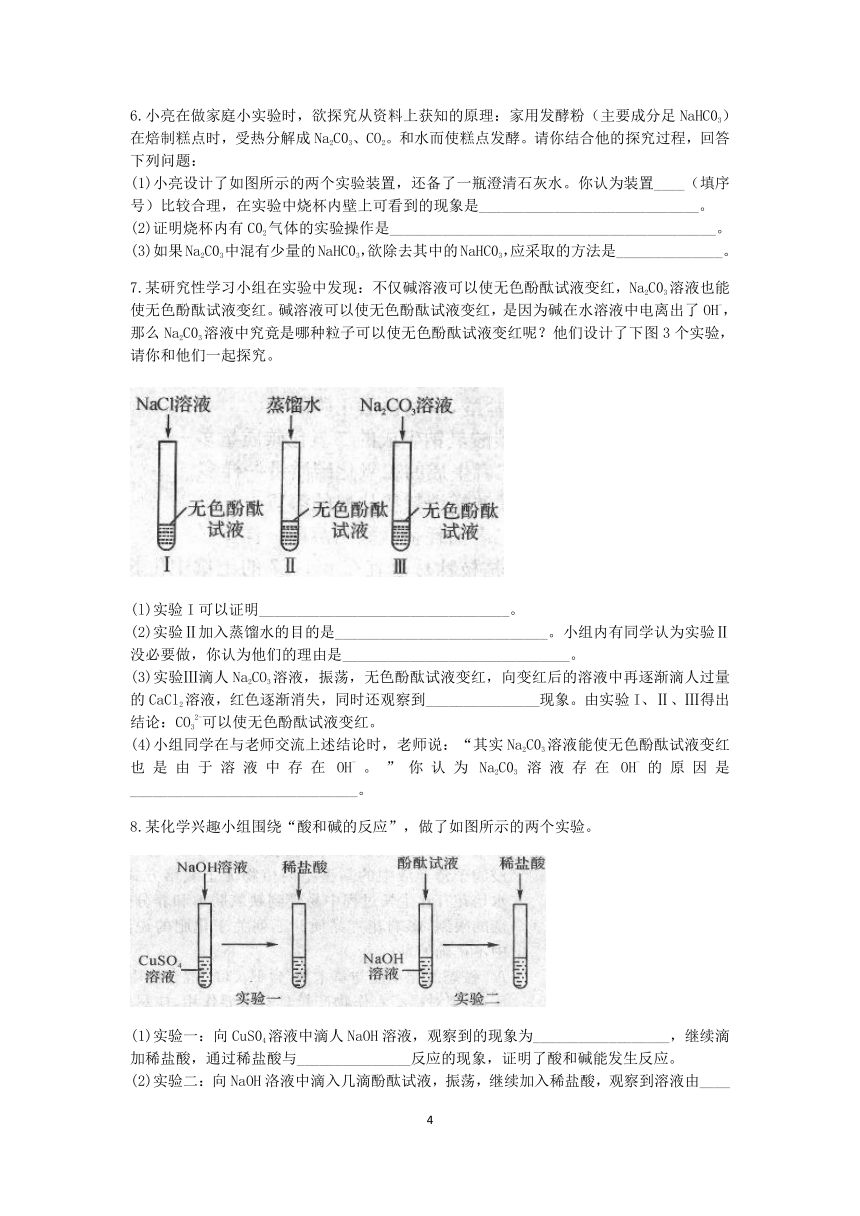
6.小亮在做家庭小实验时,欲探究从资料上获知的原理:家用发酵粉(主要成分足NaHC03)在焙制糕点时,受热分解成Na2C03、CO2。和水而使糕点发酵。请你结合他的探究过程,回答下列问题:
(1)小亮设计了如图所示的两个实验装置,还备了一瓶澄清石灰水。你认为装置____(填序号)比较合理,在实验中烧杯内壁上可看到的现象是_____________________________。
(2)证明烧杯内有C02气体的实验操作是___________________________________________。
(3)如果Na2C03中混有少量的NaHC03,欲除去其中的NaHC03,应采取的方法是______________。
7.某研究性学习小组在实验中发现:不仅碱溶液可以使无色酚酞试液变红,Na2C03溶液也能使无色酚酞试液变红。碱溶液可以使无色酚酞试液变红,是因为碱在水溶液中电离出了OH-,那么Na2C03溶液中究竟是哪种粒子可以使无色酚酞试液变红呢?他们设计了下图3个实验,请你和他们一起探究。
(l)实验I可以证明_________________________________。
(2)实验Ⅱ加入蒸馏水的目的是____________________________。小组内有同学认为实验Ⅱ没必要做,你认为他们的理由是______________________________。
(3)实验Ⅲ滴人Na2CO3溶液,振荡,无色酚酞试液变红,向变红后的溶液中再逐渐滴人过量的CaCl2溶液,红色逐渐消失,同时还观察到_______________现象。由实验I、Ⅱ、Ⅲ得出结论:CO32-可以使无色酚酞试液变红。
(4)小组同学在与老师交流上述结论时,老师说:“其实Na2C03溶液能使无色酚酞试液变红也是由于溶液中存在OH-。”你认为Na2C03溶液存在OH-的原因是______________________________。
8.某化学兴趣小组围绕“酸和碱的反应”,做了如图所示的两个实验。
(1)实验一:向CuS04溶液中滴人NaOH溶液,观察到的现象为__________________,继续滴加稀盐酸,通过稀盐酸与_______________反应的现象,证明了酸和碱能发生反应。
(2)实验二:向NaOH洛液中滴入几滴酚酞试液,振荡,继续加入稀盐酸,观察到溶液由____色变为无色,由此现象也证明了酸和碱能发生反应。
实验结束后,小组同学对实验二中试管内的无色溶液成分展开了讨论。
【提出问题】试管中无色溶液的溶质除酚酞外还有什么?
【猜想假设】猜想一:NaCl和HCl;
猜想二:______________________。
【实验设计】若要证明猜想一成立,下列试剂中不能达到实验目的的是_____。
A.紫色石蕊试液 B.Cu C.AgN03 D.Na2C03
9.某实验小组的同学用氢氧化钙溶液和稀盐酸进行酸碱反应的实验时,向烧杯中的氢氧化钙溶液滴加稀盐酸一会后,发现忘记了滴加指示剂。因此,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行探究。
I.写出该酸碱反应的化学方程式:________________________________________。
Ⅱ.探究烧杯内溶液中溶质的成分。
【提出问题】该烧杯内溶液中的溶质是什么?
猜想一:可能是CaC12和Ca(OH)2;
猜想二:可能只有CaCl2;
猜想三:可能是___________。
【查阅资料】氯化钙溶液呈中性。
【进行实验】实验步骤:取少量烧杯内溶液于试管中,滴入几滴无色酚酞试液,振荡;实验现象:____________________________;
结论:猜想一不正确。
实验步骤:取少量烧杯内溶液于另一支试管中,逐滴加入碳酸钠溶液至过量;
实骏现象:____________________________________;
结论:猜想二不正确,猜想三正确。
【反思与拓展】
(l)在分析化学反应后所得物质成分时,除考虑生成物外还需考虑反应物的用量。
(2)根据所学化学知识,验证烧杯内溶液中的溶质含有HCl,除以上方案外,下列哪些物质单独使用也能完成该实验?____。(填序号)
a.pH试纸 b.铜 c.紫色石蕊试液 d.硝酸银溶液
(3)烧杯中的溶液未经处理直接倒入下水道,可能造成的危害是_______________(写一条)。
10.通过如下实验对稀硫酸部分化学性质进行验证。
实验一:Mg和稀硫酸
实验二:Mg0和稀硫酸
实验三:Ba(N03)2溶液和稀硫酸
实验四:KOH溶液和稀硫酸
(l)实验二中发生反应的化学方程式为__________,
(2)实验四无明显现象,再将打磨过的铁丝浸入该实验后的溶液中,仍无明显现象,据此__________(填“能”或“不能”)验证KOH溶液和稀硫酸发生反应。
(3)将上述所有实验后的溶液混合,并进行如下实验:
①所取滤液a申加稀硫酸后无明显现象,说明其中不存在__________离子。
②滤液b中所含的溶质有__________。
11.在学习了稀盐酸和稀硫酸的化学知识后,同学们发现实验室中还有两瓶浓硫酸和浓硝酸。为了进一步了解酸的有关知识,老师将同学们分为甲、乙两组进行探究。
(1)甲组的同学做了如图所示实验,发现有刺激性气味的气体生成,请你完成化学反应方程式:2Zn+2H2S04(浓)=ZnS04+____↑+2H20。反应一段时间后,老师提醒还可能生成另一种气体。大家都很好奇,这是什么气体呢?请你根据酸的化学性质,推断此气体可能是_______,其理由是___________________。
(2)乙组的同学打开盛装浓硝酸的试剂瓶,观察到瓶口有白雾产生。据此可知,浓硝酸具有____(填一条物理性质)。乙组同学又取少量浓硝酸置于试管中,采用强光照射或稍加热,立即观察到溶液上方有红棕色的N02气体产生。据此现象可推知浓硝酸具有__________(填一条化学性质)。实验室应如何保存浓硝酸?____________________________。
12.甲、乙两同学进行氧化铜与稀硫酸反应的实验:
【进行实验】
(1)甲同学按实验一进行实验,很长时间后才观察到明显的现象,发生反应的他学反应方程式为_________________________________。
(2)乙同学按实验二进行实验,很快观察到黑色固体消失,溶液_______________,
(3)甲同学分析了乙同学的实验,不加其他任何试剂,只进行____操作,也很酷唧嚓到实验现象。
【实验评价】
实验二中的操作存在不足,请进行完善:____________________。
【变废为宝】
(1)实验结束后,把两只烧杯中的溶液混合,取少量烧杯中的溶液放于试管中,滴加少量NaOH溶液,并没有观察到明显现象,则烧杯中溶液的溶质是_________________________。
(2)实验结束后,可向溶液中加入适量的某种物质_________(填序号),即能除去溶液中的铜离子,又能得到具有化肥功能的溶液。
A.Fe203 B.KOH C.Ba(N03)2
13.某同学进行了如图所示的探究实验:
(1)B试管中发生反应的化学方程式是__________,写出与该反应原理有关的稀盐酸的一个用途:__________,
(2)C试管中加入足量的稀盐酸后出现的实验现象是__________;通过B、C两支试管的实验可得出稀盐酸能与__________氧化物反应。
(3)进行D实验时忘了先加无色酚酞试液,当滴入一定量的稀盐酸后滴人几滴无色酚酞试液,溶液没有变色。则D中的溶质的组成情况是:肯定含__________,可能含__________(不考虑酚酞)。
14.小徐同学做了如图所示的两个实验。
(1)试管乙有明显的实验现象,请用化学方程式解释:__________。
(2)由于在试管甲没有观察到明显的实验现象,于是小徐同学对稀盐酸能否与氢氧化钙溶液发生反应表示质疑。老师告诉他,只要在实验前向装有氢氧化钙溶液的试管中滴加几滴石蕊试液,在滴加稀盐酸,当观察到__________时,就能证明两种物质发生反应了。
(3)实验结束后,他将试管甲和试管乙的液体倒入到一个空烧杯中。
①若只观察到有气泡产生的现象,则试管甲的溶液中含有的阴离子是__________。
②若开始阶段观察到有气泡,一段时间后又出现白色沉淀的现象,待反应结束后,将烧杯中混合液过滤,滤液中的溶质除氯化钠外,还可能有__________(填化学式)。
15.有一包白色固体样品,可能由硫酸钠、氢氧化钠、碳酸钙、氯化钡、氯化镁中的一种或几种物质祖成,为探究该样品的组成,某小组取适量样品按下列流程进行实验。请回答下列问题:
滤渣a的成分是_______________,滤液中溶质的成分除氯化钠还有_________________。
参考答案
1.【查阅资料】:Na2CO3+BaCl2═BaCO3↓+2NaCl; 【提出猜想】:BaCl2【实验探究】:(1)3 ;(2)白色沉淀生成;【问题讨论】:(1)能 ;(1)不能
2.③ (1)不合理 无色酚酞试液遇酸性或中性溶液均不变色 (2)CuO+H2SO4=CuSO4+H2O ④ 防止污染水体或防止腐蚀铁质下水道
3.(1)氯化氢、硫化氢和水蒸气(2)硫酸铜 氯化氢(3)无水氯化钙(4)错误 大理石中含有硫化物,硫化物与稀盐酸反应会生成硫化氢气体逸出,把生成的气体全部作为二氧化碳处理,使碳酸钙质量分数偏大
4.碳酸钠 等质量的碳酸钠和碳酸钾与足量的稀盐酸反应,碳酸钠所产生的二氧化碳质量大于碳酸钾 小于 稀盐酸滴入过快,二氧化碳没有被吸收完全(合理即可)
5.澄清石灰水 ①固体表面有气泡冒出 ②澄清石灰水变浑浊 不能
6.(1)B 有水珠生成(2)把烧杯倒转过来,加入少量澄清石灰水,震荡,观察现象(3)加热
7.(1)Na+不会使无色酚酞试液变红(2)探究水分子是否能使无色酚酞试液变红 无色酚酞试液中就有水分子(或氯化钠溶液中含有水分子)(3)有白色沉淀产生(4)Na2CO3与H2O发生反应,使溶液中产生了OH-
8.(1)有蓝色沉淀生成 氢氧化铜(2)红 NaCl BC
9.Ca(OH)2+2HCl=CaCl2+2H20 CaCl2和HCl 溶液无明显变化(或溶液不变红色) 先有气体产生,后产生沉淀 (2)ac (3)腐蚀铁质下水管(或污染水源)
10.(1)MgO+H2SO4=MgSO4+H2↑(2)能(3)钡 硝酸钡、硝酸钾、氢氧化钡
11.(1)SO2 H2 随着硫酸的消耗和水的生成,浓硫酸变成稀盐酸,锌和稀硫酸反应产生氢气(2)挥发性 受热易分解 棕色瓶阴冷处密封保存
12.(1)CuO+H2SO4=CuSO4+H2O(2)有无色变为蓝色(3)加热 用玻璃棒搅拌 (1)硫酸铜、硫酸(2)B
13.(1)Fe2O3+6HCl=2FeCl3+3H2O 除铁锈(2)黑色粉末减少,溶液由无色变成蓝色 金属(3)NaCl HCl
14.(1)Na2CO3+2HCl=2NaCl+H2O+CO2↑(2)溶液由蓝色变为紫色,甚至红色(3)氯离子 CaCl2或Na2CO3
15.(1)CaCO3,Mg(OH)2 (2)NaOH,BaCl2
《物质及其变化》实验探究训练(2)
【查阅资料】碳酸钠溶液显碱性;氯化钠、氯化钡溶液显中性。
请你写出碳酸钠溶液与氯化钡溶液反应的化学方程式__________________。
【提出猜想】
猜想1:滤液中溶质是NaCl;
猜想2:滤液中溶质是NaCl和__________(填化学式)的混合物;
猜想3:滤液中溶质是NaCl和Na2CO3的混合物。
【实验探究】
(1)取少量滤液于试管中,滴加2~3滴无色酚酞试液,振荡,无明显现象.同学们认为猜想__________不成立。
(2)另取少量滤液于另一支试管中,滴加碳酸钠溶液,若有__________(填实验现象)证明猜想2成立。
【问题讨论】
(1)甲同学认为要证明猜想2成立也可以改用硫酸钠溶液.你认为可行吗?______________
(2)乙同学认为要证明猜想2成立也可以改用硝酸银溶液.你认为可行吗?______________
2.小鹏与小明做完酸、碱、盐相关性质实验后,很感兴趣地把稀硫酸、氢氧化钠溶液和碳酸钠溶液混合在一起,看到有大量气泡生成。他们对反应后溶液中溶质的成分很好奇,请你与他们一起进行探究。
【提出问题】反应后溶液中溶质的成分是什么?
【猜想假设】猜想①:Na2SO4、Na2CO3;
猜想②:Na2SO4、Na2CO3、NaOH;
猜想③:Na2SO4、H2SO4、Na2CO3;
猜想④:Na2SO4、H2SO4;
猜想⑤:Na2SO4。
上述猜想中,不合理的是猜想___________(填序号)。
【实验探究】
(1)小鹏取少量该溶液于试管中,向其中滴加无色酚酞试液,发现溶液颜色无变化。据此,他认为猜想⑤是正确的。你认为他的结论是(填“合理”或“不合理”)的,理由是_______________。
(2)小明向盛有少量氧化铜粉末的试管中加入适量该溶液,振荡,溶液变蓝。该反应的化学方程式是______________________________________。
【实验结论】根据上述实验探究,你认为猜想______(填序号)是正确的。
【拓展应用】工厂与实验室的酸性废水必须处理至中性再排放,这样做的意义是___________(一点即可)。
3.CaCO3广泛存在于自然畀,是一种重要的化工原料。某种大理石除主要成分为CaCO3外,还有少量的硫化物。小茜和小明同学用这种大理石和稀盐酸反应,分别开展以下探究,请你参与探究并回答相关问题。
【查阅资料】
资料一:已知复分解反应CaCO3 +2HCl =CO2↑+H2O+CaCl2可自发进行。
资料二:常见干燥剂有①浓硫酸,②无水氯化钙,③碱石灰,④生石灰,⑤五氧化二磷。
【实验探究】
小茜同学为了得到纯净的二氧化碳,设计了如下实验装置,请你分析:
(1)制备的CO2气体中,可能含有的杂质是_________________。
(2)如图所示装置中,A是_________溶液,NaHCO3溶液可以吸收________等酸性气体。
(3)上述装置中,B物质的名称可能是_________。
(4)小明同学为了计算这种大理石中含碳酸钙的质量分数,进行了如下定量实验:
小明同学通过分析计算,得出结论:该实验中生成的二氧化碳的质量是4.4g,大理石样品纯度为83.3%。请评价他的结论:_____(填“正确”或“错误”),理由是______________________。
4.小江和小南同学发现实验室有两瓶标签模糊的白色粉末状药品,分别是K2CO3和Na2CO3,他们想通过所学知识把两种药品区别出来,在老师的指导下,设计了如下实验装置。其主要步骤如下:
①按图组装仪器,称量5g样品1放入锥形瓶中,加入足量稀盐酸;
②测量一定时间内干燥管内物质增加的质量(见下列曲线);
③再称量5g样品2,重复以上实验。
【实验结果】以曲线图呈现,如图
【实骏结论】两位同学通过简单计算,认为样品1是_________。理由是_____________________。
【反思与拓展】两位同学的称量无误,但在两次实验中,干燥管内物质的增重均____(填“大于”或“小于”)理论值,请你帮助他们找出一个可能的原因:___________________________。
5.小华在吃黄花鱼时,看到其头骨上有两块白色的小石头。
【提出问题】这白色小石头中含有什么物质?
【查阅资料】小石头被称为“鱼脑石”,用来控制鱼在水中的沉浮。
【猜想与假设】“鱼脑石”中可能含有碳酸钙。
【供选试剂】10%稀盐酸,澄清石灰水,紫色石蕊试液,无色酚酞试液。
【进行实验】验证小华的猜想。
【反思】根据上述实验______(填“能”或“不能”)说明“鱼脑石”中一定含碳酸钙。
6.小亮在做家庭小实验时,欲探究从资料上获知的原理:家用发酵粉(主要成分足NaHC03)在焙制糕点时,受热分解成Na2C03、CO2。和水而使糕点发酵。请你结合他的探究过程,回答下列问题:
(1)小亮设计了如图所示的两个实验装置,还备了一瓶澄清石灰水。你认为装置____(填序号)比较合理,在实验中烧杯内壁上可看到的现象是_____________________________。
(2)证明烧杯内有C02气体的实验操作是___________________________________________。
(3)如果Na2C03中混有少量的NaHC03,欲除去其中的NaHC03,应采取的方法是______________。
7.某研究性学习小组在实验中发现:不仅碱溶液可以使无色酚酞试液变红,Na2C03溶液也能使无色酚酞试液变红。碱溶液可以使无色酚酞试液变红,是因为碱在水溶液中电离出了OH-,那么Na2C03溶液中究竟是哪种粒子可以使无色酚酞试液变红呢?他们设计了下图3个实验,请你和他们一起探究。
(l)实验I可以证明_________________________________。
(2)实验Ⅱ加入蒸馏水的目的是____________________________。小组内有同学认为实验Ⅱ没必要做,你认为他们的理由是______________________________。
(3)实验Ⅲ滴人Na2CO3溶液,振荡,无色酚酞试液变红,向变红后的溶液中再逐渐滴人过量的CaCl2溶液,红色逐渐消失,同时还观察到_______________现象。由实验I、Ⅱ、Ⅲ得出结论:CO32-可以使无色酚酞试液变红。
(4)小组同学在与老师交流上述结论时,老师说:“其实Na2C03溶液能使无色酚酞试液变红也是由于溶液中存在OH-。”你认为Na2C03溶液存在OH-的原因是______________________________。
8.某化学兴趣小组围绕“酸和碱的反应”,做了如图所示的两个实验。
(1)实验一:向CuS04溶液中滴人NaOH溶液,观察到的现象为__________________,继续滴加稀盐酸,通过稀盐酸与_______________反应的现象,证明了酸和碱能发生反应。
(2)实验二:向NaOH洛液中滴入几滴酚酞试液,振荡,继续加入稀盐酸,观察到溶液由____色变为无色,由此现象也证明了酸和碱能发生反应。
实验结束后,小组同学对实验二中试管内的无色溶液成分展开了讨论。
【提出问题】试管中无色溶液的溶质除酚酞外还有什么?
【猜想假设】猜想一:NaCl和HCl;
猜想二:______________________。
【实验设计】若要证明猜想一成立,下列试剂中不能达到实验目的的是_____。
A.紫色石蕊试液 B.Cu C.AgN03 D.Na2C03
9.某实验小组的同学用氢氧化钙溶液和稀盐酸进行酸碱反应的实验时,向烧杯中的氢氧化钙溶液滴加稀盐酸一会后,发现忘记了滴加指示剂。因此,他们停止滴加稀盐酸,并对烧杯内溶液中的溶质成分进行探究。
I.写出该酸碱反应的化学方程式:________________________________________。
Ⅱ.探究烧杯内溶液中溶质的成分。
【提出问题】该烧杯内溶液中的溶质是什么?
猜想一:可能是CaC12和Ca(OH)2;
猜想二:可能只有CaCl2;
猜想三:可能是___________。
【查阅资料】氯化钙溶液呈中性。
【进行实验】实验步骤:取少量烧杯内溶液于试管中,滴入几滴无色酚酞试液,振荡;实验现象:____________________________;
结论:猜想一不正确。
实验步骤:取少量烧杯内溶液于另一支试管中,逐滴加入碳酸钠溶液至过量;
实骏现象:____________________________________;
结论:猜想二不正确,猜想三正确。
【反思与拓展】
(l)在分析化学反应后所得物质成分时,除考虑生成物外还需考虑反应物的用量。
(2)根据所学化学知识,验证烧杯内溶液中的溶质含有HCl,除以上方案外,下列哪些物质单独使用也能完成该实验?____。(填序号)
a.pH试纸 b.铜 c.紫色石蕊试液 d.硝酸银溶液
(3)烧杯中的溶液未经处理直接倒入下水道,可能造成的危害是_______________(写一条)。
10.通过如下实验对稀硫酸部分化学性质进行验证。
实验一:Mg和稀硫酸
实验二:Mg0和稀硫酸
实验三:Ba(N03)2溶液和稀硫酸
实验四:KOH溶液和稀硫酸
(l)实验二中发生反应的化学方程式为__________,
(2)实验四无明显现象,再将打磨过的铁丝浸入该实验后的溶液中,仍无明显现象,据此__________(填“能”或“不能”)验证KOH溶液和稀硫酸发生反应。
(3)将上述所有实验后的溶液混合,并进行如下实验:
①所取滤液a申加稀硫酸后无明显现象,说明其中不存在__________离子。
②滤液b中所含的溶质有__________。
11.在学习了稀盐酸和稀硫酸的化学知识后,同学们发现实验室中还有两瓶浓硫酸和浓硝酸。为了进一步了解酸的有关知识,老师将同学们分为甲、乙两组进行探究。
(1)甲组的同学做了如图所示实验,发现有刺激性气味的气体生成,请你完成化学反应方程式:2Zn+2H2S04(浓)=ZnS04+____↑+2H20。反应一段时间后,老师提醒还可能生成另一种气体。大家都很好奇,这是什么气体呢?请你根据酸的化学性质,推断此气体可能是_______,其理由是___________________。
(2)乙组的同学打开盛装浓硝酸的试剂瓶,观察到瓶口有白雾产生。据此可知,浓硝酸具有____(填一条物理性质)。乙组同学又取少量浓硝酸置于试管中,采用强光照射或稍加热,立即观察到溶液上方有红棕色的N02气体产生。据此现象可推知浓硝酸具有__________(填一条化学性质)。实验室应如何保存浓硝酸?____________________________。
12.甲、乙两同学进行氧化铜与稀硫酸反应的实验:
【进行实验】
(1)甲同学按实验一进行实验,很长时间后才观察到明显的现象,发生反应的他学反应方程式为_________________________________。
(2)乙同学按实验二进行实验,很快观察到黑色固体消失,溶液_______________,
(3)甲同学分析了乙同学的实验,不加其他任何试剂,只进行____操作,也很酷唧嚓到实验现象。
【实验评价】
实验二中的操作存在不足,请进行完善:____________________。
【变废为宝】
(1)实验结束后,把两只烧杯中的溶液混合,取少量烧杯中的溶液放于试管中,滴加少量NaOH溶液,并没有观察到明显现象,则烧杯中溶液的溶质是_________________________。
(2)实验结束后,可向溶液中加入适量的某种物质_________(填序号),即能除去溶液中的铜离子,又能得到具有化肥功能的溶液。
A.Fe203 B.KOH C.Ba(N03)2
13.某同学进行了如图所示的探究实验:
(1)B试管中发生反应的化学方程式是__________,写出与该反应原理有关的稀盐酸的一个用途:__________,
(2)C试管中加入足量的稀盐酸后出现的实验现象是__________;通过B、C两支试管的实验可得出稀盐酸能与__________氧化物反应。
(3)进行D实验时忘了先加无色酚酞试液,当滴入一定量的稀盐酸后滴人几滴无色酚酞试液,溶液没有变色。则D中的溶质的组成情况是:肯定含__________,可能含__________(不考虑酚酞)。
14.小徐同学做了如图所示的两个实验。
(1)试管乙有明显的实验现象,请用化学方程式解释:__________。
(2)由于在试管甲没有观察到明显的实验现象,于是小徐同学对稀盐酸能否与氢氧化钙溶液发生反应表示质疑。老师告诉他,只要在实验前向装有氢氧化钙溶液的试管中滴加几滴石蕊试液,在滴加稀盐酸,当观察到__________时,就能证明两种物质发生反应了。
(3)实验结束后,他将试管甲和试管乙的液体倒入到一个空烧杯中。
①若只观察到有气泡产生的现象,则试管甲的溶液中含有的阴离子是__________。
②若开始阶段观察到有气泡,一段时间后又出现白色沉淀的现象,待反应结束后,将烧杯中混合液过滤,滤液中的溶质除氯化钠外,还可能有__________(填化学式)。
15.有一包白色固体样品,可能由硫酸钠、氢氧化钠、碳酸钙、氯化钡、氯化镁中的一种或几种物质祖成,为探究该样品的组成,某小组取适量样品按下列流程进行实验。请回答下列问题:
滤渣a的成分是_______________,滤液中溶质的成分除氯化钠还有_________________。
参考答案
1.【查阅资料】:Na2CO3+BaCl2═BaCO3↓+2NaCl; 【提出猜想】:BaCl2【实验探究】:(1)3 ;(2)白色沉淀生成;【问题讨论】:(1)能 ;(1)不能
2.③ (1)不合理 无色酚酞试液遇酸性或中性溶液均不变色 (2)CuO+H2SO4=CuSO4+H2O ④ 防止污染水体或防止腐蚀铁质下水道
3.(1)氯化氢、硫化氢和水蒸气(2)硫酸铜 氯化氢(3)无水氯化钙(4)错误 大理石中含有硫化物,硫化物与稀盐酸反应会生成硫化氢气体逸出,把生成的气体全部作为二氧化碳处理,使碳酸钙质量分数偏大
4.碳酸钠 等质量的碳酸钠和碳酸钾与足量的稀盐酸反应,碳酸钠所产生的二氧化碳质量大于碳酸钾 小于 稀盐酸滴入过快,二氧化碳没有被吸收完全(合理即可)
5.澄清石灰水 ①固体表面有气泡冒出 ②澄清石灰水变浑浊 不能
6.(1)B 有水珠生成(2)把烧杯倒转过来,加入少量澄清石灰水,震荡,观察现象(3)加热
7.(1)Na+不会使无色酚酞试液变红(2)探究水分子是否能使无色酚酞试液变红 无色酚酞试液中就有水分子(或氯化钠溶液中含有水分子)(3)有白色沉淀产生(4)Na2CO3与H2O发生反应,使溶液中产生了OH-
8.(1)有蓝色沉淀生成 氢氧化铜(2)红 NaCl BC
9.Ca(OH)2+2HCl=CaCl2+2H20 CaCl2和HCl 溶液无明显变化(或溶液不变红色) 先有气体产生,后产生沉淀 (2)ac (3)腐蚀铁质下水管(或污染水源)
10.(1)MgO+H2SO4=MgSO4+H2↑(2)能(3)钡 硝酸钡、硝酸钾、氢氧化钡
11.(1)SO2 H2 随着硫酸的消耗和水的生成,浓硫酸变成稀盐酸,锌和稀硫酸反应产生氢气(2)挥发性 受热易分解 棕色瓶阴冷处密封保存
12.(1)CuO+H2SO4=CuSO4+H2O(2)有无色变为蓝色(3)加热 用玻璃棒搅拌 (1)硫酸铜、硫酸(2)B
13.(1)Fe2O3+6HCl=2FeCl3+3H2O 除铁锈(2)黑色粉末减少,溶液由无色变成蓝色 金属(3)NaCl HCl
14.(1)Na2CO3+2HCl=2NaCl+H2O+CO2↑(2)溶液由蓝色变为紫色,甚至红色(3)氯离子 CaCl2或Na2CO3
15.(1)CaCO3,Mg(OH)2 (2)NaOH,BaCl2
《物质及其变化》实验探究训练(2)
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
