浙教版2022-2023学年上学期九年级科学分类题型训练:第一章《物质及其变化》实验题(3)【word,含答案】
文档属性
| 名称 | 浙教版2022-2023学年上学期九年级科学分类题型训练:第一章《物质及其变化》实验题(3)【word,含答案】 |

|
|
| 格式 | doc | ||
| 文件大小 | 437.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2022-09-24 00:00:00 | ||
图片预览


文档简介
1.某化学兴趣小组的同学在做氢氧化钙与稀盐酸中和反应的实验时,忘记滴加酸碱指示剂,因而无法判断酸碱是否恰好完全反应。于是他们对反应后溶质的成分大胆提出猜想,进行了以下探究,请你和他们一起完成下列实验报告。
【提出问题】该溶液中的溶质含有哪些成分?
【查阅资料】CaCl2溶液呈中性。
【猜想与假设】
(1)猜想Ⅰ:溶液中的溶质只有______________
猜想Ⅱ:溶液中的溶质有CaCl2、HCl
猜想Ⅲ:溶液中的溶质有CaCl2、Ca(OH)2
猜想Ⅳ:溶液中溶质有CaCl2、Ca(OH)2、HCl
(2)经过讨论,同学们直接得出猜想___________是不正确的。为了验证余下的哪一个猜想是正确的,同学们又做了以下实验。
【进行实验】
2.初中科学课上,同学们利用下列实验探究碱的化学性质:
(1)B实验的现象为_________________________。
实验结束后,同学们将废液倒入同一只废液缸中,
最后发现废液浑浊并显红色。
【提出问题】废液中含有什么物质?
【假设猜想】通过分析上述实验,同学们猜想:废液中除酚酞和水外一定含有氯化钠。
老师问:废液中还可能有什么物质?
(2)某同学脱口而出:废液中一定含有氢氧化钠,他的说法正确吗?同学们认为不准确,理由是:______________________________________。
【实验验证】同学们对可能含有的物质进行进一步确定,取一定量的废液过滤,向滤液中加入几滴氯化钙溶液,发现马上产生了白色沉淀。
(3)根据该现象可以确定该废液中一定还含有_____________。
【拓展提高】那么废液中是否含有氢氧化钠?
(4)请你写出在原实验的基础上作出进一步判断的方法:_______________________。
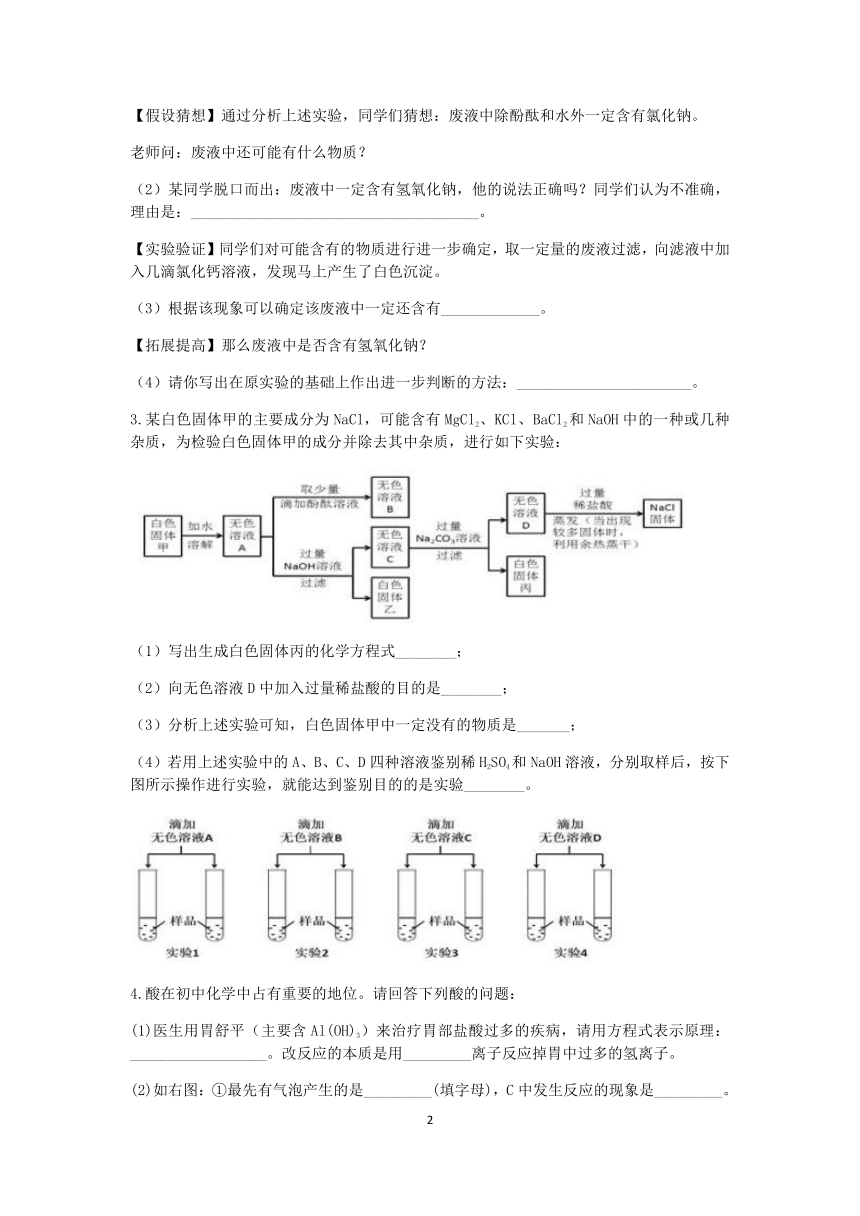
3.某白色固体甲的主要成分为NaCl,可能含有MgCl2、KCl、BaCl2和NaOH中的一种或几种杂质,为检验白色固体甲的成分并除去其中杂质,进行如下实验:
(1)写出生成白色固体丙的化学方程式________;
(2)向无色溶液D中加入过量稀盐酸的目的是________;
(3)分析上述实验可知,白色固体甲中一定没有的物质是_______;
(4)若用上述实验中的A、B、C、D四种溶液鉴别稀H2SO4和NaOH溶液,分别取样后,按下图所示操作进行实验,就能达到鉴别目的的是实验________。
4.酸在初中化学中占有重要的地位。请回答下列酸的问题:
(1)医生用胃舒平(主要含Al(OH)3)来治疗胃部盐酸过多的疾病,请用方程式表示原理:__________________。改反应的本质是用_________离子反应掉胃中过多的氢离子。
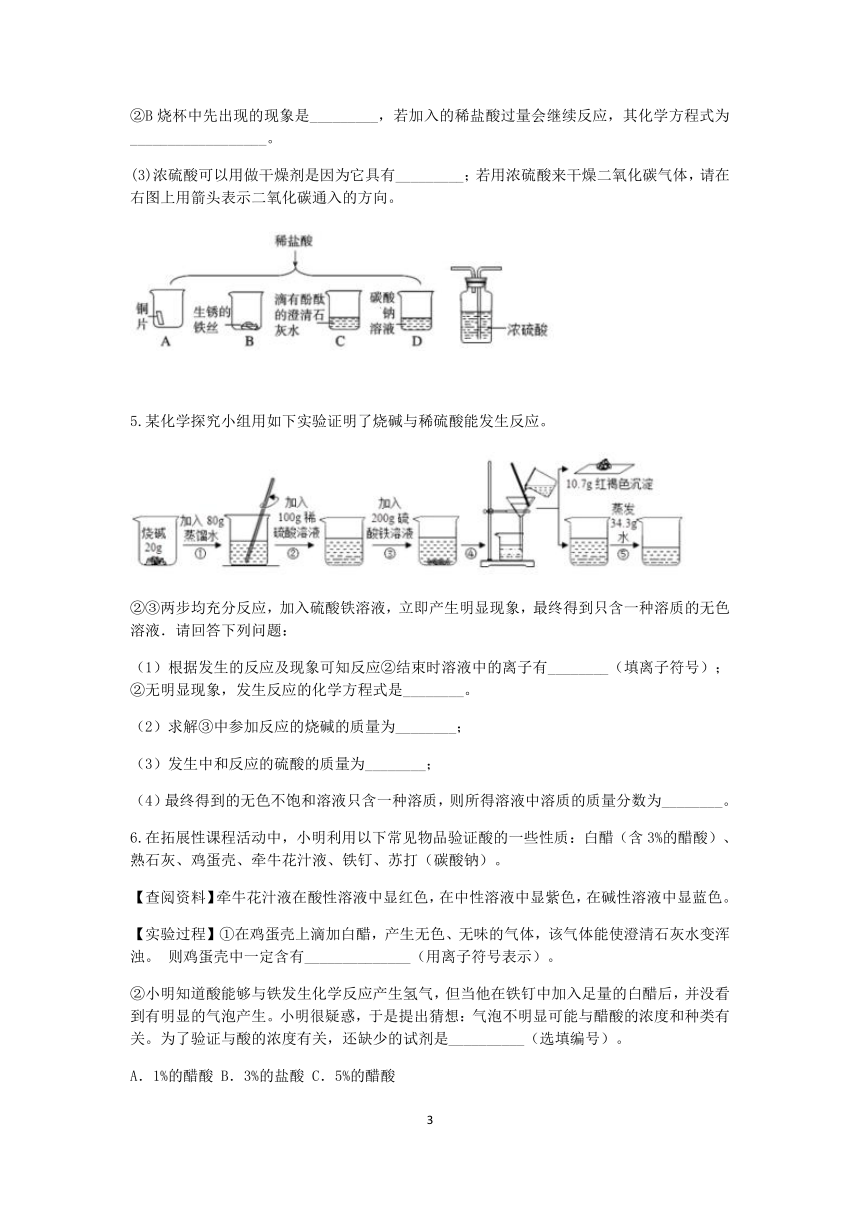
(2)如右图:①最先有气泡产生的是_________(填字母),C中发生反应的现象是_________。
②B烧杯中先出现的现象是_________,若加入的稀盐酸过量会继续反应,其化学方程式为__________________。
(3)浓硫酸可以用做干燥剂是因为它具有_________;若用浓硫酸来干燥二氧化碳气体,请在右图上用箭头表示二氧化碳通入的方向。
5.某化学探究小组用如下实验证明了烧碱与稀硫酸能发生反应。
②③两步均充分反应,加入硫酸铁溶液,立即产生明显现象,最终得到只含一种溶质的无色溶液.请回答下列问题:
(1)根据发生的反应及现象可知反应②结束时溶液中的离子有________(填离子符号);②无明显现象,发生反应的化学方程式是________。
(2)求解③中参加反应的烧碱的质量为________;
(3)发生中和反应的硫酸的质量为________;
(4)最终得到的无色不饱和溶液只含一种溶质,则所得溶液中溶质的质量分数为________。
6.在拓展性课程活动中,小明利用以下常见物品验证酸的一些性质:白醋(含3%的醋酸)、熟石灰、鸡蛋壳、牵牛花汁液、铁钉、苏打(碳酸钠)。
【查阅资料】牵牛花汁液在酸性溶液中显红色,在中性溶液中显紫色,在碱性溶液中显蓝色。
【实验过程】①在鸡蛋壳上滴加白醋,产生无色、无味的气体,该气体能使澄清石灰水变浑浊。 则鸡蛋壳中一定含有______________(用离子符号表示)。
②小明知道酸能够与铁发生化学反应产生氢气,但当他在铁钉中加入足量的白醋后,并没看到有明显的气泡产生。小明很疑惑,于是提出猜想:气泡不明显可能与醋酸的浓度和种类有关。为了验证与酸的浓度有关,还缺少的试剂是__________(选填编号)。
A.1%的醋酸 B.3%的盐酸 C.5%的醋酸
③小明利用已有物品还想验证酸与碱的反应,请你帮助完成下列实验设计。
【评价反思】科学来源于生活,生活中的一些物品能更好地帮助我们学习和理解科学。
7.为探究一瓶久置的氢氧化钠固体样品是否全部变质,小柯取少量样品配制成溶液,再取少量溶液分别装入两支试管中,进行了如甲、乙两图所示实验。(注:BaCl2溶液呈中性)
(1)小柯认为“甲图实验说明了氢氧化钠固体部分变质”。你认为小柯的观点是否正确,并说明理由____________________。
(2)分析乙图实验的现象,可以确定样品的变质情况为_____________(填“没有变质”、“部分变质”或“完全变质”)。
(3)乙图实验中加入过量BaCl2溶液的目的是__________________。
8.小金探究碳酸钠溶液与澄清石灰水的反应。
(1)碳酸钠溶液与澄清石灰水的反应的化学方程式__________________________。
(2)为确定碳酸钠溶液与澄清石灰水是否恰好完全反应,小金先将反应后的物质进行过滤,然 后对滤液的成分提出了下列四个假设: 甲:滤液中只含氢氧化钠 乙:滤液中含氢氧化钠、氢氧化钙和碳酸钠 丙:滤液中含氢氧化钠和氢氧化钙 丁:滤液中含氢氧化钠和碳酸钠 请指出哪种假设不合理,并说明理由:____________________________________。
(3)接着,小金继续进行如下探究:
小金的设计方案能说明碳酸钠溶液和澄清石灰水恰好完全反应吗?评判理由是_____________。
9.有一包白色固体,可能由硫酸钾、氢氧化钾、碳酸钙、氯化钡中的一种或几种物质组成。为探究该白色固体的组成,某小组取适量样品按如图流程进行实验.请回答下列问题:
(1)白色沉淀Ⅰ的化学式为________________
(2)白色沉淀Ⅱ的化学式为________________
(3)原白色固体中肯定没有的物质是___________(用化学式表示)。
(4)写出沉淀Ⅰ与稀盐酸反应的化学方程式________________________________。
10.某化学兴趣小组的同学在做酸碱反应时,将稀盐酸滴加到盛有氢氧化钠溶液的试管中,没有观察到明显现象(氢氧化钠未变质),该小组同学对氢氧化钠溶液与稀盐酸是否发生化学反应产生了兴趣,他们做了如下实验。
【提出猜想】稀盐酸与氢氧化钠溶液发生反应。
【收集证据】小红通过分析实验一、实验二和实验三来验证酸碱发生反应。
(1)实验一:如图1当观察到溶液由红色变成无色时可说明两种物质发生反应;
(2)实验二:如图2所示,M点溶液中溶质为___________(填化学式);
(3)实验三:如图3所示,将氢氧化钠固体放入稀盐酸中,观察到U形管中右侧红墨水液面上升,该现象不能证明氢氧化钠与稀盐酸发生了化学反应,理由是___________________。
【拓展延伸】
(4)实验四:某同学将稀盐酸滴入氢氧化钠溶液中,有气泡产生,他认为氢氧化钠溶液已经变质成Na2CO3。该同学用pH传感器测定稀盐酸与碳酸钠溶液反应过程中pH的变化。采集数据得到曲线如图 4所示。0﹣5s时,观察到溶液中并没有想象中的气泡产生,查阅资料:AB段发生反应的化学方程式为Na2CO3+HCl═NaHCO3+NaCl。5﹣10s时,观察到溶液中有气泡产生,请写出BC段发生反应的化学方程式___________________。
【反思与评价】
(5)请从微观角度分析稀盐酸与氢氧化钠溶液反应的实质_______________;由酸碱反应得出部分离子在溶液中不能共存,请再写出1组不能共存的离子_________________________。
11.兴趣小组同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验。请你与他们一起完成以下探究活动:
【对固体猜想】 猜想I:全部是NaOH;猜想Ⅱ:___________;猜想Ⅲ:_______________。
【实验和推断】
(1)完成猜想Ⅱ:________________; 猜想Ⅲ:__________________。
(2)若现象a为有气泡产生,则加入的A溶液是____________,说明氢氧化钠已经变质,有气泡产生的反应的化学方程式是_____________________。
(3)若A是Ca(OH)2溶液,现象a有白色沉淀,现象b为无色酚酞试液变红色,则白色沉淀为____________________ (填化学式),该实验_______________(填“能”或“不能”)说明样品中有NaOH。
【反思】
久置的氢氧化钠变质的原因是(用化学方程式表示) ____________________________。
12.在实验室制取二氧化碳时,大理石中含少量硫化物,使制得的CO2中混有H2S气体。欲获取纯净、干燥的CO2,需对发生装置中产生的气体进行除杂,实验装置如下:
查阅资料:I.H2S能与NaOH等碱溶液、CuSO4溶液反应。
Ⅱ.CO2中混有的HC1气体可用饱和NaHCO3溶液吸收。
(1)图1装置甲中所盛试剂应选用______(填字母)。
A.浓硫酸 B.NaOH 溶液 C.澄清石灰水 D.CuSO4溶液
(2)图1装置丙的作用是________________________。
(3)二氧化碳气体的收集装置可以选用图2中的_____________。
(4)为证明CO2和NaOH能发生反应,小高重新设计了图3所示的方案。则图3方案中所加试剂X应该是 ____________________________。
13.在研究NaOH溶液与稀盐酸反应时,某兴趣小组的同学设计并完成了如下实验:
实验1:在烧杯中注入适量NaOH溶液,测得其pH=13;然后将一定量的稀盐酸注入烧杯中与NaOH溶液充分混合,测得混合后溶液的pH=8。
实验 2:在烧杯中注入适量NaOH溶液,并滴加2滴酚酞试液,溶液呈红色;然后将一定量的稀盐酸注入烧杯中,发现红色褪去。
(1)根据实验1的现象,能否证明NaOH溶液与稀盐酸发生化学反应,请简述理由:________________。
(2)有同学猜想,实验2反应后的溶液中可能存在稀盐酸过量;利用下列试剂,不能检验该同学猜想的是____________。(选填字母)。
A 铁粉 B 氧化铜粉末 C 氢氧化铜 D AgNO3溶液
(3)写出NaOH溶液与稀盐酸反应的实质_______________。(用微观理论解释)
14.实验室现有一瓶含少量水的碳酸氢铵样品,为测定其中碳酸氢铵的质量分数,某化学兴趣小组利用如图所示装置进行实验。该装置气密性良好,装置 B、C 中所装药品均足量,碱石灰是氧化钙和氢氧化钠的混合物。已知:碳酸氢铵受热易分解,反应的化学方程式为:NH4HCO3=ΔNH3↑+H2O↑+CO2↑
部分实验步骤如下:
Ⅰ.打开弹簧夹,通入一段时间的氮气;
Ⅱ.关闭弹簧夹,给碳酸氢铵样品加热;
Ⅲ.当样品反应完全,…,再停止加热,直到玻璃管冷却;
Ⅳ.实验完毕,测得装置 B、C 中药品的质量分别增加了 m1、m2。
请回答下列问题:
(1)NH4HCO3 属于____________(填“氮肥”“磷肥”“钾肥”或“复合肥”),装置 B 中盛放
的液体是______________。
(2)步骤Ⅲ中,停止加热前应进行的操作是__________。
(3)该样品中碳酸氢铵的质量分数的表达式为:______________。(用 m1、m2 的代数式表示)。
15.不少地方喜欢吃“灰水粽”.“灰水粽”是用草木灰浸出液(俗称“灰水”)浸泡糯米做成的粽子,这种粽子清香软糯.小乐对制作“灰水粽”的草木灰展开了如下探究:
【查阅资料】①糯米中加入食用碱可中和微生物产生的酸、并能软化膳食纤维;
②草木灰中含钾盐,主要成分是 K2CO3,还有少量 K2SO4和 KCl。
【实验】检验草木灰的成分,并测定草木灰中 K2CO3的质量分数。
(1)取适量草木灰于烧杯中,加足量水浸泡,过滤得草木灰浸出液;取少量浸出液于试管中,滴加酚酞试液,观察到酚酞试液___________,说明草木灰浸出液呈碱性,可起到食用碱的作用.
(2)为了检验草木灰浸出液中存在Cl-,请写出实验的方法___________。
(3)小乐用图示装置(夹持仪器已略去)测定草木灰中 K2CO3的质量分数.实验通过测定丙装置质量的改变来计算一定质量草木灰中K2CO3的质量(草木灰中其它成分遇酸不产生气体).在滴加盐酸的过程中须持续缓缓抽气,其作用除搅拌乙、丙中的反应物外,还可以____________。
(4)有人认为通过测定丙装置质量的增加量来计算 K2CO3的质量,其结果会偏大,原因是______。
参考答案
1.(1)CaCl2 (2)猜想Ⅳ ①溶液不变红②锌粒;有气泡产生(其他合理答案均可)
2.(1)软塑料瓶变瘪(2)碳酸钠溶液和澄清石灰水都显碱性,可使酚酞变红。(3)Na2CO3 (4)向废液缸中加入足量的氯化钙溶液,溶液红色不褪去,则含有氢氧化钠。
3.(1)Na2CO3+ BaCl2= BaCO3↓+2NaCl(2)除去NaOH和Na2CO3 (3)NaOH (4)234
4.(1) 3HCl+Al(OH)3=AlCl3+3H2O;H+(2)①D 溶液由红色变成无色 ②铁锈消失,溶液变黄 Fe+2HCl=FeCl2+H2↑(3)吸水性
5.(1)Na+、OH﹣、SO42﹣;2NaOH+H2SO4═Na2SO4+2H2O(2)12g(3)9.8g(4)10%
6.(1)CO32- (2)AC(3)加入醋酸直至过量
7.(1)不对,因为碳酸钠溶液也能使酚酞变红色(2)部分变质 (3)检验碳酸钠(CO32-)的存在并除去碳酸钠(CO32-)
8.(1) Na2CO3+Ca(OH)2=CaCO3↓+2NaOH(2)因为氢氧化钙与碳酸钠会反应生成沉淀,不共存(3)不对,当氢氧化钙过量时,滴入氯化钙溶液也是无明显现象,所以不能说明是刚好完全反应
9.(1)CaCO3(2)BaCO3(3)K2SO4(硫酸钾) (4)CaCO3+2HCl==CaCl2+H2O+CO2↑
10.(2)NaCl (3)氢氧化钠固体溶于水放热 (4)NaHCO3+HCl═NaCl+H2O+CO2↑(5)氢离子和氢氧根离子结合生成水分子;Ag+、Cl-;Mg2+、OH﹣(合理即可)
11.(1)Na2CO3;NaOH和Na2CO3(答案可互换)(2)稀盐酸(合理即可)Na2CO3+2HCl=2NaCl+CO2↑+H2O(合理即可) (3)CaCO3;不能;2NaOH+CO2═Na2CO3+H2O
12.(1)D(2)除去CO2气体中的水蒸气(3)戊(4)BaCl2
13.(1)不能,滴加的稀盐酸中含水,加入使氢氧化钠溶液变稀,也会使溶液碱性减弱,PH减小(2)D (3)H++OH-=H2O
14.(1)氮肥;浓硫酸 (2)通一会N2 (3)79m2/ 44(m1+m2)
15.(1)变红(2)取少量草木灰浸出液于试管中,先加入过量的 Ba(NO3)2溶液,充分反应后过滤,往滤液中滴加AgNO3溶液和足量稀硝酸;若观察到有不溶于稀硝酸的白色沉淀,说明草木灰浸出液中 存在Cl-(3)让生成的CO2气体全部进入丙中,被NaOH溶液吸收 (4)挥发的氯化氢气体进入丙装置
《物质及其变化》实验探究训练(3)
【提出问题】该溶液中的溶质含有哪些成分?
【查阅资料】CaCl2溶液呈中性。
【猜想与假设】
(1)猜想Ⅰ:溶液中的溶质只有______________
猜想Ⅱ:溶液中的溶质有CaCl2、HCl
猜想Ⅲ:溶液中的溶质有CaCl2、Ca(OH)2
猜想Ⅳ:溶液中溶质有CaCl2、Ca(OH)2、HCl
(2)经过讨论,同学们直接得出猜想___________是不正确的。为了验证余下的哪一个猜想是正确的,同学们又做了以下实验。
【进行实验】
2.初中科学课上,同学们利用下列实验探究碱的化学性质:
(1)B实验的现象为_________________________。
实验结束后,同学们将废液倒入同一只废液缸中,
最后发现废液浑浊并显红色。
【提出问题】废液中含有什么物质?
【假设猜想】通过分析上述实验,同学们猜想:废液中除酚酞和水外一定含有氯化钠。
老师问:废液中还可能有什么物质?
(2)某同学脱口而出:废液中一定含有氢氧化钠,他的说法正确吗?同学们认为不准确,理由是:______________________________________。
【实验验证】同学们对可能含有的物质进行进一步确定,取一定量的废液过滤,向滤液中加入几滴氯化钙溶液,发现马上产生了白色沉淀。
(3)根据该现象可以确定该废液中一定还含有_____________。
【拓展提高】那么废液中是否含有氢氧化钠?
(4)请你写出在原实验的基础上作出进一步判断的方法:_______________________。
3.某白色固体甲的主要成分为NaCl,可能含有MgCl2、KCl、BaCl2和NaOH中的一种或几种杂质,为检验白色固体甲的成分并除去其中杂质,进行如下实验:
(1)写出生成白色固体丙的化学方程式________;
(2)向无色溶液D中加入过量稀盐酸的目的是________;
(3)分析上述实验可知,白色固体甲中一定没有的物质是_______;
(4)若用上述实验中的A、B、C、D四种溶液鉴别稀H2SO4和NaOH溶液,分别取样后,按下图所示操作进行实验,就能达到鉴别目的的是实验________。
4.酸在初中化学中占有重要的地位。请回答下列酸的问题:
(1)医生用胃舒平(主要含Al(OH)3)来治疗胃部盐酸过多的疾病,请用方程式表示原理:__________________。改反应的本质是用_________离子反应掉胃中过多的氢离子。
(2)如右图:①最先有气泡产生的是_________(填字母),C中发生反应的现象是_________。
②B烧杯中先出现的现象是_________,若加入的稀盐酸过量会继续反应,其化学方程式为__________________。
(3)浓硫酸可以用做干燥剂是因为它具有_________;若用浓硫酸来干燥二氧化碳气体,请在右图上用箭头表示二氧化碳通入的方向。
5.某化学探究小组用如下实验证明了烧碱与稀硫酸能发生反应。
②③两步均充分反应,加入硫酸铁溶液,立即产生明显现象,最终得到只含一种溶质的无色溶液.请回答下列问题:
(1)根据发生的反应及现象可知反应②结束时溶液中的离子有________(填离子符号);②无明显现象,发生反应的化学方程式是________。
(2)求解③中参加反应的烧碱的质量为________;
(3)发生中和反应的硫酸的质量为________;
(4)最终得到的无色不饱和溶液只含一种溶质,则所得溶液中溶质的质量分数为________。
6.在拓展性课程活动中,小明利用以下常见物品验证酸的一些性质:白醋(含3%的醋酸)、熟石灰、鸡蛋壳、牵牛花汁液、铁钉、苏打(碳酸钠)。
【查阅资料】牵牛花汁液在酸性溶液中显红色,在中性溶液中显紫色,在碱性溶液中显蓝色。
【实验过程】①在鸡蛋壳上滴加白醋,产生无色、无味的气体,该气体能使澄清石灰水变浑浊。 则鸡蛋壳中一定含有______________(用离子符号表示)。
②小明知道酸能够与铁发生化学反应产生氢气,但当他在铁钉中加入足量的白醋后,并没看到有明显的气泡产生。小明很疑惑,于是提出猜想:气泡不明显可能与醋酸的浓度和种类有关。为了验证与酸的浓度有关,还缺少的试剂是__________(选填编号)。
A.1%的醋酸 B.3%的盐酸 C.5%的醋酸
③小明利用已有物品还想验证酸与碱的反应,请你帮助完成下列实验设计。
【评价反思】科学来源于生活,生活中的一些物品能更好地帮助我们学习和理解科学。
7.为探究一瓶久置的氢氧化钠固体样品是否全部变质,小柯取少量样品配制成溶液,再取少量溶液分别装入两支试管中,进行了如甲、乙两图所示实验。(注:BaCl2溶液呈中性)
(1)小柯认为“甲图实验说明了氢氧化钠固体部分变质”。你认为小柯的观点是否正确,并说明理由____________________。
(2)分析乙图实验的现象,可以确定样品的变质情况为_____________(填“没有变质”、“部分变质”或“完全变质”)。
(3)乙图实验中加入过量BaCl2溶液的目的是__________________。
8.小金探究碳酸钠溶液与澄清石灰水的反应。
(1)碳酸钠溶液与澄清石灰水的反应的化学方程式__________________________。
(2)为确定碳酸钠溶液与澄清石灰水是否恰好完全反应,小金先将反应后的物质进行过滤,然 后对滤液的成分提出了下列四个假设: 甲:滤液中只含氢氧化钠 乙:滤液中含氢氧化钠、氢氧化钙和碳酸钠 丙:滤液中含氢氧化钠和氢氧化钙 丁:滤液中含氢氧化钠和碳酸钠 请指出哪种假设不合理,并说明理由:____________________________________。
(3)接着,小金继续进行如下探究:
小金的设计方案能说明碳酸钠溶液和澄清石灰水恰好完全反应吗?评判理由是_____________。
9.有一包白色固体,可能由硫酸钾、氢氧化钾、碳酸钙、氯化钡中的一种或几种物质组成。为探究该白色固体的组成,某小组取适量样品按如图流程进行实验.请回答下列问题:
(1)白色沉淀Ⅰ的化学式为________________
(2)白色沉淀Ⅱ的化学式为________________
(3)原白色固体中肯定没有的物质是___________(用化学式表示)。
(4)写出沉淀Ⅰ与稀盐酸反应的化学方程式________________________________。
10.某化学兴趣小组的同学在做酸碱反应时,将稀盐酸滴加到盛有氢氧化钠溶液的试管中,没有观察到明显现象(氢氧化钠未变质),该小组同学对氢氧化钠溶液与稀盐酸是否发生化学反应产生了兴趣,他们做了如下实验。
【提出猜想】稀盐酸与氢氧化钠溶液发生反应。
【收集证据】小红通过分析实验一、实验二和实验三来验证酸碱发生反应。
(1)实验一:如图1当观察到溶液由红色变成无色时可说明两种物质发生反应;
(2)实验二:如图2所示,M点溶液中溶质为___________(填化学式);
(3)实验三:如图3所示,将氢氧化钠固体放入稀盐酸中,观察到U形管中右侧红墨水液面上升,该现象不能证明氢氧化钠与稀盐酸发生了化学反应,理由是___________________。
【拓展延伸】
(4)实验四:某同学将稀盐酸滴入氢氧化钠溶液中,有气泡产生,他认为氢氧化钠溶液已经变质成Na2CO3。该同学用pH传感器测定稀盐酸与碳酸钠溶液反应过程中pH的变化。采集数据得到曲线如图 4所示。0﹣5s时,观察到溶液中并没有想象中的气泡产生,查阅资料:AB段发生反应的化学方程式为Na2CO3+HCl═NaHCO3+NaCl。5﹣10s时,观察到溶液中有气泡产生,请写出BC段发生反应的化学方程式___________________。
【反思与评价】
(5)请从微观角度分析稀盐酸与氢氧化钠溶液反应的实质_______________;由酸碱反应得出部分离子在溶液中不能共存,请再写出1组不能共存的离子_________________________。
11.兴趣小组同学为了探究实验室中久置的氢氧化钠固体的成分,进行了有关实验。请你与他们一起完成以下探究活动:
【对固体猜想】 猜想I:全部是NaOH;猜想Ⅱ:___________;猜想Ⅲ:_______________。
【实验和推断】
(1)完成猜想Ⅱ:________________; 猜想Ⅲ:__________________。
(2)若现象a为有气泡产生,则加入的A溶液是____________,说明氢氧化钠已经变质,有气泡产生的反应的化学方程式是_____________________。
(3)若A是Ca(OH)2溶液,现象a有白色沉淀,现象b为无色酚酞试液变红色,则白色沉淀为____________________ (填化学式),该实验_______________(填“能”或“不能”)说明样品中有NaOH。
【反思】
久置的氢氧化钠变质的原因是(用化学方程式表示) ____________________________。
12.在实验室制取二氧化碳时,大理石中含少量硫化物,使制得的CO2中混有H2S气体。欲获取纯净、干燥的CO2,需对发生装置中产生的气体进行除杂,实验装置如下:
查阅资料:I.H2S能与NaOH等碱溶液、CuSO4溶液反应。
Ⅱ.CO2中混有的HC1气体可用饱和NaHCO3溶液吸收。
(1)图1装置甲中所盛试剂应选用______(填字母)。
A.浓硫酸 B.NaOH 溶液 C.澄清石灰水 D.CuSO4溶液
(2)图1装置丙的作用是________________________。
(3)二氧化碳气体的收集装置可以选用图2中的_____________。
(4)为证明CO2和NaOH能发生反应,小高重新设计了图3所示的方案。则图3方案中所加试剂X应该是 ____________________________。
13.在研究NaOH溶液与稀盐酸反应时,某兴趣小组的同学设计并完成了如下实验:
实验1:在烧杯中注入适量NaOH溶液,测得其pH=13;然后将一定量的稀盐酸注入烧杯中与NaOH溶液充分混合,测得混合后溶液的pH=8。
实验 2:在烧杯中注入适量NaOH溶液,并滴加2滴酚酞试液,溶液呈红色;然后将一定量的稀盐酸注入烧杯中,发现红色褪去。
(1)根据实验1的现象,能否证明NaOH溶液与稀盐酸发生化学反应,请简述理由:________________。
(2)有同学猜想,实验2反应后的溶液中可能存在稀盐酸过量;利用下列试剂,不能检验该同学猜想的是____________。(选填字母)。
A 铁粉 B 氧化铜粉末 C 氢氧化铜 D AgNO3溶液
(3)写出NaOH溶液与稀盐酸反应的实质_______________。(用微观理论解释)
14.实验室现有一瓶含少量水的碳酸氢铵样品,为测定其中碳酸氢铵的质量分数,某化学兴趣小组利用如图所示装置进行实验。该装置气密性良好,装置 B、C 中所装药品均足量,碱石灰是氧化钙和氢氧化钠的混合物。已知:碳酸氢铵受热易分解,反应的化学方程式为:NH4HCO3=ΔNH3↑+H2O↑+CO2↑
部分实验步骤如下:
Ⅰ.打开弹簧夹,通入一段时间的氮气;
Ⅱ.关闭弹簧夹,给碳酸氢铵样品加热;
Ⅲ.当样品反应完全,…,再停止加热,直到玻璃管冷却;
Ⅳ.实验完毕,测得装置 B、C 中药品的质量分别增加了 m1、m2。
请回答下列问题:
(1)NH4HCO3 属于____________(填“氮肥”“磷肥”“钾肥”或“复合肥”),装置 B 中盛放
的液体是______________。
(2)步骤Ⅲ中,停止加热前应进行的操作是__________。
(3)该样品中碳酸氢铵的质量分数的表达式为:______________。(用 m1、m2 的代数式表示)。
15.不少地方喜欢吃“灰水粽”.“灰水粽”是用草木灰浸出液(俗称“灰水”)浸泡糯米做成的粽子,这种粽子清香软糯.小乐对制作“灰水粽”的草木灰展开了如下探究:
【查阅资料】①糯米中加入食用碱可中和微生物产生的酸、并能软化膳食纤维;
②草木灰中含钾盐,主要成分是 K2CO3,还有少量 K2SO4和 KCl。
【实验】检验草木灰的成分,并测定草木灰中 K2CO3的质量分数。
(1)取适量草木灰于烧杯中,加足量水浸泡,过滤得草木灰浸出液;取少量浸出液于试管中,滴加酚酞试液,观察到酚酞试液___________,说明草木灰浸出液呈碱性,可起到食用碱的作用.
(2)为了检验草木灰浸出液中存在Cl-,请写出实验的方法___________。
(3)小乐用图示装置(夹持仪器已略去)测定草木灰中 K2CO3的质量分数.实验通过测定丙装置质量的改变来计算一定质量草木灰中K2CO3的质量(草木灰中其它成分遇酸不产生气体).在滴加盐酸的过程中须持续缓缓抽气,其作用除搅拌乙、丙中的反应物外,还可以____________。
(4)有人认为通过测定丙装置质量的增加量来计算 K2CO3的质量,其结果会偏大,原因是______。
参考答案
1.(1)CaCl2 (2)猜想Ⅳ ①溶液不变红②锌粒;有气泡产生(其他合理答案均可)
2.(1)软塑料瓶变瘪(2)碳酸钠溶液和澄清石灰水都显碱性,可使酚酞变红。(3)Na2CO3 (4)向废液缸中加入足量的氯化钙溶液,溶液红色不褪去,则含有氢氧化钠。
3.(1)Na2CO3+ BaCl2= BaCO3↓+2NaCl(2)除去NaOH和Na2CO3 (3)NaOH (4)234
4.(1) 3HCl+Al(OH)3=AlCl3+3H2O;H+(2)①D 溶液由红色变成无色 ②铁锈消失,溶液变黄 Fe+2HCl=FeCl2+H2↑(3)吸水性
5.(1)Na+、OH﹣、SO42﹣;2NaOH+H2SO4═Na2SO4+2H2O(2)12g(3)9.8g(4)10%
6.(1)CO32- (2)AC(3)加入醋酸直至过量
7.(1)不对,因为碳酸钠溶液也能使酚酞变红色(2)部分变质 (3)检验碳酸钠(CO32-)的存在并除去碳酸钠(CO32-)
8.(1) Na2CO3+Ca(OH)2=CaCO3↓+2NaOH(2)因为氢氧化钙与碳酸钠会反应生成沉淀,不共存(3)不对,当氢氧化钙过量时,滴入氯化钙溶液也是无明显现象,所以不能说明是刚好完全反应
9.(1)CaCO3(2)BaCO3(3)K2SO4(硫酸钾) (4)CaCO3+2HCl==CaCl2+H2O+CO2↑
10.(2)NaCl (3)氢氧化钠固体溶于水放热 (4)NaHCO3+HCl═NaCl+H2O+CO2↑(5)氢离子和氢氧根离子结合生成水分子;Ag+、Cl-;Mg2+、OH﹣(合理即可)
11.(1)Na2CO3;NaOH和Na2CO3(答案可互换)(2)稀盐酸(合理即可)Na2CO3+2HCl=2NaCl+CO2↑+H2O(合理即可) (3)CaCO3;不能;2NaOH+CO2═Na2CO3+H2O
12.(1)D(2)除去CO2气体中的水蒸气(3)戊(4)BaCl2
13.(1)不能,滴加的稀盐酸中含水,加入使氢氧化钠溶液变稀,也会使溶液碱性减弱,PH减小(2)D (3)H++OH-=H2O
14.(1)氮肥;浓硫酸 (2)通一会N2 (3)79m2/ 44(m1+m2)
15.(1)变红(2)取少量草木灰浸出液于试管中,先加入过量的 Ba(NO3)2溶液,充分反应后过滤,往滤液中滴加AgNO3溶液和足量稀硝酸;若观察到有不溶于稀硝酸的白色沉淀,说明草木灰浸出液中 存在Cl-(3)让生成的CO2气体全部进入丙中,被NaOH溶液吸收 (4)挥发的氯化氢气体进入丙装置
《物质及其变化》实验探究训练(3)
同课章节目录
- 第1章 物质及其变化
- 第1节 物质的变化
- 第2节 物质的酸碱性
- 第3节 常见的酸
- 第4节 常见的碱
- 第5节 酸和碱之间发生的反应
- 第6节 几种重要的盐
- 第2章 物质转化与材料利用
- 第1节 金属材料
- 第2节 金属的化学性质
- 第3节 有机物和有机合成材料
- 第4节 物质的分类
- 第5节 物质的转化
- 第6节 材料的利用与发展
- 第3章 能量的转化与守恒
- 第1节 能量及其形式
- 第2节 机械能
- 第3节 能量转化的量度
- 第4节 简单机械
- 第5节 物体的内能
- 第6节 电能
- 第7节 核能
- 第8节 能量的转化与守恒
- 第4章 代谢与平衡
- 第1节 食物与营养
- 第2节 食物的消化与吸收
- 第3节 体内物质的运输
- 第4节 能量的获得
- 第5节 体内物质的动态平衡
- 研究性学习课题
- 一 当地酸雨情况以及对农作物和建筑物的影响
- 二 金属对社会发展的作用
- 三 寻找自行车中的杠杆
- 四 怎样防治龋齿
