人教版化学九年级上册课件 第五单元课题1《质量守恒定律》 (共27张PPT)
文档属性
| 名称 | 人教版化学九年级上册课件 第五单元课题1《质量守恒定律》 (共27张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 36.1MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-09-29 00:00:00 | ||
图片预览







文档简介
(共27张PPT)
人教版九年级化学上册第五单元化学方程式
课题1 质量守恒定律
引入新课
狄仁杰遇到的两个困惑:
1.为什么蜡烛燃烧后质量会
变小了呢?
2.为什么铁刀放置一段时间
后质量会增加呢?
知识与技能
1、认识质量守恒定律,并能运用质量守恒定律解释,解决一些化学现象和问题。
2、从微观角度认识质量守恒定律的本质。
过程与方法
在探究活动中,培养学生运用实验的方法定量研究问题和分析问题的科学探究能力。
情感态度与价值观
培养学生团结协作的团队精神,树立透过现象看本质的辩证唯物主义观点。
学习目标
提出问题
参加化学反应的各物质质量总和与反应后生成的各物质质量总和之间有何关系?
猜一猜
作出猜想
反应前各物质质量总和 反应后各物质质量总和
反应前各物质质量总和 反应后各物质质量总和
反应前各物质质量总和 反应后各物质质量总和
实验探究
红磷燃烧前后质量总和的测定
玻璃管
细沙
演示实 验
注意观察:1、锥形瓶内红磷燃烧的现象;
2、化学反应前后质量的变化情况。
实验探究
演示实验
现象:
产生大量白烟,放出大量热
气球先变大后变小
结论:反应前各物质质量总和 反应后各物质质量总和
=
物质总质量相等,天平平衡
红磷燃烧前后质量总和的测定
实验探究
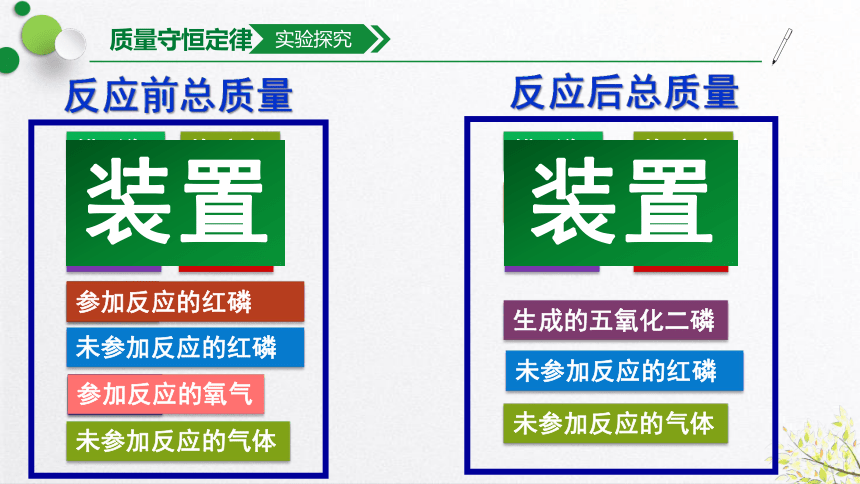
反应前总质量
红 磷
空 气
玻璃管
气 球
棉 线
橡胶塞
细 沙
锥形瓶
未参加反应的红磷
生成的五氧化二磷
参加反应的红磷
参加反应的氧气
未参加反应的气体
反应后总质量
锥形瓶
橡胶塞
玻璃管
气 球
细 沙
棉 线
未参加反应的红磷
未参加反应的气体
装置
装置
实验探究
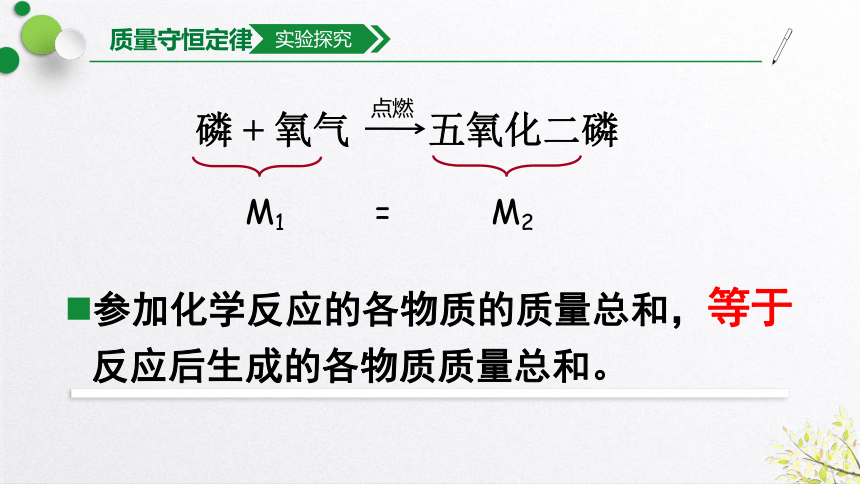
参加化学反应的各物质的质量总和,等于反应后生成的各物质质量总和。
M1 = M2
磷 + 氧气 五氧化二磷
点燃
实验探究
分组实验
1、铁钉与硫酸铜溶液反应前后质量总和的测定
2、碳酸钠与稀盐酸反应前后质量总和的测定
铁 + 硫酸铜 铜 + 硫酸亚铁
碳酸钠 + 盐酸 氯化钠 + 二氧化碳 + 水
实验探究
温馨提示
1. 根据给定的药品与器材,自行设计实验方案,小组讨
论、确定方案
2. 进行实验,分工合作,记录现象,实验数据
实验目的
实验仪器
实验药品
实验现象
实验结论
实验探究
成果展示
铁钉表面有红色固体物质析出,溶液由蓝色
变成浅绿色。天平平衡
托盘天平、烧杯、镊子
铁钉、硫酸铜溶液
反应前各物质质量总和=反应后各物质质量总和
探究铁钉与硫酸铜溶液反应前后质量总和的关系
实验探究
参加化学反应的各物质的质量总和,等于反应后生成的各物质质量总和。
M1 = M2
铁 + 硫酸铜 铜 + 硫酸亚铁
实验目的
实验仪器
实验药品
实验现象
实验结论
实验探究
成果展示
固体减少,产生大量气泡。天平指针向右偏转,天平不平衡,
碳酸钠、稀盐酸
反应前各物质质量总和 > 反应后各物质质量总和
托盘天平、烧杯、小试管、药匙
探究碳酸钠与稀盐酸反应前后质量总和的关系
实验探究
小组讨论:组装密闭装置
实验结论
参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。
质量守恒定律
只适用于化学变化,物理变化不能用质量守恒定律解释!
守恒的是“总质量”,即“参加反应的各反应物的总质量”和“生成物的总质量”如沉淀、气体等都应考虑进去
“参加”,意味着没有参加反应(剩余)的物质的质量不能算在内。
1、10克水遇冷凝结成10克冰,这一变化符合质量守恒定律,这句话对么?
2、根据质量守恒定律,2L氢气和1L氧气能反应生成3L水。这句话对么?
3、现有一反应A+B—C,有10克A和5克B,反应结束后剩余3克A,B无剩余,则生成C的质量是多少克?
深化理解
不对
不对
12克
为什么化学反应前后的物质的质量总和相等呢?
微观解释
想 一 想
水 氢气 + 氧气
通电
H
O
O
O
H
H
H
H
微观解释
质量守恒的原因
原子的种类没有改变
原子的数目没有增减
原子的质量没有改变
拓展应用
狄仁杰遇到的两个困惑:
1.为什么蜡烛燃烧后质量会变
小了呢?
2.为什么铁刀放置一段时间后
质量会增加呢?
归纳总结
从知识层面上……
从学习方法方面……
从学科思想角度……
…… ……
达标检测
1、下列现象不能用质量守恒定律解释的是( )
A.碳燃烧后质量减轻
B.100g水和100g酒精混合,总质量为200g
C.白磷在密闭容器中燃烧,反应前后总质量不变
D.高锰酸钾受热分解后,剩余固体质量比原反应物的质量小
2、化学反应遵守质量守恒定律的原因是( )
A.物质的种类没有改变 B.分子的种类没有改变
C.分子的数目没有改变 D.原子的种类、数目、质量都没有改变
3、“84消毒剂”的有效成分是次氯酸钠,制备次氯酸钠的原理可表示为: 2NaOH+Cl2==NaClO+X+H2O,则X的化学式为( )
A.Na2O B.NaCl C.NaH D.NaClO2
B
D
B
C
达标检测
4、质量守恒定律是一条重要规律,根据该规律回答:(1)原子的数目(2)分子的数目(3)元素的种类(4)物质的种类(5)原子的种类(6)物质的总质量(7)原子的质量(8)分子的种类(9)元素的质量
以上各项中,在化学反应前后,一定发生改变的是 ,一定不发生改变的是 ,可能发生改变的是 。
5、某纯净物在氧气中燃烧生成了二氧化硫和水,根据质量守恒定律推断,该物质中一定含有的元素是( )
A.氢和氧 B.硫和氧 C.氢和硫 D.硫、氢和氧
达标检测
6、现将A、B两种物质各10g混合加热,A完全反应,生成8g的C和4g的D,则参加反应的A和B的质量比是( )
A.1:1 B.2:1 C.4:1 D.5:1
7、一定条件下,甲、乙、丙、丁四种物质在密闭容器中充分反应,测得反应前后各物质的质量如下所示,下列说法正确的是( )
A.表中“a”的值为10 B.丁可能是该反应的催化剂
C.该反应为化合反应 D.反应中乙、丙变化的质量比为15:1
物质 甲 乙 丙 丁
反应前质量/g 120 90 6 5
反应后质量/g 86 108 22 a
D
B
布置作业
1、水能变成汽油,它会实现么?
2.点石成金的故事,它会成真么?
资 料 简 介
爱因斯坦提出质能公式,人们又认识到能量守恒定律。
英国化学家曼莱做了精确实验,质量变化小于千万分之一。因此科学家一致承认了这一定律。
提出假设
验证假设
验证定律
1756年
1777年
1912年
1916年
俄国化学家罗蒙诺索夫把锡放在密闭容器里燃烧,燃烧前后物质总质量不变。于是他提出在化学变化中物质总质量是守恒的。
法国化学家拉瓦锡做了大量的实验,也得到同样的结论,从而验证了罗蒙诺索夫的假设。
不断探索
聆
听
谢
谢
人教版九年级化学上册第五单元化学方程式
课题1 质量守恒定律
引入新课
狄仁杰遇到的两个困惑:
1.为什么蜡烛燃烧后质量会
变小了呢?
2.为什么铁刀放置一段时间
后质量会增加呢?
知识与技能
1、认识质量守恒定律,并能运用质量守恒定律解释,解决一些化学现象和问题。
2、从微观角度认识质量守恒定律的本质。
过程与方法
在探究活动中,培养学生运用实验的方法定量研究问题和分析问题的科学探究能力。
情感态度与价值观
培养学生团结协作的团队精神,树立透过现象看本质的辩证唯物主义观点。
学习目标
提出问题
参加化学反应的各物质质量总和与反应后生成的各物质质量总和之间有何关系?
猜一猜
作出猜想
反应前各物质质量总和 反应后各物质质量总和
反应前各物质质量总和 反应后各物质质量总和
反应前各物质质量总和 反应后各物质质量总和
实验探究
红磷燃烧前后质量总和的测定
玻璃管
细沙
演示实 验
注意观察:1、锥形瓶内红磷燃烧的现象;
2、化学反应前后质量的变化情况。
实验探究
演示实验
现象:
产生大量白烟,放出大量热
气球先变大后变小
结论:反应前各物质质量总和 反应后各物质质量总和
=
物质总质量相等,天平平衡
红磷燃烧前后质量总和的测定
实验探究
反应前总质量
红 磷
空 气
玻璃管
气 球
棉 线
橡胶塞
细 沙
锥形瓶
未参加反应的红磷
生成的五氧化二磷
参加反应的红磷
参加反应的氧气
未参加反应的气体
反应后总质量
锥形瓶
橡胶塞
玻璃管
气 球
细 沙
棉 线
未参加反应的红磷
未参加反应的气体
装置
装置
实验探究
参加化学反应的各物质的质量总和,等于反应后生成的各物质质量总和。
M1 = M2
磷 + 氧气 五氧化二磷
点燃
实验探究
分组实验
1、铁钉与硫酸铜溶液反应前后质量总和的测定
2、碳酸钠与稀盐酸反应前后质量总和的测定
铁 + 硫酸铜 铜 + 硫酸亚铁
碳酸钠 + 盐酸 氯化钠 + 二氧化碳 + 水
实验探究
温馨提示
1. 根据给定的药品与器材,自行设计实验方案,小组讨
论、确定方案
2. 进行实验,分工合作,记录现象,实验数据
实验目的
实验仪器
实验药品
实验现象
实验结论
实验探究
成果展示
铁钉表面有红色固体物质析出,溶液由蓝色
变成浅绿色。天平平衡
托盘天平、烧杯、镊子
铁钉、硫酸铜溶液
反应前各物质质量总和=反应后各物质质量总和
探究铁钉与硫酸铜溶液反应前后质量总和的关系
实验探究
参加化学反应的各物质的质量总和,等于反应后生成的各物质质量总和。
M1 = M2
铁 + 硫酸铜 铜 + 硫酸亚铁
实验目的
实验仪器
实验药品
实验现象
实验结论
实验探究
成果展示
固体减少,产生大量气泡。天平指针向右偏转,天平不平衡,
碳酸钠、稀盐酸
反应前各物质质量总和 > 反应后各物质质量总和
托盘天平、烧杯、小试管、药匙
探究碳酸钠与稀盐酸反应前后质量总和的关系
实验探究
小组讨论:组装密闭装置
实验结论
参加化学反应的各物质的质量总和等于反应后生成的各物质的质量总和。
质量守恒定律
只适用于化学变化,物理变化不能用质量守恒定律解释!
守恒的是“总质量”,即“参加反应的各反应物的总质量”和“生成物的总质量”如沉淀、气体等都应考虑进去
“参加”,意味着没有参加反应(剩余)的物质的质量不能算在内。
1、10克水遇冷凝结成10克冰,这一变化符合质量守恒定律,这句话对么?
2、根据质量守恒定律,2L氢气和1L氧气能反应生成3L水。这句话对么?
3、现有一反应A+B—C,有10克A和5克B,反应结束后剩余3克A,B无剩余,则生成C的质量是多少克?
深化理解
不对
不对
12克
为什么化学反应前后的物质的质量总和相等呢?
微观解释
想 一 想
水 氢气 + 氧气
通电
H
O
O
O
H
H
H
H
微观解释
质量守恒的原因
原子的种类没有改变
原子的数目没有增减
原子的质量没有改变
拓展应用
狄仁杰遇到的两个困惑:
1.为什么蜡烛燃烧后质量会变
小了呢?
2.为什么铁刀放置一段时间后
质量会增加呢?
归纳总结
从知识层面上……
从学习方法方面……
从学科思想角度……
…… ……
达标检测
1、下列现象不能用质量守恒定律解释的是( )
A.碳燃烧后质量减轻
B.100g水和100g酒精混合,总质量为200g
C.白磷在密闭容器中燃烧,反应前后总质量不变
D.高锰酸钾受热分解后,剩余固体质量比原反应物的质量小
2、化学反应遵守质量守恒定律的原因是( )
A.物质的种类没有改变 B.分子的种类没有改变
C.分子的数目没有改变 D.原子的种类、数目、质量都没有改变
3、“84消毒剂”的有效成分是次氯酸钠,制备次氯酸钠的原理可表示为: 2NaOH+Cl2==NaClO+X+H2O,则X的化学式为( )
A.Na2O B.NaCl C.NaH D.NaClO2
B
D
B
C
达标检测
4、质量守恒定律是一条重要规律,根据该规律回答:(1)原子的数目(2)分子的数目(3)元素的种类(4)物质的种类(5)原子的种类(6)物质的总质量(7)原子的质量(8)分子的种类(9)元素的质量
以上各项中,在化学反应前后,一定发生改变的是 ,一定不发生改变的是 ,可能发生改变的是 。
5、某纯净物在氧气中燃烧生成了二氧化硫和水,根据质量守恒定律推断,该物质中一定含有的元素是( )
A.氢和氧 B.硫和氧 C.氢和硫 D.硫、氢和氧
达标检测
6、现将A、B两种物质各10g混合加热,A完全反应,生成8g的C和4g的D,则参加反应的A和B的质量比是( )
A.1:1 B.2:1 C.4:1 D.5:1
7、一定条件下,甲、乙、丙、丁四种物质在密闭容器中充分反应,测得反应前后各物质的质量如下所示,下列说法正确的是( )
A.表中“a”的值为10 B.丁可能是该反应的催化剂
C.该反应为化合反应 D.反应中乙、丙变化的质量比为15:1
物质 甲 乙 丙 丁
反应前质量/g 120 90 6 5
反应后质量/g 86 108 22 a
D
B
布置作业
1、水能变成汽油,它会实现么?
2.点石成金的故事,它会成真么?
资 料 简 介
爱因斯坦提出质能公式,人们又认识到能量守恒定律。
英国化学家曼莱做了精确实验,质量变化小于千万分之一。因此科学家一致承认了这一定律。
提出假设
验证假设
验证定律
1756年
1777年
1912年
1916年
俄国化学家罗蒙诺索夫把锡放在密闭容器里燃烧,燃烧前后物质总质量不变。于是他提出在化学变化中物质总质量是守恒的。
法国化学家拉瓦锡做了大量的实验,也得到同样的结论,从而验证了罗蒙诺索夫的假设。
不断探索
聆
听
谢
谢
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
