1.3 细胞中的蛋白质 课件(共45张PPT)
文档属性
| 名称 | 1.3 细胞中的蛋白质 课件(共45张PPT) |

|
|
| 格式 | pptx | ||
| 文件大小 | 9.8MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 苏教版(2019) | ||
| 科目 | 生物学 | ||
| 更新时间 | 2022-09-27 00:00:00 | ||
图片预览




文档简介
(共45张PPT)
第1章 细胞的分子组成
第3节 细胞中的蛋白质
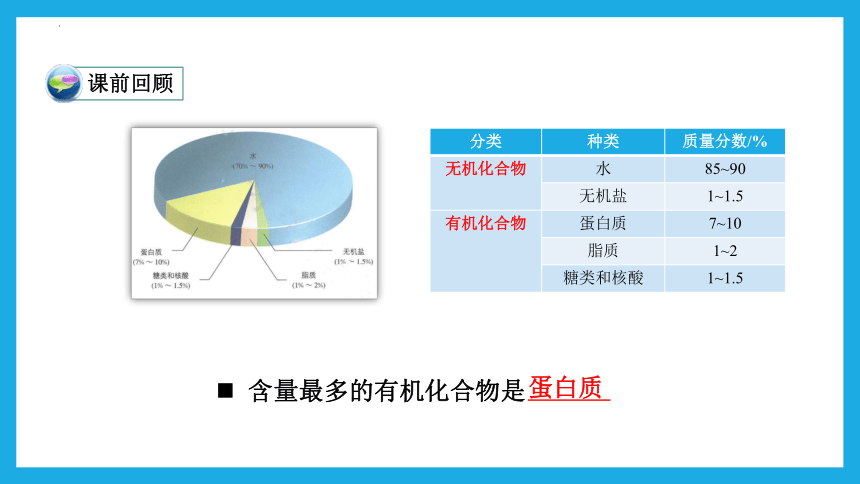
课前回顾
分类 种类 质量分数/%
无机化合物 水 85~90
无机盐 1~1.5
有机化合物 蛋白质 7~10
脂质 1~2
糖类和核酸 1~1.5
含量最多的有机化合物是
蛋白质
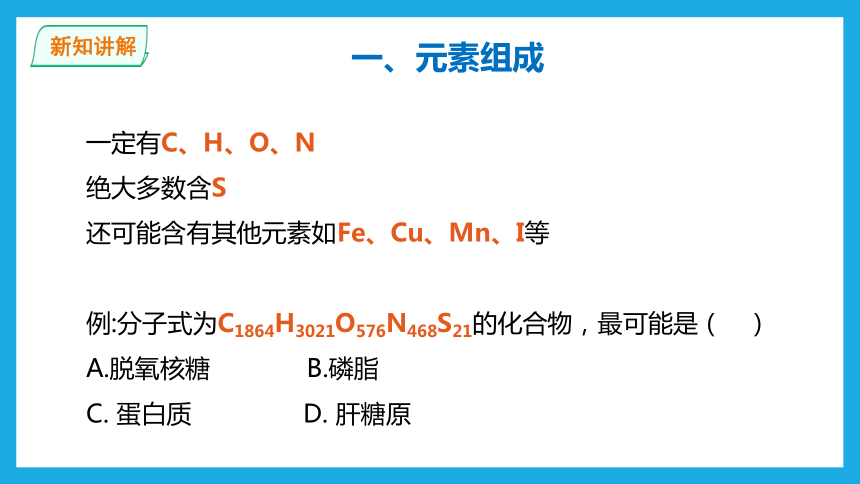
一、元素组成
一定有C、H、O、N
绝大多数含S
还可能含有其他元素如Fe、Cu、Mn、I等
例:分子式为C1864H3021O576N468S21的化合物,最可能是( )
A.脱氧核糖 B.磷脂
C. 蛋白质 D. 肝糖原
新知讲解
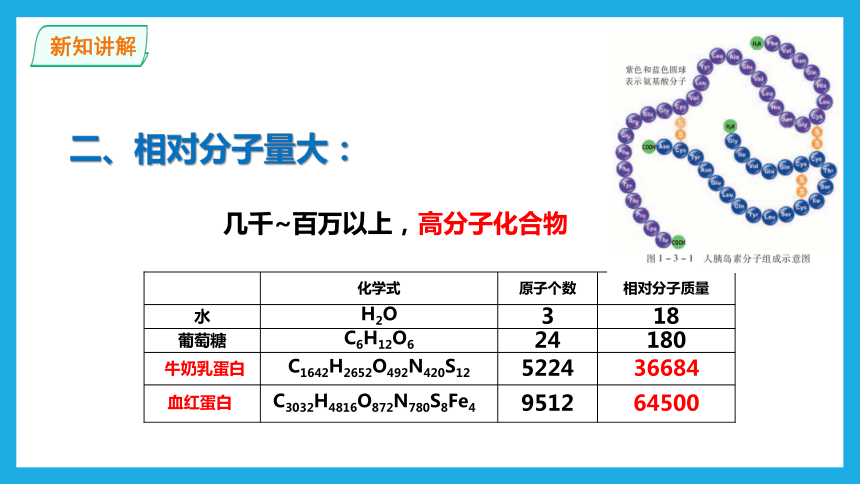
二、相对分子量大:
64500
9512
C3032H4816O872N780S8Fe4
血红蛋白
36684
5224
C1642H2652O492N420S12
牛奶乳蛋白
180
24
C6H12O6
葡萄糖
18
3
H2O
水
相对分子质量
原子个数
化学式
几千~百万以上,高分子化合物
新知讲解
回答:蛋白质含量比较丰富的食物?
奶类
蛋类
瘦肉类
豆类
思考: 我们从食物中摄取的蛋白质如何为我们所用?
蛋白质必需经过消化成氨基酸才能被人体吸收和利用。
氨基酸是组成蛋白质的基本单位。
三、蛋白质的基本组成单位——氨基酸
新知讲解
C
H
C
H
H2N
OH
O
C
H
C
H2N
OH
O
CH3
CH3
CH
C
H
C
H2N
OH
O
CH3
C
H
C
H2N
OH
O
CH2
CH3
CH3
CH
甘氨酸
缬氨酸
丙氨酸
亮氨酸
几种氨基酸的结构式
问题1 :这些氨基酸的结构具有什么共同特点?
问题2:不同氨基酸的区别又在哪里?
—NH2 (氨基)
—COOH (羧基)
R基
—H (氢原子)
—R (R基)侧链基团
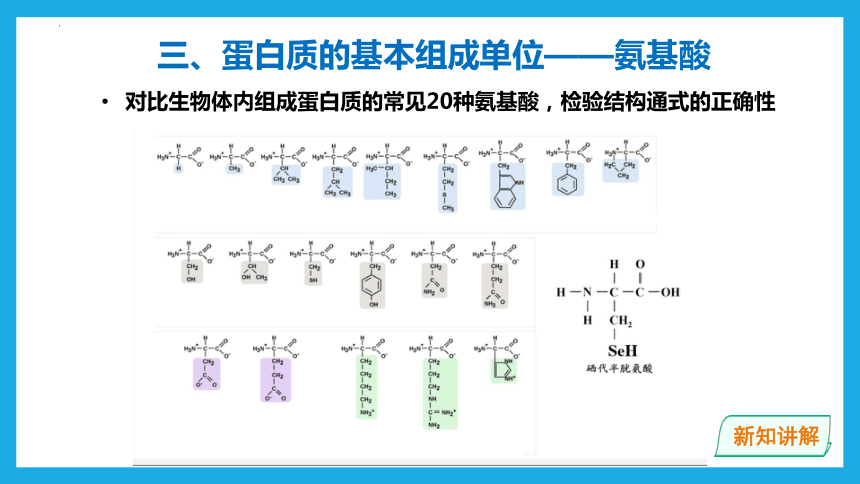
对比生物体内组成蛋白质的常见20种氨基酸,检验结构通式的正确性
三、蛋白质的基本组成单位——氨基酸
新知讲解
三、蛋白质的基本组成单位——氨基酸
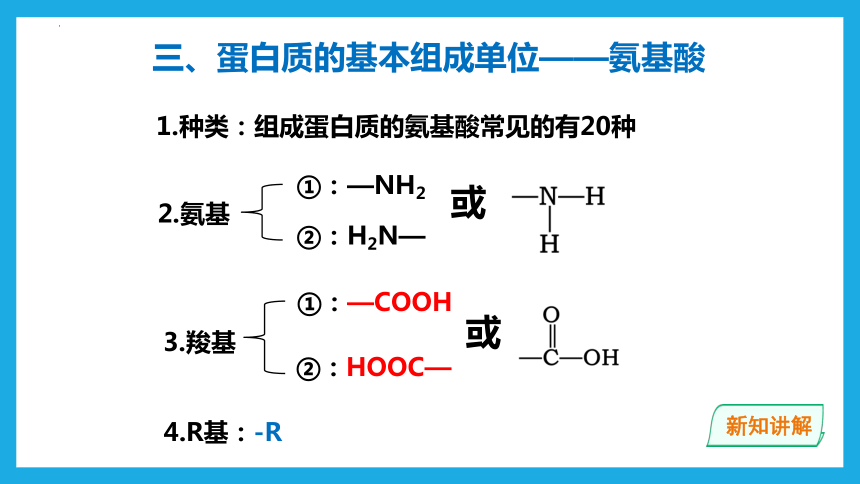
1.种类:组成蛋白质的氨基酸常见的有20种
2.氨基
①:—NH2
②:H2N—
或
3.羧基
①:—COOH
②:HOOC—
或
4.R基:-R
新知讲解
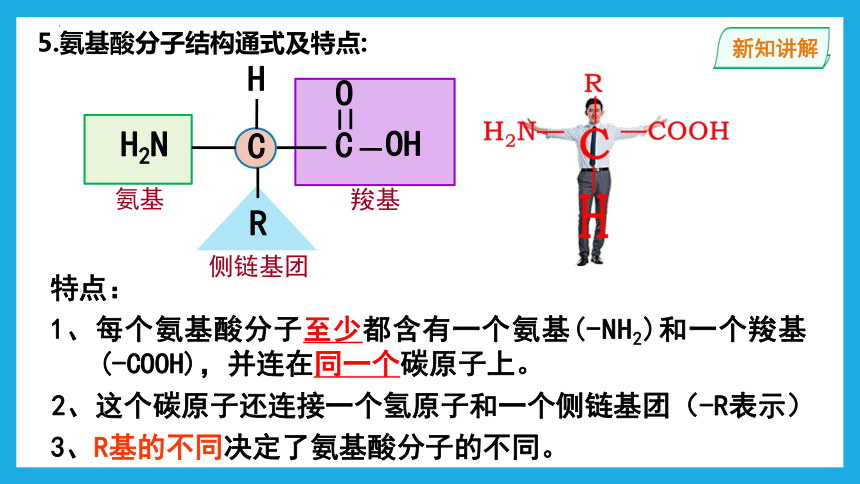
5.氨基酸分子结构通式及特点:
新知讲解
C
R
C
H2N
OH
O
H
氨基
羧基
侧链基团
特点:
1、每个氨基酸分子至少都含有一个氨基(-NH2)和一个羧基(-COOH),并连在同一个碳原子上。
2、这个碳原子还连接一个氢原子和一个侧链基团(-R表示)
3、R基的不同决定了氨基酸分子的不同。
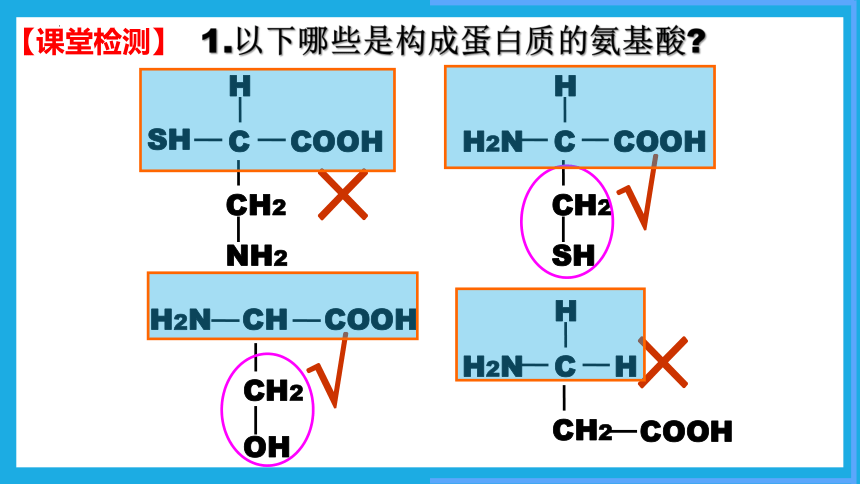
1.以下哪些是构成蛋白质的氨基酸
C
H
H2N
COOH
CH2
SH
C
H
NH2
COOH
CH2
SH
CH
H2N
COOH
CH2
OH
C
H
H2N
H
CH2
COOH
√
√
×
×
【课堂检测】
例2:半胱氨酸是组成生物体蛋白质的氨基酸之一,其R基是-CH2-SH,则它的结构式是:
C
CH2-SH
C
H
H2N
OOH
分子式为:C3H7O2NS
知识补充
必需氨基酸:
半必需氨基酸:
非必需氨基酸:
8种,人体细胞不能合成。
人体能自行合成并满足自身需要,不必由食物供给的氨基酸。
甲硫氨酸、缬氨酸、赖氨酸、异亮氨酸、苯丙氨酸、 亮氨酸、色氨酸、苏氨酸
组氨酸、精氨酸
甲 携 来 一 本 亮 色 书
人体中氨基酸常见的20种,蛋白质为1010-1012种。那么20种氨基酸是如何形成种类繁多的蛋白质的呢?
氨基酸形成蛋白质的过程
C
H
R1
NH2
OH
C
O
H2O
C
H
COOH
R2
H
N
H
脱水缩合
新知讲解
四、蛋白质脱水缩合形成多肽链
1.水中氢来自:
水中氧来自:
氨基和羧基
羧基
C
H
R1
NH2
C
O
C
H
COOH
R2
H
N
H2O
二肽
肽键
1.肽键:连接两个氨基酸分子的化学键:
2.二肽:由 氨基酸分子缩合而成的化合物。
-NH-CO-或-CO-NH-
两个
3.生成一个肽键,脱去( )水
一分子
肽键
肽键
2. 二肽
(四)蛋白质的结构及多样性
C
C
H
R1
NH2
C
O
C
H
R2
H
N
O
肽键
二肽
C
H
COOH
R2
H
N
H2O
肽键
三肽
H2O
1.三肽(多肽):
由三个或多个氨基酸分子缩合而成的化合物。
2.肽链:多肽通常呈链状结构,所以多肽通常又叫肽链。
3. 三肽、多肽和肽链
(四)蛋白质的结构及多样性
蛋白质的结构层次
氨基酸
二肽
三肽
多肽
这条肽链进一步盘绕形成一定的空间结构
几条多肽链折叠形成蛋白质
折叠盘曲成空间结构
氨基酸 肽链(一条或多条)
许多氨基酸通过肽键相互结合形成肽链,多肽链盘曲折叠构成了蛋白质分子的结构。
既然蛋白质都是按照上述方式构成的多肽链,为什么会有那么多种类的蛋白质呢?
?
蛋白质
脱水缩合 盘曲折叠
◇-◇-◇-◇-◇-◇-◇-◇-◇-◇
◎-◎-◎-◎-◎-◎-◎-◎-◎-◎
(1)氨基酸种类不同,肽链结构不同
◇-◇-◇-◇-◇-◇
◇-◇-◇-◇
(3)氨基酸排列顺序不同,肽链结构不同
◇-◇-◎-◎-
◇-◇-◎-◎-
◎-◎-
◇-◇
-◎-◇-◇-◎-
(4)肽链空间结构不同,蛋白质种类不同
(2)氨基酸数目不同, 肽链结构不同
新知讲解
五、蛋白质的多样性
氨基酸种类不同
氨基酸数目不同
氨基酸顺序不同
肽链空间结构不同
蛋白质结构
多种多样
蛋白质功能
多种多样
结构多样性决定了功能多样性!
新知讲解
五、蛋白质的多样性
头发
蛛丝
肌肉
许多蛋白质是构成细胞和生物体结构的重要物质。
肌肉中的一些蛋白质与肌肉的收缩、舒张有关。
肌肉纤维
新知讲解
六、蛋白质的功能
细胞中的化学反应离不开酶的催化。绝大多数酶
都是蛋白质。
新知讲解
酶
六、蛋白质的功能
新知讲解
血红蛋白示意图
血红蛋白是红细胞内包含的一种蛋白质,具有运输O2的功能。
此外,在细胞质膜上也有很多起到运输载体功能的蛋白质,它能把物质运输进入细胞,(参与物质跨膜运输)。
载体蛋白示意图
有些蛋白质具有运输功能。
六、蛋白质的功能
有些蛋白质能够调节机体的生命活动,如胰岛素、生长激素。
新知讲解
糖尿病患者注射胰岛素
胰腺
胰岛
六、蛋白质的功能
有些蛋白质有免疫功能。人体内的抗体是蛋白质,可以
帮助人体抵御病菌和病毒等抗原的侵害。
新知讲解
六、蛋白质的功能
①结构功能:许多蛋白质是构成细胞和生物体结构的重要物
质,称为结构蛋白。例如肌肉纤维。
②催化功能:起生物催化作用,如绝大多数酶。
③运输功能:运输功能,如血红蛋白能运输氧。
⑥调控功能:调节生命活动,如胰岛素和生长激素等。
⑤防御功能:免疫过程中产生的抗体,可以帮助人体抵御病菌和病毒等抗原的侵害。
一切生命活动都离不开蛋白质,蛋白质是生命活动的主要承担者。
④运动功能:肌肉中的一些蛋白质与肌肉的收缩、舒张有关。
蛋白质的相关计算
3个同学手拉手成一排, 左右手相连,还有几只手没参与进来 4个、5个呢……
如果类比氨基酸的话, 3个氨基酸缩合成一条链,至少还有几个游离的氨基和羧基
六、计算
—C
NH2
H
R1
—C—
O
N—
H
C
H
R2
—C—
O
N—
H
C—
COOH
H
R3
一条肽链至少含有____个羧基和_____个氨基。
一
一
m条肽链至少含有____个羧基和_____个氨基。
m
m
1.蛋白质中至少含有的游离的氨基数目或羧基数目=肽链的条数。
氨基数和羧基数的计算
游离氨基(羧基)数=肽链数+R基上的氨基(羧基)数
2.某一多肽链内共有肽键109个,则此分子中含有—NH2和—COOH 的数目至少为( )
A.110、110 B.109、109
C.9、9 D.1、1
3.人体免疫球蛋白由4条肽链构成,共有764个氨基酸,则该蛋白质分子中至少含有游离的氨基和羧基数分别是( )
A.746和764 B.760和760
C.762和762 D.4和4
答案:D
答案:D
3个同学手拉手成一排, 左右手相连的地方有几处
如果类比氨基酸的话, 3个氨基酸缩合成一条链,形成几个肽键?脱掉几个水分子?
肽键数= 脱去水分子个数 =6-1
肽键数= 脱去水分子个数 =8-1
肽链数为1时:肽键数 = 脱去水分子个数 =氨基酸数-1
肽键数= 脱去水分子个数 =14-2
肽链数为2时:肽键数 = 脱去水分子个数=氨基酸数-2
2.肽键数 = 脱去水分子个数 = 氨基酸数-肽链条数
肽键数和水分子数计算
氨基酸
肽键
4.胰岛素分子有a、b两条肽链,a链有21个氨基酸,b链有30个氨基酸, 胰岛素分子中肽键的数目是( )
A、48个; B、49个;C、50个;D、51个。
5.血红蛋白分子由4条多肽链组成,共含574个氨基酸,那么该分子中含有的肽键数和脱去的水分子数分别是( )
A.570和570 B.572和570
C.574和574 D.578和578
答案:B
答案:A
思考:n个氨基酸脱水缩合成环状肽?
由n个氨基酸构成的环状肽:
肽键数=脱水数=n。
肽键数和水分子数计算
(重点)
蛋白质相对分子量的计算
—C
NH2
H
R1
—C—
O
N—
H
C
H
R2
—C—
O
N—
H
C—
COOH
H
R3
思考:已知图中每个氨基酸平均分子量是128,图中多肽的分子量怎么计算
128x3-18x2=348
3.蛋白质相对分子质量
=氨基酸的分子质量总和-水分子的分子质量总和
=氨基酸平均相对分子质量×氨基酸数量-18×失去水分子数
蛋白质相对分子量的计算
—C
NH2
H
R1
—C—
O
N—
H
C
H
R2
—C—
O
N—
H
C—
COOH
H
R3
思考:已知图中每个氨基酸平均分子量是128,图中多肽的分子量怎么计算
128x3-18x2=348
6、某种蛋白质是由1条多肽链构成的,共含100个氨基酸,若每个氨基酸分子质量平均是120,则该蛋白质的相对分子量是?
7、某种蛋白质是由3条多肽链构成的,共含1000个氨基酸,若每个氨基酸分子质量平均是120,则该蛋白质的相对分子量是?
100×120-(100-1)×18=10218
1000×120-(1000-3)×18=103054
六、蛋白质的检测和观察
选材:含蛋白质丰富的豆浆或鸡蛋清溶液。
黄豆浆滤液或蛋清稀释液
制备样液
呈色反应
组织样
液2mL
双缩脲试剂A液2mL
双缩脲试剂B液3~4滴
摇匀后变成紫色
结论:
组织样液中存在蛋白质。
新知讲解
双缩脲试剂:
A液:(质量浓度为0.1g/mL的NaOH溶液)
B液:(质量浓度为0.01g/mL的CuSO4溶液)
蛋白质的检测结果
新知讲解
实验结果
4
斐林试剂和双缩脲试剂对比
易错讲解
斐林试剂 双缩脲试剂 成分 甲液 乙液 A液 B液
0.1 g/mL NaOH溶液 0.05 g/mL CuSO4溶液 0.1 g/mL NaOH溶液 0.01 g/mL CuSO4溶液
反应原理 可溶性还原糖将Cu(OH)2 还原为砖红色Cu2O沉淀 具有两个或两个以上肽键的化合物在碱性条件下与Cu2+反应生成紫色络合物 添加顺序 甲、乙两液等量混匀后立即使用 先加入A液 2 mL摇匀,再加3~4滴B液摇匀 反应条件 50℃~65℃水浴加热 不需加热 反应现象 浅蓝色→棕色→砖红色 紫色 知识补充
蛋白质的变性
在化学因素或物理因素(如高温、强酸、强碱和重金属盐等)的作用下,蛋白质的空间结构发生改变,导致蛋白质的生物活性丧失。
注:1.蛋白质变性只是空间结构遭到破坏,其肽键不会断裂。因此变性的蛋白质也可以和双缩脲试剂发生紫色反应。
2.蛋白质变性是化学变化,是化学现象。
3.蛋白质的变性是不可逆的。
蛋白质的水解反应是和脱水缩合相反的反应
C
H
R1
H2N
C
O
C
H
COOH
R2
H
N
H
OH
C
H
R1
H2N
C
O
C
H
COOH
R2
H
N
+
H2O
水解
+
许多蛋白质含有两条或多条多肽链,他们通过一定的化学键如二硫键结合在一起
H
O
C
CH2
C
H2N
OH
SH
H2C
O
C
H
C
H2N
OH
SH
H
O
C
CH2
C
H2N
OH
S
H2C
O
C
H
C
H2N
OH
S
二硫键
肽链的形成过程
【课堂检测】
8. 下图为牛胰岛素结构图,该物质中—S—S—是由两个—SH脱去两个H形成的。下列说法正确的是( )
A.牛胰岛素含有50个肽键
B.牛胰岛素中至少含有2个游离的—NH2和2个游离的—COOH
C.牛胰岛素水解产物含有21种不同的氨基酸
D.牛胰岛素形成时,减少的相对分子质量为882
B
+ 2H
第1章 细胞的分子组成
第3节 细胞中的蛋白质
课前回顾
分类 种类 质量分数/%
无机化合物 水 85~90
无机盐 1~1.5
有机化合物 蛋白质 7~10
脂质 1~2
糖类和核酸 1~1.5
含量最多的有机化合物是
蛋白质
一、元素组成
一定有C、H、O、N
绝大多数含S
还可能含有其他元素如Fe、Cu、Mn、I等
例:分子式为C1864H3021O576N468S21的化合物,最可能是( )
A.脱氧核糖 B.磷脂
C. 蛋白质 D. 肝糖原
新知讲解
二、相对分子量大:
64500
9512
C3032H4816O872N780S8Fe4
血红蛋白
36684
5224
C1642H2652O492N420S12
牛奶乳蛋白
180
24
C6H12O6
葡萄糖
18
3
H2O
水
相对分子质量
原子个数
化学式
几千~百万以上,高分子化合物
新知讲解
回答:蛋白质含量比较丰富的食物?
奶类
蛋类
瘦肉类
豆类
思考: 我们从食物中摄取的蛋白质如何为我们所用?
蛋白质必需经过消化成氨基酸才能被人体吸收和利用。
氨基酸是组成蛋白质的基本单位。
三、蛋白质的基本组成单位——氨基酸
新知讲解
C
H
C
H
H2N
OH
O
C
H
C
H2N
OH
O
CH3
CH3
CH
C
H
C
H2N
OH
O
CH3
C
H
C
H2N
OH
O
CH2
CH3
CH3
CH
甘氨酸
缬氨酸
丙氨酸
亮氨酸
几种氨基酸的结构式
问题1 :这些氨基酸的结构具有什么共同特点?
问题2:不同氨基酸的区别又在哪里?
—NH2 (氨基)
—COOH (羧基)
R基
—H (氢原子)
—R (R基)侧链基团
对比生物体内组成蛋白质的常见20种氨基酸,检验结构通式的正确性
三、蛋白质的基本组成单位——氨基酸
新知讲解
三、蛋白质的基本组成单位——氨基酸
1.种类:组成蛋白质的氨基酸常见的有20种
2.氨基
①:—NH2
②:H2N—
或
3.羧基
①:—COOH
②:HOOC—
或
4.R基:-R
新知讲解
5.氨基酸分子结构通式及特点:
新知讲解
C
R
C
H2N
OH
O
H
氨基
羧基
侧链基团
特点:
1、每个氨基酸分子至少都含有一个氨基(-NH2)和一个羧基(-COOH),并连在同一个碳原子上。
2、这个碳原子还连接一个氢原子和一个侧链基团(-R表示)
3、R基的不同决定了氨基酸分子的不同。
1.以下哪些是构成蛋白质的氨基酸
C
H
H2N
COOH
CH2
SH
C
H
NH2
COOH
CH2
SH
CH
H2N
COOH
CH2
OH
C
H
H2N
H
CH2
COOH
√
√
×
×
【课堂检测】
例2:半胱氨酸是组成生物体蛋白质的氨基酸之一,其R基是-CH2-SH,则它的结构式是:
C
CH2-SH
C
H
H2N
OOH
分子式为:C3H7O2NS
知识补充
必需氨基酸:
半必需氨基酸:
非必需氨基酸:
8种,人体细胞不能合成。
人体能自行合成并满足自身需要,不必由食物供给的氨基酸。
甲硫氨酸、缬氨酸、赖氨酸、异亮氨酸、苯丙氨酸、 亮氨酸、色氨酸、苏氨酸
组氨酸、精氨酸
甲 携 来 一 本 亮 色 书
人体中氨基酸常见的20种,蛋白质为1010-1012种。那么20种氨基酸是如何形成种类繁多的蛋白质的呢?
氨基酸形成蛋白质的过程
C
H
R1
NH2
OH
C
O
H2O
C
H
COOH
R2
H
N
H
脱水缩合
新知讲解
四、蛋白质脱水缩合形成多肽链
1.水中氢来自:
水中氧来自:
氨基和羧基
羧基
C
H
R1
NH2
C
O
C
H
COOH
R2
H
N
H2O
二肽
肽键
1.肽键:连接两个氨基酸分子的化学键:
2.二肽:由 氨基酸分子缩合而成的化合物。
-NH-CO-或-CO-NH-
两个
3.生成一个肽键,脱去( )水
一分子
肽键
肽键
2. 二肽
(四)蛋白质的结构及多样性
C
C
H
R1
NH2
C
O
C
H
R2
H
N
O
肽键
二肽
C
H
COOH
R2
H
N
H2O
肽键
三肽
H2O
1.三肽(多肽):
由三个或多个氨基酸分子缩合而成的化合物。
2.肽链:多肽通常呈链状结构,所以多肽通常又叫肽链。
3. 三肽、多肽和肽链
(四)蛋白质的结构及多样性
蛋白质的结构层次
氨基酸
二肽
三肽
多肽
这条肽链进一步盘绕形成一定的空间结构
几条多肽链折叠形成蛋白质
折叠盘曲成空间结构
氨基酸 肽链(一条或多条)
许多氨基酸通过肽键相互结合形成肽链,多肽链盘曲折叠构成了蛋白质分子的结构。
既然蛋白质都是按照上述方式构成的多肽链,为什么会有那么多种类的蛋白质呢?
?
蛋白质
脱水缩合 盘曲折叠
◇-◇-◇-◇-◇-◇-◇-◇-◇-◇
◎-◎-◎-◎-◎-◎-◎-◎-◎-◎
(1)氨基酸种类不同,肽链结构不同
◇-◇-◇-◇-◇-◇
◇-◇-◇-◇
(3)氨基酸排列顺序不同,肽链结构不同
◇-◇-◎-◎-
◇-◇-◎-◎-
◎-◎-
◇-◇
-◎-◇-◇-◎-
(4)肽链空间结构不同,蛋白质种类不同
(2)氨基酸数目不同, 肽链结构不同
新知讲解
五、蛋白质的多样性
氨基酸种类不同
氨基酸数目不同
氨基酸顺序不同
肽链空间结构不同
蛋白质结构
多种多样
蛋白质功能
多种多样
结构多样性决定了功能多样性!
新知讲解
五、蛋白质的多样性
头发
蛛丝
肌肉
许多蛋白质是构成细胞和生物体结构的重要物质。
肌肉中的一些蛋白质与肌肉的收缩、舒张有关。
肌肉纤维
新知讲解
六、蛋白质的功能
细胞中的化学反应离不开酶的催化。绝大多数酶
都是蛋白质。
新知讲解
酶
六、蛋白质的功能
新知讲解
血红蛋白示意图
血红蛋白是红细胞内包含的一种蛋白质,具有运输O2的功能。
此外,在细胞质膜上也有很多起到运输载体功能的蛋白质,它能把物质运输进入细胞,(参与物质跨膜运输)。
载体蛋白示意图
有些蛋白质具有运输功能。
六、蛋白质的功能
有些蛋白质能够调节机体的生命活动,如胰岛素、生长激素。
新知讲解
糖尿病患者注射胰岛素
胰腺
胰岛
六、蛋白质的功能
有些蛋白质有免疫功能。人体内的抗体是蛋白质,可以
帮助人体抵御病菌和病毒等抗原的侵害。
新知讲解
六、蛋白质的功能
①结构功能:许多蛋白质是构成细胞和生物体结构的重要物
质,称为结构蛋白。例如肌肉纤维。
②催化功能:起生物催化作用,如绝大多数酶。
③运输功能:运输功能,如血红蛋白能运输氧。
⑥调控功能:调节生命活动,如胰岛素和生长激素等。
⑤防御功能:免疫过程中产生的抗体,可以帮助人体抵御病菌和病毒等抗原的侵害。
一切生命活动都离不开蛋白质,蛋白质是生命活动的主要承担者。
④运动功能:肌肉中的一些蛋白质与肌肉的收缩、舒张有关。
蛋白质的相关计算
3个同学手拉手成一排, 左右手相连,还有几只手没参与进来 4个、5个呢……
如果类比氨基酸的话, 3个氨基酸缩合成一条链,至少还有几个游离的氨基和羧基
六、计算
—C
NH2
H
R1
—C—
O
N—
H
C
H
R2
—C—
O
N—
H
C—
COOH
H
R3
一条肽链至少含有____个羧基和_____个氨基。
一
一
m条肽链至少含有____个羧基和_____个氨基。
m
m
1.蛋白质中至少含有的游离的氨基数目或羧基数目=肽链的条数。
氨基数和羧基数的计算
游离氨基(羧基)数=肽链数+R基上的氨基(羧基)数
2.某一多肽链内共有肽键109个,则此分子中含有—NH2和—COOH 的数目至少为( )
A.110、110 B.109、109
C.9、9 D.1、1
3.人体免疫球蛋白由4条肽链构成,共有764个氨基酸,则该蛋白质分子中至少含有游离的氨基和羧基数分别是( )
A.746和764 B.760和760
C.762和762 D.4和4
答案:D
答案:D
3个同学手拉手成一排, 左右手相连的地方有几处
如果类比氨基酸的话, 3个氨基酸缩合成一条链,形成几个肽键?脱掉几个水分子?
肽键数= 脱去水分子个数 =6-1
肽键数= 脱去水分子个数 =8-1
肽链数为1时:肽键数 = 脱去水分子个数 =氨基酸数-1
肽键数= 脱去水分子个数 =14-2
肽链数为2时:肽键数 = 脱去水分子个数=氨基酸数-2
2.肽键数 = 脱去水分子个数 = 氨基酸数-肽链条数
肽键数和水分子数计算
氨基酸
肽键
4.胰岛素分子有a、b两条肽链,a链有21个氨基酸,b链有30个氨基酸, 胰岛素分子中肽键的数目是( )
A、48个; B、49个;C、50个;D、51个。
5.血红蛋白分子由4条多肽链组成,共含574个氨基酸,那么该分子中含有的肽键数和脱去的水分子数分别是( )
A.570和570 B.572和570
C.574和574 D.578和578
答案:B
答案:A
思考:n个氨基酸脱水缩合成环状肽?
由n个氨基酸构成的环状肽:
肽键数=脱水数=n。
肽键数和水分子数计算
(重点)
蛋白质相对分子量的计算
—C
NH2
H
R1
—C—
O
N—
H
C
H
R2
—C—
O
N—
H
C—
COOH
H
R3
思考:已知图中每个氨基酸平均分子量是128,图中多肽的分子量怎么计算
128x3-18x2=348
3.蛋白质相对分子质量
=氨基酸的分子质量总和-水分子的分子质量总和
=氨基酸平均相对分子质量×氨基酸数量-18×失去水分子数
蛋白质相对分子量的计算
—C
NH2
H
R1
—C—
O
N—
H
C
H
R2
—C—
O
N—
H
C—
COOH
H
R3
思考:已知图中每个氨基酸平均分子量是128,图中多肽的分子量怎么计算
128x3-18x2=348
6、某种蛋白质是由1条多肽链构成的,共含100个氨基酸,若每个氨基酸分子质量平均是120,则该蛋白质的相对分子量是?
7、某种蛋白质是由3条多肽链构成的,共含1000个氨基酸,若每个氨基酸分子质量平均是120,则该蛋白质的相对分子量是?
100×120-(100-1)×18=10218
1000×120-(1000-3)×18=103054
六、蛋白质的检测和观察
选材:含蛋白质丰富的豆浆或鸡蛋清溶液。
黄豆浆滤液或蛋清稀释液
制备样液
呈色反应
组织样
液2mL
双缩脲试剂A液2mL
双缩脲试剂B液3~4滴
摇匀后变成紫色
结论:
组织样液中存在蛋白质。
新知讲解
双缩脲试剂:
A液:(质量浓度为0.1g/mL的NaOH溶液)
B液:(质量浓度为0.01g/mL的CuSO4溶液)
蛋白质的检测结果
新知讲解
实验结果
4
斐林试剂和双缩脲试剂对比
易错讲解
斐林试剂 双缩脲试剂 成分 甲液 乙液 A液 B液
0.1 g/mL NaOH溶液 0.05 g/mL CuSO4溶液 0.1 g/mL NaOH溶液 0.01 g/mL CuSO4溶液
反应原理 可溶性还原糖将Cu(OH)2 还原为砖红色Cu2O沉淀 具有两个或两个以上肽键的化合物在碱性条件下与Cu2+反应生成紫色络合物 添加顺序 甲、乙两液等量混匀后立即使用 先加入A液 2 mL摇匀,再加3~4滴B液摇匀 反应条件 50℃~65℃水浴加热 不需加热 反应现象 浅蓝色→棕色→砖红色 紫色 知识补充
蛋白质的变性
在化学因素或物理因素(如高温、强酸、强碱和重金属盐等)的作用下,蛋白质的空间结构发生改变,导致蛋白质的生物活性丧失。
注:1.蛋白质变性只是空间结构遭到破坏,其肽键不会断裂。因此变性的蛋白质也可以和双缩脲试剂发生紫色反应。
2.蛋白质变性是化学变化,是化学现象。
3.蛋白质的变性是不可逆的。
蛋白质的水解反应是和脱水缩合相反的反应
C
H
R1
H2N
C
O
C
H
COOH
R2
H
N
H
OH
C
H
R1
H2N
C
O
C
H
COOH
R2
H
N
+
H2O
水解
+
许多蛋白质含有两条或多条多肽链,他们通过一定的化学键如二硫键结合在一起
H
O
C
CH2
C
H2N
OH
SH
H2C
O
C
H
C
H2N
OH
SH
H
O
C
CH2
C
H2N
OH
S
H2C
O
C
H
C
H2N
OH
S
二硫键
肽链的形成过程
【课堂检测】
8. 下图为牛胰岛素结构图,该物质中—S—S—是由两个—SH脱去两个H形成的。下列说法正确的是( )
A.牛胰岛素含有50个肽键
B.牛胰岛素中至少含有2个游离的—NH2和2个游离的—COOH
C.牛胰岛素水解产物含有21种不同的氨基酸
D.牛胰岛素形成时,减少的相对分子质量为882
B
+ 2H
