高中化学人教版(2019)必修第一册2.3.1物质的量 摩尔质量(共33张ppt)
文档属性
| 名称 | 高中化学人教版(2019)必修第一册2.3.1物质的量 摩尔质量(共33张ppt) |  | |
| 格式 | zip | ||
| 文件大小 | 41.2MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-09-27 20:42:41 | ||
图片预览







文档简介
(共33张PPT)
m n N
÷M
×M
×NA
÷NA
质量
物质的量
粒子数
m/M = n = N/NA
可称量物质的质量
物 质 的 量
该物质含有的粒子数
桥梁
物质的量
第一课时
理解物质的量的含义
知道摩尔是物质的量的单位,是国际单位制的7个基本单位之一
学习目标
e
理解阿伏加德罗常数、摩尔质量取值的含义
能利用物质的量、阿伏加德罗常数、摩尔质量进行质量与微粒数间的换算
1000粒米
碗饭
300据
★★
洁云
Hygienix
加韧卫生纸
C血缪
一包
12个鸡蛋的集合体
300张纸巾的集合体
12支笔
1滴水(约0.05g)含有多少个水分子?
→
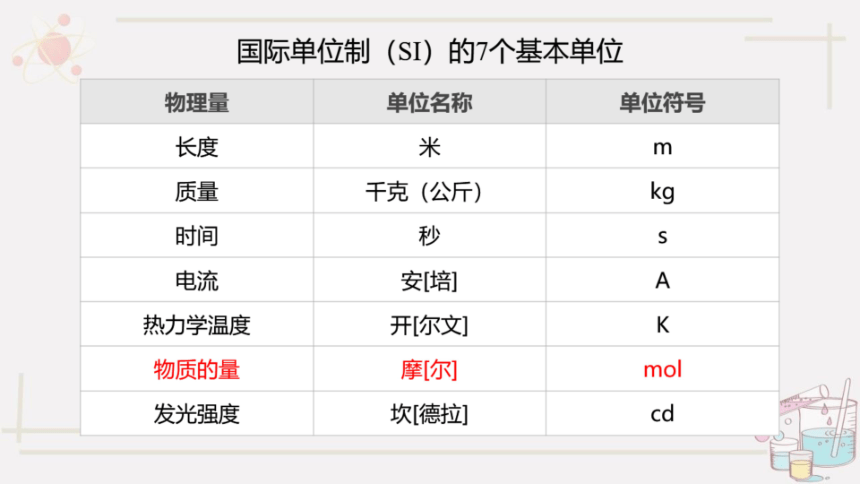
国际单位制(S)的7个基本单位
物理量
单位名称
单位符号
长度
米
m
质量
千克(公斤)
kg
时间
秒
电流
安[培]
A
热力学温度
开尔文]
K
物质的量
摩尔
mol
发光强度
坎[德拉]
cd
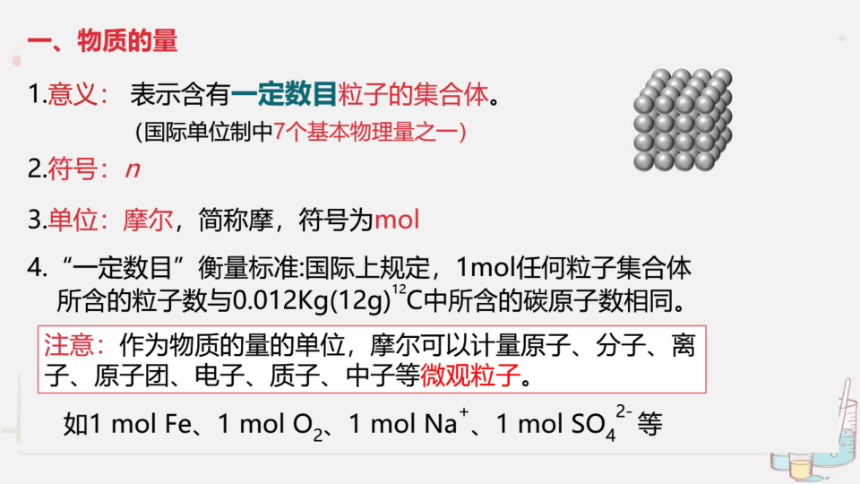
一、物质的量
1意义:表示含有一定数目粒子的集合体。
(国际单位制中7个基本物理量之一)
2.符号:n
3.单位:摩尔,简称摩,符号为mol
4.”一定数目”衡量标准:国际上规定,1mo任何粒子集合体
所含的粒子数与0.012Kg(12g)C中所含的碳原子数相同。
注意:作为物质的量的单位,摩尔可以计量原子、分子、离
子、原子团、电子、质子、中子等微观粒子。
如1 mol Fe、1mol02、1 mol Na、1molS042等
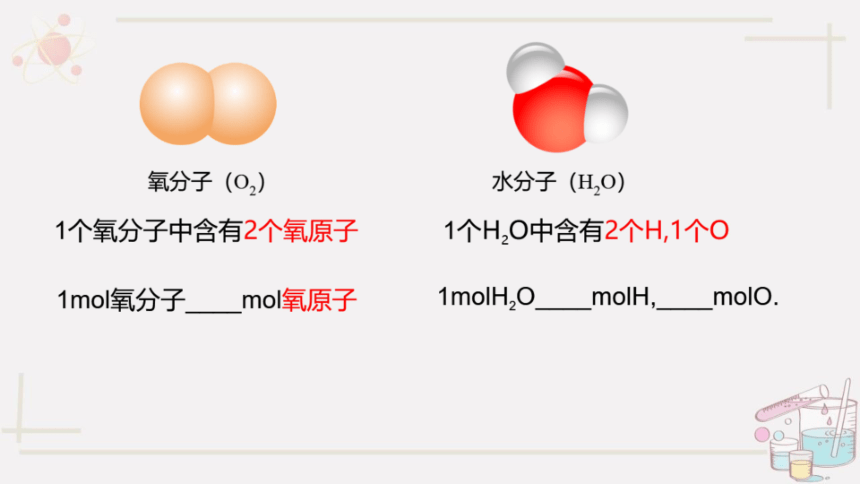
氧分子(02)
水分子(H,0)
1个氧分子中含有2个氧原子
1个H,O中含有2个H,1个O
1mol氧分子mo氧原子
1molH2O_molH,__molO.
注意事项
①专有名词,
②物质的量描述的是微观粒子不是宏观物质;
如:1mol土豆
③可以计量纯净物,也可以计量混合物。前提是微观粒子;
(如:1molN和O,的混合气体)
④必须指明具体粒子的种类
思考:“1mol氢”这种说法是否正确?
你说的是氢气?氢原子?还是氢离子?指代不明
物质的量
意义:表示含有一定数目粒子的集合体。
”一定数目”衡量标准:国际上规定,1mo任何粒子集合体
所含的粒子数与0.012Kg(12g)'C中所含的碳原子数相同。
思考:1mo粒子数有多少个?
P9温故知新
结论:1mol任何粒子集合体所含粒子数都是6.02×102
阿伏加德罗常数
意义:1mol任何粒子的粒子数叫做阿伏加德罗常数,≈6.02×103mo
符号:W%
单位:
mol
表达式:W≈6.02×103mol1
思考:2mol粒子有多少个?
nmol粒子有多少个?
m n N
÷M
×M
×NA
÷NA
质量
物质的量
粒子数
m/M = n = N/NA
可称量物质的质量
物 质 的 量
该物质含有的粒子数
桥梁
物质的量
第一课时
理解物质的量的含义
知道摩尔是物质的量的单位,是国际单位制的7个基本单位之一
学习目标
e
理解阿伏加德罗常数、摩尔质量取值的含义
能利用物质的量、阿伏加德罗常数、摩尔质量进行质量与微粒数间的换算
1000粒米
碗饭
300据
★★
洁云
Hygienix
加韧卫生纸
C血缪
一包
12个鸡蛋的集合体
300张纸巾的集合体
12支笔
1滴水(约0.05g)含有多少个水分子?
→
国际单位制(S)的7个基本单位
物理量
单位名称
单位符号
长度
米
m
质量
千克(公斤)
kg
时间
秒
电流
安[培]
A
热力学温度
开尔文]
K
物质的量
摩尔
mol
发光强度
坎[德拉]
cd
一、物质的量
1意义:表示含有一定数目粒子的集合体。
(国际单位制中7个基本物理量之一)
2.符号:n
3.单位:摩尔,简称摩,符号为mol
4.”一定数目”衡量标准:国际上规定,1mo任何粒子集合体
所含的粒子数与0.012Kg(12g)C中所含的碳原子数相同。
注意:作为物质的量的单位,摩尔可以计量原子、分子、离
子、原子团、电子、质子、中子等微观粒子。
如1 mol Fe、1mol02、1 mol Na、1molS042等
氧分子(02)
水分子(H,0)
1个氧分子中含有2个氧原子
1个H,O中含有2个H,1个O
1mol氧分子mo氧原子
1molH2O_molH,__molO.
注意事项
①专有名词,
②物质的量描述的是微观粒子不是宏观物质;
如:1mol土豆
③可以计量纯净物,也可以计量混合物。前提是微观粒子;
(如:1molN和O,的混合气体)
④必须指明具体粒子的种类
思考:“1mol氢”这种说法是否正确?
你说的是氢气?氢原子?还是氢离子?指代不明
物质的量
意义:表示含有一定数目粒子的集合体。
”一定数目”衡量标准:国际上规定,1mo任何粒子集合体
所含的粒子数与0.012Kg(12g)'C中所含的碳原子数相同。
思考:1mo粒子数有多少个?
P9温故知新
结论:1mol任何粒子集合体所含粒子数都是6.02×102
阿伏加德罗常数
意义:1mol任何粒子的粒子数叫做阿伏加德罗常数,≈6.02×103mo
符号:W%
单位:
mol
表达式:W≈6.02×103mol1
思考:2mol粒子有多少个?
nmol粒子有多少个?
