鲁教版九年级化学 第四单元 第二节 第2课时 化合价和化学式 课件(共18张PPT)
文档属性
| 名称 | 鲁教版九年级化学 第四单元 第二节 第2课时 化合价和化学式 课件(共18张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 2.5MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-09-28 00:00:00 | ||
图片预览





文档简介
(共18张PPT)
化学九年级上册 L
第四单元 我们周围的空气
第二节 物质组成的表示
第2课时 化合价与化学式
观察与思考:
化学式 HCl H2O NH3
微粒个数比
1:3
MgCl2 AlCl3
1:2
1:1
2:1
1:3
观察下列元素化合价,归纳表示方法
C O2 CuCl2
观察与思考
+4 -2 +2 -1
(1)写在元素符号的正上方。
(2) “+”、“-” 符号在前,数值在后。
(3)“+” 和“1”不能省略。
+2
+1
对比元素化合价和离子的表示方法
化合价 MgO Na
离子 Mg2+ Na+
区别:
联系:
化合价与离子所带电荷书写位置不同,
符号与数值前后位置不同,
符号和数值相同
Cl
Na
+
-
NaCl
+1
-1
化合价的数值和符号是由什么决定的?
交流与共享
Cl
Mg
Cl
2+
-
-
MgCl2
+2
-1
化合价的数值和符号是由什么决定的?
小结:化合价的数值由该元素的一个原子得失电子的数目决定的,得电子元素显负价,失电子元素显正价。
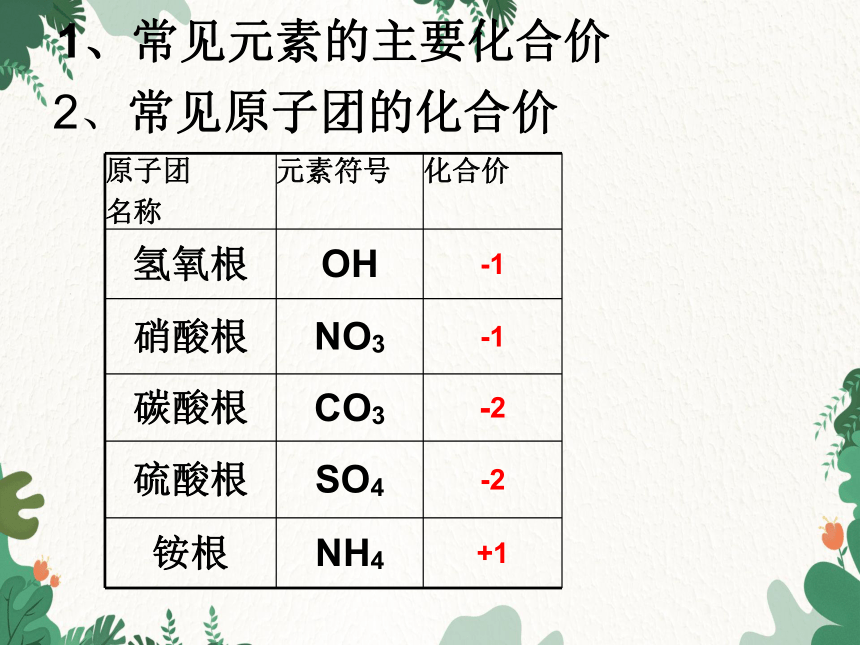
原子团
名称 元素符号 化合价
氢氧根 OH -1
硝酸根 NO3 -1
碳酸根 CO3 -2
硫酸根 SO4 -2
铵根 NH4 +1
1、常见元素的主要化合价
2、常见原子团的化合价
化合价的记忆口诀
正一铵银钾钠氢 NH4 Ag K Na H
正二钙镁铜钡锌 Ca Mg Cu Ba Zn
正三铝来要记清 Al
负一硝酸氢氧氯 NO3 OH Cl
负二碳酸硫酸氧 CO3 SO4 O
+1 +1 +1 +1 +1
+2 +2 +2 +2 +2
+3
-1 -1 -1
-2 -2 -2
计算下列化学式中元素化合价的代数和
+2 -2 +1 -2 +3 -1
MgO H2 O AlCl3
活动与探究一
化合物中,各种元素的正负化合价的代数和为零。
化学式的书写
化学式的书写原则依据:
1、任何化合物中各元素的正负化合价的代数和为零。
2、客观事实。不能任意书写不存在的物质的化学式。
化学式的书写方法
观察下列物质的化学式中元素的化合价与右下角微粒个数,你能发现什么规律?
+1 -1 +1-2
NaCl H2O
+3 -2 +5 -2
Fe2O3 P2O5
观察下列物质的化学式和各元素的化合价,
能用前面的方法吗?
+4-2
C O2
正价前、负价后、交叉化简不遗漏
化简
+4 -2 +4 -2
C O C O C O C2O4 CO2
已知下列元素的化合价,写出它们组成的化学式。
Cu Cl
+2 -1
CuCl2
化学式
P O
+5 -2
化学式
P2O5
S O
+4 -2
化学式
SO2
完成下列化学式
H
K
Mg
Al
Cl 化学式
名 称
O 化学式
名 称
OH 化学式
名 称
SO4 化学式
名 称
+1
+1
+2
+3
-2
-1
-2
-1
KCl MgCl2 AlCl3
H2O K2O MgO Al2O3
H2O KOH Mg(OH)2 Al(OH)3
H2SO4 K2SO4 MgSO4 Al2(SO4)3
HCl
完成下列化学式
H
K
Mg
Al
Cl 化学式
名 称
O 化学式
名 称
OH 化学式
名 称
SO4 化学式
名 称 硫酸
+1
+1
+2
+3
-2
-1
-2
-1
KCl MgCl2 AlCl3
H2O K2O MgO Al2O3
氯化氢 氯化钾 氯化镁 氯化铝
H2O KOH Mg(OH)2 Al(OH)3
H2SO4 K2SO4 MgSO4 Al2(SO4)3
HCl
水 氧化钾 氧化镁 氧化铝
水 氢氧化钾 氢氧化镁 氢氧化铝
硫酸钾 硫酸镁 硫酸铝
根据化合价原则求化学式中元素的化合价
已知下列化学式,求其中红色的元素符号的化合价.
NO2 FeO WO3
活动与探究三
+4
+2
+6
已知下列化学式,求其中红色元素符号的化合价.
K2CO3 Na2R2O3 Ca(NO3)2
+4
+2
你做对了吗?
+5
完成下列习题
(1)判断化学式正误:
BaOH CaO2
(2)求红色元素化合价:
NH3 CuSO4 NaHCO3
(3)写化学式:
氯化铝 氧化铜
氧化钨(W+6) 碳酸钾
X
Ba(OH)2
X
CaO
-3
+6
+4
AlCl3 CuO
WO3 K2CO3
化学九年级上册 L
第四单元 我们周围的空气
第二节 物质组成的表示
第2课时 化合价与化学式
观察与思考:
化学式 HCl H2O NH3
微粒个数比
1:3
MgCl2 AlCl3
1:2
1:1
2:1
1:3
观察下列元素化合价,归纳表示方法
C O2 CuCl2
观察与思考
+4 -2 +2 -1
(1)写在元素符号的正上方。
(2) “+”、“-” 符号在前,数值在后。
(3)“+” 和“1”不能省略。
+2
+1
对比元素化合价和离子的表示方法
化合价 MgO Na
离子 Mg2+ Na+
区别:
联系:
化合价与离子所带电荷书写位置不同,
符号与数值前后位置不同,
符号和数值相同
Cl
Na
+
-
NaCl
+1
-1
化合价的数值和符号是由什么决定的?
交流与共享
Cl
Mg
Cl
2+
-
-
MgCl2
+2
-1
化合价的数值和符号是由什么决定的?
小结:化合价的数值由该元素的一个原子得失电子的数目决定的,得电子元素显负价,失电子元素显正价。
原子团
名称 元素符号 化合价
氢氧根 OH -1
硝酸根 NO3 -1
碳酸根 CO3 -2
硫酸根 SO4 -2
铵根 NH4 +1
1、常见元素的主要化合价
2、常见原子团的化合价
化合价的记忆口诀
正一铵银钾钠氢 NH4 Ag K Na H
正二钙镁铜钡锌 Ca Mg Cu Ba Zn
正三铝来要记清 Al
负一硝酸氢氧氯 NO3 OH Cl
负二碳酸硫酸氧 CO3 SO4 O
+1 +1 +1 +1 +1
+2 +2 +2 +2 +2
+3
-1 -1 -1
-2 -2 -2
计算下列化学式中元素化合价的代数和
+2 -2 +1 -2 +3 -1
MgO H2 O AlCl3
活动与探究一
化合物中,各种元素的正负化合价的代数和为零。
化学式的书写
化学式的书写原则依据:
1、任何化合物中各元素的正负化合价的代数和为零。
2、客观事实。不能任意书写不存在的物质的化学式。
化学式的书写方法
观察下列物质的化学式中元素的化合价与右下角微粒个数,你能发现什么规律?
+1 -1 +1-2
NaCl H2O
+3 -2 +5 -2
Fe2O3 P2O5
观察下列物质的化学式和各元素的化合价,
能用前面的方法吗?
+4-2
C O2
正价前、负价后、交叉化简不遗漏
化简
+4 -2 +4 -2
C O C O C O C2O4 CO2
已知下列元素的化合价,写出它们组成的化学式。
Cu Cl
+2 -1
CuCl2
化学式
P O
+5 -2
化学式
P2O5
S O
+4 -2
化学式
SO2
完成下列化学式
H
K
Mg
Al
Cl 化学式
名 称
O 化学式
名 称
OH 化学式
名 称
SO4 化学式
名 称
+1
+1
+2
+3
-2
-1
-2
-1
KCl MgCl2 AlCl3
H2O K2O MgO Al2O3
H2O KOH Mg(OH)2 Al(OH)3
H2SO4 K2SO4 MgSO4 Al2(SO4)3
HCl
完成下列化学式
H
K
Mg
Al
Cl 化学式
名 称
O 化学式
名 称
OH 化学式
名 称
SO4 化学式
名 称 硫酸
+1
+1
+2
+3
-2
-1
-2
-1
KCl MgCl2 AlCl3
H2O K2O MgO Al2O3
氯化氢 氯化钾 氯化镁 氯化铝
H2O KOH Mg(OH)2 Al(OH)3
H2SO4 K2SO4 MgSO4 Al2(SO4)3
HCl
水 氧化钾 氧化镁 氧化铝
水 氢氧化钾 氢氧化镁 氢氧化铝
硫酸钾 硫酸镁 硫酸铝
根据化合价原则求化学式中元素的化合价
已知下列化学式,求其中红色的元素符号的化合价.
NO2 FeO WO3
活动与探究三
+4
+2
+6
已知下列化学式,求其中红色元素符号的化合价.
K2CO3 Na2R2O3 Ca(NO3)2
+4
+2
你做对了吗?
+5
完成下列习题
(1)判断化学式正误:
BaOH CaO2
(2)求红色元素化合价:
NH3 CuSO4 NaHCO3
(3)写化学式:
氯化铝 氧化铜
氧化钨(W+6) 碳酸钾
X
Ba(OH)2
X
CaO
-3
+6
+4
AlCl3 CuO
WO3 K2CO3
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
