3.1 分子和原子(第2课时)课件 -2022-2023学年九年级化学人教版上册(共17张PPT)
文档属性
| 名称 | 3.1 分子和原子(第2课时)课件 -2022-2023学年九年级化学人教版上册(共17张PPT) |

|
|
| 格式 | zip | ||
| 文件大小 | 903.9KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-09-28 00:00:00 | ||
图片预览





文档简介
(共17张PPT)
3.1 分子和原子第2课时
复习巩固:
1.生活中的下列现象,用分子的相关知识解释不正确的是 ( )
A.湿衣服晾在太阳底下干得快,说明分子运动速率与温度有关
B.成熟的菠萝蜜会散发出浓浓的香味,说明分子在不断地运动
C.水沸腾时,掀起壶盖,说明分子大小随温度升高而增大
D.液化石油气须加压后贮存在钢瓶中,说明分子之间有间隙
C
2.右图信息能说明 ( )
A.分子很小 B.分子间有同隔
C.分子总是在不断运动 D.分子是构成物质的唯一微粒
A
复习引入:上节课我们讲到,水等都是由分子构成的。那么分子是不是构成物质的最小的粒子,它能不能再进行分割呢?如果能分,那分子又是什么构成的呢?
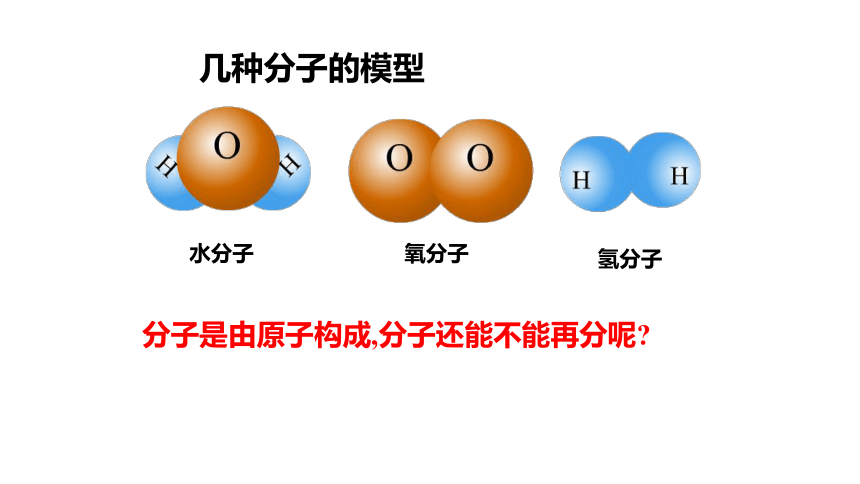
几种分子的模型
水分子
氧分子
氢分子
分子是由原子构成,分子还能不能再分呢
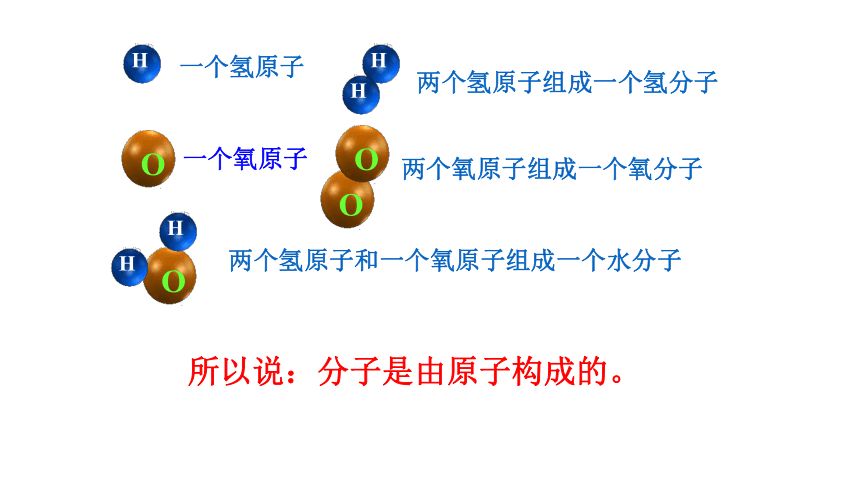
一个氢原子
一个氧原子
两个氢原子组成一个氢分子
两个氧原子组成一个氧分子
两个氢原子和一个氧原子组成一个水分子
所以说:分子是由原子构成的。
H
H
H
O
O
O
O
H
H
1、氧气分子是由 构成的。
一个氧气分子由 构成的。
2、水分子是由 和 构成的。
一个水分子是由___________
和 构成的。
几种说法:
氧原子
二个氧原子
氢原子
氧原子
二个氢原子
一个氧原子
二、分子可以分为原子
1、由分子构成的物质在发生物理变化时,分子本身没有变化。
2、由分子构成的物质在发生化学变化时,一种物质的分子会变成其他物质的分子。
用分子的观点解释(由分子构成的物质)
物理变化:
化学变化:
分子本身没有发生变化,只
是分子间的间隔发生变化。
分子本身发生变化 ,生成新 的分子。
由分子构成的物质在物质发生物理变化时,分子没有变化,物质的化学性质也没变化。由分子构成的物质在物质发生化学变化时,分子变了,变成了别的物质的分子,但原子不变。可见,
分子是保持物质化学性质的最小微粒。
分子的概念
分子是保持物质化学性质的最小粒子
氧气
受热
水
水蒸气
水
氢气
+
通电
物理变化,分子本身不改变
化学变化,分子本身
发生了变化
同种物质的分子性质相同,不同物质的分子性质不同
分子是保持物质化学性质的最小粒子。
理解:(1)由同种分子构成的物质,化学性质相同; 不同种分子构成的物质,化学性质不同。
(2)物质发生化学变化时,分子发生了改变;
物质发生物理变化时,分子未变,只是分子间间隔
发生了改变。
练习
保持水的化学性质的最小微粒是( ),保持氧
气的化学性质的最小微粒是( ),保持二氧化
碳的化学性质的最小微粒是( )
水分子
氧气分子
二氧化碳分子
HH+氢气(H2)氧气(O2)水(H2O)OOOHHO通电HHHHOO重新组合化学变化中最小的粒子---分子和原子的本质区别:原子在化学变化中,分子可分,原子不可分(由分子构成的物质)保持物质化学性质的最小粒子:分子HHHH1.化学变化的实质是:
分子 。
原子
新分子
2过氧化氢分解的过程中不能再分的粒子是 和
,所以说原子是 中最小的粒子。
氢原子
氧原子
化学变化
如:C + O2 CO2的变化中,最小的微粒是
和 。
氧原子
碳原子
分解为
重新组合
点燃
分子与原子的区别和联系
分子 原子
基本性质 定义
本质区别 联系 体积小、质量小、不停地运动、微粒之间有间隔
化学变化中的最小粒子
化学变化中分子可以再分,而原子不能再分
分子可以分裂为原子,原子可以相互结合形成分子
保持物质化学性质的最小粒子
2.氧气是由 构成的,其化学式为 ,金属汞
是由 构成的,汞的化学式为 。
1.氧化汞分子分解为 和 ,每两个
氧原子结合成 ,许多的氧气分子聚集成氧
气,许多 聚集成金属汞。
汞原子
分子
原子
氧原子
1个氧气分子
汞原子
O2
Hg
氧化汞分子
汞原子、氧气分子
汞原子 氧原子
探究总结
1、下列关于物质构成的叙述错误的是( )
A、水是由氢分子和氧分子构成的
B、金属铜由铜原子构成
C、二氧化碳由二氧化碳分子构成
D、氧气由氧分子构成
A
我会应用
2、 下列物质由原子直接构成的是 ( )
A.二氧化碳 B.二氧化硫 C.铁 D.氧气
我会应用
c
3、根据课本上“用扫描隧道显微镜获得的苯分子的图象” 图片不可以直接得出的结论是( )
A.分子、原子的体积是很小的
B.分子、原子是真实存在的
C.分子、原子间有一定的间隔
D.分子、原子能保持物质的化学性质
D
4、在氢气燃烧的反应中,没有发生变化的微粒是 ( )
A.氧分子 B.氢分子
C.水分子 D. 氢原子和氧原子
D
我会应用
3.1 分子和原子第2课时
复习巩固:
1.生活中的下列现象,用分子的相关知识解释不正确的是 ( )
A.湿衣服晾在太阳底下干得快,说明分子运动速率与温度有关
B.成熟的菠萝蜜会散发出浓浓的香味,说明分子在不断地运动
C.水沸腾时,掀起壶盖,说明分子大小随温度升高而增大
D.液化石油气须加压后贮存在钢瓶中,说明分子之间有间隙
C
2.右图信息能说明 ( )
A.分子很小 B.分子间有同隔
C.分子总是在不断运动 D.分子是构成物质的唯一微粒
A
复习引入:上节课我们讲到,水等都是由分子构成的。那么分子是不是构成物质的最小的粒子,它能不能再进行分割呢?如果能分,那分子又是什么构成的呢?
几种分子的模型
水分子
氧分子
氢分子
分子是由原子构成,分子还能不能再分呢
一个氢原子
一个氧原子
两个氢原子组成一个氢分子
两个氧原子组成一个氧分子
两个氢原子和一个氧原子组成一个水分子
所以说:分子是由原子构成的。
H
H
H
O
O
O
O
H
H
1、氧气分子是由 构成的。
一个氧气分子由 构成的。
2、水分子是由 和 构成的。
一个水分子是由___________
和 构成的。
几种说法:
氧原子
二个氧原子
氢原子
氧原子
二个氢原子
一个氧原子
二、分子可以分为原子
1、由分子构成的物质在发生物理变化时,分子本身没有变化。
2、由分子构成的物质在发生化学变化时,一种物质的分子会变成其他物质的分子。
用分子的观点解释(由分子构成的物质)
物理变化:
化学变化:
分子本身没有发生变化,只
是分子间的间隔发生变化。
分子本身发生变化 ,生成新 的分子。
由分子构成的物质在物质发生物理变化时,分子没有变化,物质的化学性质也没变化。由分子构成的物质在物质发生化学变化时,分子变了,变成了别的物质的分子,但原子不变。可见,
分子是保持物质化学性质的最小微粒。
分子的概念
分子是保持物质化学性质的最小粒子
氧气
受热
水
水蒸气
水
氢气
+
通电
物理变化,分子本身不改变
化学变化,分子本身
发生了变化
同种物质的分子性质相同,不同物质的分子性质不同
分子是保持物质化学性质的最小粒子。
理解:(1)由同种分子构成的物质,化学性质相同; 不同种分子构成的物质,化学性质不同。
(2)物质发生化学变化时,分子发生了改变;
物质发生物理变化时,分子未变,只是分子间间隔
发生了改变。
练习
保持水的化学性质的最小微粒是( ),保持氧
气的化学性质的最小微粒是( ),保持二氧化
碳的化学性质的最小微粒是( )
水分子
氧气分子
二氧化碳分子
HH+氢气(H2)氧气(O2)水(H2O)OOOHHO通电HHHHOO重新组合化学变化中最小的粒子---分子和原子的本质区别:原子在化学变化中,分子可分,原子不可分(由分子构成的物质)保持物质化学性质的最小粒子:分子HHHH1.化学变化的实质是:
分子 。
原子
新分子
2过氧化氢分解的过程中不能再分的粒子是 和
,所以说原子是 中最小的粒子。
氢原子
氧原子
化学变化
如:C + O2 CO2的变化中,最小的微粒是
和 。
氧原子
碳原子
分解为
重新组合
点燃
分子与原子的区别和联系
分子 原子
基本性质 定义
本质区别 联系 体积小、质量小、不停地运动、微粒之间有间隔
化学变化中的最小粒子
化学变化中分子可以再分,而原子不能再分
分子可以分裂为原子,原子可以相互结合形成分子
保持物质化学性质的最小粒子
2.氧气是由 构成的,其化学式为 ,金属汞
是由 构成的,汞的化学式为 。
1.氧化汞分子分解为 和 ,每两个
氧原子结合成 ,许多的氧气分子聚集成氧
气,许多 聚集成金属汞。
汞原子
分子
原子
氧原子
1个氧气分子
汞原子
O2
Hg
氧化汞分子
汞原子、氧气分子
汞原子 氧原子
探究总结
1、下列关于物质构成的叙述错误的是( )
A、水是由氢分子和氧分子构成的
B、金属铜由铜原子构成
C、二氧化碳由二氧化碳分子构成
D、氧气由氧分子构成
A
我会应用
2、 下列物质由原子直接构成的是 ( )
A.二氧化碳 B.二氧化硫 C.铁 D.氧气
我会应用
c
3、根据课本上“用扫描隧道显微镜获得的苯分子的图象” 图片不可以直接得出的结论是( )
A.分子、原子的体积是很小的
B.分子、原子是真实存在的
C.分子、原子间有一定的间隔
D.分子、原子能保持物质的化学性质
D
4、在氢气燃烧的反应中,没有发生变化的微粒是 ( )
A.氧分子 B.氢分子
C.水分子 D. 氢原子和氧原子
D
我会应用
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
