2022-2023学年鲁教版化学第八单元--海水中的化学(有答案)
文档属性
| 名称 | 2022-2023学年鲁教版化学第八单元--海水中的化学(有答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 167.2KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-09-30 00:00:00 | ||
图片预览



文档简介
2022-2023学年鲁教版化学第八单元--海水中的化学
一、单选题
1.下列有关实验现象描述正确的是
A.细铁丝在氧气中燃烧生成红色固体 B.红磷在空气中燃烧产生大量白烟
C.Na2CO3溶液中滴加澄清石灰水,无明显现象 D.硝酸铵溶于水时会放出大量的热
2.下列关于碳酸钠与碳酸氢钠的说法错误的是( )
A.溶液呈碱性 B.固体难溶于水
C.“纯碱”是碳酸钠的俗名 D.可用于烘焙糕点
3.下列物质属于盐的是
A.Fe B.CuO C.Na2CO3 D.H2SO4
4.化学与生活密切相关。下列说法错误的是
A.活性炭可用作冰箱除味剂
B.碳酸钡可用于胃肠X射线造影检查
C.氢氧化铝可用于中和过多胃酸
D.碳酸钠可用于去除餐具的油污
5.下列物质既可以做治疗胃酸的胃药,又可以做面点发酵剂的是
A.NaCl
B.NaOH
C.NaHCO3
D.Na2SO4
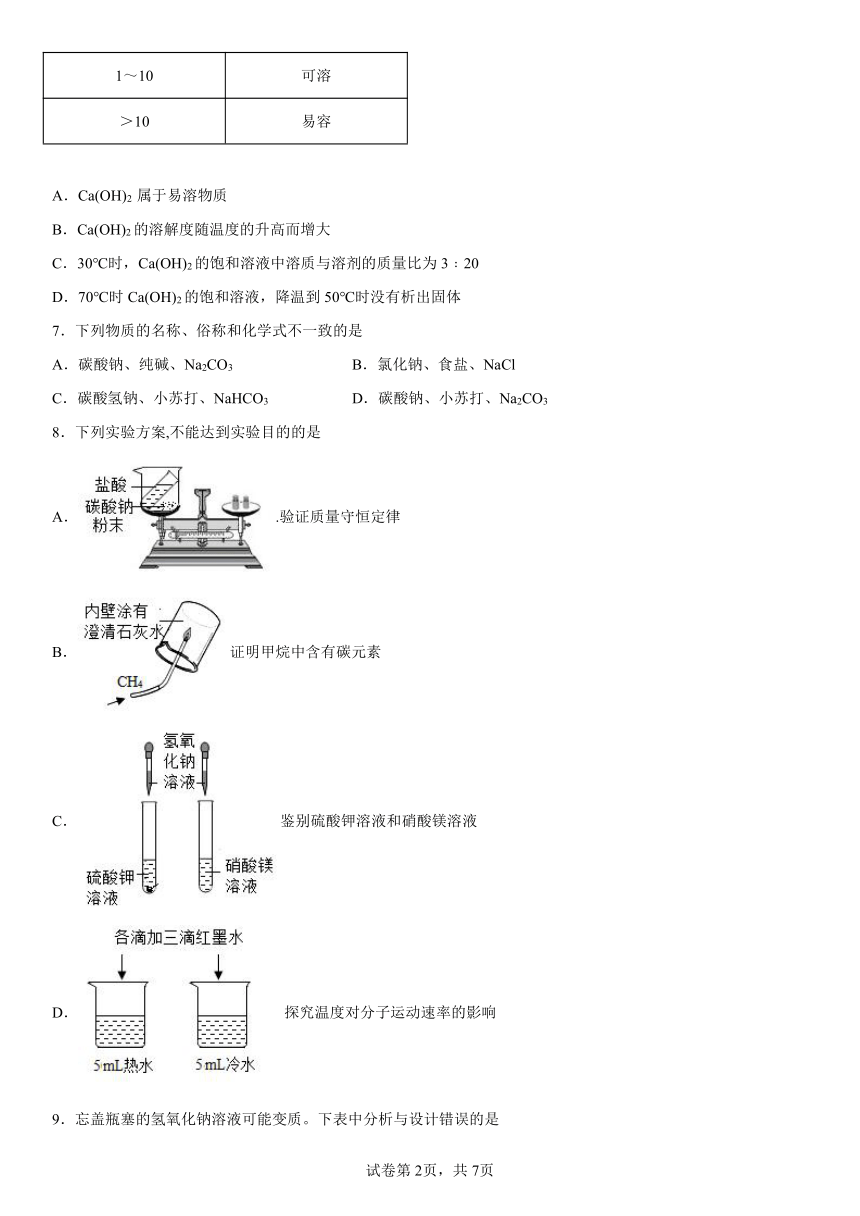
6.下图为Ca(OH)2的溶解度曲线;下表为20℃时溶解度的相对大小。下列说法正确的是( )
溶解度/g 一般称为
<0.01 难溶
0.01~1 微溶
1~10 可溶
>10 易容
A.Ca(OH)2 属于易溶物质
B.Ca(OH)2的溶解度随温度的升高而增大
C.30℃时,Ca(OH)2的饱和溶液中溶质与溶剂的质量比为3﹕20
D.70℃时Ca(OH)2的饱和溶液,降温到50℃时没有析出固体
7.下列物质的名称、俗称和化学式不一致的是
A.碳酸钠、纯碱、Na2CO3 B.氯化钠、食盐、NaCl
C.碳酸氢钠、小苏打、NaHCO3 D.碳酸钠、小苏打、Na2CO3
8.下列实验方案,不能达到实验目的的是
A..验证质量守恒定律
B.证明甲烷中含有碳元素
C.鉴别硫酸钾溶液和硝酸镁溶液
D.探究温度对分子运动速率的影响
9.忘盖瓶塞的氢氧化钠溶液可能变质。下表中分析与设计错误的是
选项 问题 分析与设计
A 为何变质 2NaOH + CO2 = Na2CO3 + H2O
B 是否变质 取样,加入足量稀盐酸,观察是否产生气泡
C 是否全部变质 取样,加入足量氯化钙溶液,观察产生沉淀多少
D 如何除去杂质 取样,加入适量氢氧化钙溶液,过滤
A.A B.B C.C D.D
10.下列有关溶液的叙述正确的是
A.植物油与水混合一定形成溶液 B.食盐水倒出一半后浓度降低
C.升温会降低二氧化碳在水中的溶解度 D.蔗糖可以无限溶解在一定量的水中
11.向一定质量的某H2SO4溶液中加入足量的BaCl2溶液,所得沉淀质量等于原H2SO4溶液质量的1/2。则原H2SO4溶液中溶质的质量分数约为
A.45% B.30% C.21% D.11%
12.某同学在探究物质溶解的热现象及温度对物质溶解度影响时,设计了如下实验,现象如图一所示,溶解度曲线如图二所示,下列说法正确的是
A.M的溶解度曲线为a曲线
B.升温可以使N的饱和溶液变浑浊
C.M的饱和溶液从t2℃降温到t1℃时,溶质质量分数变大
D.如果t2℃时,M、N的饱和溶液质量相等,则溶剂质量M>N
13.如图是a、b、c三种物质的溶解度曲线,下列说法正确的是
A.t2℃时,等质量的a、b、c配成饱和溶液,所得溶液质量a>b>c
B.将t2℃a、b、c的饱和溶液降温至t1℃,析出晶体的质量a>b>c
C.t2℃时,a、b、c的饱和溶液蒸发相同质量的水,析出晶体质量a>b>c
D.将t1℃时,a、b、c三种物质的饱和溶液升温至t2℃,其溶质质量分数由大到小的顺序是a>b>c
14.鉴别①NaCl ②MgSO4 ③CuCl2 ④BaCl2 ⑤NaOH五种溶液,不用其它试剂,则被鉴别出来物质的顺序正确的是
A.③②⑤④① B.③⑤②④① C.③⑤④①② D.③②⑤①④
15.某同学总结的Ca(OH)2的化学性质如图,下列说法错误的是
A.甲一定是碳酸盐
B.反应②为放热反应
C.反应③可用于检验某种温室气体
D.向澄清石灰水中加入紫色石蕊试液,试液由紫色变为蓝色
二、填空题
16.如图,是某实验小组制取蒸馏水的简易装置,请回答:
(1)为了使烧瓶受热均匀,瓶底应垫_____(填仪器名称)。烧杯中的水应装_____(填序号:A 沸水 B温水 C 冷水)。
(2)制得一试管蒸馏水,实验完成后,下列操作的顺序先后为_____(填序号)。
A 移出酒精灯并熄灭
B 移开试管和烧杯
17.为了探究“水的净化”过程,某实验小组从河水中取来水样进行实验:
(1)实验小组的同学应用_____量取50 mL的水,读数时视线应与_____保持水平;
(2)如图是某同学制作的简易净水器,请回答有关问题:
在简易净水器中装入小卵石、石英砂的目的是_____;活性炭的作用是_____。
(3)如果某硬水通过该简易净水器净化,则净化后得到的水是_____(填“硬水”或“软水”)。
(4)长期饮用硬水对健康不利,要降低水的硬度,可采取_____的方法。
18.甲、乙、丙三种固体物质的溶解度曲线如下图所示,回答下列问题:
(1)A点的含义是_____。
(2)将图中N点的甲溶液转化为M点的甲溶液的方法中一定可行的是_____。
(3)将甲、乙、丙三种物质的饱和溶液从降到,所得溶液的溶质的质量分数从大到小的顺序是_____。
(4)当乙物质中混有少量甲物质时,可采用_____(填“降温结晶”或“蒸发结晶”)的方法提纯乙物质;
(5)A、B两杯的质量分别为100g和200g的乙物质的不饱和溶液,已知二者的溶质的质量分数相同。现对两杯溶液同时恒温蒸发水(蒸发水的速率相同),则先有晶体析出的是_____。(填“A”或“B”)
(6)欲用50g的丙的饱和溶液配制5%的丙的稀溶液需要加入水的质量为_____。配制过程中若量取丙的饱和溶液时采用俯视读数则会造成所配溶液的质量分数_____。(填“偏大”或“偏小”)
19.根据如图所示的甲、乙、丙的溶解度曲线,回答以下问题:
(1)P点表示的意义______。
(2)乙中含有少量甲,要提纯乙可采用的方法是______。
(3)写出一种将丙的接近饱和的溶液变成饱和溶液的方法______。
(4)t3℃时,等质量的甲、乙、丙分别配成饱和溶液,需水的质量由多到少的顺序是______。
(5)下列说法错误的是______(填序号)。
①在t2℃时,将15g甲物质放入50g水中,所得到的溶液质量为65g
②将甲的溶液由t3℃降温到t2℃,一定有晶体析出
③将t3℃时等质量的甲、乙、丙三种物质的饱和溶液都降温到t2℃,三种溶液中溶质的质量分数由大到小的顺序为乙>甲=丙
三、实验题
20.用下图所示装置(气密性良好)验证氢氧化钠的性质。已知:碳酸钠溶液显碱性。
(1)实验时,关闭K1、K2和K3,先将注射器中少量(约2mL)20%的NaOH溶液缓慢推入A中后停止推动活塞,剩余的NaOH溶液能够自动吸入A中,产生该现象的原因是_____。
(2)打开K1、K3,能观察到C中溶液进入A中,C中导管下端露出液面。
(3)再打开K2,B中溶液进入A和C。能证明A中二氧化碳与氢氧化钠反应生成新物质的现象____;能证明氢氧化钠与盐酸反应的现象是____,反应的化学方程式为____。
21.水是生命之源,请回答下列问题。
(1)在水的净化过程中常加入明矾,明矾的作用是_________ ;
(2)制蒸馏水时,在蒸馏烧瓶中加入沸石(或碎瓷片),沸石(或碎瓷片)的作用是________ ;
(3)如图为电解水的装置,通电前,为增强导电性加入了少量的硫酸钠,再加入酚酞溶液,溶液呈无色,通电一段时间后,a试管中收集到的气体是_________,b试管中的水溶液呈红色,说明b试管中溶液pH______7(填“>”、“<”或“=”)。
四、计算题
22.高温煅烧12.5g大理石,完全分解产生4.4g二氧化碳。求:
(1)大理石中碳酸钙的质量为___________g。(根据化学方程式列式计算)
(2)大理石中碳酸钙的质量分数为___________。
23.鸡蛋壳的主要成分是碳酸钙。某兴趣小组为了测定鸡蛋壳中CaCO3的含量,取12.5g干燥的鸡蛋壳,捣碎放在烧杯中,然后向其中滴加某浓度的稀盐酸滴加过程中产生气体质量与所加稀盐酸质量的关系如图所示(鸡蛋壳中除CaCO3外的其他成分都不溶于水,也不与稀盐酸反应)。试计算:
(1)产生CO2的质量为 g。
(2)该鸡蛋壳中CaCO3的质量分数;
(3)所用稀盐酸溶质的质量分数。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.B
3.D
4.B
5.C
6.D
7.D
8.A
9.C
10.C
11.C
12.D
13.C
14.B
15.A
16.(1) 石棉网 C (2)BA
17.(1) 50 mL的量筒 液体凹液面的最低处 (2) 过滤 吸附色素和异味等(3) 硬水 煮沸(或蒸馏)
18.(1) t2℃时,甲、丙物质的溶解度相等 (2) 增加溶质或恒温蒸发 乙>甲>丙 蒸发结晶(3) A 150g 偏小
19.(1)t2℃时,甲、丙物质的溶解度相等
(2)蒸发结晶
(3)增加溶质(或升高温度或蒸发溶剂)
(4)丙>乙>甲
(5)①②③
20.(1) CO2与NaOH溶液反应而消耗,使A中压强低于外界大气压,NaOH溶液被压入 (2) A中有气泡产生 C中红色溶液褪为无色 (3) NaOH+HCl=NaCl+H2O
21.(1) 吸附悬浮杂质,加快沉降 (2) 防止液体暴沸 (3) 氧气(或O2) >
22.(1)大理石中碳酸钙的质量为10g;
(2)大理石中碳酸钙的质量分数为。
23.(1)4.4(2)80%(3)7.3%
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列有关实验现象描述正确的是
A.细铁丝在氧气中燃烧生成红色固体 B.红磷在空气中燃烧产生大量白烟
C.Na2CO3溶液中滴加澄清石灰水,无明显现象 D.硝酸铵溶于水时会放出大量的热
2.下列关于碳酸钠与碳酸氢钠的说法错误的是( )
A.溶液呈碱性 B.固体难溶于水
C.“纯碱”是碳酸钠的俗名 D.可用于烘焙糕点
3.下列物质属于盐的是
A.Fe B.CuO C.Na2CO3 D.H2SO4
4.化学与生活密切相关。下列说法错误的是
A.活性炭可用作冰箱除味剂
B.碳酸钡可用于胃肠X射线造影检查
C.氢氧化铝可用于中和过多胃酸
D.碳酸钠可用于去除餐具的油污
5.下列物质既可以做治疗胃酸的胃药,又可以做面点发酵剂的是
A.NaCl
B.NaOH
C.NaHCO3
D.Na2SO4
6.下图为Ca(OH)2的溶解度曲线;下表为20℃时溶解度的相对大小。下列说法正确的是( )
溶解度/g 一般称为
<0.01 难溶
0.01~1 微溶
1~10 可溶
>10 易容
A.Ca(OH)2 属于易溶物质
B.Ca(OH)2的溶解度随温度的升高而增大
C.30℃时,Ca(OH)2的饱和溶液中溶质与溶剂的质量比为3﹕20
D.70℃时Ca(OH)2的饱和溶液,降温到50℃时没有析出固体
7.下列物质的名称、俗称和化学式不一致的是
A.碳酸钠、纯碱、Na2CO3 B.氯化钠、食盐、NaCl
C.碳酸氢钠、小苏打、NaHCO3 D.碳酸钠、小苏打、Na2CO3
8.下列实验方案,不能达到实验目的的是
A..验证质量守恒定律
B.证明甲烷中含有碳元素
C.鉴别硫酸钾溶液和硝酸镁溶液
D.探究温度对分子运动速率的影响
9.忘盖瓶塞的氢氧化钠溶液可能变质。下表中分析与设计错误的是
选项 问题 分析与设计
A 为何变质 2NaOH + CO2 = Na2CO3 + H2O
B 是否变质 取样,加入足量稀盐酸,观察是否产生气泡
C 是否全部变质 取样,加入足量氯化钙溶液,观察产生沉淀多少
D 如何除去杂质 取样,加入适量氢氧化钙溶液,过滤
A.A B.B C.C D.D
10.下列有关溶液的叙述正确的是
A.植物油与水混合一定形成溶液 B.食盐水倒出一半后浓度降低
C.升温会降低二氧化碳在水中的溶解度 D.蔗糖可以无限溶解在一定量的水中
11.向一定质量的某H2SO4溶液中加入足量的BaCl2溶液,所得沉淀质量等于原H2SO4溶液质量的1/2。则原H2SO4溶液中溶质的质量分数约为
A.45% B.30% C.21% D.11%
12.某同学在探究物质溶解的热现象及温度对物质溶解度影响时,设计了如下实验,现象如图一所示,溶解度曲线如图二所示,下列说法正确的是
A.M的溶解度曲线为a曲线
B.升温可以使N的饱和溶液变浑浊
C.M的饱和溶液从t2℃降温到t1℃时,溶质质量分数变大
D.如果t2℃时,M、N的饱和溶液质量相等,则溶剂质量M>N
13.如图是a、b、c三种物质的溶解度曲线,下列说法正确的是
A.t2℃时,等质量的a、b、c配成饱和溶液,所得溶液质量a>b>c
B.将t2℃a、b、c的饱和溶液降温至t1℃,析出晶体的质量a>b>c
C.t2℃时,a、b、c的饱和溶液蒸发相同质量的水,析出晶体质量a>b>c
D.将t1℃时,a、b、c三种物质的饱和溶液升温至t2℃,其溶质质量分数由大到小的顺序是a>b>c
14.鉴别①NaCl ②MgSO4 ③CuCl2 ④BaCl2 ⑤NaOH五种溶液,不用其它试剂,则被鉴别出来物质的顺序正确的是
A.③②⑤④① B.③⑤②④① C.③⑤④①② D.③②⑤①④
15.某同学总结的Ca(OH)2的化学性质如图,下列说法错误的是
A.甲一定是碳酸盐
B.反应②为放热反应
C.反应③可用于检验某种温室气体
D.向澄清石灰水中加入紫色石蕊试液,试液由紫色变为蓝色
二、填空题
16.如图,是某实验小组制取蒸馏水的简易装置,请回答:
(1)为了使烧瓶受热均匀,瓶底应垫_____(填仪器名称)。烧杯中的水应装_____(填序号:A 沸水 B温水 C 冷水)。
(2)制得一试管蒸馏水,实验完成后,下列操作的顺序先后为_____(填序号)。
A 移出酒精灯并熄灭
B 移开试管和烧杯
17.为了探究“水的净化”过程,某实验小组从河水中取来水样进行实验:
(1)实验小组的同学应用_____量取50 mL的水,读数时视线应与_____保持水平;
(2)如图是某同学制作的简易净水器,请回答有关问题:
在简易净水器中装入小卵石、石英砂的目的是_____;活性炭的作用是_____。
(3)如果某硬水通过该简易净水器净化,则净化后得到的水是_____(填“硬水”或“软水”)。
(4)长期饮用硬水对健康不利,要降低水的硬度,可采取_____的方法。
18.甲、乙、丙三种固体物质的溶解度曲线如下图所示,回答下列问题:
(1)A点的含义是_____。
(2)将图中N点的甲溶液转化为M点的甲溶液的方法中一定可行的是_____。
(3)将甲、乙、丙三种物质的饱和溶液从降到,所得溶液的溶质的质量分数从大到小的顺序是_____。
(4)当乙物质中混有少量甲物质时,可采用_____(填“降温结晶”或“蒸发结晶”)的方法提纯乙物质;
(5)A、B两杯的质量分别为100g和200g的乙物质的不饱和溶液,已知二者的溶质的质量分数相同。现对两杯溶液同时恒温蒸发水(蒸发水的速率相同),则先有晶体析出的是_____。(填“A”或“B”)
(6)欲用50g的丙的饱和溶液配制5%的丙的稀溶液需要加入水的质量为_____。配制过程中若量取丙的饱和溶液时采用俯视读数则会造成所配溶液的质量分数_____。(填“偏大”或“偏小”)
19.根据如图所示的甲、乙、丙的溶解度曲线,回答以下问题:
(1)P点表示的意义______。
(2)乙中含有少量甲,要提纯乙可采用的方法是______。
(3)写出一种将丙的接近饱和的溶液变成饱和溶液的方法______。
(4)t3℃时,等质量的甲、乙、丙分别配成饱和溶液,需水的质量由多到少的顺序是______。
(5)下列说法错误的是______(填序号)。
①在t2℃时,将15g甲物质放入50g水中,所得到的溶液质量为65g
②将甲的溶液由t3℃降温到t2℃,一定有晶体析出
③将t3℃时等质量的甲、乙、丙三种物质的饱和溶液都降温到t2℃,三种溶液中溶质的质量分数由大到小的顺序为乙>甲=丙
三、实验题
20.用下图所示装置(气密性良好)验证氢氧化钠的性质。已知:碳酸钠溶液显碱性。
(1)实验时,关闭K1、K2和K3,先将注射器中少量(约2mL)20%的NaOH溶液缓慢推入A中后停止推动活塞,剩余的NaOH溶液能够自动吸入A中,产生该现象的原因是_____。
(2)打开K1、K3,能观察到C中溶液进入A中,C中导管下端露出液面。
(3)再打开K2,B中溶液进入A和C。能证明A中二氧化碳与氢氧化钠反应生成新物质的现象____;能证明氢氧化钠与盐酸反应的现象是____,反应的化学方程式为____。
21.水是生命之源,请回答下列问题。
(1)在水的净化过程中常加入明矾,明矾的作用是_________ ;
(2)制蒸馏水时,在蒸馏烧瓶中加入沸石(或碎瓷片),沸石(或碎瓷片)的作用是________ ;
(3)如图为电解水的装置,通电前,为增强导电性加入了少量的硫酸钠,再加入酚酞溶液,溶液呈无色,通电一段时间后,a试管中收集到的气体是_________,b试管中的水溶液呈红色,说明b试管中溶液pH______7(填“>”、“<”或“=”)。
四、计算题
22.高温煅烧12.5g大理石,完全分解产生4.4g二氧化碳。求:
(1)大理石中碳酸钙的质量为___________g。(根据化学方程式列式计算)
(2)大理石中碳酸钙的质量分数为___________。
23.鸡蛋壳的主要成分是碳酸钙。某兴趣小组为了测定鸡蛋壳中CaCO3的含量,取12.5g干燥的鸡蛋壳,捣碎放在烧杯中,然后向其中滴加某浓度的稀盐酸滴加过程中产生气体质量与所加稀盐酸质量的关系如图所示(鸡蛋壳中除CaCO3外的其他成分都不溶于水,也不与稀盐酸反应)。试计算:
(1)产生CO2的质量为 g。
(2)该鸡蛋壳中CaCO3的质量分数;
(3)所用稀盐酸溶质的质量分数。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.B
3.D
4.B
5.C
6.D
7.D
8.A
9.C
10.C
11.C
12.D
13.C
14.B
15.A
16.(1) 石棉网 C (2)BA
17.(1) 50 mL的量筒 液体凹液面的最低处 (2) 过滤 吸附色素和异味等(3) 硬水 煮沸(或蒸馏)
18.(1) t2℃时,甲、丙物质的溶解度相等 (2) 增加溶质或恒温蒸发 乙>甲>丙 蒸发结晶(3) A 150g 偏小
19.(1)t2℃时,甲、丙物质的溶解度相等
(2)蒸发结晶
(3)增加溶质(或升高温度或蒸发溶剂)
(4)丙>乙>甲
(5)①②③
20.(1) CO2与NaOH溶液反应而消耗,使A中压强低于外界大气压,NaOH溶液被压入 (2) A中有气泡产生 C中红色溶液褪为无色 (3) NaOH+HCl=NaCl+H2O
21.(1) 吸附悬浮杂质,加快沉降 (2) 防止液体暴沸 (3) 氧气(或O2) >
22.(1)大理石中碳酸钙的质量为10g;
(2)大理石中碳酸钙的质量分数为。
23.(1)4.4(2)80%(3)7.3%
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第七单元 常见的酸和碱
- 第一节 酸及其性质
- 第二节 碱及其性质
- 第三节 溶液的酸碱性
- 第四节 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 第八单元 海水中的化学
- 第一节 海洋化学资源
- 第二节 海水“晒盐“
- 第三节 海水“制碱“
- 到实验室去:粗盐中难溶性杂质的去除
- 第九单元 金属
- 第一节 常见的金属材料
- 第二节 金属的化学性质
- 第三节 钢铁的锈蚀与防护
- 到实验室去 探究金属的性质
- 第十单元 化学与健康
- 第一节 食物中的有机物
- 第二节 化学元素与人体健康
- 第三节 远离有毒物质
- 第十一单元 化学与社会发展
- 第一节 化学与能源开发
- 第二节 化学与材料研制
- 第三节 化学与农业生产
- 第四节 化学与环境保护
