2022—203学年化学人教九上第6单元 碳和碳的氧化物 分层优习题 (有答案)
文档属性
| 名称 | 2022—203学年化学人教九上第6单元 碳和碳的氧化物 分层优习题 (有答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 1.6MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-10-01 00:00:00 | ||
图片预览




文档简介
2022—203学年化学人教九上第6单元 碳和碳的氧化物 分层优习题含答案
**人教九上第6单元 碳和碳的氧化物**
一、选择题。
1、定向爆破伴有反应:2Al+Fe2O3Al2O3+2Fe,此反应中还原剂是( )
A.Al B.Fe C.Fe2O3 D.Al2O3
2、下列药品组合最适合用来实验室制取二氧化碳的是( )
A.浓盐酸、石灰石 B.稀硫酸、大理石
C.稀盐酸、碳酸钠粉末 D.稀盐酸、石灰石
3、小明用软塑料瓶自制了一套气体发生装置(如图),下列关于该装置的说法错误的是( )
A.通过捏放瓶身可随时控制反应的发生和停止
B.利用该装置可制取二氧化碳
C.利用该装置制取氧气,液体药品为过氧化氢溶液
D.利用该装置制取氧气,无纺布包内二氧化锰越多,生成氧气就越多
4、实验室制取二氧化碳常用的方法是( )
A.木炭在氧气中燃烧 B.碳酸钠和稀盐酸反应
C.大理石和稀硫酸反应 D.石灰石和稀盐酸反应
5、可用同一化学原理解释的现象是( )
①久置的石灰水,液面上出现一层硬壳状薄膜
②向澄清石灰水中通入人体呼出的气体,澄清石灰水变浑浊
③为了使石灰浆粉刷的墙壁快点晾干,在室内生起一盆炭火,开始时墙壁反而潮湿
④人们用澄清石灰水保鲜鸡蛋
A.①②③④ B.①②④ C.①③④ D.②③④
6、汽车尾气中的CO在四氧化三钴(Co3O4)纳米棒的催化作用下,低温即与O2反应生成CO2.下列关于该反应的说法中,错误的是( )
A.反应类型为化合反应 B.可降低汽车尾气对大气的污染
C.反应前后Co3O4化学组成改变 D.反应前后碳元素的化合价改变
7、空气与按5:1的体积比混合后与足量的赤热焦炭反应,最后得到混合气体的主要成分是( )
A.和 B.和CO C.和CO D.和
8、检验集气瓶内的二氧化碳是否集满的正确方法是( )
A.注入澄清石灰水 B.将燃着的木条放在集气瓶口
C.注入紫色石蕊试液 D.将燃着的木条伸入集气瓶内
9、镁带能在CO2气体中燃烧:2Mg+CO22MgO+C,该反应中的还原剂是( )
A.Mg B.CO2 C.MgO D.C
10、能证明某气体是CO2的操作及现象是( )
选项 实验操作 实验现象
A 将燃着的木条伸入集气瓶 木条熄灭
B 将带火星的木条伸入集气瓶 木条复燃
C 将气体通入澄清石灰水中 石灰水变浑浊
D 将气体通入紫色石蕊溶液中 溶液变红
A.A B.B C.C D.D
11、鉴别氧气、氢气和二氧化碳3瓶气体时,最简便的方法( )
A.用燃着的木条伸入集气瓶中
B.测定3种气体在标准情况下的密度
C.将3种气体分别通过澄清的石灰水
D.比较3种气体的溶解度
12、列有关碳单质的说法错误的是( )
A.金刚石、石墨充分燃烧的产物都是二氧化碳
B.金刚石和石墨的物理性质不同的原因是碳原子的排列方式不同
C.书写档案时规定使用碳素墨水,是因为常温下碳的化学性质不活泼
D.金刚石和石墨都是硬度最大的物质
13、在氧化还原反应中,得到氧(即有元素化合价升高)的物质是还原剂;失去氧(即有元素化合价降低)的物质是氧化剂.在反应:H2+CuO Cu+H2O中,属于还原剂的是( )
A.H2 B.CuO C.Cu D.H2O
14、NO是一种无色气体,实验室制备NO必须用排水法收集。由此可以得出的结论是( )
A.NO难溶于水 B.NO会与氧气反应
C.NO有毒 D.NO密度与空气接近
15、在任何条件下也不与反应的物质( )
A. B.C C. D.
16、实验室制取干燥的CO2气体,不会用到的装置是( )
二、填空题。
17、自然界中存在一种非常漂亮的孔雀石,其主要成分是碱式碳酸铜,俗称铜绿,化学式为[Cu2(OH)2CO3],受热可分解生成氧化铜、水和二氧化碳。
(1)孔雀石多在原始森林中,人类很早就发现,孔雀石在熊熊燃烧的树木中灼烧后,余烬里有一种红色光亮的金属显露出来,请用两个主要的反应方程式说明这种变化_____;_____。
(2)铜绿分解生成44g二氧化碳的同时,生成CuO的质量_____。
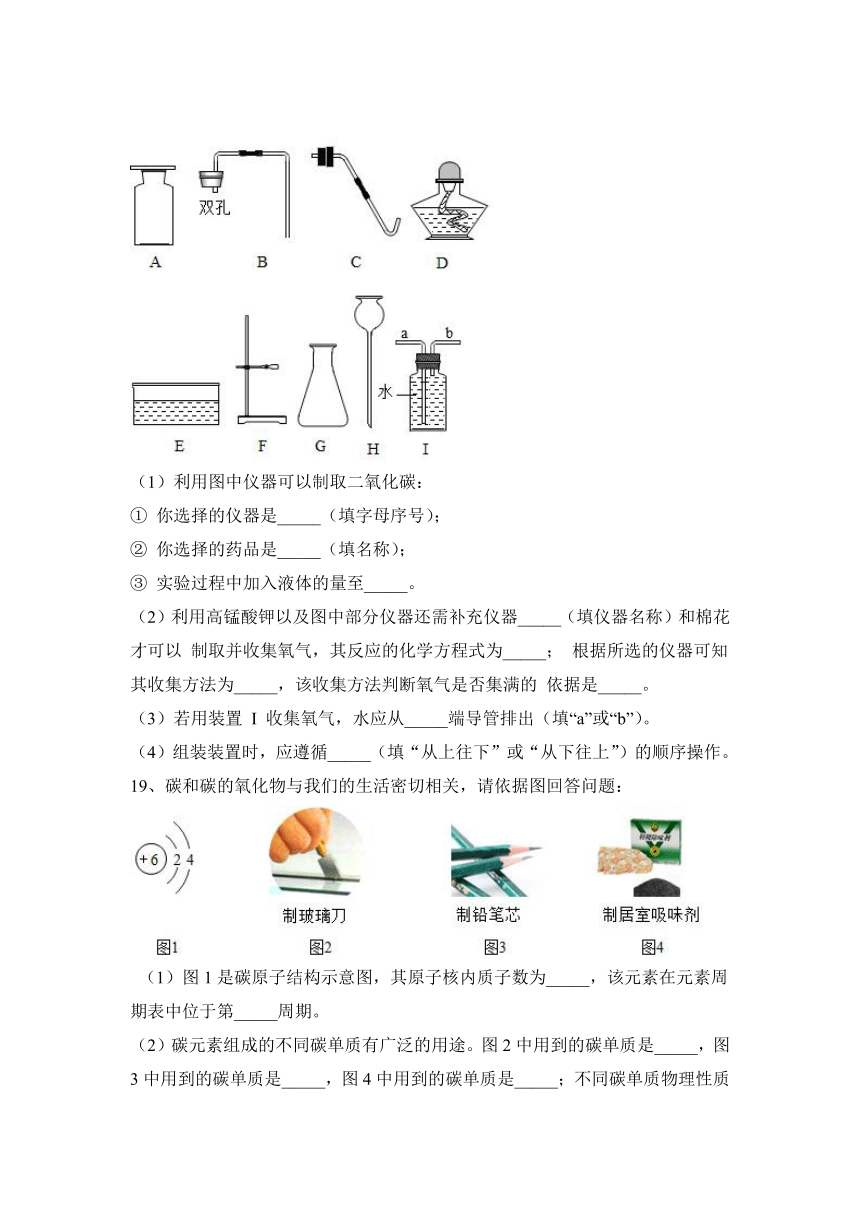
18、在实验室中利用下列仪器进行制取气体的实验,请回答下列问题:
(1)利用图中仪器可以制取二氧化碳:
① 你选择的仪器是_____(填字母序号);
② 你选择的药品是_____(填名称);
③ 实验过程中加入液体的量至_____。
(2)利用高锰酸钾以及图中部分仪器还需补充仪器_____(填仪器名称)和棉花才可以 制取并收集氧气,其反应的化学方程式为_____; 根据所选的仪器可知其收集方法为_____,该收集方法判断氧气是否集满的 依据是_____。
(3)若用装置 I 收集氧气,水应从_____端导管排出(填“a”或“b”)。
(4)组装装置时,应遵循_____(填“从上往下”或“从下往上”)的顺序操作。
19、碳和碳的氧化物与我们的生活密切相关,请依据图回答问题:
(1)图1是碳原子结构示意图,其原子核内质子数为_____,该元素在元素周期表中位于第_____周期。
(2)碳元素组成的不同碳单质有广泛的用途。图2中用到的碳单质是_____,图3中用到的碳单质是_____,图4中用到的碳单质是_____;不同碳单质物理性质存在明显差异的原因是_____。
(3)CO和CO2是碳的两种氧化物。
CO可作燃料,其在空气中燃烧的化学方程式是_____ 。
CO2可制作饮料,其和水反应的化学方程式是_____ 。
20、根据下列装置图,回答问题。
图甲
(1)用高锰酸钾制取氧气,选用的发生装置是________(填序号),为防止高锰酸钾粉末进入导管,该装置需做的一点改进是______________________,若用D装置收集氧气,当观察到__________________时,便可开始收集。
(2)实验室制取二氧化碳应选用的一组装置是________(填序号),反应的化学方程式是_______________________________________________________。
图乙是某同学利用报废试管设计的制取二氧化碳的发生装置,该设计除了废物利用的优点外,请另写一个优点:_____________________________________。
图乙
(3)用收集的氧气完成图E铁丝燃烧的实验,集气瓶中预先放少量水的原因是________________________;如图F向装满CO2的软塑料瓶注入约体积的水,立即旋紧瓶盖,振荡,观察到的现象是________________________。
21、二氧化锰粉末与铝粉在较高温度下发生如下反应:3MnO2+4Al3Mn+2Al2O3,并放出大量的热.在工业上可用此法冶炼难熔金属锰.从得氧、失氧的角度看,二氧化锰在此反应中 (得到或失去)氧而变成单质锰,发生了 反应.该反应中那种物质具有还原性? .
22、实验室制取CO2的药品是_____________ (或_____________)和_________,化学方程式为_____________________ 。
23、实验室久盛石灰水的试剂瓶内壁常附有一层白色污渍,其成分是 ,化学式为 ,写出其形成的化学方程式: 。此污渍 (填“能”或“不能”)用水洗掉,清除此污渍的方法是 ,写出此反应的化学方程式 。
24、下图是某同学设计的实验室制取二氧化碳并验证其性质的实验装置图。
请回答下列问题。
(1)将A、E装置连接时,应将A装置的导管a与E装置的导管________(填“b”或“c”)相连接。检验E装置中二氧化碳已收集满的方法是________________________________。
(2)将A、B装置连接,观察到的现象是____________________________________________,可验证二氧化碳的性质是___________________________________。
(3)将A、C装置连接,可验证二氧化碳能与氢氧化钙反应,该反应的化学方程式为________________________________________________。
(4)用E装置收集满一瓶二氧化碳,取下双孔橡胶塞,将瓶中的气体沿D装置烧杯左侧内壁缓慢倒入,观察到的现象是________________________________________,这些现象说明二氧化碳具有的物理性质是______________________,化学性质是______________,________________。
三、实验类综合题题。
25、学习完二氧化碳制取的研究后,小东在妈妈的帮助下,用家中的用品设计了如下二氧化碳制取与体积测量的实验装置。请回答相关问题:
(1)其中吸管可代替实验室内的________(填仪器名称)。
(2)小东设计的甲装置的优点是______________________________,它与虚线框内的______(填序号)装置具有相同的效果。
(3)小药瓶中植物油上方的空气对实验结果______(填“有”或“无”)影响。请将乙装置中的吸管补画完整。
(4)小东通过丙装置中收集到的液体体积和上网查到的二氧化碳的密度计算出反应生成了0.66 g二氧化碳,请你计算所用蛋壳中碳酸钙的质量。
(相对原子质量:C-12 O-16 Ca-40)
四、计算类题。
26、化学实验小组同学取40g碳和氧化铜的粉末在高温条件下加热一段时间后,称得剩余固体混合物的质量为31.2g,请回答下列问题:
(1)该反应的化学方程式为 。
(2)列出求解参加反应的氧化铜的质量(x)的比例式 。
(3)反应后生成铜的质量为 。
(4)若碳完全反应了,则原混合物中氧化铜的质量分数为 。
2022—203学年化学人教九上第6单元 碳和碳的氧化物 分层优习题含答案
**人教九上第6单元 碳和碳的氧化物**
一、选择题。
1、定向爆破伴有反应:2Al+Fe2O3Al2O3+2Fe,此反应中还原剂是( )
A.Al B.Fe C.Fe2O3 D.Al2O3
【答案】A
2、下列药品组合最适合用来实验室制取二氧化碳的是( )
A.浓盐酸、石灰石 B.稀硫酸、大理石
C.稀盐酸、碳酸钠粉末 D.稀盐酸、石灰石
【答案】D
3、小明用软塑料瓶自制了一套气体发生装置(如图),下列关于该装置的说法错误的是( )
A.通过捏放瓶身可随时控制反应的发生和停止
B.利用该装置可制取二氧化碳
C.利用该装置制取氧气,液体药品为过氧化氢溶液
D.利用该装置制取氧气,无纺布包内二氧化锰越多,生成氧气就越多
【答案】D
4、实验室制取二氧化碳常用的方法是( )
A.木炭在氧气中燃烧 B.碳酸钠和稀盐酸反应
C.大理石和稀硫酸反应 D.石灰石和稀盐酸反应
【答案】D
5、可用同一化学原理解释的现象是( )
①久置的石灰水,液面上出现一层硬壳状薄膜
②向澄清石灰水中通入人体呼出的气体,澄清石灰水变浑浊
③为了使石灰浆粉刷的墙壁快点晾干,在室内生起一盆炭火,开始时墙壁反而潮湿
④人们用澄清石灰水保鲜鸡蛋
A.①②③④ B.①②④ C.①③④ D.②③④
【答案】A
6、汽车尾气中的CO在四氧化三钴(Co3O4)纳米棒的催化作用下,低温即与O2反应生成CO2.下列关于该反应的说法中,错误的是( )
A.反应类型为化合反应 B.可降低汽车尾气对大气的污染
C.反应前后Co3O4化学组成改变 D.反应前后碳元素的化合价改变
【答案】C
7、空气与按5:1的体积比混合后与足量的赤热焦炭反应,最后得到混合气体的主要成分是( )
A.和B.和COC.和COD.和
【答案】B
8、检验集气瓶内的二氧化碳是否集满的正确方法是( )
A.注入澄清石灰水 B.将燃着的木条放在集气瓶口
C.注入紫色石蕊试液 D.将燃着的木条伸入集气瓶内
【答案】B
9、镁带能在CO2气体中燃烧:2Mg+CO22MgO+C,该反应中的还原剂是( )
A.Mg B.CO2 C.MgO D.C
【答案】A
10、能证明某气体是CO2的操作及现象是( )
选项 实验操作 实验现象
A 将燃着的木条伸入集气瓶 木条熄灭
B 将带火星的木条伸入集气瓶 木条复燃
C 将气体通入澄清石灰水中 石灰水变浑浊
D 将气体通入紫色石蕊溶液中 溶液变红
A.A B.B C.C D.D
【答案】C
11、鉴别氧气、氢气和二氧化碳3瓶气体时,最简便的方法( )
A.用燃着的木条伸入集气瓶中
B.测定3种气体在标准情况下的密度
C.将3种气体分别通过澄清的石灰水
D.比较3种气体的溶解度
【答案】A
12、列有关碳单质的说法错误的是( )
A.金刚石、石墨充分燃烧的产物都是二氧化碳
B.金刚石和石墨的物理性质不同的原因是碳原子的排列方式不同
C.书写档案时规定使用碳素墨水,是因为常温下碳的化学性质不活泼
D.金刚石和石墨都是硬度最大的物质
【答案】D
13、在氧化还原反应中,得到氧(即有元素化合价升高)的物质是还原剂;失去氧(即有元素化合价降低)的物质是氧化剂.在反应:H2+CuO Cu+H2O中,属于还原剂的是( )
A.H2 B.CuO C.Cu D.H2O
【答案】A
14、NO是一种无色气体,实验室制备NO必须用排水法收集。由此可以得出的结论是( )
A.NO难溶于水 B.NO会与氧气反应
C.NO有毒 D.NO密度与空气接近
【答案】A
15、在任何条件下也不与反应的物质( )
A. B.C C. D.
【答案】A
16、实验室制取干燥的CO2气体,不会用到的装置是( )
【答案】A
二、填空题。
17、自然界中存在一种非常漂亮的孔雀石,其主要成分是碱式碳酸铜,俗称铜绿,化学式为[Cu2(OH)2CO3],受热可分解生成氧化铜、水和二氧化碳。
(1)孔雀石多在原始森林中,人类很早就发现,孔雀石在熊熊燃烧的树木中灼烧后,余烬里有一种红色光亮的金属显露出来,请用两个主要的反应方程式说明这种变化_____;_____。
(2)铜绿分解生成44g二氧化碳的同时,生成CuO的质量_____。
【答案】
160g
18、在实验室中利用下列仪器进行制取气体的实验,请回答下列问题:
(1)利用图中仪器可以制取二氧化碳:
① 你选择的仪器是_____(填字母序号);
② 你选择的药品是_____(填名称);
③ 实验过程中加入液体的量至_____。
(2)利用高锰酸钾以及图中部分仪器还需补充仪器_____(填仪器名称)和棉花才可以 制取并收集氧气,其反应的化学方程式为_____; 根据所选的仪器可知其收集方法为_____,该收集方法判断氧气是否集满的 依据是_____。
(3)若用装置 I 收集氧气,水应从_____端导管排出(填“a”或“b”)。
(4)组装装置时,应遵循_____(填“从上往下”或“从下往上”)的顺序操作。
【答案】(1)ABGH 大理石和稀盐酸 形成液封
(2)试管 2KMnO4K2MnO4+MnO2+O2↑
排水法 有大气泡从起集气瓶口冒出 (3)a (4)从下往上
19、碳和碳的氧化物与我们的生活密切相关,请依据图回答问题:
(1)图1是碳原子结构示意图,其原子核内质子数为_____,该元素在元素周期表中位于第_____周期。
(2)碳元素组成的不同碳单质有广泛的用途。图2中用到的碳单质是_____,图3中用到的碳单质是_____,图4中用到的碳单质是_____;不同碳单质物理性质存在明显差异的原因是_____。
(3)CO和CO2是碳的两种氧化物。
CO可作燃料,其在空气中燃烧的化学方程式是_____ 。
CO2可制作饮料,其和水反应的化学方程式是_____ 。
【答案】(1). 6 (2). 二 (3). 金刚石
(4). 石墨 (5). 活性炭 (6). 碳原子排列方式不同
(7). 2CO+O22CO2 (8). CO2+H2O=H2CO3
20、根据下列装置图,回答问题。
图甲
(1)用高锰酸钾制取氧气,选用的发生装置是________(填序号),为防止高锰酸钾粉末进入导管,该装置需做的一点改进是______________________,若用D装置收集氧气,当观察到__________________时,便可开始收集。
(2)实验室制取二氧化碳应选用的一组装置是________(填序号),反应的化学方程式是_______________________________________________________。
图乙是某同学利用报废试管设计的制取二氧化碳的发生装置,该设计除了废物利用的优点外,请另写一个优点:_____________________________________。
图乙
(3)用收集的氧气完成图E铁丝燃烧的实验,集气瓶中预先放少量水的原因是________________________;如图F向装满CO2的软塑料瓶注入约体积的水,立即旋紧瓶盖,振荡,观察到的现象是________________________。
【答案】(1)A 在试管口放一团棉花(或其他合理答案均可)
气泡连续均匀冒出
(2)BC CaCO3+2HCl===CaCl2+H2O+CO2↑
节约药品(或可随时控制反应的发生或停止)(其他合理答案均可)
(3)防止集气瓶炸裂(或防止高温熔融物溅落,使瓶底炸裂) 软塑料瓶变瘪
21、二氧化锰粉末与铝粉在较高温度下发生如下反应:3MnO2+4Al3Mn+2Al2O3,并放出大量的热.在工业上可用此法冶炼难熔金属锰.从得氧、失氧的角度看,二氧化锰在此反应中 (得到或失去)氧而变成单质锰,发生了 反应.该反应中那种物质具有还原性? .
【答案】失去;还原;Al.
22、实验室制取CO2的药品是_____________ (或_____________)和_________,化学方程式为_____________________ 。
【答案】石灰石 大理石 稀盐酸 CaCO3+2HCl===CaCl2+H2O+CO2↑
23、实验室久盛石灰水的试剂瓶内壁常附有一层白色污渍,其成分是 ,化学式为 ,写出其形成的化学方程式: 。此污渍 (填“能”或“不能”)用水洗掉,清除此污渍的方法是 ,写出此反应的化学方程式 。
【答案】碳酸钙 CaCO3 CO2+Ca(OH)2CaCO3↓+H2O 不能 加稀盐酸
CaCO3+2HClCaCl2+H2O+CO2↑
24、下图是某同学设计的实验室制取二氧化碳并验证其性质的实验装置图。
请回答下列问题。
(1)将A、E装置连接时,应将A装置的导管a与E装置的导管________(填“b”或“c”)相连接。检验E装置中二氧化碳已收集满的方法是________________________________。
(2)将A、B装置连接,观察到的现象是____________________________________________,可验证二氧化碳的性质是___________________________________。
(3)将A、C装置连接,可验证二氧化碳能与氢氧化钙反应,该反应的化学方程式为________________________________________________。
(4)用E装置收集满一瓶二氧化碳,取下双孔橡胶塞,将瓶中的气体沿D装置烧杯左侧内壁缓慢倒入,观察到的现象是________________________________________,这些现象说明二氧化碳具有的物理性质是______________________,化学性质是______________,________________。
【答案】(1)b 将燃着的木条靠近E瓶c导管口,观察木条是否熄灭 (2)B中溶液由紫色变为红色 二氧化碳能与水反应
(3)Ca(OH)2+CO2===CaCO3↓+H2O
(4)燃着的蜡烛由下至上依次熄灭 密度比空气大 不能燃烧 不支持燃烧
三、实验类综合题题。
25、学习完二氧化碳制取的研究后,小东在妈妈的帮助下,用家中的用品设计了如下二氧化碳制取与体积测量的实验装置。请回答相关问题:
(1)其中吸管可代替实验室内的________(填仪器名称)。
(2)小东设计的甲装置的优点是______________________________,它与虚线框内的______(填序号)装置具有相同的效果。
(3)小药瓶中植物油上方的空气对实验结果______(填“有”或“无”)影响。请将乙装置中的吸管补画完整。
(4)小东通过丙装置中收集到的液体体积和上网查到的二氧化碳的密度计算出反应生成了0.66 g二氧化碳,请你计算所用蛋壳中碳酸钙的质量。
(相对原子质量:C-12 O-16 Ca-40)
【答案】(1)导管 (2)可以随时控制反应的发生和停止 A
(3)无
(4)解:设所用蛋壳中碳酸钙的质量为x。
CaCO3+2HCl=== CaCl2+H2O+CO2↑
100 44
x 0.66 g
=,x=1.5 g
答:所用蛋壳中碳酸钙的质量为1.5 g。
四、计算类题。
26、化学实验小组同学取40g碳和氧化铜的粉末在高温条件下加热一段时间后,称得剩余固体混合物的质量为31.2g,请回答下列问题:
(1)该反应的化学方程式为 。
(2)列出求解参加反应的氧化铜的质量(x)的比例式 。
(3)反应后生成铜的质量为 。
(4)若碳完全反应了,则原混合物中氧化铜的质量分数为 。
【答案】(1)C+2CuO2Cu+CO2↑;
(2)根据质量守恒定律可知,反应生成二氧化碳质量:40g-31.2g=8.8g,
设参加反应的氧化铜的质量为x,
;
(3)设反应后生成铜的质量为y,
y=25.6g;
(4)设碳质量为z,
z=2.4g,
若碳完全反应了,则原混合物中氧化铜的质量分数为:×100%=94%。
**人教九上第6单元 碳和碳的氧化物**
一、选择题。
1、定向爆破伴有反应:2Al+Fe2O3Al2O3+2Fe,此反应中还原剂是( )
A.Al B.Fe C.Fe2O3 D.Al2O3
2、下列药品组合最适合用来实验室制取二氧化碳的是( )
A.浓盐酸、石灰石 B.稀硫酸、大理石
C.稀盐酸、碳酸钠粉末 D.稀盐酸、石灰石
3、小明用软塑料瓶自制了一套气体发生装置(如图),下列关于该装置的说法错误的是( )
A.通过捏放瓶身可随时控制反应的发生和停止
B.利用该装置可制取二氧化碳
C.利用该装置制取氧气,液体药品为过氧化氢溶液
D.利用该装置制取氧气,无纺布包内二氧化锰越多,生成氧气就越多
4、实验室制取二氧化碳常用的方法是( )
A.木炭在氧气中燃烧 B.碳酸钠和稀盐酸反应
C.大理石和稀硫酸反应 D.石灰石和稀盐酸反应
5、可用同一化学原理解释的现象是( )
①久置的石灰水,液面上出现一层硬壳状薄膜
②向澄清石灰水中通入人体呼出的气体,澄清石灰水变浑浊
③为了使石灰浆粉刷的墙壁快点晾干,在室内生起一盆炭火,开始时墙壁反而潮湿
④人们用澄清石灰水保鲜鸡蛋
A.①②③④ B.①②④ C.①③④ D.②③④
6、汽车尾气中的CO在四氧化三钴(Co3O4)纳米棒的催化作用下,低温即与O2反应生成CO2.下列关于该反应的说法中,错误的是( )
A.反应类型为化合反应 B.可降低汽车尾气对大气的污染
C.反应前后Co3O4化学组成改变 D.反应前后碳元素的化合价改变
7、空气与按5:1的体积比混合后与足量的赤热焦炭反应,最后得到混合气体的主要成分是( )
A.和 B.和CO C.和CO D.和
8、检验集气瓶内的二氧化碳是否集满的正确方法是( )
A.注入澄清石灰水 B.将燃着的木条放在集气瓶口
C.注入紫色石蕊试液 D.将燃着的木条伸入集气瓶内
9、镁带能在CO2气体中燃烧:2Mg+CO22MgO+C,该反应中的还原剂是( )
A.Mg B.CO2 C.MgO D.C
10、能证明某气体是CO2的操作及现象是( )
选项 实验操作 实验现象
A 将燃着的木条伸入集气瓶 木条熄灭
B 将带火星的木条伸入集气瓶 木条复燃
C 将气体通入澄清石灰水中 石灰水变浑浊
D 将气体通入紫色石蕊溶液中 溶液变红
A.A B.B C.C D.D
11、鉴别氧气、氢气和二氧化碳3瓶气体时,最简便的方法( )
A.用燃着的木条伸入集气瓶中
B.测定3种气体在标准情况下的密度
C.将3种气体分别通过澄清的石灰水
D.比较3种气体的溶解度
12、列有关碳单质的说法错误的是( )
A.金刚石、石墨充分燃烧的产物都是二氧化碳
B.金刚石和石墨的物理性质不同的原因是碳原子的排列方式不同
C.书写档案时规定使用碳素墨水,是因为常温下碳的化学性质不活泼
D.金刚石和石墨都是硬度最大的物质
13、在氧化还原反应中,得到氧(即有元素化合价升高)的物质是还原剂;失去氧(即有元素化合价降低)的物质是氧化剂.在反应:H2+CuO Cu+H2O中,属于还原剂的是( )
A.H2 B.CuO C.Cu D.H2O
14、NO是一种无色气体,实验室制备NO必须用排水法收集。由此可以得出的结论是( )
A.NO难溶于水 B.NO会与氧气反应
C.NO有毒 D.NO密度与空气接近
15、在任何条件下也不与反应的物质( )
A. B.C C. D.
16、实验室制取干燥的CO2气体,不会用到的装置是( )
二、填空题。
17、自然界中存在一种非常漂亮的孔雀石,其主要成分是碱式碳酸铜,俗称铜绿,化学式为[Cu2(OH)2CO3],受热可分解生成氧化铜、水和二氧化碳。
(1)孔雀石多在原始森林中,人类很早就发现,孔雀石在熊熊燃烧的树木中灼烧后,余烬里有一种红色光亮的金属显露出来,请用两个主要的反应方程式说明这种变化_____;_____。
(2)铜绿分解生成44g二氧化碳的同时,生成CuO的质量_____。
18、在实验室中利用下列仪器进行制取气体的实验,请回答下列问题:
(1)利用图中仪器可以制取二氧化碳:
① 你选择的仪器是_____(填字母序号);
② 你选择的药品是_____(填名称);
③ 实验过程中加入液体的量至_____。
(2)利用高锰酸钾以及图中部分仪器还需补充仪器_____(填仪器名称)和棉花才可以 制取并收集氧气,其反应的化学方程式为_____; 根据所选的仪器可知其收集方法为_____,该收集方法判断氧气是否集满的 依据是_____。
(3)若用装置 I 收集氧气,水应从_____端导管排出(填“a”或“b”)。
(4)组装装置时,应遵循_____(填“从上往下”或“从下往上”)的顺序操作。
19、碳和碳的氧化物与我们的生活密切相关,请依据图回答问题:
(1)图1是碳原子结构示意图,其原子核内质子数为_____,该元素在元素周期表中位于第_____周期。
(2)碳元素组成的不同碳单质有广泛的用途。图2中用到的碳单质是_____,图3中用到的碳单质是_____,图4中用到的碳单质是_____;不同碳单质物理性质存在明显差异的原因是_____。
(3)CO和CO2是碳的两种氧化物。
CO可作燃料,其在空气中燃烧的化学方程式是_____ 。
CO2可制作饮料,其和水反应的化学方程式是_____ 。
20、根据下列装置图,回答问题。
图甲
(1)用高锰酸钾制取氧气,选用的发生装置是________(填序号),为防止高锰酸钾粉末进入导管,该装置需做的一点改进是______________________,若用D装置收集氧气,当观察到__________________时,便可开始收集。
(2)实验室制取二氧化碳应选用的一组装置是________(填序号),反应的化学方程式是_______________________________________________________。
图乙是某同学利用报废试管设计的制取二氧化碳的发生装置,该设计除了废物利用的优点外,请另写一个优点:_____________________________________。
图乙
(3)用收集的氧气完成图E铁丝燃烧的实验,集气瓶中预先放少量水的原因是________________________;如图F向装满CO2的软塑料瓶注入约体积的水,立即旋紧瓶盖,振荡,观察到的现象是________________________。
21、二氧化锰粉末与铝粉在较高温度下发生如下反应:3MnO2+4Al3Mn+2Al2O3,并放出大量的热.在工业上可用此法冶炼难熔金属锰.从得氧、失氧的角度看,二氧化锰在此反应中 (得到或失去)氧而变成单质锰,发生了 反应.该反应中那种物质具有还原性? .
22、实验室制取CO2的药品是_____________ (或_____________)和_________,化学方程式为_____________________ 。
23、实验室久盛石灰水的试剂瓶内壁常附有一层白色污渍,其成分是 ,化学式为 ,写出其形成的化学方程式: 。此污渍 (填“能”或“不能”)用水洗掉,清除此污渍的方法是 ,写出此反应的化学方程式 。
24、下图是某同学设计的实验室制取二氧化碳并验证其性质的实验装置图。
请回答下列问题。
(1)将A、E装置连接时,应将A装置的导管a与E装置的导管________(填“b”或“c”)相连接。检验E装置中二氧化碳已收集满的方法是________________________________。
(2)将A、B装置连接,观察到的现象是____________________________________________,可验证二氧化碳的性质是___________________________________。
(3)将A、C装置连接,可验证二氧化碳能与氢氧化钙反应,该反应的化学方程式为________________________________________________。
(4)用E装置收集满一瓶二氧化碳,取下双孔橡胶塞,将瓶中的气体沿D装置烧杯左侧内壁缓慢倒入,观察到的现象是________________________________________,这些现象说明二氧化碳具有的物理性质是______________________,化学性质是______________,________________。
三、实验类综合题题。
25、学习完二氧化碳制取的研究后,小东在妈妈的帮助下,用家中的用品设计了如下二氧化碳制取与体积测量的实验装置。请回答相关问题:
(1)其中吸管可代替实验室内的________(填仪器名称)。
(2)小东设计的甲装置的优点是______________________________,它与虚线框内的______(填序号)装置具有相同的效果。
(3)小药瓶中植物油上方的空气对实验结果______(填“有”或“无”)影响。请将乙装置中的吸管补画完整。
(4)小东通过丙装置中收集到的液体体积和上网查到的二氧化碳的密度计算出反应生成了0.66 g二氧化碳,请你计算所用蛋壳中碳酸钙的质量。
(相对原子质量:C-12 O-16 Ca-40)
四、计算类题。
26、化学实验小组同学取40g碳和氧化铜的粉末在高温条件下加热一段时间后,称得剩余固体混合物的质量为31.2g,请回答下列问题:
(1)该反应的化学方程式为 。
(2)列出求解参加反应的氧化铜的质量(x)的比例式 。
(3)反应后生成铜的质量为 。
(4)若碳完全反应了,则原混合物中氧化铜的质量分数为 。
2022—203学年化学人教九上第6单元 碳和碳的氧化物 分层优习题含答案
**人教九上第6单元 碳和碳的氧化物**
一、选择题。
1、定向爆破伴有反应:2Al+Fe2O3Al2O3+2Fe,此反应中还原剂是( )
A.Al B.Fe C.Fe2O3 D.Al2O3
【答案】A
2、下列药品组合最适合用来实验室制取二氧化碳的是( )
A.浓盐酸、石灰石 B.稀硫酸、大理石
C.稀盐酸、碳酸钠粉末 D.稀盐酸、石灰石
【答案】D
3、小明用软塑料瓶自制了一套气体发生装置(如图),下列关于该装置的说法错误的是( )
A.通过捏放瓶身可随时控制反应的发生和停止
B.利用该装置可制取二氧化碳
C.利用该装置制取氧气,液体药品为过氧化氢溶液
D.利用该装置制取氧气,无纺布包内二氧化锰越多,生成氧气就越多
【答案】D
4、实验室制取二氧化碳常用的方法是( )
A.木炭在氧气中燃烧 B.碳酸钠和稀盐酸反应
C.大理石和稀硫酸反应 D.石灰石和稀盐酸反应
【答案】D
5、可用同一化学原理解释的现象是( )
①久置的石灰水,液面上出现一层硬壳状薄膜
②向澄清石灰水中通入人体呼出的气体,澄清石灰水变浑浊
③为了使石灰浆粉刷的墙壁快点晾干,在室内生起一盆炭火,开始时墙壁反而潮湿
④人们用澄清石灰水保鲜鸡蛋
A.①②③④ B.①②④ C.①③④ D.②③④
【答案】A
6、汽车尾气中的CO在四氧化三钴(Co3O4)纳米棒的催化作用下,低温即与O2反应生成CO2.下列关于该反应的说法中,错误的是( )
A.反应类型为化合反应 B.可降低汽车尾气对大气的污染
C.反应前后Co3O4化学组成改变 D.反应前后碳元素的化合价改变
【答案】C
7、空气与按5:1的体积比混合后与足量的赤热焦炭反应,最后得到混合气体的主要成分是( )
A.和B.和COC.和COD.和
【答案】B
8、检验集气瓶内的二氧化碳是否集满的正确方法是( )
A.注入澄清石灰水 B.将燃着的木条放在集气瓶口
C.注入紫色石蕊试液 D.将燃着的木条伸入集气瓶内
【答案】B
9、镁带能在CO2气体中燃烧:2Mg+CO22MgO+C,该反应中的还原剂是( )
A.Mg B.CO2 C.MgO D.C
【答案】A
10、能证明某气体是CO2的操作及现象是( )
选项 实验操作 实验现象
A 将燃着的木条伸入集气瓶 木条熄灭
B 将带火星的木条伸入集气瓶 木条复燃
C 将气体通入澄清石灰水中 石灰水变浑浊
D 将气体通入紫色石蕊溶液中 溶液变红
A.A B.B C.C D.D
【答案】C
11、鉴别氧气、氢气和二氧化碳3瓶气体时,最简便的方法( )
A.用燃着的木条伸入集气瓶中
B.测定3种气体在标准情况下的密度
C.将3种气体分别通过澄清的石灰水
D.比较3种气体的溶解度
【答案】A
12、列有关碳单质的说法错误的是( )
A.金刚石、石墨充分燃烧的产物都是二氧化碳
B.金刚石和石墨的物理性质不同的原因是碳原子的排列方式不同
C.书写档案时规定使用碳素墨水,是因为常温下碳的化学性质不活泼
D.金刚石和石墨都是硬度最大的物质
【答案】D
13、在氧化还原反应中,得到氧(即有元素化合价升高)的物质是还原剂;失去氧(即有元素化合价降低)的物质是氧化剂.在反应:H2+CuO Cu+H2O中,属于还原剂的是( )
A.H2 B.CuO C.Cu D.H2O
【答案】A
14、NO是一种无色气体,实验室制备NO必须用排水法收集。由此可以得出的结论是( )
A.NO难溶于水 B.NO会与氧气反应
C.NO有毒 D.NO密度与空气接近
【答案】A
15、在任何条件下也不与反应的物质( )
A. B.C C. D.
【答案】A
16、实验室制取干燥的CO2气体,不会用到的装置是( )
【答案】A
二、填空题。
17、自然界中存在一种非常漂亮的孔雀石,其主要成分是碱式碳酸铜,俗称铜绿,化学式为[Cu2(OH)2CO3],受热可分解生成氧化铜、水和二氧化碳。
(1)孔雀石多在原始森林中,人类很早就发现,孔雀石在熊熊燃烧的树木中灼烧后,余烬里有一种红色光亮的金属显露出来,请用两个主要的反应方程式说明这种变化_____;_____。
(2)铜绿分解生成44g二氧化碳的同时,生成CuO的质量_____。
【答案】
160g
18、在实验室中利用下列仪器进行制取气体的实验,请回答下列问题:
(1)利用图中仪器可以制取二氧化碳:
① 你选择的仪器是_____(填字母序号);
② 你选择的药品是_____(填名称);
③ 实验过程中加入液体的量至_____。
(2)利用高锰酸钾以及图中部分仪器还需补充仪器_____(填仪器名称)和棉花才可以 制取并收集氧气,其反应的化学方程式为_____; 根据所选的仪器可知其收集方法为_____,该收集方法判断氧气是否集满的 依据是_____。
(3)若用装置 I 收集氧气,水应从_____端导管排出(填“a”或“b”)。
(4)组装装置时,应遵循_____(填“从上往下”或“从下往上”)的顺序操作。
【答案】(1)ABGH 大理石和稀盐酸 形成液封
(2)试管 2KMnO4K2MnO4+MnO2+O2↑
排水法 有大气泡从起集气瓶口冒出 (3)a (4)从下往上
19、碳和碳的氧化物与我们的生活密切相关,请依据图回答问题:
(1)图1是碳原子结构示意图,其原子核内质子数为_____,该元素在元素周期表中位于第_____周期。
(2)碳元素组成的不同碳单质有广泛的用途。图2中用到的碳单质是_____,图3中用到的碳单质是_____,图4中用到的碳单质是_____;不同碳单质物理性质存在明显差异的原因是_____。
(3)CO和CO2是碳的两种氧化物。
CO可作燃料,其在空气中燃烧的化学方程式是_____ 。
CO2可制作饮料,其和水反应的化学方程式是_____ 。
【答案】(1). 6 (2). 二 (3). 金刚石
(4). 石墨 (5). 活性炭 (6). 碳原子排列方式不同
(7). 2CO+O22CO2 (8). CO2+H2O=H2CO3
20、根据下列装置图,回答问题。
图甲
(1)用高锰酸钾制取氧气,选用的发生装置是________(填序号),为防止高锰酸钾粉末进入导管,该装置需做的一点改进是______________________,若用D装置收集氧气,当观察到__________________时,便可开始收集。
(2)实验室制取二氧化碳应选用的一组装置是________(填序号),反应的化学方程式是_______________________________________________________。
图乙是某同学利用报废试管设计的制取二氧化碳的发生装置,该设计除了废物利用的优点外,请另写一个优点:_____________________________________。
图乙
(3)用收集的氧气完成图E铁丝燃烧的实验,集气瓶中预先放少量水的原因是________________________;如图F向装满CO2的软塑料瓶注入约体积的水,立即旋紧瓶盖,振荡,观察到的现象是________________________。
【答案】(1)A 在试管口放一团棉花(或其他合理答案均可)
气泡连续均匀冒出
(2)BC CaCO3+2HCl===CaCl2+H2O+CO2↑
节约药品(或可随时控制反应的发生或停止)(其他合理答案均可)
(3)防止集气瓶炸裂(或防止高温熔融物溅落,使瓶底炸裂) 软塑料瓶变瘪
21、二氧化锰粉末与铝粉在较高温度下发生如下反应:3MnO2+4Al3Mn+2Al2O3,并放出大量的热.在工业上可用此法冶炼难熔金属锰.从得氧、失氧的角度看,二氧化锰在此反应中 (得到或失去)氧而变成单质锰,发生了 反应.该反应中那种物质具有还原性? .
【答案】失去;还原;Al.
22、实验室制取CO2的药品是_____________ (或_____________)和_________,化学方程式为_____________________ 。
【答案】石灰石 大理石 稀盐酸 CaCO3+2HCl===CaCl2+H2O+CO2↑
23、实验室久盛石灰水的试剂瓶内壁常附有一层白色污渍,其成分是 ,化学式为 ,写出其形成的化学方程式: 。此污渍 (填“能”或“不能”)用水洗掉,清除此污渍的方法是 ,写出此反应的化学方程式 。
【答案】碳酸钙 CaCO3 CO2+Ca(OH)2CaCO3↓+H2O 不能 加稀盐酸
CaCO3+2HClCaCl2+H2O+CO2↑
24、下图是某同学设计的实验室制取二氧化碳并验证其性质的实验装置图。
请回答下列问题。
(1)将A、E装置连接时,应将A装置的导管a与E装置的导管________(填“b”或“c”)相连接。检验E装置中二氧化碳已收集满的方法是________________________________。
(2)将A、B装置连接,观察到的现象是____________________________________________,可验证二氧化碳的性质是___________________________________。
(3)将A、C装置连接,可验证二氧化碳能与氢氧化钙反应,该反应的化学方程式为________________________________________________。
(4)用E装置收集满一瓶二氧化碳,取下双孔橡胶塞,将瓶中的气体沿D装置烧杯左侧内壁缓慢倒入,观察到的现象是________________________________________,这些现象说明二氧化碳具有的物理性质是______________________,化学性质是______________,________________。
【答案】(1)b 将燃着的木条靠近E瓶c导管口,观察木条是否熄灭 (2)B中溶液由紫色变为红色 二氧化碳能与水反应
(3)Ca(OH)2+CO2===CaCO3↓+H2O
(4)燃着的蜡烛由下至上依次熄灭 密度比空气大 不能燃烧 不支持燃烧
三、实验类综合题题。
25、学习完二氧化碳制取的研究后,小东在妈妈的帮助下,用家中的用品设计了如下二氧化碳制取与体积测量的实验装置。请回答相关问题:
(1)其中吸管可代替实验室内的________(填仪器名称)。
(2)小东设计的甲装置的优点是______________________________,它与虚线框内的______(填序号)装置具有相同的效果。
(3)小药瓶中植物油上方的空气对实验结果______(填“有”或“无”)影响。请将乙装置中的吸管补画完整。
(4)小东通过丙装置中收集到的液体体积和上网查到的二氧化碳的密度计算出反应生成了0.66 g二氧化碳,请你计算所用蛋壳中碳酸钙的质量。
(相对原子质量:C-12 O-16 Ca-40)
【答案】(1)导管 (2)可以随时控制反应的发生和停止 A
(3)无
(4)解:设所用蛋壳中碳酸钙的质量为x。
CaCO3+2HCl=== CaCl2+H2O+CO2↑
100 44
x 0.66 g
=,x=1.5 g
答:所用蛋壳中碳酸钙的质量为1.5 g。
四、计算类题。
26、化学实验小组同学取40g碳和氧化铜的粉末在高温条件下加热一段时间后,称得剩余固体混合物的质量为31.2g,请回答下列问题:
(1)该反应的化学方程式为 。
(2)列出求解参加反应的氧化铜的质量(x)的比例式 。
(3)反应后生成铜的质量为 。
(4)若碳完全反应了,则原混合物中氧化铜的质量分数为 。
【答案】(1)C+2CuO2Cu+CO2↑;
(2)根据质量守恒定律可知,反应生成二氧化碳质量:40g-31.2g=8.8g,
设参加反应的氧化铜的质量为x,
;
(3)设反应后生成铜的质量为y,
y=25.6g;
(4)设碳质量为z,
z=2.4g,
若碳完全反应了,则原混合物中氧化铜的质量分数为:×100%=94%。
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
