第一章 第一节 物质的分类及转化 第二课时 物质的转化(共69张ppt)
文档属性
| 名称 | 第一章 第一节 物质的分类及转化 第二课时 物质的转化(共69张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 3.7MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-10-01 00:00:00 | ||
图片预览









文档简介
(共69张PPT)
第二课时 物质的转化
第一章 物质及其变化
【课程标准要求】
1.能根据物质的微观结构预测物质在特定条件下可能具有的性质和可能发生的变化,并能解释其原因。
2.同类物质具有相似的性质,一定条件下各类物质可以相互转化。
新知自主预习
课堂互动探究
目
录
CONTENTS
///////
///////
课后巩固训练
///////
课堂达标训练
///////
一、酸、碱、盐的性质
1.酸的主要化学性质
以稀硫酸为例,列举反应实例归纳酸的主要化学性质(写出反应的化学方程式)。
(1)能使紫色石蕊溶液______色。
(2)与活泼金属(如Fe)反应:
__________________________________________。
(3)与碱性氧化物(如MgO)反应:
____________________________________________。
变红
Fe+H2SO4===FeSO4+H2↑
MgO+H2SO4===MgSO4+H2O
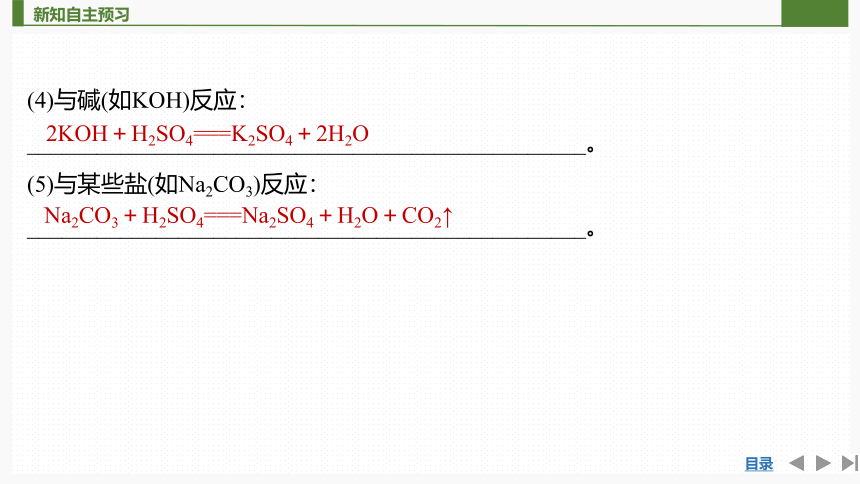
(4)与碱(如KOH)反应:
________________________________________________。
(5)与某些盐(如Na2CO3)反应:
________________________________________________。
2KOH+H2SO4===K2SO4+2H2O
Na2CO3+H2SO4===Na2SO4+H2O+CO2↑
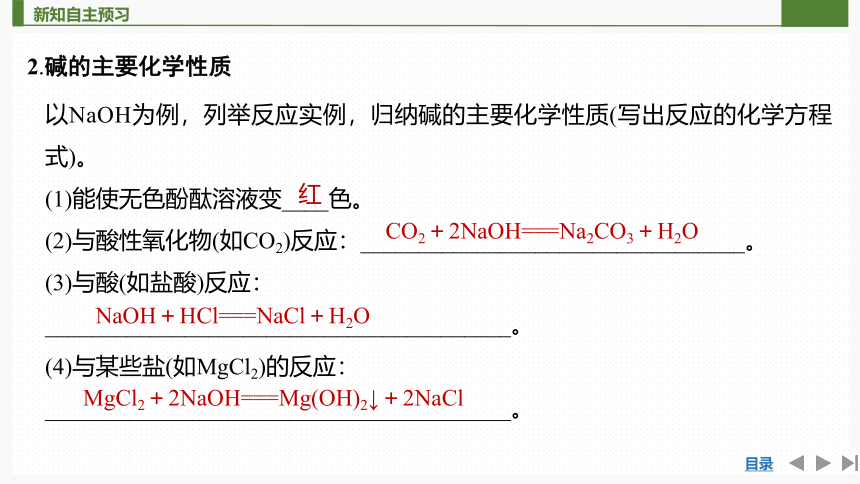
2.碱的主要化学性质
以NaOH为例,列举反应实例,归纳碱的主要化学性质(写出反应的化学方程式)。
(1)能使无色酚酞溶液变____色。
(2)与酸性氧化物(如CO2)反应:_________________________________。
(3)与酸(如盐酸)反应:
________________________________________。
(4)与某些盐(如MgCl2)的反应:
________________________________________。
红
CO2+2NaOH===Na2CO3+H2O
NaOH+HCl===NaCl+H2O
MgCl2+2NaOH===Mg(OH)2↓+2NaCl
3.盐的主要化学性质
以Na2CO3为例,列举反应实例,归纳盐的主要化学性质(写出反应的化学方程式)。
(1)与酸(如HCl)反应:
________________________________________________。
(2)与碱[Ca(OH)2]反应:
________________________________________________。
(3)与某些盐(如BaCl2)反应:
________________________________________________。
Na2CO3+2HCl===2NaCl+H2O+CO2↑
Ca(OH)2+Na2CO3===CaCO3↓+2NaOH
BaCl2+Na2CO3===BaCO3↓+2NaCl
【微自测】
1.判断正误,正确的打“√”,错误的打“×”。
(1)HCl、H2SO4溶液中都含有H+,因此它们具有相似的化学性质( )
(2)NaOH、Ca(OH)2溶液中都含有OH-,因此它们具有相似的化学性质( )
(3)Na2CO3、K2CO3都是碳酸盐,具有相似的化学性质( )
(4)酸与金属之间能发生置换反应,但金属与盐之间不能发生置换反应( )
答案 (1)√ (2)√ (3)√ (4)×
二、物质的转化
1.物质转化的基本依据
在化学变化过程中,______是不会改变的,这是考虑如何实现物质之间转化时的基本依据。
元素
2.由单质到盐的转化关系
(1)金属单质到盐的转化
写出上述物质转化反应的化学方程式,并指明反应类型:
①____________________________;__________。
②____________________________;__________。
③___________________________________;____________。
2Ca+O2===2CaO
化合反应
CaO+H2O===Ca(OH)2
化合反应
Ca(OH)2+H2SO4===CaSO4+2H2O
复分解反应
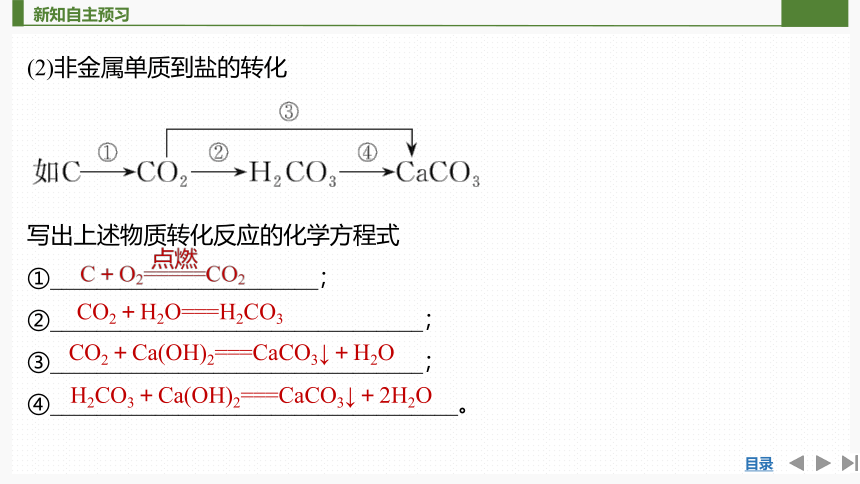
(2)非金属单质到盐的转化
写出上述物质转化反应的化学方程式
①_______________________;
②________________________________;
③________________________________;
④___________________________________。
CO2+H2O===H2CO3
CO2+Ca(OH)2===CaCO3↓+H2O
H2CO3+Ca(OH)2===CaCO3↓+2H2O
【微自测】
2.判断正误,正确的打“√”,错误的打“×”。
(1)工业上可用反应:CaO+H2O===Ca(OH)2、Na2CO3+Ca(OH)2===CaCO3↓+2NaOH制取烧碱( )
(2)工业上制取NaOH不采用Na2O和H2O反应的原因是:Na2O作为原料,来源少、成本高( )
(3)非金属单质到盐的转化过程中必须是:非金属单质→氧化物→酸→盐( )
答案 (1)√ (2)√ (3)×
二、物质的转化和化学反应类型
一、与酸、碱、盐性质相关的反应条件
一、与酸、碱、盐性质相关的反应条件
四类反应的条件
金属与酸反 应的条件 ①在金属活动性顺序表中,金属要排在氢前
②浓硫酸、硝酸与金属反应不能生成氢气
③铁发生置换反应时,生成+2价的铁的化合物
金属与盐反 应的条件 ①在金属活动性顺序表中,单质的金属要比盐中金属活泼
②反应物中的盐要可溶
③K、Ca、Na、Ba等金属与盐反应不能生成另一种盐和另一种金属
盐与盐反应的条件 反应物都要可溶,生成物要有沉淀
盐与碱反应的条件 反应物都要可溶,生成物要有沉淀或气体
1.下列物质在常温下能反应的是( )
A.Cu与稀H2SO4
B.Na2CO3与KCl溶液
C.Na2CO3与BaCl2溶液
D.Fe与ZnSO4溶液
C
2.下列各组物质相互混合后,不会发生反应的是( )
A.Na2SO4溶液和MgCl2溶液
B.Na2CO3溶液和稀硫酸
C.NaOH溶液和Fe2(SO4)3溶液
D.Ca(OH)2溶液和盐酸
解析 物质在溶液中是否能够发生化学反应,可根据是否生成沉淀、气体或H2O来进行判断。Na2SO4和MgCl2溶液混合后既没有沉淀、也没有气体和H2O生成,故不反应。
A
3.在一定条件下,能跟某些酸、碱、盐发生反应的物质是( )
A.Na2CO3 B.CuO
C.CaCO3 D.CO2
解析 Na2CO3在一定条件下能跟某些酸、碱、盐反应,如Na2CO3+2HCl===2NaCl+CO2↑+H2O,Na2CO3+Ca(OH)2===CaCO3↓+2NaOH,Na2CO3+CaCl2===CaCO3↓+2NaCl。CuO和CaCO3均不与碱、盐反应。CO2不与酸反应。
A
二、物质的转化和化学反应类型
1.从物质分类的角度分析,“铜绿”属于哪类物质?写出“铜绿”与盐酸反应的化学方程式。
提示 “铜绿”属于碱式盐;反应的化学方程式为Cu2(OH)2CO3+4HCl===2CuCl2+CO2↑+3H2O。
2.上述转化关系中,若②中加入的是稀盐酸,试指出转化关系中A、B分别是何种物质?写出④、⑤的化学方程式并指明反应类型。
3.设计实现CuO到Cu(OH)2的转化,并写出反应的化学方程式。
1.单质、氧化物、酸、碱、盐之间的相互转化
2.无机基本反应类型
(1)化合反应:A+B+……―→C;
(2)分解反应:A―→B+C+……;
(3)置换反应:A+BC―→AC+B;
(4)复分解反应:AB+CD―→AD+CB。
(1)常见的置换反应有a.金属与酸、盐的置换反应;b.H2还原某些金属氧化物(如CuO);c.碳与H2O(g)反应制取水煤气等。
(2)复分解反应一般是酸、碱、盐之间的反应。
4.以下表示的是碳及其化合物的转化关系,其中涉及的基本反应类型依次是( )
D
5.如图中,“——”表示相连的物质间在一定条件下可以反应,“―→”表示丁在一定条件下通过置换反应可以转化为乙。下面四组选项中,符合图示要求的是( )
C
选项 甲 乙 丙 丁
A H2SO4 Na2SO4 NaOH NaCl
B BaCl2 K2CO3 HCl KOH
C O2 CO CuO C
D Fe CuCl2 Zn HCl
1.KOH是我国古代纺织业常用作漂洗的洗涤剂。古代制取KOH的流程如下:
上述流程中没有涉及的化学反应类型是( )
A.化合反应 B.分解反应
C.置换反应 D.复分解反应
C
2.一同学设计了两种由CuO→Cu的实验方案:
B
3.推理是学习化学的一种重要方法。以下推理正确的是( )
A.酸碱发生中和反应生成盐和水,所以生成盐和水的反应一定是中和反应
B.碱中都含有氢氧根,所以碱中一定含有氢元素
C.酸能使紫色石蕊溶液变红,CO2通入紫色石蕊溶液后溶液变红,所以CO2是酸
D.碱能使无色酚酞溶液变红,所以能使无色酚酞溶液变红的都是碱
B
解析 A.CuO与HCl反应,生成CuCl2和H2O,虽然产物为盐和水,但反应不属于中和反应,A不正确;B.碱中含有氢氧根,氢氧根由氢元素和氧元素组成,所以碱中一定含有氢元素,B正确;C.CO2通入紫色石蕊溶液后溶液变红,是由CO2与水反应生成的碳酸引起的,CO2不是酸,C不正确;D.能使无色酚酞溶液变红的物质呈碱性,可能是碱,也可能是盐(如碳酸钠),D不正确。
4.下列各组物质之间可以按下图所示关系直接转化的是( )
解析 选项A中, Fe2O3→FeSO4不能一步实现;选项B中,H2CO3→CO不能一步实现;选项C中,NaCl→Na2CO3不能一步实现。
D
5.如图所示,A、B、C、D、E各代表水、锌、二氧化碳、硫酸铜溶液、氢氧化钡溶液中的一种物质。常温下,相连环物质间能发生反应,不相连环物质间不能发生反应,且A的相对分子(或原子)质量大于D。
请填空:
(1)写出下列物质的化学式:A________,D________,
E________。
(2)写出B与C反应的化学方程式:______________________________。
(3)相连环物质间发生的反应中,置换反应共有________个。
答案 (1)Zn CO2 H2O (2)CuSO4+Ba(OH)2===Cu(OH)2↓+BaSO4↓ (3)1
1.北京冬奥会或第24届冬季奥林匹克运动会于2022年2月
4日至2022年2月20日在中华人民共和国北京市和河北
省张家口市联合举行。某同学在奥运五连环中填入了5
种物质,相连环物质间能发生反应,不相连环物质间不能发生反应。你认为“五连环”中物质间发生的反应,没有涉及的基本反应类型( )
A.分解反应 B.复分解反应
C.化合反应 D.置换反应
A
解析 Fe与稀盐酸发生置换反应;稀盐酸与NaOH溶液发生复分解反应;NaOH溶液与CO2发生反应时,可认为CO2先与水化合成碳酸,再与NaOH发生复分解反应;CO2与C发生化合反应生成CO,所以没有涉及的基本反应类型为分解反应,故选A。
2.魔术“水变红”(如图),杯子中先涂有酚酞溶液,然后加入“水”,则加入的“水”是( )
A.H2O B.HNO3溶液
C.NaOH溶液 D.NaCl溶液
解析 只有碱(如NaOH)溶液能使酚酞变红。
C
3.既能跟稀硫酸反应又能跟熟石灰反应的物质是( )
A.硫酸铜 B.碳酸钠
C.氢氧化钠 D.碳酸钙
解析 A项,硫酸铜不与稀硫酸反应,能和熟石灰反应,错误;B项,碳酸钠既能和稀硫酸反应生成硫酸钠、水和二氧化碳,又能和熟石灰反应生成碳酸钙沉淀和氢氧化钠,正确;C项,氢氧化钠只能和稀硫酸反应,不能和熟石灰反应,错误;D项,碳酸钙只能和稀硫酸反应,不能和熟石灰反应,错误。
B
4.下列各选项中,不能通过一步反应实现如图所示转化关系的是( )
A.X为铜、Y为氧化铜、Z为硫酸铜
B.X为二氧化碳、Y为碳、Z为一氧化碳
C.X为碳酸钙、Y为氧化钙、Z为氢氧化钙
D.X为氢氧化钠、Y为氯化钠、Z为碳酸钠
D
解析 铜与氧气反应生成氧化铜,氧化铜与硫酸反应生成硫酸铜,硫酸铜溶液与铁反应生成铜,故A不符合题意;二氧化碳与Mg反应生成碳单质和氧化镁,碳在氧气中不完全燃烧生成一氧化碳;一氧化碳在氧气中燃烧生成二氧化碳,故B不符合题意;碳酸钙高温分解生成氧化钙,氧化钙与水反应生成氢氧化钙,氢氧化钙与二氧化碳反应生成碳酸钙,故C不符合题意;氢氧化钠与盐酸反应生成氯化钠,氯化钠不能通过一步反应转化生成碳酸钠,故D符合题意。
5.下表所列各组物质中,物质之间按箭头方向不能通过一步反应实现如图所示转化的是( )
A.甲为CuO、乙为CO2、丙为H2O
B.甲为C、乙为CO、丙为CO2
C.甲为CaCO3、乙为CaO、丙为Ca(OH)2
D.甲为H2SO4、乙为H2O、丙为H2
解析 C中碳酸钙难溶于水,不与碱溶液发生反应,不能通过一步反应生成氢氧化钙。
C
6.某同学为了区别氢氧化钠溶液和澄清石灰水,设计了如图所示的四组实验方案,其中能达到目的的是( )
解析 澄清石灰水中通入二氧化碳产生沉淀,而氢氧化钠溶液中通入二氧化碳无沉淀产生。
D
7.化学变化多姿多彩,美丽如花。如图中甲、乙、丙、X分别是Fe2O3、C、CO、盐酸中的某一种,甲、乙、丙均能与X发生化学反应,则X是( )
A.C B.Fe2O3 C.CO D.盐酸
B
8.(2021·广州外国语学校高一期末)X、Y、Z、W各代表一种物质,若X+Y===Z+W,则X和Y之间不可能是( )
A.碱和盐的反应
B.碱性氧化物和水的反应
C.盐与盐的反应
D.酸性氧化物和碱的反应
B
解析 碱与盐可发生反应生成另一种碱和另一种盐,如Ca(OH)2+Na2CO3===CaCO3↓+2NaOH,A可能;碱性氧化物和水反应生成碱,产物只有一种,如CaO+H2O===Ca(OH)2,B不可能;盐与盐发生复分解反应,可以生成另外两种盐,如NaCl+AgNO3===AgCl↓+NaNO3,C可能;酸性氧化物与碱反应生成盐和水,如CO2+Ca(OH)2===CaCO3↓+H2O,D可能。
9.构建知识网络是一种重要的学习方法。如图是关于盐酸化学性质的知识网络图:“—”表示相连的两种物质能发生反应,“→”表示一种物质能转化为另一种物质。若A、B、C分别属于不同类别的化合物,则A、B、C可能是( )
A.CuO、Ba(OH)2、CuSO4
B.NaOH、HNO3、K2CO3
C.KOH、FeCl3、Na2CO3
D.NaOH、Ba(NO3)2、H2SO4
B
解析 A.盐酸不与硫酸铜反应,盐酸不能转化为氢氧化钡,氢氧化钡不与氧化铜反应,故A不符合题意;B.盐酸和氢氧化钠、碳酸钾都能反应,和硝酸银反应生成硝酸,硝酸和氢氧化钠、碳酸钾都能反应,故B符合题意;C.氯化铁和碳酸钠均为盐,属于相同类别的化合物,故C不符合题意;D.盐酸不能转化为硝酸钡,盐酸不与硫酸反应,氢氧化钠与硝酸钡不反应,故D不符合题意。
10.A、B、C、D、E中都含有同一种元素,它们之间的相互转化关系如图所示,其中所含的相同元素是( )
A.铜 B.碳 C.铁 D.钙
解析 A为CaO,B为Ca(OH)2,C为Ca(NO3)2,D为CaCl2,E为CaCO3。
D
11.如图以稀盐酸为例的反应关系体现了酸的化学性质,其中X与图中所给物质的类别不同。结合此图回答下列问题。
(1)稀盐酸中阳离子的符号是________。
(2)反应①中石蕊溶液变为________色。
(3)反应⑤的化学方程式为_____________________。
(4)图中只生成盐和水的反应有________(填序号)。
(5)若X溶液既能跟稀盐酸反应,又能跟Ca(OH)2反应,则X可能是(BaCl2、CuSO4、Na2CO3)中的________。
答案 (1)H+ (2)红 (3)Al2O3+6HCl===2AlCl3+3H2O (4)③⑤ (5)Na2CO3
解析 (1)稀盐酸中阳离子为H+;(2)稀盐酸显酸性,能使石蕊溶液变为红色;(3)反应⑤是氧化铝和盐酸反应生成氯化铝和水,反应的化学方程式为Al2O3+6HCl===2AlCl3+3H2O;(4)③氢氧化钙与稀盐酸反应生成氯化钙和水,⑤氧化铝与稀盐酸反应生成氯化铝和水,生成物均为盐和水,符合题意;(5)BaCl2不能与稀盐酸反应,且与Ca(OH)2不能发生反应,不符合题意;CuSO4不能与稀盐酸反应,不符合题意;Na2CO3能与稀盐酸反应生成氯化钠、水、二氧化碳,能与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,符合题意。
12.“碳捕捉技术”,常用于去除或分离气流中的二氧化碳。利用NaOH溶液“捕捉”CO2的基本过程如图(部分条件及物质已略去):
(1)反应分离室中,发生反应的化学方程式分别为CaO+H2O===Ca(OH)2和___________________________________________________________
__________________________________________________________。
(2)高温反应炉中,涉及反应的基本反应类型为____________。
(3)整个过程中,可以循环利用的物质化学式为______________。
NaHCO3+Ca(OH)2===NaOH+CaCO3↓+H2O
[或Na2CO3+Ca(OH)2===2NaOH+CaCO3↓]
分解反应
NaOH、CaO
解析 (1)由题干及图示知,捕捉室中氢氧化钠溶液吸收二氧化碳生成碳酸钠(或碳酸氢钠),则反应分离室中还存在的反应是Na2CO3+Ca(OH)2===2NaOH+CaCO3↓[或NaHCO3+Ca(OH)2===NaOH+CaCO3↓+H2O]。(2)根据图示,高温反应炉中发生的反应是碳酸钙分解生成氧化钙和二氧化碳,基本反应类型为分解反应。(3)参加反应且又生成的物质为可循环利用的物质,整个过程中,可以循环利用的物质为NaOH、CaO。
13.如图是小红学习《常见的碱》课题后,总结出氢氧化钙的化学性质。下列说法中不正确的是( )
A.①中的酚酞溶液变红色
B.②中与盐酸反应的化学方程式为Ca(OH)2+2HCl===CaCl2+2H2O
C.③中与硝酸钠溶液能发生反应
D.④可解释久置的澄清石灰水变质
C
解析 ①中Ca(OH)2能使酚酞溶液变红,A正确;②中Ca(OH)2与HCl反应的化学方程式为Ca(OH)2+2HCl===CaCl2+2H2O,B正确;③中NaNO3溶液与Ca(OH)2不反应,C错误;④中久置的澄清石灰水变质的原因是Ca(OH)2+CO2===CaCO3↓+H2O,D正确。
14.(2020·广东云浮高一期中)由单质到盐的转化关系可表示为:
C
解析 CuO不能与水反应生成Cu(OH)2,A错误;MgCl2不能与Na2SO4发生反应,B错误;碳在氧气中燃烧生成CO2,CO2与水反应生成H2CO3,H2CO3与氢氧化钙反应生成CaCO3沉淀,C正确;硫在氧气中燃烧生成SO2,SO2与水反应生成H2SO3,H2SO3与NaOH反应生成Na2SO3,D错误。
15.对牙膏的探究要用到许多化学知识。
(1)下表列出了两种牙膏中的摩擦剂,请在表中填写两种摩擦剂所属的物质类别:
X牙膏 Y牙膏
摩擦剂 碳酸钙 二氧化硅
摩擦剂的物质类别(指酸、碱、盐、氧化物)
(2)根据你的推测,牙膏摩擦剂在水中的溶解性是________(填“易溶”或“难溶”)。
盐
氧化物
难溶
CaO+H2O===Ca(OH)2
Ca(OH)2+Na2CO3===CaCO3↓+2NaOH
Thanks!
本讲内容结束
第二课时 物质的转化
第一章 物质及其变化
【课程标准要求】
1.能根据物质的微观结构预测物质在特定条件下可能具有的性质和可能发生的变化,并能解释其原因。
2.同类物质具有相似的性质,一定条件下各类物质可以相互转化。
新知自主预习
课堂互动探究
目
录
CONTENTS
///////
///////
课后巩固训练
///////
课堂达标训练
///////
一、酸、碱、盐的性质
1.酸的主要化学性质
以稀硫酸为例,列举反应实例归纳酸的主要化学性质(写出反应的化学方程式)。
(1)能使紫色石蕊溶液______色。
(2)与活泼金属(如Fe)反应:
__________________________________________。
(3)与碱性氧化物(如MgO)反应:
____________________________________________。
变红
Fe+H2SO4===FeSO4+H2↑
MgO+H2SO4===MgSO4+H2O
(4)与碱(如KOH)反应:
________________________________________________。
(5)与某些盐(如Na2CO3)反应:
________________________________________________。
2KOH+H2SO4===K2SO4+2H2O
Na2CO3+H2SO4===Na2SO4+H2O+CO2↑
2.碱的主要化学性质
以NaOH为例,列举反应实例,归纳碱的主要化学性质(写出反应的化学方程式)。
(1)能使无色酚酞溶液变____色。
(2)与酸性氧化物(如CO2)反应:_________________________________。
(3)与酸(如盐酸)反应:
________________________________________。
(4)与某些盐(如MgCl2)的反应:
________________________________________。
红
CO2+2NaOH===Na2CO3+H2O
NaOH+HCl===NaCl+H2O
MgCl2+2NaOH===Mg(OH)2↓+2NaCl
3.盐的主要化学性质
以Na2CO3为例,列举反应实例,归纳盐的主要化学性质(写出反应的化学方程式)。
(1)与酸(如HCl)反应:
________________________________________________。
(2)与碱[Ca(OH)2]反应:
________________________________________________。
(3)与某些盐(如BaCl2)反应:
________________________________________________。
Na2CO3+2HCl===2NaCl+H2O+CO2↑
Ca(OH)2+Na2CO3===CaCO3↓+2NaOH
BaCl2+Na2CO3===BaCO3↓+2NaCl
【微自测】
1.判断正误,正确的打“√”,错误的打“×”。
(1)HCl、H2SO4溶液中都含有H+,因此它们具有相似的化学性质( )
(2)NaOH、Ca(OH)2溶液中都含有OH-,因此它们具有相似的化学性质( )
(3)Na2CO3、K2CO3都是碳酸盐,具有相似的化学性质( )
(4)酸与金属之间能发生置换反应,但金属与盐之间不能发生置换反应( )
答案 (1)√ (2)√ (3)√ (4)×
二、物质的转化
1.物质转化的基本依据
在化学变化过程中,______是不会改变的,这是考虑如何实现物质之间转化时的基本依据。
元素
2.由单质到盐的转化关系
(1)金属单质到盐的转化
写出上述物质转化反应的化学方程式,并指明反应类型:
①____________________________;__________。
②____________________________;__________。
③___________________________________;____________。
2Ca+O2===2CaO
化合反应
CaO+H2O===Ca(OH)2
化合反应
Ca(OH)2+H2SO4===CaSO4+2H2O
复分解反应
(2)非金属单质到盐的转化
写出上述物质转化反应的化学方程式
①_______________________;
②________________________________;
③________________________________;
④___________________________________。
CO2+H2O===H2CO3
CO2+Ca(OH)2===CaCO3↓+H2O
H2CO3+Ca(OH)2===CaCO3↓+2H2O
【微自测】
2.判断正误,正确的打“√”,错误的打“×”。
(1)工业上可用反应:CaO+H2O===Ca(OH)2、Na2CO3+Ca(OH)2===CaCO3↓+2NaOH制取烧碱( )
(2)工业上制取NaOH不采用Na2O和H2O反应的原因是:Na2O作为原料,来源少、成本高( )
(3)非金属单质到盐的转化过程中必须是:非金属单质→氧化物→酸→盐( )
答案 (1)√ (2)√ (3)×
二、物质的转化和化学反应类型
一、与酸、碱、盐性质相关的反应条件
一、与酸、碱、盐性质相关的反应条件
四类反应的条件
金属与酸反 应的条件 ①在金属活动性顺序表中,金属要排在氢前
②浓硫酸、硝酸与金属反应不能生成氢气
③铁发生置换反应时,生成+2价的铁的化合物
金属与盐反 应的条件 ①在金属活动性顺序表中,单质的金属要比盐中金属活泼
②反应物中的盐要可溶
③K、Ca、Na、Ba等金属与盐反应不能生成另一种盐和另一种金属
盐与盐反应的条件 反应物都要可溶,生成物要有沉淀
盐与碱反应的条件 反应物都要可溶,生成物要有沉淀或气体
1.下列物质在常温下能反应的是( )
A.Cu与稀H2SO4
B.Na2CO3与KCl溶液
C.Na2CO3与BaCl2溶液
D.Fe与ZnSO4溶液
C
2.下列各组物质相互混合后,不会发生反应的是( )
A.Na2SO4溶液和MgCl2溶液
B.Na2CO3溶液和稀硫酸
C.NaOH溶液和Fe2(SO4)3溶液
D.Ca(OH)2溶液和盐酸
解析 物质在溶液中是否能够发生化学反应,可根据是否生成沉淀、气体或H2O来进行判断。Na2SO4和MgCl2溶液混合后既没有沉淀、也没有气体和H2O生成,故不反应。
A
3.在一定条件下,能跟某些酸、碱、盐发生反应的物质是( )
A.Na2CO3 B.CuO
C.CaCO3 D.CO2
解析 Na2CO3在一定条件下能跟某些酸、碱、盐反应,如Na2CO3+2HCl===2NaCl+CO2↑+H2O,Na2CO3+Ca(OH)2===CaCO3↓+2NaOH,Na2CO3+CaCl2===CaCO3↓+2NaCl。CuO和CaCO3均不与碱、盐反应。CO2不与酸反应。
A
二、物质的转化和化学反应类型
1.从物质分类的角度分析,“铜绿”属于哪类物质?写出“铜绿”与盐酸反应的化学方程式。
提示 “铜绿”属于碱式盐;反应的化学方程式为Cu2(OH)2CO3+4HCl===2CuCl2+CO2↑+3H2O。
2.上述转化关系中,若②中加入的是稀盐酸,试指出转化关系中A、B分别是何种物质?写出④、⑤的化学方程式并指明反应类型。
3.设计实现CuO到Cu(OH)2的转化,并写出反应的化学方程式。
1.单质、氧化物、酸、碱、盐之间的相互转化
2.无机基本反应类型
(1)化合反应:A+B+……―→C;
(2)分解反应:A―→B+C+……;
(3)置换反应:A+BC―→AC+B;
(4)复分解反应:AB+CD―→AD+CB。
(1)常见的置换反应有a.金属与酸、盐的置换反应;b.H2还原某些金属氧化物(如CuO);c.碳与H2O(g)反应制取水煤气等。
(2)复分解反应一般是酸、碱、盐之间的反应。
4.以下表示的是碳及其化合物的转化关系,其中涉及的基本反应类型依次是( )
D
5.如图中,“——”表示相连的物质间在一定条件下可以反应,“―→”表示丁在一定条件下通过置换反应可以转化为乙。下面四组选项中,符合图示要求的是( )
C
选项 甲 乙 丙 丁
A H2SO4 Na2SO4 NaOH NaCl
B BaCl2 K2CO3 HCl KOH
C O2 CO CuO C
D Fe CuCl2 Zn HCl
1.KOH是我国古代纺织业常用作漂洗的洗涤剂。古代制取KOH的流程如下:
上述流程中没有涉及的化学反应类型是( )
A.化合反应 B.分解反应
C.置换反应 D.复分解反应
C
2.一同学设计了两种由CuO→Cu的实验方案:
B
3.推理是学习化学的一种重要方法。以下推理正确的是( )
A.酸碱发生中和反应生成盐和水,所以生成盐和水的反应一定是中和反应
B.碱中都含有氢氧根,所以碱中一定含有氢元素
C.酸能使紫色石蕊溶液变红,CO2通入紫色石蕊溶液后溶液变红,所以CO2是酸
D.碱能使无色酚酞溶液变红,所以能使无色酚酞溶液变红的都是碱
B
解析 A.CuO与HCl反应,生成CuCl2和H2O,虽然产物为盐和水,但反应不属于中和反应,A不正确;B.碱中含有氢氧根,氢氧根由氢元素和氧元素组成,所以碱中一定含有氢元素,B正确;C.CO2通入紫色石蕊溶液后溶液变红,是由CO2与水反应生成的碳酸引起的,CO2不是酸,C不正确;D.能使无色酚酞溶液变红的物质呈碱性,可能是碱,也可能是盐(如碳酸钠),D不正确。
4.下列各组物质之间可以按下图所示关系直接转化的是( )
解析 选项A中, Fe2O3→FeSO4不能一步实现;选项B中,H2CO3→CO不能一步实现;选项C中,NaCl→Na2CO3不能一步实现。
D
5.如图所示,A、B、C、D、E各代表水、锌、二氧化碳、硫酸铜溶液、氢氧化钡溶液中的一种物质。常温下,相连环物质间能发生反应,不相连环物质间不能发生反应,且A的相对分子(或原子)质量大于D。
请填空:
(1)写出下列物质的化学式:A________,D________,
E________。
(2)写出B与C反应的化学方程式:______________________________。
(3)相连环物质间发生的反应中,置换反应共有________个。
答案 (1)Zn CO2 H2O (2)CuSO4+Ba(OH)2===Cu(OH)2↓+BaSO4↓ (3)1
1.北京冬奥会或第24届冬季奥林匹克运动会于2022年2月
4日至2022年2月20日在中华人民共和国北京市和河北
省张家口市联合举行。某同学在奥运五连环中填入了5
种物质,相连环物质间能发生反应,不相连环物质间不能发生反应。你认为“五连环”中物质间发生的反应,没有涉及的基本反应类型( )
A.分解反应 B.复分解反应
C.化合反应 D.置换反应
A
解析 Fe与稀盐酸发生置换反应;稀盐酸与NaOH溶液发生复分解反应;NaOH溶液与CO2发生反应时,可认为CO2先与水化合成碳酸,再与NaOH发生复分解反应;CO2与C发生化合反应生成CO,所以没有涉及的基本反应类型为分解反应,故选A。
2.魔术“水变红”(如图),杯子中先涂有酚酞溶液,然后加入“水”,则加入的“水”是( )
A.H2O B.HNO3溶液
C.NaOH溶液 D.NaCl溶液
解析 只有碱(如NaOH)溶液能使酚酞变红。
C
3.既能跟稀硫酸反应又能跟熟石灰反应的物质是( )
A.硫酸铜 B.碳酸钠
C.氢氧化钠 D.碳酸钙
解析 A项,硫酸铜不与稀硫酸反应,能和熟石灰反应,错误;B项,碳酸钠既能和稀硫酸反应生成硫酸钠、水和二氧化碳,又能和熟石灰反应生成碳酸钙沉淀和氢氧化钠,正确;C项,氢氧化钠只能和稀硫酸反应,不能和熟石灰反应,错误;D项,碳酸钙只能和稀硫酸反应,不能和熟石灰反应,错误。
B
4.下列各选项中,不能通过一步反应实现如图所示转化关系的是( )
A.X为铜、Y为氧化铜、Z为硫酸铜
B.X为二氧化碳、Y为碳、Z为一氧化碳
C.X为碳酸钙、Y为氧化钙、Z为氢氧化钙
D.X为氢氧化钠、Y为氯化钠、Z为碳酸钠
D
解析 铜与氧气反应生成氧化铜,氧化铜与硫酸反应生成硫酸铜,硫酸铜溶液与铁反应生成铜,故A不符合题意;二氧化碳与Mg反应生成碳单质和氧化镁,碳在氧气中不完全燃烧生成一氧化碳;一氧化碳在氧气中燃烧生成二氧化碳,故B不符合题意;碳酸钙高温分解生成氧化钙,氧化钙与水反应生成氢氧化钙,氢氧化钙与二氧化碳反应生成碳酸钙,故C不符合题意;氢氧化钠与盐酸反应生成氯化钠,氯化钠不能通过一步反应转化生成碳酸钠,故D符合题意。
5.下表所列各组物质中,物质之间按箭头方向不能通过一步反应实现如图所示转化的是( )
A.甲为CuO、乙为CO2、丙为H2O
B.甲为C、乙为CO、丙为CO2
C.甲为CaCO3、乙为CaO、丙为Ca(OH)2
D.甲为H2SO4、乙为H2O、丙为H2
解析 C中碳酸钙难溶于水,不与碱溶液发生反应,不能通过一步反应生成氢氧化钙。
C
6.某同学为了区别氢氧化钠溶液和澄清石灰水,设计了如图所示的四组实验方案,其中能达到目的的是( )
解析 澄清石灰水中通入二氧化碳产生沉淀,而氢氧化钠溶液中通入二氧化碳无沉淀产生。
D
7.化学变化多姿多彩,美丽如花。如图中甲、乙、丙、X分别是Fe2O3、C、CO、盐酸中的某一种,甲、乙、丙均能与X发生化学反应,则X是( )
A.C B.Fe2O3 C.CO D.盐酸
B
8.(2021·广州外国语学校高一期末)X、Y、Z、W各代表一种物质,若X+Y===Z+W,则X和Y之间不可能是( )
A.碱和盐的反应
B.碱性氧化物和水的反应
C.盐与盐的反应
D.酸性氧化物和碱的反应
B
解析 碱与盐可发生反应生成另一种碱和另一种盐,如Ca(OH)2+Na2CO3===CaCO3↓+2NaOH,A可能;碱性氧化物和水反应生成碱,产物只有一种,如CaO+H2O===Ca(OH)2,B不可能;盐与盐发生复分解反应,可以生成另外两种盐,如NaCl+AgNO3===AgCl↓+NaNO3,C可能;酸性氧化物与碱反应生成盐和水,如CO2+Ca(OH)2===CaCO3↓+H2O,D可能。
9.构建知识网络是一种重要的学习方法。如图是关于盐酸化学性质的知识网络图:“—”表示相连的两种物质能发生反应,“→”表示一种物质能转化为另一种物质。若A、B、C分别属于不同类别的化合物,则A、B、C可能是( )
A.CuO、Ba(OH)2、CuSO4
B.NaOH、HNO3、K2CO3
C.KOH、FeCl3、Na2CO3
D.NaOH、Ba(NO3)2、H2SO4
B
解析 A.盐酸不与硫酸铜反应,盐酸不能转化为氢氧化钡,氢氧化钡不与氧化铜反应,故A不符合题意;B.盐酸和氢氧化钠、碳酸钾都能反应,和硝酸银反应生成硝酸,硝酸和氢氧化钠、碳酸钾都能反应,故B符合题意;C.氯化铁和碳酸钠均为盐,属于相同类别的化合物,故C不符合题意;D.盐酸不能转化为硝酸钡,盐酸不与硫酸反应,氢氧化钠与硝酸钡不反应,故D不符合题意。
10.A、B、C、D、E中都含有同一种元素,它们之间的相互转化关系如图所示,其中所含的相同元素是( )
A.铜 B.碳 C.铁 D.钙
解析 A为CaO,B为Ca(OH)2,C为Ca(NO3)2,D为CaCl2,E为CaCO3。
D
11.如图以稀盐酸为例的反应关系体现了酸的化学性质,其中X与图中所给物质的类别不同。结合此图回答下列问题。
(1)稀盐酸中阳离子的符号是________。
(2)反应①中石蕊溶液变为________色。
(3)反应⑤的化学方程式为_____________________。
(4)图中只生成盐和水的反应有________(填序号)。
(5)若X溶液既能跟稀盐酸反应,又能跟Ca(OH)2反应,则X可能是(BaCl2、CuSO4、Na2CO3)中的________。
答案 (1)H+ (2)红 (3)Al2O3+6HCl===2AlCl3+3H2O (4)③⑤ (5)Na2CO3
解析 (1)稀盐酸中阳离子为H+;(2)稀盐酸显酸性,能使石蕊溶液变为红色;(3)反应⑤是氧化铝和盐酸反应生成氯化铝和水,反应的化学方程式为Al2O3+6HCl===2AlCl3+3H2O;(4)③氢氧化钙与稀盐酸反应生成氯化钙和水,⑤氧化铝与稀盐酸反应生成氯化铝和水,生成物均为盐和水,符合题意;(5)BaCl2不能与稀盐酸反应,且与Ca(OH)2不能发生反应,不符合题意;CuSO4不能与稀盐酸反应,不符合题意;Na2CO3能与稀盐酸反应生成氯化钠、水、二氧化碳,能与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,符合题意。
12.“碳捕捉技术”,常用于去除或分离气流中的二氧化碳。利用NaOH溶液“捕捉”CO2的基本过程如图(部分条件及物质已略去):
(1)反应分离室中,发生反应的化学方程式分别为CaO+H2O===Ca(OH)2和___________________________________________________________
__________________________________________________________。
(2)高温反应炉中,涉及反应的基本反应类型为____________。
(3)整个过程中,可以循环利用的物质化学式为______________。
NaHCO3+Ca(OH)2===NaOH+CaCO3↓+H2O
[或Na2CO3+Ca(OH)2===2NaOH+CaCO3↓]
分解反应
NaOH、CaO
解析 (1)由题干及图示知,捕捉室中氢氧化钠溶液吸收二氧化碳生成碳酸钠(或碳酸氢钠),则反应分离室中还存在的反应是Na2CO3+Ca(OH)2===2NaOH+CaCO3↓[或NaHCO3+Ca(OH)2===NaOH+CaCO3↓+H2O]。(2)根据图示,高温反应炉中发生的反应是碳酸钙分解生成氧化钙和二氧化碳,基本反应类型为分解反应。(3)参加反应且又生成的物质为可循环利用的物质,整个过程中,可以循环利用的物质为NaOH、CaO。
13.如图是小红学习《常见的碱》课题后,总结出氢氧化钙的化学性质。下列说法中不正确的是( )
A.①中的酚酞溶液变红色
B.②中与盐酸反应的化学方程式为Ca(OH)2+2HCl===CaCl2+2H2O
C.③中与硝酸钠溶液能发生反应
D.④可解释久置的澄清石灰水变质
C
解析 ①中Ca(OH)2能使酚酞溶液变红,A正确;②中Ca(OH)2与HCl反应的化学方程式为Ca(OH)2+2HCl===CaCl2+2H2O,B正确;③中NaNO3溶液与Ca(OH)2不反应,C错误;④中久置的澄清石灰水变质的原因是Ca(OH)2+CO2===CaCO3↓+H2O,D正确。
14.(2020·广东云浮高一期中)由单质到盐的转化关系可表示为:
C
解析 CuO不能与水反应生成Cu(OH)2,A错误;MgCl2不能与Na2SO4发生反应,B错误;碳在氧气中燃烧生成CO2,CO2与水反应生成H2CO3,H2CO3与氢氧化钙反应生成CaCO3沉淀,C正确;硫在氧气中燃烧生成SO2,SO2与水反应生成H2SO3,H2SO3与NaOH反应生成Na2SO3,D错误。
15.对牙膏的探究要用到许多化学知识。
(1)下表列出了两种牙膏中的摩擦剂,请在表中填写两种摩擦剂所属的物质类别:
X牙膏 Y牙膏
摩擦剂 碳酸钙 二氧化硅
摩擦剂的物质类别(指酸、碱、盐、氧化物)
(2)根据你的推测,牙膏摩擦剂在水中的溶解性是________(填“易溶”或“难溶”)。
盐
氧化物
难溶
CaO+H2O===Ca(OH)2
Ca(OH)2+Na2CO3===CaCO3↓+2NaOH
Thanks!
本讲内容结束
