课题3+利用化学方程式的简单计算(第1课时)-2022-2023学年九年级化学上册同步精品课件(14页)(人教版)
文档属性
| 名称 | 课题3+利用化学方程式的简单计算(第1课时)-2022-2023学年九年级化学上册同步精品课件(14页)(人教版) |

|
|
| 格式 | pptx | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-10-03 00:00:00 | ||
图片预览






文档简介
(共14张PPT)
第五单元 化学方程式
课题3 利用化学方程式的简单计算第1课时
学习目标
知道质量守恒定律是根据化学方程式计算的理论依据。
01
02
学会利用化学方程式的简单计算,掌握解题步骤和格式。
1、计算相对分子质量:
KMnO4 KClO3
2H2O 2 P2O5
158
122.5
36
284
2.写出下列反应的化学方程式
(1)用高锰酸钾制取氧气 : ;
(2)电解水: ;
(3)实验室用双氧水制氧气: ;
2KMnO4
K2MnO4 + MnO2 + O2↑
2H2O + O2↑
MnO2
2H2O2
2H2O
通电
2H2 ↑ + O2↑
回顾旧知
158
36
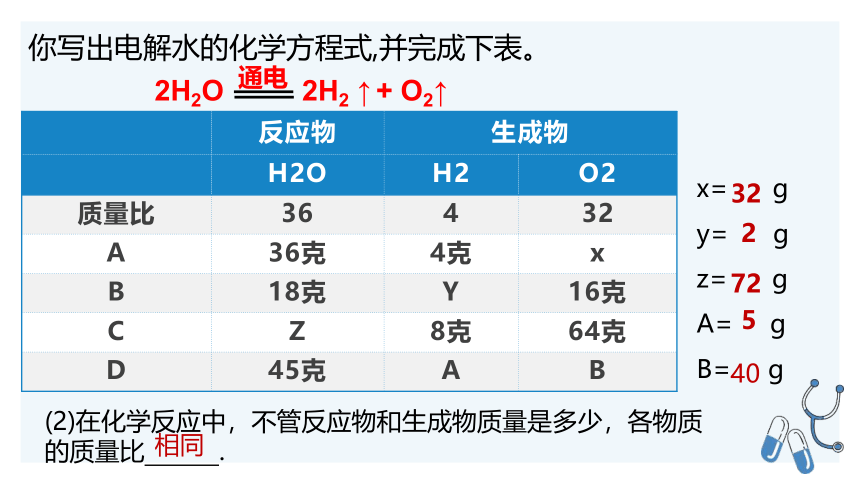
你写出电解水的化学方程式,并完成下表。
反应物 生成物 H2O H2 O2
质量比 36 4 32
A 36克 4克 x
B 18克 Y 16克
C Z 8克 64克
D 45克 A B
x= g
y= g
z= g
A= g
B= g
32
2
72
5
40
(2)在化学反应中,不管反应物和生成物质量是多少,各物质的质量比 .
相同
2H2O
通电
2H2 ↑ + O2↑
01
利用化学方程式计算的步骤
加热分解6.3g高锰酸钾,可以得到氧气的质量是多少?(计算结果保留一位小数)
例题1
1. 已知反应物的质量求生成物的质量
(1)设未知量
(2)写出反应的化学方程式
(3)标出相关物质的化学计
量数与相对分子质量的
乘积以及已知量、未知量
(4)列出比例式,求解
(5)简明地写出答案
2KMnO4 K2MnO4 + MnO2 + O2↑
△
2×(39+55+16×4)
6.3g
2×16
x
2×158
6.3g
=
x
32
x
=
32 × 6.3g
2 × 158
= 0.6g
解:可以得到氧气的质量为x 。
答:可以得到氧气的质量为0.6g 。
工业上,煅烧石灰石(主要成分是CaCO3)可制得生石灰(CaO)和二氧化碳。如果要制取5.6t氧化钙,需要碳酸钙的质量是多少?
例题2
2. 已知生成的质量求反应物的质量
100 56
答:需要碳酸钙10 t 。
解:设需要碳酸钙的质量为 x 。
100
5.6 t
=
x
56
CaCO3 CaO + CO2↑
高温
x
5.6 t
x
=
100×5.6 t
= 10 t
56
(1)设未知量时一定要注意质量单位,已知量和未知量单位不一致的一定要进行单位换算,单位必须一致才能计算。
(2)写出方程式要注意配平,而且要注意方程式的完整,反应条件、气体和沉淀的符号要注意标明。
(3)相关物质的相对分子质量写在相应化学式的下面,一定要注意用相对分子质量乘以化学式前面的系数,已知量和未知量写在相应相对分子质量的下边。
(4)计算结果的小数位保留按题中要求进行,若题中没有要求,一般保留一位小数。
注意:
02
化学方程式的计算练习
如果你是火箭推进器设计师,当确定升空的火箭需要液氢4kg、20kg或100kg时,你会在火箭助燃剂仓中填充多少千克的液氧使这些液氢完全燃烧?
练习1
解:设完全燃烧4kg、20kg、100kg液氢所需液氧的质量为x、y、z。
2H2 + O2 2H2O
4
32
4kg
x
4
4kg
32
x
=
x = 32kg
答:所需液氧的质量分别为32kg、160kg、800kg。
点燃
20kg
y
100kg
z
20kg
y
=
y = 160kg
100kg
z
=
z = 800kg
位于贵州省的“中国天眼”FAST,其“眼镜片”由金刚砂(SiC)制造。生产SiC的化学方程式为
SiO2+3C==SiC + 2CO↑,消耗C的质量为36 kg时,理论上可生产SiC的质量为多少?
练习2
1.锌与盐酸(主要成分为HCl)反应生成氢气和氯化锌。实验室里用6.5 g锌与足量盐酸反应,可制得氢气和氯化锌的质量各是多少 【相对原子质量:H-1 Cl-35.5 Zn-65】
练习3
解:设制得氢气的质量为x,氯化锌的质量为y。
Zn+2HCl══ZnCl2+H2↑
65 136 2
6.5 g y x
x=0.2 g y=13.6 g
答:可制得氢气0.2 g,氯化锌13.6 g。
谢谢聆听
单/击/此/处/添/加/副/标/题/内/容
第五单元 化学方程式
课题3 利用化学方程式的简单计算第1课时
学习目标
知道质量守恒定律是根据化学方程式计算的理论依据。
01
02
学会利用化学方程式的简单计算,掌握解题步骤和格式。
1、计算相对分子质量:
KMnO4 KClO3
2H2O 2 P2O5
158
122.5
36
284
2.写出下列反应的化学方程式
(1)用高锰酸钾制取氧气 : ;
(2)电解水: ;
(3)实验室用双氧水制氧气: ;
2KMnO4
K2MnO4 + MnO2 + O2↑
2H2O + O2↑
MnO2
2H2O2
2H2O
通电
2H2 ↑ + O2↑
回顾旧知
158
36
你写出电解水的化学方程式,并完成下表。
反应物 生成物 H2O H2 O2
质量比 36 4 32
A 36克 4克 x
B 18克 Y 16克
C Z 8克 64克
D 45克 A B
x= g
y= g
z= g
A= g
B= g
32
2
72
5
40
(2)在化学反应中,不管反应物和生成物质量是多少,各物质的质量比 .
相同
2H2O
通电
2H2 ↑ + O2↑
01
利用化学方程式计算的步骤
加热分解6.3g高锰酸钾,可以得到氧气的质量是多少?(计算结果保留一位小数)
例题1
1. 已知反应物的质量求生成物的质量
(1)设未知量
(2)写出反应的化学方程式
(3)标出相关物质的化学计
量数与相对分子质量的
乘积以及已知量、未知量
(4)列出比例式,求解
(5)简明地写出答案
2KMnO4 K2MnO4 + MnO2 + O2↑
△
2×(39+55+16×4)
6.3g
2×16
x
2×158
6.3g
=
x
32
x
=
32 × 6.3g
2 × 158
= 0.6g
解:可以得到氧气的质量为x 。
答:可以得到氧气的质量为0.6g 。
工业上,煅烧石灰石(主要成分是CaCO3)可制得生石灰(CaO)和二氧化碳。如果要制取5.6t氧化钙,需要碳酸钙的质量是多少?
例题2
2. 已知生成的质量求反应物的质量
100 56
答:需要碳酸钙10 t 。
解:设需要碳酸钙的质量为 x 。
100
5.6 t
=
x
56
CaCO3 CaO + CO2↑
高温
x
5.6 t
x
=
100×5.6 t
= 10 t
56
(1)设未知量时一定要注意质量单位,已知量和未知量单位不一致的一定要进行单位换算,单位必须一致才能计算。
(2)写出方程式要注意配平,而且要注意方程式的完整,反应条件、气体和沉淀的符号要注意标明。
(3)相关物质的相对分子质量写在相应化学式的下面,一定要注意用相对分子质量乘以化学式前面的系数,已知量和未知量写在相应相对分子质量的下边。
(4)计算结果的小数位保留按题中要求进行,若题中没有要求,一般保留一位小数。
注意:
02
化学方程式的计算练习
如果你是火箭推进器设计师,当确定升空的火箭需要液氢4kg、20kg或100kg时,你会在火箭助燃剂仓中填充多少千克的液氧使这些液氢完全燃烧?
练习1
解:设完全燃烧4kg、20kg、100kg液氢所需液氧的质量为x、y、z。
2H2 + O2 2H2O
4
32
4kg
x
4
4kg
32
x
=
x = 32kg
答:所需液氧的质量分别为32kg、160kg、800kg。
点燃
20kg
y
100kg
z
20kg
y
=
y = 160kg
100kg
z
=
z = 800kg
位于贵州省的“中国天眼”FAST,其“眼镜片”由金刚砂(SiC)制造。生产SiC的化学方程式为
SiO2+3C==SiC + 2CO↑,消耗C的质量为36 kg时,理论上可生产SiC的质量为多少?
练习2
1.锌与盐酸(主要成分为HCl)反应生成氢气和氯化锌。实验室里用6.5 g锌与足量盐酸反应,可制得氢气和氯化锌的质量各是多少 【相对原子质量:H-1 Cl-35.5 Zn-65】
练习3
解:设制得氢气的质量为x,氯化锌的质量为y。
Zn+2HCl══ZnCl2+H2↑
65 136 2
6.5 g y x
x=0.2 g y=13.6 g
答:可制得氢气0.2 g,氯化锌13.6 g。
谢谢聆听
单/击/此/处/添/加/副/标/题/内/容
同课章节目录
- 绪言 化学使世界变得更加绚丽多彩
- 第一单元 走进化学世界
- 课题1 物质的变化和性质
- 课题2 化学是一门以实验为基础的科学
- 课题3 走进化学实验室
- 第二单元 我们周围的空气
- 课题1 空气
- 课题2 氧气
- 课题3 制取氧气
- 实验活动1 氧气的实验室制取与性质
- 第三单元 物质构成的奥秘
- 课题1 分子和原子
- 课题2 原子的结构
- 课题3 元素
- 第四单元 自然界的水
- 课题1 爱护水资源
- 课题2 水的净化
- 课题3 水的组成
- 课题4 化学式与化合价
- 第五单元 化学方程式
- 课题 1 质量守恒定律
- 课题 2 如何正确书写化学方程式
- 课题 3 利用化学方程式的简单计算
- 第六单元 碳和碳的氧化物
- 课题1 金刚石、石墨和C60
- 课题2 二氧化碳制取的研究
- 课题3 二氧化碳和一氧化碳
- 实验活动2 二氧化碳的实验室制取与性质
- 第七单元 燃料及其利用
- 课题 1 燃烧和灭火
- 课题2 燃料的合理利用与开发
- 实验活动 3 燃烧的条件
