第三单元海水中的化学单元测试题--2022-2023学年九年级化学鲁教版(五四学制)全一册(有答案)
文档属性
| 名称 | 第三单元海水中的化学单元测试题--2022-2023学年九年级化学鲁教版(五四学制)全一册(有答案) |  | |
| 格式 | zip | ||
| 文件大小 | 238.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-10-03 10:57:17 | ||
图片预览


文档简介
第三单元海水中的化学单元测试题
一、单选题
1.我市地处沿海,海洋资源丰富,综合开发海洋资源前景十分广阔。你认为海水中含量最多的金属元素是
A.铝 B.钠 C.钙 D.铁
2.侯德榜是我国杰出的化学家,由他创立的“侯氏制碱法”中有这样一个反应:,则的化学式是
A.CO B.CO2 C.H2 D.CH4
3.下列有关水的说法中,不正确的是
A.用肥皂水可区分硬水和软水
B.水是实验室中最常用的溶剂
C.电解水实验中得到的氧气和氢气的质量比为1:2
D.海水淡化是向海水要淡水的一种方法
4.提出联合制碱法的中国化工专家是( )
A.徐光宪 B.侯德榜
C.张青莲 D.屠呦呦
5.有关“粗盐中难溶性杂质的去除”实验中说法不正确的是
A.多加水,让粗盐加速溶解
B.玻璃棒用了4次,但作用各不相同
C.粗盐经过溶解、过滤、蒸发、结晶可以得到初步提纯
D.当蒸发皿中出现较多量固体时,停止加热,利用余热使滤液蒸干
6.将珍珠加入稀盐酸中,有气泡产生,生成的气体能使澄清石灰水变浑浊,则珍珠中含有下列离子中的( )
A.氯离子 B.硫酸根离子 C.碳酸根离子 D.氢氧根离子
7.“NaCl+CO2+NH3+H2O=NaHCO3+NH4Cl”是著名的“侯氏制碱法”的重要反应。下列有关叙述正确的是
A.NaHCO3是纯碱
B.析出晶体后剩余溶液中溶质只有NH4Cl
C.配制饱和食盐水时,可通过搅拌来提高食盐的溶解度
D.向饱和食盐水中先通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收
8.除去下列物质中的杂质,选用试剂和方法均正确的是
选项 物质 杂质(少量) 试剂和方法
A 氯化钾 氯酸钾 加入少量二氧化锰粉末,加热
B 稀硫酸 稀盐酸 加入适量的氯化钡溶液,过滤
C 氯化钙溶液 氢氧化钙 加入稍微过量的稀盐酸,加热
D 硝酸钾溶液 硫酸钾 加入过量的硝酸钡溶液,过滤
A.A B.B C.C D.D
9.欲将粗盐提纯并用所得精盐配制一定溶质质量分数的氯化钠溶液。下列说法正确的是
A.过滤时,用玻璃棒搅拌加快过滤速度
B.蒸发时,将蒸发皿中晶体全部析出后才停止加热
C.配制溶液时必须使用的仪器有托盘天平、酒精灯、量筒、烧杯、玻璃棒等
D.配制溶液需要经过计算、称量、溶解、装瓶存放等步骤
10.下列溶液分别能跟硫酸铜、盐酸、碳酸钠溶液反应,并产生不同现象的是( )
A.Ca(OH)2 B.AgNO3 C.H2SO4 D.NaOH
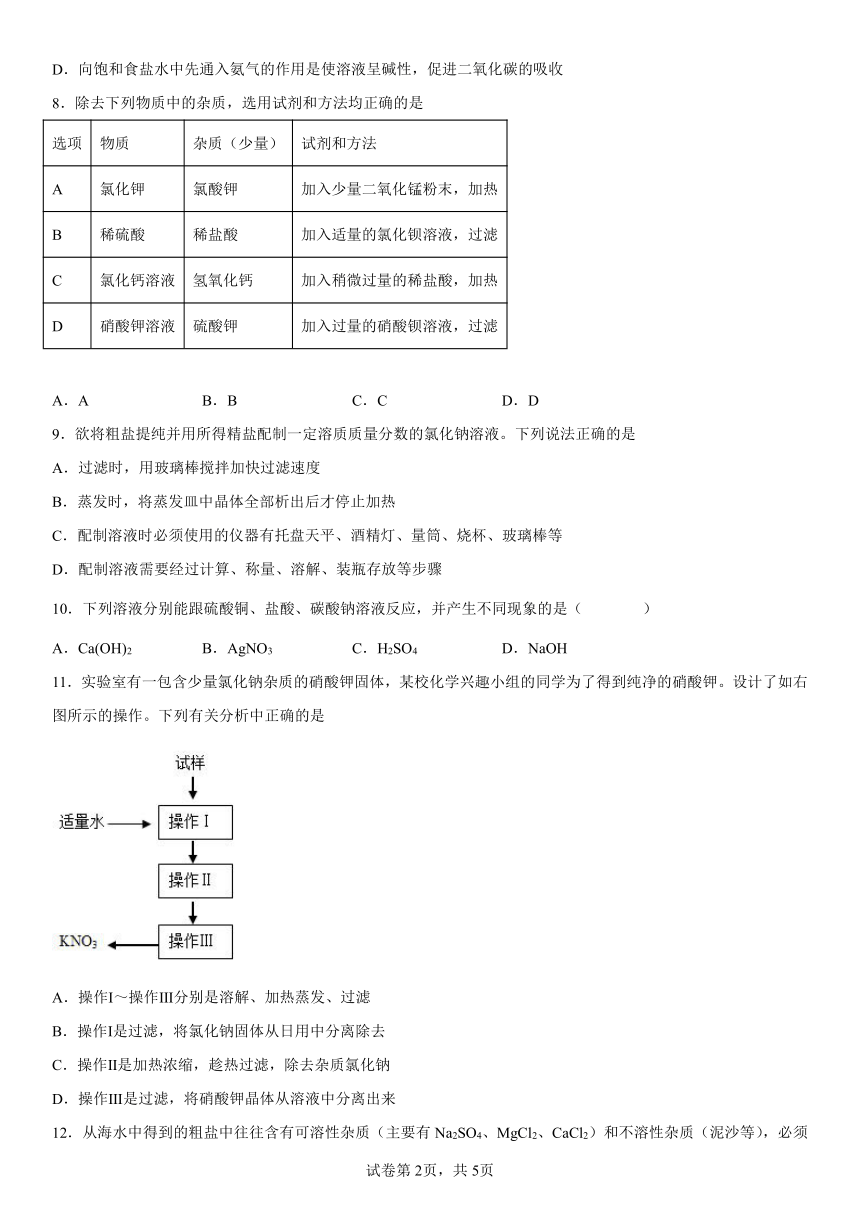
11.实验室有一包含少量氯化钠杂质的硝酸钾固体,某校化学兴趣小组的同学为了得到纯净的硝酸钾。设计了如右图所示的操作。下列有关分析中正确的是
A.操作Ⅰ~操作Ⅲ分别是溶解、加热蒸发、过滤
B.操作Ⅰ是过滤,将氯化钠固体从日用中分离除去
C.操作Ⅱ是加热浓缩,趁热过滤,除去杂质氯化钠
D.操作Ⅲ是过滤,将硝酸钾晶体从溶液中分离出来
12.从海水中得到的粗盐中往往含有可溶性杂质(主要有Na2SO4、MgCl2、CaCl2)和不溶性杂质(泥沙等),必须进行分离和提纯后才能使用。粗盐提纯的部分流程如图。有关该流程说法错误的是( )
A.不溶性杂质主要是泥沙
B.过滤时玻璃棒的作用是搅拌,以便加快过滤速度
C.蒸发时,当蒸发皿中出现较多固体时,停止加热,利用蒸发皿的余热使滤液蒸干
D.操作①②③依次加入的试剂可以为BaCl2溶液、NaOH溶液、Na2CO3溶液
二、填空题
13.现有五种溶液:①稀硫酸;②FeCl3;③NaOH;④BaCl2;⑤Na2SO4。将它们两两混合,能发生的反应共有_____个。若不用任何外加试剂将它们区分开来,其中不用化学方法就可鉴别出的是_____,余下四种溶液被鉴别出的先后顺序是_____(填序号)。
14.为了除去粗盐中CaCl2、MgCl2、Na2SO4等可溶性杂质,需进行如下操作:①溶解;②依次加入过量BaCl2、NaOH、Na2CO3溶液;③过滤;④加适量盐酸;⑤蒸发、结晶。加入NaOH溶液时发生反应的现象为_________;操作③中用到的玻璃仪器有___________;若将操作②中BaCl2和Na2CO3溶液的加入顺序对调,则过滤之后得到滤液中的溶质有_________ (用化学式表示)。
15.西汉刘安所著《淮南万毕术》记载的湿法炼铜术,表明我国是最早利用硫酸铜的国家。
(1)微观认识:构成硫酸铜的粒子是___________(填符号)。
(2)宏观分析:用硫酸铜炼铜的化学反应中,铜元素的化合价由___________价变成___________价。
(3)用途推测:硫酸铜是白色粉末,遇水变成蓝色,推测其用途为___________。
(4)工业制法:
方案一:
方案二:将废铜屑倒入稀硫酸中,控温80℃并通入空气,生成硫酸铜和水。该反应的现象为___________。
方案三:
请选出较好方案并阐述理由:___________。
16.材料一:侯德榜是我国著名的化学家,发明了侯氏制碱法,为纯碱和氮肥工业技术的发展作出了杰出的贡献。下面是实验室模拟侯氏制碱法原理的生产过程:
①20℃时,将CO2通入含NH3的饱和NaCl溶液中,生成 NaHCO3晶体和NH4Cl溶液。
②将①中的产物 NaHCO3晶体充分加热分解,得到Na2CO3、H2O和CO2。
材料二:20℃时几种物质在水中的溶解度/g
NaCl NH4Cl NaHCO3
36.0 37.2 9.6
请回答下列问题:
(1)在第①步反应中,有 NaHCO3晶体析出,而没有NH4Cl和NaCl晶体析出的原因是_____。
(2)该生产过程中部分生成物可作为原料循环使用的是_____,同时得到的副产品NH4Cl是一种氮肥。
三、实验题
17.某化学兴趣小组的同学参照教科书内容,在学校实验室里完成了以下两个实验:
实验一:配制溶质质量分数为6%的溶液,按如下步骤进行操作:计算→称量→溶解→装瓶。
实验二 :称取粗盐进行提纯,粗盐除外,还含有、 以及泥沙等杂质,为了有效地将粗盐提纯,实验的各步操作流程如图所示:
请你根据以上信息回答下列问题:
(1)配制溶质质量分数为6%的溶液,需______,水 ______。
(2)溶解过程中用到了玻璃棒,它的作用是 ______ 。
(3)粗盐提纯时,操作I的名称为 ______ 。
(4)某同学所得精盐比其它同学明显要少,原因可能是 ______ (填序号)。
A 溶解时将粗盐一次性全部倒入水中,立即过滤
B 蒸发时有一些液体、固体溅出
C 提纯后所得精盐尚未完全干燥
18.粗盐提纯和溶液配制都是中学化学的重要实验。
(1)粗盐提纯实验过程中发现过滤速度较慢,可能的原因是____;在蒸发操作中,当蒸发皿中出现____时,停止加热。
(2)配制100g质量分数为6%的氯化钠溶液,计算需要水的质量为____g;从上图选出配制该溶液的主要操作顺序____(选填序号);若向烧杯中倒水时部分水洒出,最终会导致配制的溶液中溶质的质量分数____(填“>”或“=”或“<”)6%。
四、计算题
19.某碳酸钠样品中混有少量氯化钠,根据下图所示信息,计算该样品中碳酸钠的质量分数(计算结果精确到0.1%)。
20.厨房中使用的食用碱(主要成分碳酸钠)中往往含有少量的氯化钠,化学兴趣小组的同学通过实验来测定某品牌的食用碱样品中碳酸钠的质量分数。他们实验的过程和数据如下图所示。
计算:该食用碱中碳酸钠的质量分数是__________ (计算结果精确至0.1%)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.B
3.C
4.B
5.A
6.C
7.D
8.C
9.D
10.A
11.D
12.B
13. (1) 四 ② (2) ③①④⑤
14.(1) 烧 杯、漏斗、玻璃棒 (2) NaCl 、NaOH、BaCl2
15.(1)Cu2+、
(2) +2 0
(3)检验水
(4) 方案二较好,安全、环保无污染、原料的利用率高
16. (1) 在20℃,NaHCO3的溶解度远小于NH4Cl和NaCl的溶解度 (2) CO2和H2O
17.(1) 3 47 (2) 搅拌,加速溶解 (3) 过滤 AB
18.(1) 滤纸没有紧贴漏斗内壁,中间有气泡(或“固体颗粒阻碍了液体通过滤纸孔隙”或“滤纸选择的规格不对”或“漏斗下端尖口没紧靠烧杯内壁”) 较多固体
(2) 94 AEB >
19.70.7%
20.88.3%
答案第1页,共2页
答案第1页,共2页
一、单选题
1.我市地处沿海,海洋资源丰富,综合开发海洋资源前景十分广阔。你认为海水中含量最多的金属元素是
A.铝 B.钠 C.钙 D.铁
2.侯德榜是我国杰出的化学家,由他创立的“侯氏制碱法”中有这样一个反应:,则的化学式是
A.CO B.CO2 C.H2 D.CH4
3.下列有关水的说法中,不正确的是
A.用肥皂水可区分硬水和软水
B.水是实验室中最常用的溶剂
C.电解水实验中得到的氧气和氢气的质量比为1:2
D.海水淡化是向海水要淡水的一种方法
4.提出联合制碱法的中国化工专家是( )
A.徐光宪 B.侯德榜
C.张青莲 D.屠呦呦
5.有关“粗盐中难溶性杂质的去除”实验中说法不正确的是
A.多加水,让粗盐加速溶解
B.玻璃棒用了4次,但作用各不相同
C.粗盐经过溶解、过滤、蒸发、结晶可以得到初步提纯
D.当蒸发皿中出现较多量固体时,停止加热,利用余热使滤液蒸干
6.将珍珠加入稀盐酸中,有气泡产生,生成的气体能使澄清石灰水变浑浊,则珍珠中含有下列离子中的( )
A.氯离子 B.硫酸根离子 C.碳酸根离子 D.氢氧根离子
7.“NaCl+CO2+NH3+H2O=NaHCO3+NH4Cl”是著名的“侯氏制碱法”的重要反应。下列有关叙述正确的是
A.NaHCO3是纯碱
B.析出晶体后剩余溶液中溶质只有NH4Cl
C.配制饱和食盐水时,可通过搅拌来提高食盐的溶解度
D.向饱和食盐水中先通入氨气的作用是使溶液呈碱性,促进二氧化碳的吸收
8.除去下列物质中的杂质,选用试剂和方法均正确的是
选项 物质 杂质(少量) 试剂和方法
A 氯化钾 氯酸钾 加入少量二氧化锰粉末,加热
B 稀硫酸 稀盐酸 加入适量的氯化钡溶液,过滤
C 氯化钙溶液 氢氧化钙 加入稍微过量的稀盐酸,加热
D 硝酸钾溶液 硫酸钾 加入过量的硝酸钡溶液,过滤
A.A B.B C.C D.D
9.欲将粗盐提纯并用所得精盐配制一定溶质质量分数的氯化钠溶液。下列说法正确的是
A.过滤时,用玻璃棒搅拌加快过滤速度
B.蒸发时,将蒸发皿中晶体全部析出后才停止加热
C.配制溶液时必须使用的仪器有托盘天平、酒精灯、量筒、烧杯、玻璃棒等
D.配制溶液需要经过计算、称量、溶解、装瓶存放等步骤
10.下列溶液分别能跟硫酸铜、盐酸、碳酸钠溶液反应,并产生不同现象的是( )
A.Ca(OH)2 B.AgNO3 C.H2SO4 D.NaOH
11.实验室有一包含少量氯化钠杂质的硝酸钾固体,某校化学兴趣小组的同学为了得到纯净的硝酸钾。设计了如右图所示的操作。下列有关分析中正确的是
A.操作Ⅰ~操作Ⅲ分别是溶解、加热蒸发、过滤
B.操作Ⅰ是过滤,将氯化钠固体从日用中分离除去
C.操作Ⅱ是加热浓缩,趁热过滤,除去杂质氯化钠
D.操作Ⅲ是过滤,将硝酸钾晶体从溶液中分离出来
12.从海水中得到的粗盐中往往含有可溶性杂质(主要有Na2SO4、MgCl2、CaCl2)和不溶性杂质(泥沙等),必须进行分离和提纯后才能使用。粗盐提纯的部分流程如图。有关该流程说法错误的是( )
A.不溶性杂质主要是泥沙
B.过滤时玻璃棒的作用是搅拌,以便加快过滤速度
C.蒸发时,当蒸发皿中出现较多固体时,停止加热,利用蒸发皿的余热使滤液蒸干
D.操作①②③依次加入的试剂可以为BaCl2溶液、NaOH溶液、Na2CO3溶液
二、填空题
13.现有五种溶液:①稀硫酸;②FeCl3;③NaOH;④BaCl2;⑤Na2SO4。将它们两两混合,能发生的反应共有_____个。若不用任何外加试剂将它们区分开来,其中不用化学方法就可鉴别出的是_____,余下四种溶液被鉴别出的先后顺序是_____(填序号)。
14.为了除去粗盐中CaCl2、MgCl2、Na2SO4等可溶性杂质,需进行如下操作:①溶解;②依次加入过量BaCl2、NaOH、Na2CO3溶液;③过滤;④加适量盐酸;⑤蒸发、结晶。加入NaOH溶液时发生反应的现象为_________;操作③中用到的玻璃仪器有___________;若将操作②中BaCl2和Na2CO3溶液的加入顺序对调,则过滤之后得到滤液中的溶质有_________ (用化学式表示)。
15.西汉刘安所著《淮南万毕术》记载的湿法炼铜术,表明我国是最早利用硫酸铜的国家。
(1)微观认识:构成硫酸铜的粒子是___________(填符号)。
(2)宏观分析:用硫酸铜炼铜的化学反应中,铜元素的化合价由___________价变成___________价。
(3)用途推测:硫酸铜是白色粉末,遇水变成蓝色,推测其用途为___________。
(4)工业制法:
方案一:
方案二:将废铜屑倒入稀硫酸中,控温80℃并通入空气,生成硫酸铜和水。该反应的现象为___________。
方案三:
请选出较好方案并阐述理由:___________。
16.材料一:侯德榜是我国著名的化学家,发明了侯氏制碱法,为纯碱和氮肥工业技术的发展作出了杰出的贡献。下面是实验室模拟侯氏制碱法原理的生产过程:
①20℃时,将CO2通入含NH3的饱和NaCl溶液中,生成 NaHCO3晶体和NH4Cl溶液。
②将①中的产物 NaHCO3晶体充分加热分解,得到Na2CO3、H2O和CO2。
材料二:20℃时几种物质在水中的溶解度/g
NaCl NH4Cl NaHCO3
36.0 37.2 9.6
请回答下列问题:
(1)在第①步反应中,有 NaHCO3晶体析出,而没有NH4Cl和NaCl晶体析出的原因是_____。
(2)该生产过程中部分生成物可作为原料循环使用的是_____,同时得到的副产品NH4Cl是一种氮肥。
三、实验题
17.某化学兴趣小组的同学参照教科书内容,在学校实验室里完成了以下两个实验:
实验一:配制溶质质量分数为6%的溶液,按如下步骤进行操作:计算→称量→溶解→装瓶。
实验二 :称取粗盐进行提纯,粗盐除外,还含有、 以及泥沙等杂质,为了有效地将粗盐提纯,实验的各步操作流程如图所示:
请你根据以上信息回答下列问题:
(1)配制溶质质量分数为6%的溶液,需______,水 ______。
(2)溶解过程中用到了玻璃棒,它的作用是 ______ 。
(3)粗盐提纯时,操作I的名称为 ______ 。
(4)某同学所得精盐比其它同学明显要少,原因可能是 ______ (填序号)。
A 溶解时将粗盐一次性全部倒入水中,立即过滤
B 蒸发时有一些液体、固体溅出
C 提纯后所得精盐尚未完全干燥
18.粗盐提纯和溶液配制都是中学化学的重要实验。
(1)粗盐提纯实验过程中发现过滤速度较慢,可能的原因是____;在蒸发操作中,当蒸发皿中出现____时,停止加热。
(2)配制100g质量分数为6%的氯化钠溶液,计算需要水的质量为____g;从上图选出配制该溶液的主要操作顺序____(选填序号);若向烧杯中倒水时部分水洒出,最终会导致配制的溶液中溶质的质量分数____(填“>”或“=”或“<”)6%。
四、计算题
19.某碳酸钠样品中混有少量氯化钠,根据下图所示信息,计算该样品中碳酸钠的质量分数(计算结果精确到0.1%)。
20.厨房中使用的食用碱(主要成分碳酸钠)中往往含有少量的氯化钠,化学兴趣小组的同学通过实验来测定某品牌的食用碱样品中碳酸钠的质量分数。他们实验的过程和数据如下图所示。
计算:该食用碱中碳酸钠的质量分数是__________ (计算结果精确至0.1%)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.B
3.C
4.B
5.A
6.C
7.D
8.C
9.D
10.A
11.D
12.B
13. (1) 四 ② (2) ③①④⑤
14.(1) 烧 杯、漏斗、玻璃棒 (2) NaCl 、NaOH、BaCl2
15.(1)Cu2+、
(2) +2 0
(3)检验水
(4) 方案二较好,安全、环保无污染、原料的利用率高
16. (1) 在20℃,NaHCO3的溶解度远小于NH4Cl和NaCl的溶解度 (2) CO2和H2O
17.(1) 3 47 (2) 搅拌,加速溶解 (3) 过滤 AB
18.(1) 滤纸没有紧贴漏斗内壁,中间有气泡(或“固体颗粒阻碍了液体通过滤纸孔隙”或“滤纸选择的规格不对”或“漏斗下端尖口没紧靠烧杯内壁”) 较多固体
(2) 94 AEB >
19.70.7%
20.88.3%
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第一单元 溶液
- 1 溶液的形成
- 2 溶液组成的定量表示
- 3物质的溶解性
- 到实验室去:配制一定溶质质量分数的溶液
- 第二单元 常见的酸和碱
- 1 酸及其性质
- 2 碱及其性质
- 3 溶液的酸碱性
- 4 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 到图书馆去:分子变成离子
- 第三单元 海水中的化学
- 1 海洋化学资源
- 2 海水“晒盐”
- 3 海水“制碱”
- 到实验室去:粗盐中难溶性杂质的去除
- 第四单元 金属
- 1 常见的金属材料
- 2 金属的化学性质
- 3 钢铁的锈蚀与防护
- 到实验室去:探究金属的性质
- 第五单元 化学与健康
- 1 食物中的有机物
- 2 化学元素与人体健康
- 3 远离有毒物质
- 第六单元 化学与社会发展
- 1 化学与能源开发
- 2 化学与材料研制
- 3 化学与农业生产
- 4 化学与环境保护
