化学人教版(2019)选择性必修1 3.2酸碱中和滴定误差分析(共22张ppt)
文档属性
| 名称 | 化学人教版(2019)选择性必修1 3.2酸碱中和滴定误差分析(共22张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 371.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-10-04 16:10:45 | ||
图片预览






文档简介
(共22张PPT)
酸碱中和滴定误差分析
误差分析
以标准液滴定待测液为例:
分析依据
c待测·V待测=c标准·V标准
c待测=
c标准、V待测均为定值,误差均体现在V标准的大小上。
1.
结论:c(待)与V(标)成正比; V(标)偏大,结果__________;V(标)偏小,结果___________;
2.
偏大
偏小
误差产生的原因
洗涤误差
1
操作 V标准 c待测
滴定管未用标准溶液润洗
滴定管(移液管)未用待测溶液润洗
锥形瓶用待测溶液润洗
锥形瓶洗净后还留有蒸馏水
误差产生的原因
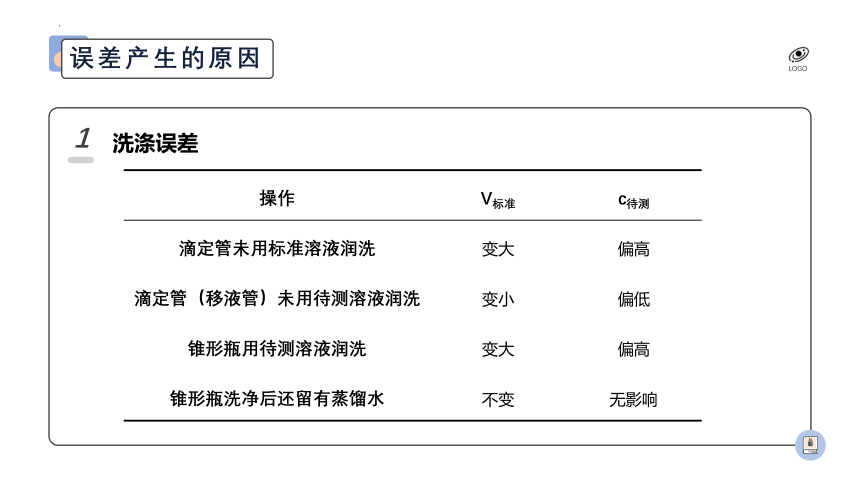
洗涤误差
1
操作 V标准 c待测
滴定管未用标准溶液润洗 变大 偏高
滴定管(移液管)未用待测溶液润洗 变小 偏低
锥形瓶用待测溶液润洗 变大 偏高
锥形瓶洗净后还留有蒸馏水 不变 无影响
误差产生的原因
气泡误差
2
操作 V标准 c待测
放出待测液的滴定管开始有气泡,放出液体后气泡消失
盛有标准液的滴定管滴定前有气泡,滴定终点时气泡消失
盛有标准液的滴定管滴定前没有气泡,滴定终点时有气泡
误差产生的原因
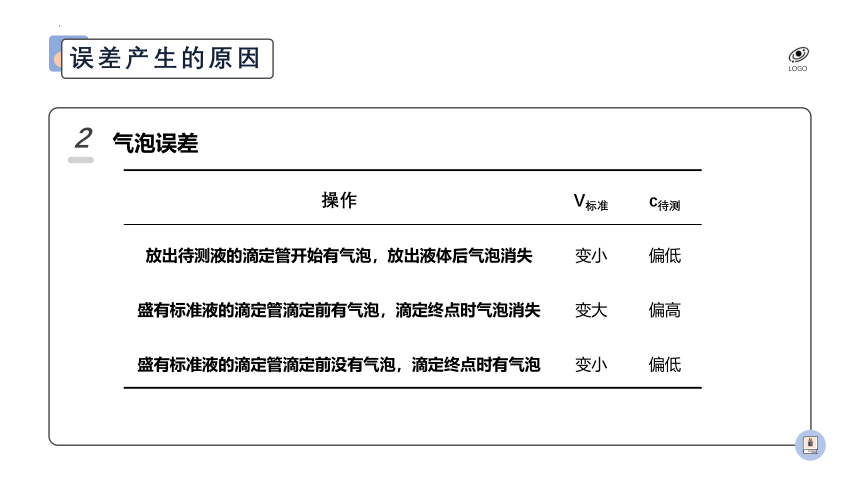
气泡误差
2
操作 V标准 c待测
放出待测液的滴定管开始有气泡,放出液体后气泡消失 变小 偏低
盛有标准液的滴定管滴定前有气泡,滴定终点时气泡消失 变大 偏高
盛有标准液的滴定管滴定前没有气泡,滴定终点时有气泡 变小 偏低
误差产生的原因
操作误差
3
操作 V标准 c待测
移液管尖端残液吹入锥形瓶
振荡锥形瓶时部分液体溅出
部分标准液滴出锥形瓶外
向锥形瓶中加蒸馏水冲洗内壁的标准液
误差产生的原因
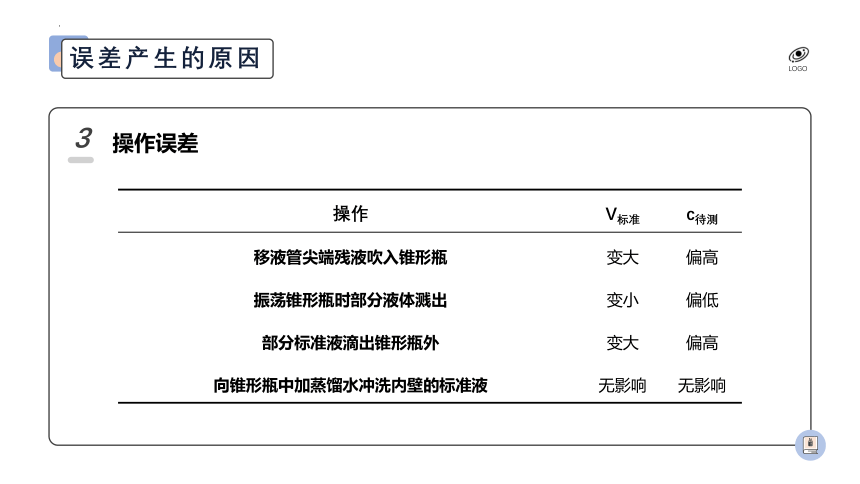
操作误差
3
操作 V标准 c待测
移液管尖端残液吹入锥形瓶 变大 偏高
振荡锥形瓶时部分液体溅出 变小 偏低
部分标准液滴出锥形瓶外 变大 偏高
向锥形瓶中加蒸馏水冲洗内壁的标准液 无影响 无影响
误差产生的原因
终点误差
4
操作 V标准 c待测
强酸滴定弱碱时,甲基橙由黄色变为红色时停止滴定
强碱滴定弱酸时,酚酞由无色变为粉红时立即停止滴定
滴定终点时滴定管尖嘴处半滴尚未滴下,或一滴标准液附着在锥形瓶内壁上未流下
溶液颜色较浅时滴入酸液过快,停止滴定后再加一滴NaOH溶液无变化
误差产生的原因
终点误差
4
操作 V标准 c待测
强酸滴定弱碱时,甲基橙由黄色变为红色时停止滴定 变大 偏高
强碱滴定弱酸时,酚酞由无色变为粉红时立即停止滴定 变小 偏低
滴定终点时滴定管尖嘴处半滴尚未滴下,或一滴标准液附着在锥形瓶内壁上未流下 变大 偏高
溶液颜色较浅时滴入酸液过快,停止滴定后再加一滴NaOH溶液无变化 变大 偏高
误差产生的原因
读数误差
5
操作 V标准 c待测
滴定前平视,滴定后俯视
滴定前仰视,滴定后平视
滴定前仰视,滴定后俯视
滴定前平视,滴定后仰视
滴定前俯视,滴定后平视
滴定前俯视,滴定后仰视
误差产生的原因
读数误差
5
V实
V实
读出值
读出值
滴定前
滴定后
滴定前
滴定后
误差产生的原因
读数误差
5
操作 V标准 c待测
滴定前平视,滴定后俯视 变小 偏低
滴定前仰视,滴定后平视 变小 偏低
滴定前仰视,滴定后俯视 变小 偏低
滴定前平视,滴定后仰视 变大 偏高
滴定前俯视,滴定后平视 变大 偏高
滴定前俯视,滴定后仰视 变大 偏高
误差产生的原因
读数误差
5
量筒——量取一定体积的溶液
俯视:实际量取的液体体积偏小
仰视:实际量取的液体体积偏大
容量瓶——用容量瓶定容
俯视:溶液体积偏小,所配制溶液的浓度偏高
仰视:溶液体积偏大,所配制溶液的浓度偏低
误差产生的原因
杂质误差
6
配置NaOH标准溶液时有杂质
NaOH固体潮解
用NaOH配制的因存放不当而变质的标液来测定盐酸的浓度
V(标)↑
c(待)↑
NaOH中掺有杂质
不与酸反应的杂质(如NaCl)
混有中和1 mol H+所需质量大于40g的杂质(如Na2CO3、K2CO3)
混有中和1 mol H+所需质量小于40g的杂质(如Na2O)
V(标)↑
c(待)↑
V(标)↑
c(待)↑
V(标) ↓
c(待) ↓
无影响
误差产生的原因
指示剂误差
7
用强酸滴定弱碱,指示剂选用酚酞。
用强碱滴定弱酸,指示剂选用甲基橙。
误差产生的原因
指示剂误差
7
用强酸滴定弱碱,指示剂选用酚酞。由于酚酞的变色范围在8.2∽10之间,造成消耗强酸标准液体积偏小,待测液浓度偏低。
用强碱滴定弱酸,指示剂选用甲基橙。由于甲基橙的变色范围在3.1∽4.4之间,造成消耗强碱标准液体积偏小,待测液浓度偏低。
误差产生的原因
练习
某同学欲用已知物质的量浓度为0.1000 mol·L-1的盐酸测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂。请填写下列空白:
(1)用标准的盐酸滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视 。直到因加入半滴盐酸,溶液的颜色由 色变为 色,半分钟不恢复原色,立即停止滴定。
锥形瓶内溶液颜色的变化
粉红
无
误差产生的原因
练习
(2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是 (填字母)。
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
E.滴定过程中,锥形瓶的振荡过于激烈,使少量溶液溅出
DE
误差产生的原因
练习
用已知浓度的NaOH溶液测定某H2SO4溶液的浓度,参考右图,从表中选出正确选项( )
D
误差产生的原因
练习
下列实验操作不会引起误差的是( )
A.酸碱中和滴定时,用待测液润洗锥形瓶
B.酸碱中和滴定时,用冲洗干净的滴定管盛装标准溶液
C.用NaOH标准溶液测定未知浓度的盐酸溶液时,在滴定过程中向锥形瓶加入 5 mL的蒸馏水
D.用标准盐酸测定未知浓度NaOH溶液,实验结束时,酸式滴定管尖嘴部分有气泡,开始实验时无气泡
C
误差产生的原因
练习
用已知浓度的盐酸测定未知浓度NaOH溶液的物质的量浓度,待测液放在锥形瓶中。中和滴定时下列操作会使测定结果偏低的是(锥形瓶中溶液用滴定管量取)( )
A.碱式滴定管未用待测碱液润洗
B.酸式滴定管未用标准盐酸润洗
C.滴定过程中滴定管内不慎有标准液溅出
D.滴定前俯视读数,滴定后读数正确
A
酸碱中和滴定误差分析
误差分析
以标准液滴定待测液为例:
分析依据
c待测·V待测=c标准·V标准
c待测=
c标准、V待测均为定值,误差均体现在V标准的大小上。
1.
结论:c(待)与V(标)成正比; V(标)偏大,结果__________;V(标)偏小,结果___________;
2.
偏大
偏小
误差产生的原因
洗涤误差
1
操作 V标准 c待测
滴定管未用标准溶液润洗
滴定管(移液管)未用待测溶液润洗
锥形瓶用待测溶液润洗
锥形瓶洗净后还留有蒸馏水
误差产生的原因
洗涤误差
1
操作 V标准 c待测
滴定管未用标准溶液润洗 变大 偏高
滴定管(移液管)未用待测溶液润洗 变小 偏低
锥形瓶用待测溶液润洗 变大 偏高
锥形瓶洗净后还留有蒸馏水 不变 无影响
误差产生的原因
气泡误差
2
操作 V标准 c待测
放出待测液的滴定管开始有气泡,放出液体后气泡消失
盛有标准液的滴定管滴定前有气泡,滴定终点时气泡消失
盛有标准液的滴定管滴定前没有气泡,滴定终点时有气泡
误差产生的原因
气泡误差
2
操作 V标准 c待测
放出待测液的滴定管开始有气泡,放出液体后气泡消失 变小 偏低
盛有标准液的滴定管滴定前有气泡,滴定终点时气泡消失 变大 偏高
盛有标准液的滴定管滴定前没有气泡,滴定终点时有气泡 变小 偏低
误差产生的原因
操作误差
3
操作 V标准 c待测
移液管尖端残液吹入锥形瓶
振荡锥形瓶时部分液体溅出
部分标准液滴出锥形瓶外
向锥形瓶中加蒸馏水冲洗内壁的标准液
误差产生的原因
操作误差
3
操作 V标准 c待测
移液管尖端残液吹入锥形瓶 变大 偏高
振荡锥形瓶时部分液体溅出 变小 偏低
部分标准液滴出锥形瓶外 变大 偏高
向锥形瓶中加蒸馏水冲洗内壁的标准液 无影响 无影响
误差产生的原因
终点误差
4
操作 V标准 c待测
强酸滴定弱碱时,甲基橙由黄色变为红色时停止滴定
强碱滴定弱酸时,酚酞由无色变为粉红时立即停止滴定
滴定终点时滴定管尖嘴处半滴尚未滴下,或一滴标准液附着在锥形瓶内壁上未流下
溶液颜色较浅时滴入酸液过快,停止滴定后再加一滴NaOH溶液无变化
误差产生的原因
终点误差
4
操作 V标准 c待测
强酸滴定弱碱时,甲基橙由黄色变为红色时停止滴定 变大 偏高
强碱滴定弱酸时,酚酞由无色变为粉红时立即停止滴定 变小 偏低
滴定终点时滴定管尖嘴处半滴尚未滴下,或一滴标准液附着在锥形瓶内壁上未流下 变大 偏高
溶液颜色较浅时滴入酸液过快,停止滴定后再加一滴NaOH溶液无变化 变大 偏高
误差产生的原因
读数误差
5
操作 V标准 c待测
滴定前平视,滴定后俯视
滴定前仰视,滴定后平视
滴定前仰视,滴定后俯视
滴定前平视,滴定后仰视
滴定前俯视,滴定后平视
滴定前俯视,滴定后仰视
误差产生的原因
读数误差
5
V实
V实
读出值
读出值
滴定前
滴定后
滴定前
滴定后
误差产生的原因
读数误差
5
操作 V标准 c待测
滴定前平视,滴定后俯视 变小 偏低
滴定前仰视,滴定后平视 变小 偏低
滴定前仰视,滴定后俯视 变小 偏低
滴定前平视,滴定后仰视 变大 偏高
滴定前俯视,滴定后平视 变大 偏高
滴定前俯视,滴定后仰视 变大 偏高
误差产生的原因
读数误差
5
量筒——量取一定体积的溶液
俯视:实际量取的液体体积偏小
仰视:实际量取的液体体积偏大
容量瓶——用容量瓶定容
俯视:溶液体积偏小,所配制溶液的浓度偏高
仰视:溶液体积偏大,所配制溶液的浓度偏低
误差产生的原因
杂质误差
6
配置NaOH标准溶液时有杂质
NaOH固体潮解
用NaOH配制的因存放不当而变质的标液来测定盐酸的浓度
V(标)↑
c(待)↑
NaOH中掺有杂质
不与酸反应的杂质(如NaCl)
混有中和1 mol H+所需质量大于40g的杂质(如Na2CO3、K2CO3)
混有中和1 mol H+所需质量小于40g的杂质(如Na2O)
V(标)↑
c(待)↑
V(标)↑
c(待)↑
V(标) ↓
c(待) ↓
无影响
误差产生的原因
指示剂误差
7
用强酸滴定弱碱,指示剂选用酚酞。
用强碱滴定弱酸,指示剂选用甲基橙。
误差产生的原因
指示剂误差
7
用强酸滴定弱碱,指示剂选用酚酞。由于酚酞的变色范围在8.2∽10之间,造成消耗强酸标准液体积偏小,待测液浓度偏低。
用强碱滴定弱酸,指示剂选用甲基橙。由于甲基橙的变色范围在3.1∽4.4之间,造成消耗强碱标准液体积偏小,待测液浓度偏低。
误差产生的原因
练习
某同学欲用已知物质的量浓度为0.1000 mol·L-1的盐酸测定未知物质的量浓度的氢氧化钠溶液时,选择酚酞作指示剂。请填写下列空白:
(1)用标准的盐酸滴定待测的氢氧化钠溶液时,左手把握酸式滴定管的活塞,右手摇动锥形瓶,眼睛注视 。直到因加入半滴盐酸,溶液的颜色由 色变为 色,半分钟不恢复原色,立即停止滴定。
锥形瓶内溶液颜色的变化
粉红
无
误差产生的原因
练习
(2)下列操作中可能使所测氢氧化钠溶液的浓度数值偏低的是 (填字母)。
A.酸式滴定管未用标准盐酸润洗就直接注入标准盐酸
B.滴定前盛放氢氧化钠溶液的锥形瓶用蒸馏水洗净后没有干燥
C.酸式滴定管在滴定前有气泡,滴定后气泡消失
D.读取盐酸体积时,开始仰视读数,滴定结束时俯视读数
E.滴定过程中,锥形瓶的振荡过于激烈,使少量溶液溅出
DE
误差产生的原因
练习
用已知浓度的NaOH溶液测定某H2SO4溶液的浓度,参考右图,从表中选出正确选项( )
D
误差产生的原因
练习
下列实验操作不会引起误差的是( )
A.酸碱中和滴定时,用待测液润洗锥形瓶
B.酸碱中和滴定时,用冲洗干净的滴定管盛装标准溶液
C.用NaOH标准溶液测定未知浓度的盐酸溶液时,在滴定过程中向锥形瓶加入 5 mL的蒸馏水
D.用标准盐酸测定未知浓度NaOH溶液,实验结束时,酸式滴定管尖嘴部分有气泡,开始实验时无气泡
C
误差产生的原因
练习
用已知浓度的盐酸测定未知浓度NaOH溶液的物质的量浓度,待测液放在锥形瓶中。中和滴定时下列操作会使测定结果偏低的是(锥形瓶中溶液用滴定管量取)( )
A.碱式滴定管未用待测碱液润洗
B.酸式滴定管未用标准盐酸润洗
C.滴定过程中滴定管内不慎有标准液溅出
D.滴定前俯视读数,滴定后读数正确
A
