第二单元溶液单元测试题--2022-2023学年九年级化学人教版(五四学制)全一册(有答案)
文档属性
| 名称 | 第二单元溶液单元测试题--2022-2023学年九年级化学人教版(五四学制)全一册(有答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 187.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-10-04 00:00:00 | ||
图片预览


文档简介
第二单元溶液单元测试题--2022-2023学年九年级化学人教版(五四学制)全一册
一、单选题
1.把下列生活中常见的物质分别放入水中,充分搅拌,可以得到溶液的是
A.面粉 B.酒精 C.花生油 D.泥土
2.下列关于溶液的说法正确的是
A.溶液一定是混合物
B.饱和溶液的浓度比不饱和溶液的浓度一定大
C.医用碘酒是碘的水溶液
D.添加溶质是不饱和溶液变成饱和溶液的唯一方法
3.下列有关水的说法正确的是
A.利用肥皂水可以鉴别硬水和软水
B.将植物油加入水中可形成溶液
C.自来水经过沉淀、过滤、吸附、消毒后得到的水为纯净物
D.水是一种很好的溶剂,它可以溶解任何化学物质
4.某同学需要配制50g质量分数为15%的氯化钠溶液,步骤如下图所示,下列分析正确的是
A.配制过程中出现了两处操作错误
B.实验操作步骤为:计算、称量、量取、蒸发
C.若所有操作都正确,完全溶解后有液滴溅出,会导致溶质的质量分数偏小
D.配制时应称量氯化钠固体质量为70g
5.配制50g质量分数为6%的氯化钠溶液,不需要用到的仪器是( )
A.烧杯 B.量筒 C.铁架台 D.玻璃棒
6.能使气体物质溶解度增大的操作是
A.增加溶剂 B.振荡溶液 C.增大压强 D.升高温度
7.下列有关溶液的叙述正确的是
A.植物油与水混合一定形成溶液 B.食盐水倒出一半后浓度降低
C.升温会降低二氧化碳在水中的溶解度 D.蔗糖可以无限溶解在一定量的水中
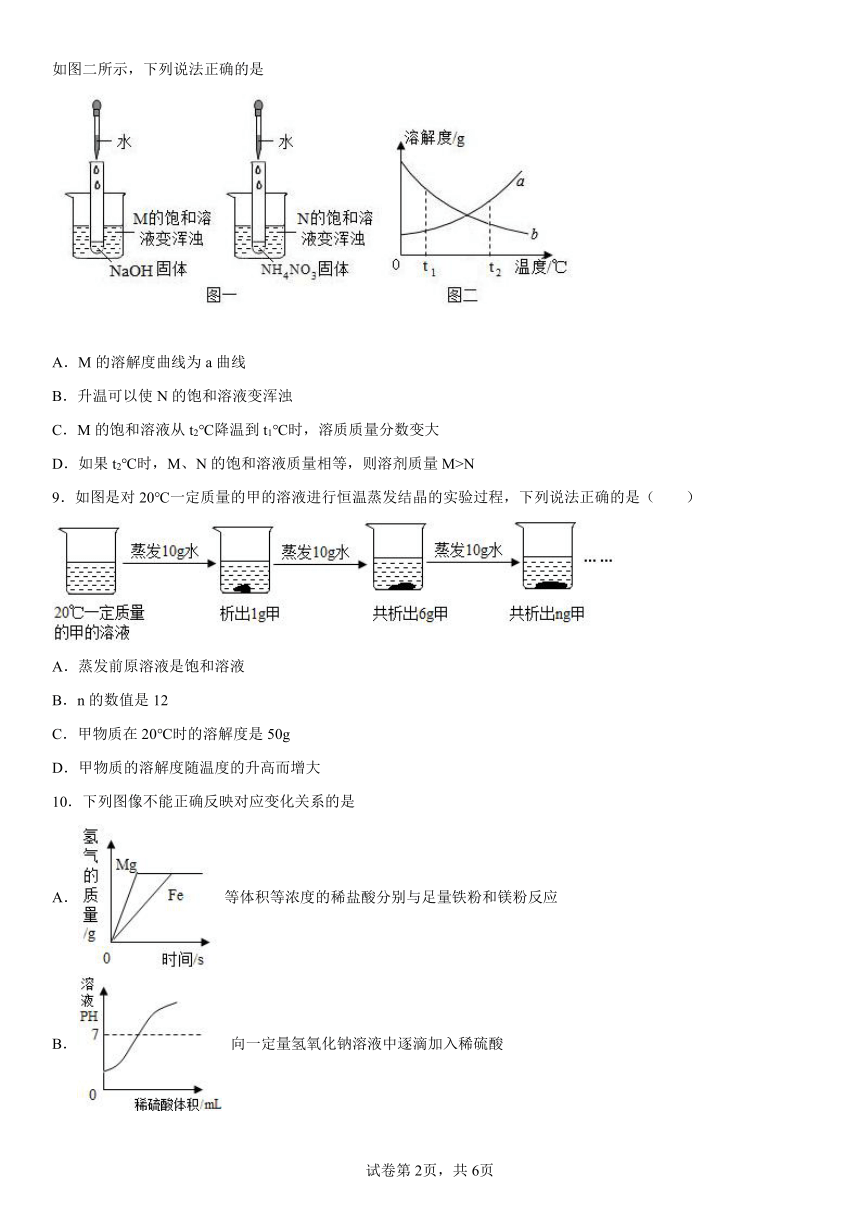
8.某同学在探究物质溶解的热现象及温度对物质溶解度影响时,设计了如下实验,现象如图一所示,溶解度曲线如图二所示,下列说法正确的是
A.M的溶解度曲线为a曲线
B.升温可以使N的饱和溶液变浑浊
C.M的饱和溶液从t2℃降温到t1℃时,溶质质量分数变大
D.如果t2℃时,M、N的饱和溶液质量相等,则溶剂质量M>N
9.如图是对20℃一定质量的甲的溶液进行恒温蒸发结晶的实验过程,下列说法正确的是( )
A.蒸发前原溶液是饱和溶液
B.n的数值是12
C.甲物质在20℃时的溶解度是50g
D.甲物质的溶解度随温度的升高而增大
10.下列图像不能正确反映对应变化关系的是
A. 等体积等浓度的稀盐酸分别与足量铁粉和镁粉反应
B. 向一定量氢氧化钠溶液中逐滴加入稀硫酸
C. 向一定量硫酸铜溶液中加入过量铁粉
D. 加热一定量高锰酸钾固体制氧气
11.20℃时KCl的溶解度是34g/100g水,按如图所示进行操作(整个过程中无溶剂损失)。以下说法正确的是
A.甲和丙都是KCl的饱和溶液
B.丁中溶液的溶质质量分数为34%
C.溶液中溶质质量大小的关系是:甲>丙=丁
D.若乙溶液恰好饱和,则40℃时KCl的溶解度为40g/100g水
12.某学生要配制一定溶质质量分数的NaOH溶液,实验操作如图所示,其中正确的是
A.取用NaOH固体
B.称量NaOH固体
C.量取一定体积的水
D.溶解NaOH固体
二、填空题
13.小岗分别试用以下方法清洗餐具:
a.只用冷水 b.只用热水 c.在冷水中加入几滴洗涤剂 d.在热水中加入几滴洗涤剂
(1)上述方法中清洗餐具最干净的是______(填序号)。
(2)以上对比实验说明温度越_______(填“高”或“低”)洗涤效果越好。
(3)用下列选项填空:
A.反应 B.溶解 C.乳化 D.过滤
①洗涤剂对油污有_______作用。
②小岗认为汽油也能去除油污,但去污的原理与洗涤剂的不同。汽油可以________油污。
14.2020年中国水周的主题是“坚持节水优先,建设幸福河湖”。
(1)向某自来水样品中加入一定量的肥皂水,振荡,观察到泡沫较少,浮渣较多,说明该自来水属于_____________(填“硬水”或“软水”)。
(2)生活中常用____________的方法降低水的硬度。
(3)用洗剂清洗餐具上的油污,利用了洗涤剂对油污的_____________作用。
(4)珍惜水资源是每个公民应尽的责任和义务。下列做法有利于保护水资源的是__________(填字母序号)。
A实验室的废液经处理达标后排放
B洗净试管后,忘记关闭水龙头
C在实验室中安装节水的水龙头
15.如图是A、B两种固体物质的溶解度曲线,读图回答以下问题:
(1)若A物质中混合少量B物质,提纯A可用的方法是___________。
(2)将t2℃时A和B的饱和溶液同时降温至t1℃,则A和B的溶质质量分数为A__________B(< ,=,或>);
(3) t2℃时,向50gA物质的饱和溶液中加入60g水,所得溶液中溶质的质量分数为___________ (精确到小数点后一位 )。
16.水与人类的生活和生产密切相关,请回答下列问题:
①图1是水通电分解的示意图,该反应的现象为___________________,b管中产生的气体是___________。
②家用净水器中通常加入活性炭,其作用是______________________。
③图2是甲、乙、丙三种固体物质的溶解度曲线。请根据图回答下列问题:
Ⅰ.t3℃时,甲、乙、丙三种物质溶解度大小关系是_________________。
Ⅱ.若甲中混有少量的乙,提纯甲物质可采取的方法是____________________。
Ⅲ.在t2℃时,配制90g甲物质的饱和溶液,需要甲物质的质量是________g。
Ⅳ.t3℃时,将甲、乙、丙三种物质的饱和溶液分别降温到t1℃,下列叙述正确的是_______(填字母序号)。
A.溶质质量分数的大小关系是:乙>甲>丙
B.溶剂质量的大小关系是:丙>乙>甲
C.溶液质量的大小关系是:丙>乙>甲
D.析出固体质量的大小关系是:甲>乙>丙
三、实验题
17.食盐是生活中必备的调味品,人们食用的通常都是食盐溶液。通过学习和生活体验,我们发现多种因素都能影响食盐在水中的溶解速率。
(1)写出两个你认为可能影响食盐在水中溶解速率的因素,并预测其食盐溶解速率的影响。
因素①:________,你的预测是_________________________________________________;
因素②:________,你的预测是_________________________________________________。
(2)从你所列因素中选出一个,通过实验验证你的预测,你设计的实验方案是____________________。
(3)要使验证实验达到预测的效果,必须控制________。
18.配制并稀释一定质量分数的溶液。
(1)配制50g质量分数为6%的溶液:①计算:需要3.0g,水4.0g;②称量:用托盘天平称量3.0g的。天平调零后,分别在天平左右托盘放上质量相同的纸片,先__________________,然后___________,至托盘天平恰好平衡;③量取:用量筒量取47.0mL水。请在图(1)中画出47.0mL水的液面位置______________;④溶解:若采用图(2)所示操作可能产生的后果是______________。
(2)稀释溶液:(由于整个配制过程中溶液很稀,其密度可近似看作1g/mL)①取1mL6%的溶液加水稀释至100mL,得到溶液a;②若用3.0g配制与溶液a浓度相同的溶液,其体积是________ mL。
四、计算题
19.用400g溶质质量分数为20%的氢氧化钠溶液,配制成溶质质量分数为10%的氢氧化钠溶液,需要加入水的质量为多少克?
20.为了测定某银、锌合金(假设合金中只含银和锌)中银的质量分数,某同学称取20g银锌合金粉末进行实验,现将125g稀硫酸分五次加入合金粉末中,充分反应后测得生成气体的总质量如表所示:
第1次 第2次 第3次 第4次 第5次
滴入稀硫酸的质量/g 25 25 25 25 25
生成气体的总质量/g 0.05 m 0.15 0.20 0.20
请完成下列问题:
(1)表中m的值为 ;
(2)银、锌合金中银的质量分数为 ;
(3)所用稀硫酸的溶质质量分数是多少?(写出具体计算过程)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.A
3.A
4.A
5.C
6.C
7.C
8.D
9.C
10.B
11.D
12.D
13.(1)d
(2)高
(3) 乳化##C 溶解##B
14. (1) 硬水 煮沸 (2) 乳化 AC
15. (1) 冷却热饱和溶液(或降温结晶) (2) > 10.5%
16.(1) 氢气/H2 吸附 (2) 甲>乙>丙或丙<乙<甲 (3) 降温结晶 40 A
17. (1) 温度 温度越高,食盐溶解速率越快 (2) 搅拌 搅拌加快溶解速率 (3) 取等质量的食盐,分别加入等体积的20℃和100℃的水,观察溶解速率 其他条件相同
18. (1) 在右盘添加3g砝码 向左盘中添加药品 (2) 蒸馏水溅出,使配制结果偏高 (3) 5000
19.400g
解:需要加入水的质量为x。400g×20%=(400g+x)×10%,x=400g答:需要加入水的质量为400g。
20.(1)0.10(2)67.5%(3)9.8%
答案第1页,共2页
答案第1页,共2页
一、单选题
1.把下列生活中常见的物质分别放入水中,充分搅拌,可以得到溶液的是
A.面粉 B.酒精 C.花生油 D.泥土
2.下列关于溶液的说法正确的是
A.溶液一定是混合物
B.饱和溶液的浓度比不饱和溶液的浓度一定大
C.医用碘酒是碘的水溶液
D.添加溶质是不饱和溶液变成饱和溶液的唯一方法
3.下列有关水的说法正确的是
A.利用肥皂水可以鉴别硬水和软水
B.将植物油加入水中可形成溶液
C.自来水经过沉淀、过滤、吸附、消毒后得到的水为纯净物
D.水是一种很好的溶剂,它可以溶解任何化学物质
4.某同学需要配制50g质量分数为15%的氯化钠溶液,步骤如下图所示,下列分析正确的是
A.配制过程中出现了两处操作错误
B.实验操作步骤为:计算、称量、量取、蒸发
C.若所有操作都正确,完全溶解后有液滴溅出,会导致溶质的质量分数偏小
D.配制时应称量氯化钠固体质量为70g
5.配制50g质量分数为6%的氯化钠溶液,不需要用到的仪器是( )
A.烧杯 B.量筒 C.铁架台 D.玻璃棒
6.能使气体物质溶解度增大的操作是
A.增加溶剂 B.振荡溶液 C.增大压强 D.升高温度
7.下列有关溶液的叙述正确的是
A.植物油与水混合一定形成溶液 B.食盐水倒出一半后浓度降低
C.升温会降低二氧化碳在水中的溶解度 D.蔗糖可以无限溶解在一定量的水中
8.某同学在探究物质溶解的热现象及温度对物质溶解度影响时,设计了如下实验,现象如图一所示,溶解度曲线如图二所示,下列说法正确的是
A.M的溶解度曲线为a曲线
B.升温可以使N的饱和溶液变浑浊
C.M的饱和溶液从t2℃降温到t1℃时,溶质质量分数变大
D.如果t2℃时,M、N的饱和溶液质量相等,则溶剂质量M>N
9.如图是对20℃一定质量的甲的溶液进行恒温蒸发结晶的实验过程,下列说法正确的是( )
A.蒸发前原溶液是饱和溶液
B.n的数值是12
C.甲物质在20℃时的溶解度是50g
D.甲物质的溶解度随温度的升高而增大
10.下列图像不能正确反映对应变化关系的是
A. 等体积等浓度的稀盐酸分别与足量铁粉和镁粉反应
B. 向一定量氢氧化钠溶液中逐滴加入稀硫酸
C. 向一定量硫酸铜溶液中加入过量铁粉
D. 加热一定量高锰酸钾固体制氧气
11.20℃时KCl的溶解度是34g/100g水,按如图所示进行操作(整个过程中无溶剂损失)。以下说法正确的是
A.甲和丙都是KCl的饱和溶液
B.丁中溶液的溶质质量分数为34%
C.溶液中溶质质量大小的关系是:甲>丙=丁
D.若乙溶液恰好饱和,则40℃时KCl的溶解度为40g/100g水
12.某学生要配制一定溶质质量分数的NaOH溶液,实验操作如图所示,其中正确的是
A.取用NaOH固体
B.称量NaOH固体
C.量取一定体积的水
D.溶解NaOH固体
二、填空题
13.小岗分别试用以下方法清洗餐具:
a.只用冷水 b.只用热水 c.在冷水中加入几滴洗涤剂 d.在热水中加入几滴洗涤剂
(1)上述方法中清洗餐具最干净的是______(填序号)。
(2)以上对比实验说明温度越_______(填“高”或“低”)洗涤效果越好。
(3)用下列选项填空:
A.反应 B.溶解 C.乳化 D.过滤
①洗涤剂对油污有_______作用。
②小岗认为汽油也能去除油污,但去污的原理与洗涤剂的不同。汽油可以________油污。
14.2020年中国水周的主题是“坚持节水优先,建设幸福河湖”。
(1)向某自来水样品中加入一定量的肥皂水,振荡,观察到泡沫较少,浮渣较多,说明该自来水属于_____________(填“硬水”或“软水”)。
(2)生活中常用____________的方法降低水的硬度。
(3)用洗剂清洗餐具上的油污,利用了洗涤剂对油污的_____________作用。
(4)珍惜水资源是每个公民应尽的责任和义务。下列做法有利于保护水资源的是__________(填字母序号)。
A实验室的废液经处理达标后排放
B洗净试管后,忘记关闭水龙头
C在实验室中安装节水的水龙头
15.如图是A、B两种固体物质的溶解度曲线,读图回答以下问题:
(1)若A物质中混合少量B物质,提纯A可用的方法是___________。
(2)将t2℃时A和B的饱和溶液同时降温至t1℃,则A和B的溶质质量分数为A__________B(< ,=,或>);
(3) t2℃时,向50gA物质的饱和溶液中加入60g水,所得溶液中溶质的质量分数为___________ (精确到小数点后一位 )。
16.水与人类的生活和生产密切相关,请回答下列问题:
①图1是水通电分解的示意图,该反应的现象为___________________,b管中产生的气体是___________。
②家用净水器中通常加入活性炭,其作用是______________________。
③图2是甲、乙、丙三种固体物质的溶解度曲线。请根据图回答下列问题:
Ⅰ.t3℃时,甲、乙、丙三种物质溶解度大小关系是_________________。
Ⅱ.若甲中混有少量的乙,提纯甲物质可采取的方法是____________________。
Ⅲ.在t2℃时,配制90g甲物质的饱和溶液,需要甲物质的质量是________g。
Ⅳ.t3℃时,将甲、乙、丙三种物质的饱和溶液分别降温到t1℃,下列叙述正确的是_______(填字母序号)。
A.溶质质量分数的大小关系是:乙>甲>丙
B.溶剂质量的大小关系是:丙>乙>甲
C.溶液质量的大小关系是:丙>乙>甲
D.析出固体质量的大小关系是:甲>乙>丙
三、实验题
17.食盐是生活中必备的调味品,人们食用的通常都是食盐溶液。通过学习和生活体验,我们发现多种因素都能影响食盐在水中的溶解速率。
(1)写出两个你认为可能影响食盐在水中溶解速率的因素,并预测其食盐溶解速率的影响。
因素①:________,你的预测是_________________________________________________;
因素②:________,你的预测是_________________________________________________。
(2)从你所列因素中选出一个,通过实验验证你的预测,你设计的实验方案是____________________。
(3)要使验证实验达到预测的效果,必须控制________。
18.配制并稀释一定质量分数的溶液。
(1)配制50g质量分数为6%的溶液:①计算:需要3.0g,水4.0g;②称量:用托盘天平称量3.0g的。天平调零后,分别在天平左右托盘放上质量相同的纸片,先__________________,然后___________,至托盘天平恰好平衡;③量取:用量筒量取47.0mL水。请在图(1)中画出47.0mL水的液面位置______________;④溶解:若采用图(2)所示操作可能产生的后果是______________。
(2)稀释溶液:(由于整个配制过程中溶液很稀,其密度可近似看作1g/mL)①取1mL6%的溶液加水稀释至100mL,得到溶液a;②若用3.0g配制与溶液a浓度相同的溶液,其体积是________ mL。
四、计算题
19.用400g溶质质量分数为20%的氢氧化钠溶液,配制成溶质质量分数为10%的氢氧化钠溶液,需要加入水的质量为多少克?
20.为了测定某银、锌合金(假设合金中只含银和锌)中银的质量分数,某同学称取20g银锌合金粉末进行实验,现将125g稀硫酸分五次加入合金粉末中,充分反应后测得生成气体的总质量如表所示:
第1次 第2次 第3次 第4次 第5次
滴入稀硫酸的质量/g 25 25 25 25 25
生成气体的总质量/g 0.05 m 0.15 0.20 0.20
请完成下列问题:
(1)表中m的值为 ;
(2)银、锌合金中银的质量分数为 ;
(3)所用稀硫酸的溶质质量分数是多少?(写出具体计算过程)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.A
3.A
4.A
5.C
6.C
7.C
8.D
9.C
10.B
11.D
12.D
13.(1)d
(2)高
(3) 乳化##C 溶解##B
14. (1) 硬水 煮沸 (2) 乳化 AC
15. (1) 冷却热饱和溶液(或降温结晶) (2) > 10.5%
16.(1) 氢气/H2 吸附 (2) 甲>乙>丙或丙<乙<甲 (3) 降温结晶 40 A
17. (1) 温度 温度越高,食盐溶解速率越快 (2) 搅拌 搅拌加快溶解速率 (3) 取等质量的食盐,分别加入等体积的20℃和100℃的水,观察溶解速率 其他条件相同
18. (1) 在右盘添加3g砝码 向左盘中添加药品 (2) 蒸馏水溅出,使配制结果偏高 (3) 5000
19.400g
解:需要加入水的质量为x。400g×20%=(400g+x)×10%,x=400g答:需要加入水的质量为400g。
20.(1)0.10(2)67.5%(3)9.8%
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第一单元 金属和金属材料
- 课题1 金属材料
- 课题2 金属的化学性质
- 课题3 金属资源的利用和保护
- 实验活动1 金属的物理性质和某些化学性质
- 第二单元 溶液
- 课题1 溶液的形成
- 课题2 溶解度
- 课题3 溶液的浓度
- 实验活动2 一定溶质质量分数的氯化钠溶液的配制
- 第三单元 酸和碱
- 课题1 常见的酸和碱
- 课题2 酸和碱的中和反应
- 实验活动3 酸、碱的化学性质
- 实验活动4 溶液酸碱性的检验
- 第四单元 盐 化肥
- 课题1 生活中常见的盐
- 课题2 化学肥料
- 实验活动5 粗盐中难溶性杂志的去除
- 第五单元 化学与生活
- 课题1 人类重要的营养物质
- 课题2 化学元素与人体健康
- 课题3 有机合成材料
- 旧版目录
- 课题3 溶质的质量分数
- 课题2 酸和碱之间会发生什么反应
