第二单元常见的酸和碱单元测试题--2022-2023学年九年级化学鲁教版(五四学制)全一册(有答案)
文档属性
| 名称 | 第二单元常见的酸和碱单元测试题--2022-2023学年九年级化学鲁教版(五四学制)全一册(有答案) |
|
|
| 格式 | zip | ||
| 文件大小 | 93.8KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-10-07 00:00:00 | ||
图片预览


文档简介
第二单元常见的酸和碱单元测试题--2022-2023学年九年级化学鲁教版(五四学制)全一册
一、单选题
1.不同的物质溶于水后会形成酸碱性不同的溶液,下列溶液显酸性的是
A.食醋 B.氨水 C.NaCl溶液 D.Na2CO3溶液
2.正常情况下pH小于7的液体是
A.人体胃液 B.人体血液 C.纯碱溶液 D.生理盐水
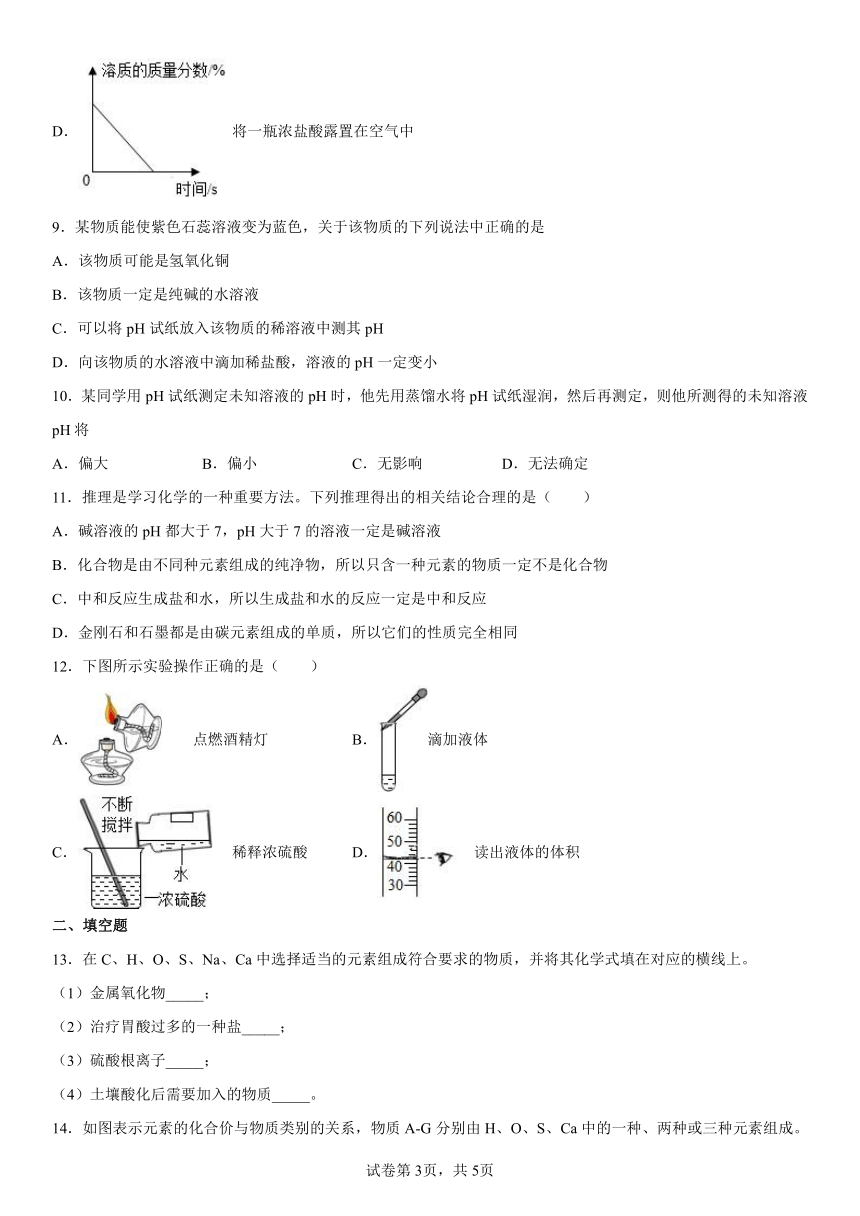
3.为探究二氧化碳能否和水反应,用四朵石蕊溶液染成紫色的干燥小花完成下图四个实验。实验I、Ⅳ中小花变红,实验Ⅱ、Ⅲ中小花不变色。下列说法不正确的是( )
A.实验Ⅰ、Ⅱ说明醋酸可以使小花变红
B.实验Ⅲ说明二氧化碳不能使小花变红
C.实验Ⅱ、Ⅲ、Ⅳ说明二氧化碳能与水发生化学反应
D.上述实验说明二氧化碳和醋酸具有相似的化学性质
4.下列各组物质能大量共存于水溶液中的是
A.CuSO4与NaOH B.Na2CO3与H2SO4
C.KOH与HNO3 D.Mg(NO3)2与CaCl2
5.下列稀溶液,仅用酚酞及同组物质之间反应就能鉴别出来的一组是
A.NaOH H2SO4 HNO3 B.KOH HCI Ba (OH)2
C.NaOH NaCl Na2CO3 D.NaOH NaCl HNO3
6.用如图所示装置探究CO2能否与H2O反应。滴加盐酸,待试管乙中液体变红后,将其加热至沸腾,红色不褪去。下列说法正确的是
A.甲中逸出的气体只含CO2
B.乙中液体变红,证明CO2能与水反应
C.加热后红色不褪去,说明碳酸受热不分解
D.欲达到实验目的,可将盐酸改为稀硫酸
7.下列有关溶液酸碱性的说法错误的是( )
A.pH=7的溶液呈中性
B.pH>7的溶液一定呈碱性
C.pH<7的雨水一定是酸雨
D.酸溶液的pH越小酸性越强
8.下列图像有关量的变化趋势能正确反映其对应操作的是
A.一定质量的饱和石灰水中加入生石灰
B.等质量CaCO3分别与等体积等质量分数的稀盐酸(足量)反应
C.用等体积,等浓度的双氧水制取氧气
D.将一瓶浓盐酸露置在空气中
9.某物质能使紫色石蕊溶液变为蓝色,关于该物质的下列说法中正确的是
A.该物质可能是氢氧化铜
B.该物质一定是纯碱的水溶液
C.可以将pH试纸放入该物质的稀溶液中测其pH
D.向该物质的水溶液中滴加稀盐酸,溶液的pH一定变小
10.某同学用pH试纸测定未知溶液的pH时,他先用蒸馏水将pH试纸湿润,然后再测定,则他所测得的未知溶液pH将
A.偏大 B.偏小 C.无影响 D.无法确定
11.推理是学习化学的一种重要方法。下列推理得出的相关结论合理的是( )
A.碱溶液的pH都大于7,pH大于7的溶液一定是碱溶液
B.化合物是由不同种元素组成的纯净物,所以只含一种元素的物质一定不是化合物
C.中和反应生成盐和水,所以生成盐和水的反应一定是中和反应
D.金刚石和石墨都是由碳元素组成的单质,所以它们的性质完全相同
12.下图所示实验操作正确的是( )
A. 点燃酒精灯 B.滴加液体
C. 稀释浓硫酸 D. 读出液体的体积
二、填空题
13.在C、H、O、S、Na、Ca中选择适当的元素组成符合要求的物质,并将其化学式填在对应的横线上。
(1)金属氧化物_____;
(2)治疗胃酸过多的一种盐_____;
(3)硫酸根离子_____;
(4)土壤酸化后需要加入的物质_____。
14.如图表示元素的化合价与物质类别的关系,物质A-G分别由H、O、S、Ca中的一种、两种或三种元素组成。各物质均有某种组成元素的化合价与横坐标的数值对应,“→”表示物质之间的转化方向。请回答:
(1)E的化学式为___________,F的化学式为___________。
(2)A→B反应的现象为___________。
(3)C→D反应的现象为___________。
15.调味剂的主要作用是补充、增强或增加食品的味道。食醋是一种能增强食品酸味的调味剂,主要成分为醋酸(CH3COOH),与我们的生活密切相连。根据所学知识回答:
(1)食醋能作酸味的调味剂,是因为醋酸在水溶液中能解离出CH3COO-和_____(填离子符号)。
(2)食醋的酸味能促进人胃酸的分泌,胃酸的成分是_____(填化学式)。
(3)食醋能软化鱼骨和鸡蛋壳,原因是醋酸能与_____(填化学式)反应。
(4)生活中常用酒来制取食醋,原理是酒中的酒精CH3CH2OH在酶的作用下与空气中O2反应得到醋酸和水,请你尝试写出该反应的现象_____。
(5)用铁锅炒菜时,放一点食醋能补铁的原因是_____。
16.实验室有 4 种试剂,分别为 HNO3 溶液、CuSO4 溶液、MgCl2 溶液和 KOH 溶液。
(1)有颜色的试剂是______。
(2)有一种试剂能与另外三种试剂发生反应,该试剂是______。
(3)书写现象:
①CuSO4 溶液与 KOH 溶液混合:____________________________________。
②HNO3 溶液与 NaHCO3 溶液混合:__________________________________。
三、实验题
17.用如图装置进行实验,挤出浓盐酸。(信息:盐酸可以使紫色石蕊试液变红)
(1)实验现象是_______________。
(2)该实验说明分子具有的性质是_______________。
18.小明为探究酸、碱、盐的化学性质,做了如图实验:
(1)实验后液体颜色变红的试管是_______;
(2)反应后试管C的溶液中一定有的阳离子是_______;
(3)小明把D、E反应后的液体倒入一个洁净的烧杯中,观察到只有白色沉淀生成,过滤后得到白色沉淀和无色滤液,小明分别对试管D、E反应时的反应物用量有如下描述,正确的是_______。
A 试管D:氢氧化钙溶液一定过量
B 试管D:稀盐酸可能不足
C 试管E:碳酸钠一定过量
D 试管E:稀盐酸一定过量
四、计算题
19.小青同学为了制作叶脉书签,打算配制125g10%的NaOH溶液。
(1)计算小青需要称取NaOH的质量。
(2)小青将洗净的树叶放在配制好的溶液中煮沸后取出,溶液的质量减少了5g,溶质质量分数也有所减小。为了测定剩下溶液中NaOH的质量分数,小青向溶液中逐渐加入7.3%的稀盐酸,当溶液PH=7时,消耗盐酸50g。计算:
①生成NaCl的质量。
②剩下溶液中NaOH的质量分数。
20.为测定某盐酸的质量分数,往20 g 40%的氢氧化钠溶液中逐滴加入该盐酸,加入盐酸的质量与烧杯中溶液pH的变化关系如图所示。
(1)所用氢氧化钠溶液中溶质的质量为_________。
(2)当滴加盐酸到图像中D点时,烧杯中溶液的溶质是_________ (填化学式)。
(3)该盐酸中溶质质量分数是多少_________?
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
2.A
3.D
4.D
5.D
6.D
7.C
8.B
9.D
10.D
11.B
12.D
13. (1) CaO NaHCO3 (2) SO42﹣ Ca(OH)2
14. (1) CaSO4 (2)Ca(OH)2
15.(1) H+ HCl CaCO3 (2) 铁锅与食醋反应产生Fe2+
16. (1) CuSO4 溶液 (2) KOH 溶液
17. (1) 湿润的紫色石蕊小花变红 (2) 分子在不断运动。
18.(1) A Fe3+ (2) BC
19.小青需要称取NaOH的质量为12.5g, 生成NaCl的质量是5.85g,剩下溶液中NaOH的质量分数是3.3%
20.(1)8g(2)NaCl、HCl(3)29.2%
答案第1页,共2页
答案第1页,共2页
一、单选题
1.不同的物质溶于水后会形成酸碱性不同的溶液,下列溶液显酸性的是
A.食醋 B.氨水 C.NaCl溶液 D.Na2CO3溶液
2.正常情况下pH小于7的液体是
A.人体胃液 B.人体血液 C.纯碱溶液 D.生理盐水
3.为探究二氧化碳能否和水反应,用四朵石蕊溶液染成紫色的干燥小花完成下图四个实验。实验I、Ⅳ中小花变红,实验Ⅱ、Ⅲ中小花不变色。下列说法不正确的是( )
A.实验Ⅰ、Ⅱ说明醋酸可以使小花变红
B.实验Ⅲ说明二氧化碳不能使小花变红
C.实验Ⅱ、Ⅲ、Ⅳ说明二氧化碳能与水发生化学反应
D.上述实验说明二氧化碳和醋酸具有相似的化学性质
4.下列各组物质能大量共存于水溶液中的是
A.CuSO4与NaOH B.Na2CO3与H2SO4
C.KOH与HNO3 D.Mg(NO3)2与CaCl2
5.下列稀溶液,仅用酚酞及同组物质之间反应就能鉴别出来的一组是
A.NaOH H2SO4 HNO3 B.KOH HCI Ba (OH)2
C.NaOH NaCl Na2CO3 D.NaOH NaCl HNO3
6.用如图所示装置探究CO2能否与H2O反应。滴加盐酸,待试管乙中液体变红后,将其加热至沸腾,红色不褪去。下列说法正确的是
A.甲中逸出的气体只含CO2
B.乙中液体变红,证明CO2能与水反应
C.加热后红色不褪去,说明碳酸受热不分解
D.欲达到实验目的,可将盐酸改为稀硫酸
7.下列有关溶液酸碱性的说法错误的是( )
A.pH=7的溶液呈中性
B.pH>7的溶液一定呈碱性
C.pH<7的雨水一定是酸雨
D.酸溶液的pH越小酸性越强
8.下列图像有关量的变化趋势能正确反映其对应操作的是
A.一定质量的饱和石灰水中加入生石灰
B.等质量CaCO3分别与等体积等质量分数的稀盐酸(足量)反应
C.用等体积,等浓度的双氧水制取氧气
D.将一瓶浓盐酸露置在空气中
9.某物质能使紫色石蕊溶液变为蓝色,关于该物质的下列说法中正确的是
A.该物质可能是氢氧化铜
B.该物质一定是纯碱的水溶液
C.可以将pH试纸放入该物质的稀溶液中测其pH
D.向该物质的水溶液中滴加稀盐酸,溶液的pH一定变小
10.某同学用pH试纸测定未知溶液的pH时,他先用蒸馏水将pH试纸湿润,然后再测定,则他所测得的未知溶液pH将
A.偏大 B.偏小 C.无影响 D.无法确定
11.推理是学习化学的一种重要方法。下列推理得出的相关结论合理的是( )
A.碱溶液的pH都大于7,pH大于7的溶液一定是碱溶液
B.化合物是由不同种元素组成的纯净物,所以只含一种元素的物质一定不是化合物
C.中和反应生成盐和水,所以生成盐和水的反应一定是中和反应
D.金刚石和石墨都是由碳元素组成的单质,所以它们的性质完全相同
12.下图所示实验操作正确的是( )
A. 点燃酒精灯 B.滴加液体
C. 稀释浓硫酸 D. 读出液体的体积
二、填空题
13.在C、H、O、S、Na、Ca中选择适当的元素组成符合要求的物质,并将其化学式填在对应的横线上。
(1)金属氧化物_____;
(2)治疗胃酸过多的一种盐_____;
(3)硫酸根离子_____;
(4)土壤酸化后需要加入的物质_____。
14.如图表示元素的化合价与物质类别的关系,物质A-G分别由H、O、S、Ca中的一种、两种或三种元素组成。各物质均有某种组成元素的化合价与横坐标的数值对应,“→”表示物质之间的转化方向。请回答:
(1)E的化学式为___________,F的化学式为___________。
(2)A→B反应的现象为___________。
(3)C→D反应的现象为___________。
15.调味剂的主要作用是补充、增强或增加食品的味道。食醋是一种能增强食品酸味的调味剂,主要成分为醋酸(CH3COOH),与我们的生活密切相连。根据所学知识回答:
(1)食醋能作酸味的调味剂,是因为醋酸在水溶液中能解离出CH3COO-和_____(填离子符号)。
(2)食醋的酸味能促进人胃酸的分泌,胃酸的成分是_____(填化学式)。
(3)食醋能软化鱼骨和鸡蛋壳,原因是醋酸能与_____(填化学式)反应。
(4)生活中常用酒来制取食醋,原理是酒中的酒精CH3CH2OH在酶的作用下与空气中O2反应得到醋酸和水,请你尝试写出该反应的现象_____。
(5)用铁锅炒菜时,放一点食醋能补铁的原因是_____。
16.实验室有 4 种试剂,分别为 HNO3 溶液、CuSO4 溶液、MgCl2 溶液和 KOH 溶液。
(1)有颜色的试剂是______。
(2)有一种试剂能与另外三种试剂发生反应,该试剂是______。
(3)书写现象:
①CuSO4 溶液与 KOH 溶液混合:____________________________________。
②HNO3 溶液与 NaHCO3 溶液混合:__________________________________。
三、实验题
17.用如图装置进行实验,挤出浓盐酸。(信息:盐酸可以使紫色石蕊试液变红)
(1)实验现象是_______________。
(2)该实验说明分子具有的性质是_______________。
18.小明为探究酸、碱、盐的化学性质,做了如图实验:
(1)实验后液体颜色变红的试管是_______;
(2)反应后试管C的溶液中一定有的阳离子是_______;
(3)小明把D、E反应后的液体倒入一个洁净的烧杯中,观察到只有白色沉淀生成,过滤后得到白色沉淀和无色滤液,小明分别对试管D、E反应时的反应物用量有如下描述,正确的是_______。
A 试管D:氢氧化钙溶液一定过量
B 试管D:稀盐酸可能不足
C 试管E:碳酸钠一定过量
D 试管E:稀盐酸一定过量
四、计算题
19.小青同学为了制作叶脉书签,打算配制125g10%的NaOH溶液。
(1)计算小青需要称取NaOH的质量。
(2)小青将洗净的树叶放在配制好的溶液中煮沸后取出,溶液的质量减少了5g,溶质质量分数也有所减小。为了测定剩下溶液中NaOH的质量分数,小青向溶液中逐渐加入7.3%的稀盐酸,当溶液PH=7时,消耗盐酸50g。计算:
①生成NaCl的质量。
②剩下溶液中NaOH的质量分数。
20.为测定某盐酸的质量分数,往20 g 40%的氢氧化钠溶液中逐滴加入该盐酸,加入盐酸的质量与烧杯中溶液pH的变化关系如图所示。
(1)所用氢氧化钠溶液中溶质的质量为_________。
(2)当滴加盐酸到图像中D点时,烧杯中溶液的溶质是_________ (填化学式)。
(3)该盐酸中溶质质量分数是多少_________?
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.A
2.A
3.D
4.D
5.D
6.D
7.C
8.B
9.D
10.D
11.B
12.D
13. (1) CaO NaHCO3 (2) SO42﹣ Ca(OH)2
14. (1) CaSO4 (2)Ca(OH)2
15.(1) H+ HCl CaCO3 (2) 铁锅与食醋反应产生Fe2+
16. (1) CuSO4 溶液 (2) KOH 溶液
17. (1) 湿润的紫色石蕊小花变红 (2) 分子在不断运动。
18.(1) A Fe3+ (2) BC
19.小青需要称取NaOH的质量为12.5g, 生成NaCl的质量是5.85g,剩下溶液中NaOH的质量分数是3.3%
20.(1)8g(2)NaCl、HCl(3)29.2%
答案第1页,共2页
答案第1页,共2页
同课章节目录
- 第一单元 溶液
- 1 溶液的形成
- 2 溶液组成的定量表示
- 3物质的溶解性
- 到实验室去:配制一定溶质质量分数的溶液
- 第二单元 常见的酸和碱
- 1 酸及其性质
- 2 碱及其性质
- 3 溶液的酸碱性
- 4 酸碱中和反应
- 到实验室去:探究酸和碱的化学性质
- 到图书馆去:分子变成离子
- 第三单元 海水中的化学
- 1 海洋化学资源
- 2 海水“晒盐”
- 3 海水“制碱”
- 到实验室去:粗盐中难溶性杂质的去除
- 第四单元 金属
- 1 常见的金属材料
- 2 金属的化学性质
- 3 钢铁的锈蚀与防护
- 到实验室去:探究金属的性质
- 第五单元 化学与健康
- 1 食物中的有机物
- 2 化学元素与人体健康
- 3 远离有毒物质
- 第六单元 化学与社会发展
- 1 化学与能源开发
- 2 化学与材料研制
- 3 化学与农业生产
- 4 化学与环境保护
