第六单元 燃烧与燃料 单元整合 课件 2022-2023 鲁教版 化学 八年级(共18张PPT)
文档属性
| 名称 | 第六单元 燃烧与燃料 单元整合 课件 2022-2023 鲁教版 化学 八年级(共18张PPT) |

|
|
| 格式 | ppt | ||
| 文件大小 | 1.0MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 鲁教版(五四学制) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-10-08 00:00:00 | ||
图片预览






文档简介
(共18张PPT)
第六单元 单元整合
体系 脉络构建
我的答案:①温度达到着火点
②增大氧气的浓度 ③CH4
④CO2+H2O===H2CO3
⑤CO2+Ca(OH)2===CaCO3↓+H2O ⑥CaCO3+2HCl===CaCl2+H2O+CO2↑
易错 分类归纳
易错点 二氧化碳制取和性质把握不准
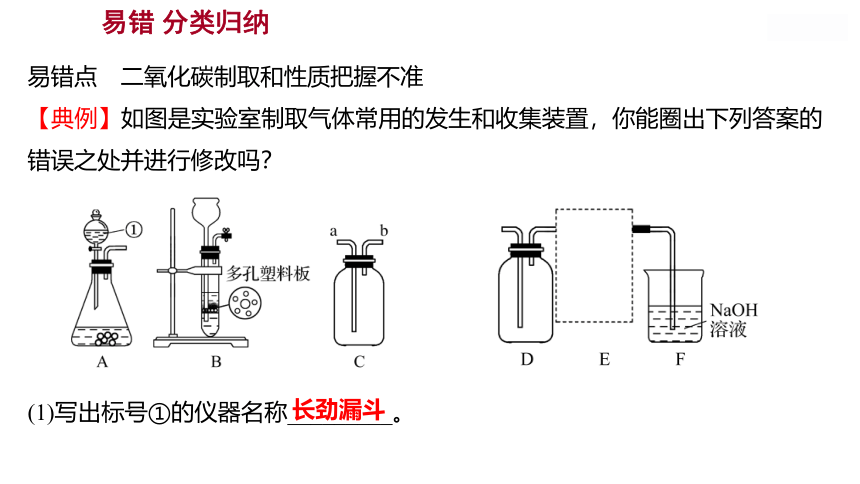
【典例】如图是实验室制取气体常用的发生和收集装置,你能圈出下列答案的错误之处并进行修改吗?
(1)写出标号①的仪器名称_________。
长劲漏斗
(2)实验室用装置A制取CO2的原料为_______________(填物质名称)。若将装置A
改为装置B,其优点是_____________。若用装置C收集CO2,气体应从__(填
“a”或“b”)端通入。
(3)FeS固体和稀硫酸之间可发生反应,该反应常用于实验室制取H2S同时生成
硫酸亚铁。H2S气体有毒,能溶于水,其水溶液为氢硫酸。
①写出制取H2S气体的化学方程式_______________________________。
②某同学用D、E、F装置组合收集H2S。E装置的作用是防倒吸,则虚线框内最
合适的装置是___(填“甲”或“乙”,请从下图中选择)。
石灰石和稀硫酸
控制反应速率
b
FeS+3H2SO4===Fe2(SO4)3+3H2S↑
甲
【错因分析】
1.仪器名称书写错误
长颈漏斗、分液漏斗要辨识清楚,书写要准确。
2.装置的选择与评价
分液漏斗能控制反应速率,带隔板的装置可控制反应的发生和停止,利用多功能瓶使用排空气法收集气体,密度大的气体从长端进入。防倒吸装置应避免NaOH溶液进入,导气管应与NaOH溶液脱离接触。
【解析】(1)标号①的仪器名称是分液漏斗;(2)实验室用石灰石(或大理石)和稀盐酸反应制备二氧化碳,不用稀硫酸,因为稀硫酸和碳酸钙反应生成的硫酸钙是微溶物,会附着在石灰石上,阻止反应的进行;若将装置A改为装置B,装置B的优点是可以控制反应的发生和停止;二氧化碳的密度比空气大,用向上排空气法收集二氧化碳,应从装置C的a端通入;(3)①FeS和稀硫酸反应生成硫酸亚铁和硫化氢,化学方程式为FeS+H2SO4===FeSO4+H2S↑;②防止倒吸,导气管应与NaOH溶液脱离,所以应选乙装置。
答案:(1)“长劲”改为“分液”
(2)“稀硫酸”改为“稀盐酸” “速率”改为“的发生和停止” “b”改为“a”
(3)①“3H2SO4”改为“H2SO4”;“Fe2(SO4)3”改为“FeSO4”;“3H2S”改为“H2S” ②“甲”改为“乙”
考点一 燃烧与灭火
【典例1】(2021·滨州中考)下列关于燃烧与灭火的说法正确的是( )
A.只要达到可燃物燃烧所需的最低温度,可燃物就能燃烧
B.工厂锅炉用煤加工成粉末状,可使煤燃烧更剧烈、更充分
C.室内起火,应该迅速打开所有门窗通风
D.水能灭火,主要是因为水蒸发吸热,降低了可燃物的着火点
【解析】A.可燃物燃烧的条件是与氧气接触,温度达到着火点,故不正确;B.将煤粉碎后能够增大煤与氧气的接触面积,再燃烧能够使其燃烧更充分,故正确;C.室内起火时,不能立即打开门窗,否则空气流通,使氧气更充足,火势更旺,会导致火势迅速蔓延,不利于灭火,故不正确;D.用水灭火,利用了水能使可燃物温度降低到其着火点以下,而不是降低可燃物的着火点,故不正确。
考点 定向突破
B
【变式训练】
1.使燃料充分燃烧的下列措施不合理的是( )
A.固体燃料粉碎 B.液体燃料喷成雾状
C.增加空气用量 D.增加燃料用量
【解析】A、固体燃料粉碎可以增大可燃物与氧气的接触面积,可以促进燃料的燃烧,故A合理;B、液体燃料喷成雾状可以增大可燃物与氧气的接触面积,可以促进燃料的燃烧,故B合理;C、增加空气用量增大了单位时间内可燃物与氧气的接触几率,相当于增大氧气的浓度,可以促进燃料的燃烧,故C合理;D、增加燃料用量不能促进燃料的燃烧,故D不合理。
D
2.(2021·常德中考改编)目前,人们使用的燃料大多来自化石燃料,它是不
可再生能源。回答下列问题:
(1)在石油、煤、天然气中,比较清洁的燃料是___________。
(2)煤燃烧时排放出SO2、NO2等污染物,这些气体或气体在空气中发生反应后
的生成物溶于雨水,会形成_________。
天然气
酸雨
(3)化石燃料的燃烧还会向大气中排放大量的CO2,导致温室效应增强。但CO2
用途相当广泛。如图是工业上利用CO2作原料生产尿素的微观结构示意图:
写出该反应的化学方程式_______________________________________。
(4)为缓解化石燃料面临耗尽的问题,人们正在利用和开发许多其他能源。
埋于海底将来可能会替代化石燃料的新能源是___________。
CO2+2NH3 CO(NH2)2+H2O
可燃冰
一定条件
========
【方法点拨】
燃烧与灭火的原理
1.燃烧所需的三个条件
①可燃物;②与氧气或空气接触;③温度达到着火点。三个条件缺一不可。
2.灭火的原理
破坏燃烧的三个条件之一就能达到灭火的目的。灭火原理包括清除或隔离可燃物、隔绝氧气、降温到该物质的着火点以下。满足上述三个条件之一,就能达到灭火的目的。
3.燃料充分燃烧的条件
燃烧时要有足够的空气(或氧气);燃料和空气(或氧气)要有足够大的接触面积。
考点二 二氧化碳的制取
【典例2】(2021·百色中考)如图是实验室制取气体的装置图,请回答下列问题:
(1)仪器a的名称为___________。
(2)实验室用过氧化氢溶液和二氧化锰制取氧气的化学方程式为__________________
________。若用高锰酸钾制取氧气时,所选用的发生装置是______(填字母序号,下
同)。
(3)实验室用大理石和稀盐酸制取二氧化碳,选用的发生装置是______,收集较为干燥
的二氧化碳气体,选用的收集装置是______,检验该气体是否收集满的操作是_______
___________________________________________________________。
集气瓶
2H2O2 2H2O
+O2↑
B
A
E
把燃
着的木条放在集气瓶口,如果燃着的木条熄灭,说明已经收集满
MnO2
====
【变式训练】
1.(2021·自贡中考)实验室制取气体时,下列因素不需要考虑的是( )
A.药品容易获得,能生成所要制取的气体
B.反应条件易于控制,反应速率适中
C.操作简便易行,安全可靠,节能环保
D.所要制取气体的颜色和气味
【解析】A、实验室制取气体时,应该选择能生成所要制取的气体且容易获得的药品;B、如果反应条件不容易控制,就可能造成反应速率太快或太慢;为了便于操作,反应速率要适中;C.实验室制取气体,操作应该简便易行,安全可靠,节能环保;D.实验室制取气体时,需要考虑采用什么原理,选择什么药品,选择什么实验装置,不需要考虑所要制取气体的颜色和气味。
D
2.(2021·遵义中考改编)实验室制备CO2并探究其性质。
(1)制取CO2可选择的发生装置是______(填字母序号)。
(2)用C装置收集CO2,验满的方法是________________________________________。
(3)D装置中,m、n处分别放有湿润、干燥的蓝色石蕊试纸,证明CO2能与水反应的现
象是___________________________________________________________;通过E装置
产生的现象可证明CO2具有_____________________________________的性质。
B
将燃着的木条放在a端,木条熄灭则集满
m处湿润的蓝色石蕊试纸变红,n处干燥的蓝色石蕊试纸不变色
密度比空气大,不燃烧也不支持燃烧
【解析】(1)实验室制取二氧化碳发生装置是固液常温型,故选B;(2)由于二氧化碳的密度比空气大,收集时,应从b端通入,验满的方法是在a端导管口处放燃着的小木条,木条熄灭则集满;(3)干燥的二氧化碳气体不能使蓝色石蕊试纸变色,二氧化碳与水反应生成碳酸,碳酸能使蓝色石蕊试纸变红;由于二氧化碳的密度比空气大,且二氧化碳不燃烧也不支持燃烧,可观察到E装置中蜡烛自下而上依次熄灭。
第六单元 单元整合
体系 脉络构建
我的答案:①温度达到着火点
②增大氧气的浓度 ③CH4
④CO2+H2O===H2CO3
⑤CO2+Ca(OH)2===CaCO3↓+H2O ⑥CaCO3+2HCl===CaCl2+H2O+CO2↑
易错 分类归纳
易错点 二氧化碳制取和性质把握不准
【典例】如图是实验室制取气体常用的发生和收集装置,你能圈出下列答案的错误之处并进行修改吗?
(1)写出标号①的仪器名称_________。
长劲漏斗
(2)实验室用装置A制取CO2的原料为_______________(填物质名称)。若将装置A
改为装置B,其优点是_____________。若用装置C收集CO2,气体应从__(填
“a”或“b”)端通入。
(3)FeS固体和稀硫酸之间可发生反应,该反应常用于实验室制取H2S同时生成
硫酸亚铁。H2S气体有毒,能溶于水,其水溶液为氢硫酸。
①写出制取H2S气体的化学方程式_______________________________。
②某同学用D、E、F装置组合收集H2S。E装置的作用是防倒吸,则虚线框内最
合适的装置是___(填“甲”或“乙”,请从下图中选择)。
石灰石和稀硫酸
控制反应速率
b
FeS+3H2SO4===Fe2(SO4)3+3H2S↑
甲
【错因分析】
1.仪器名称书写错误
长颈漏斗、分液漏斗要辨识清楚,书写要准确。
2.装置的选择与评价
分液漏斗能控制反应速率,带隔板的装置可控制反应的发生和停止,利用多功能瓶使用排空气法收集气体,密度大的气体从长端进入。防倒吸装置应避免NaOH溶液进入,导气管应与NaOH溶液脱离接触。
【解析】(1)标号①的仪器名称是分液漏斗;(2)实验室用石灰石(或大理石)和稀盐酸反应制备二氧化碳,不用稀硫酸,因为稀硫酸和碳酸钙反应生成的硫酸钙是微溶物,会附着在石灰石上,阻止反应的进行;若将装置A改为装置B,装置B的优点是可以控制反应的发生和停止;二氧化碳的密度比空气大,用向上排空气法收集二氧化碳,应从装置C的a端通入;(3)①FeS和稀硫酸反应生成硫酸亚铁和硫化氢,化学方程式为FeS+H2SO4===FeSO4+H2S↑;②防止倒吸,导气管应与NaOH溶液脱离,所以应选乙装置。
答案:(1)“长劲”改为“分液”
(2)“稀硫酸”改为“稀盐酸” “速率”改为“的发生和停止” “b”改为“a”
(3)①“3H2SO4”改为“H2SO4”;“Fe2(SO4)3”改为“FeSO4”;“3H2S”改为“H2S” ②“甲”改为“乙”
考点一 燃烧与灭火
【典例1】(2021·滨州中考)下列关于燃烧与灭火的说法正确的是( )
A.只要达到可燃物燃烧所需的最低温度,可燃物就能燃烧
B.工厂锅炉用煤加工成粉末状,可使煤燃烧更剧烈、更充分
C.室内起火,应该迅速打开所有门窗通风
D.水能灭火,主要是因为水蒸发吸热,降低了可燃物的着火点
【解析】A.可燃物燃烧的条件是与氧气接触,温度达到着火点,故不正确;B.将煤粉碎后能够增大煤与氧气的接触面积,再燃烧能够使其燃烧更充分,故正确;C.室内起火时,不能立即打开门窗,否则空气流通,使氧气更充足,火势更旺,会导致火势迅速蔓延,不利于灭火,故不正确;D.用水灭火,利用了水能使可燃物温度降低到其着火点以下,而不是降低可燃物的着火点,故不正确。
考点 定向突破
B
【变式训练】
1.使燃料充分燃烧的下列措施不合理的是( )
A.固体燃料粉碎 B.液体燃料喷成雾状
C.增加空气用量 D.增加燃料用量
【解析】A、固体燃料粉碎可以增大可燃物与氧气的接触面积,可以促进燃料的燃烧,故A合理;B、液体燃料喷成雾状可以增大可燃物与氧气的接触面积,可以促进燃料的燃烧,故B合理;C、增加空气用量增大了单位时间内可燃物与氧气的接触几率,相当于增大氧气的浓度,可以促进燃料的燃烧,故C合理;D、增加燃料用量不能促进燃料的燃烧,故D不合理。
D
2.(2021·常德中考改编)目前,人们使用的燃料大多来自化石燃料,它是不
可再生能源。回答下列问题:
(1)在石油、煤、天然气中,比较清洁的燃料是___________。
(2)煤燃烧时排放出SO2、NO2等污染物,这些气体或气体在空气中发生反应后
的生成物溶于雨水,会形成_________。
天然气
酸雨
(3)化石燃料的燃烧还会向大气中排放大量的CO2,导致温室效应增强。但CO2
用途相当广泛。如图是工业上利用CO2作原料生产尿素的微观结构示意图:
写出该反应的化学方程式_______________________________________。
(4)为缓解化石燃料面临耗尽的问题,人们正在利用和开发许多其他能源。
埋于海底将来可能会替代化石燃料的新能源是___________。
CO2+2NH3 CO(NH2)2+H2O
可燃冰
一定条件
========
【方法点拨】
燃烧与灭火的原理
1.燃烧所需的三个条件
①可燃物;②与氧气或空气接触;③温度达到着火点。三个条件缺一不可。
2.灭火的原理
破坏燃烧的三个条件之一就能达到灭火的目的。灭火原理包括清除或隔离可燃物、隔绝氧气、降温到该物质的着火点以下。满足上述三个条件之一,就能达到灭火的目的。
3.燃料充分燃烧的条件
燃烧时要有足够的空气(或氧气);燃料和空气(或氧气)要有足够大的接触面积。
考点二 二氧化碳的制取
【典例2】(2021·百色中考)如图是实验室制取气体的装置图,请回答下列问题:
(1)仪器a的名称为___________。
(2)实验室用过氧化氢溶液和二氧化锰制取氧气的化学方程式为__________________
________。若用高锰酸钾制取氧气时,所选用的发生装置是______(填字母序号,下
同)。
(3)实验室用大理石和稀盐酸制取二氧化碳,选用的发生装置是______,收集较为干燥
的二氧化碳气体,选用的收集装置是______,检验该气体是否收集满的操作是_______
___________________________________________________________。
集气瓶
2H2O2 2H2O
+O2↑
B
A
E
把燃
着的木条放在集气瓶口,如果燃着的木条熄灭,说明已经收集满
MnO2
====
【变式训练】
1.(2021·自贡中考)实验室制取气体时,下列因素不需要考虑的是( )
A.药品容易获得,能生成所要制取的气体
B.反应条件易于控制,反应速率适中
C.操作简便易行,安全可靠,节能环保
D.所要制取气体的颜色和气味
【解析】A、实验室制取气体时,应该选择能生成所要制取的气体且容易获得的药品;B、如果反应条件不容易控制,就可能造成反应速率太快或太慢;为了便于操作,反应速率要适中;C.实验室制取气体,操作应该简便易行,安全可靠,节能环保;D.实验室制取气体时,需要考虑采用什么原理,选择什么药品,选择什么实验装置,不需要考虑所要制取气体的颜色和气味。
D
2.(2021·遵义中考改编)实验室制备CO2并探究其性质。
(1)制取CO2可选择的发生装置是______(填字母序号)。
(2)用C装置收集CO2,验满的方法是________________________________________。
(3)D装置中,m、n处分别放有湿润、干燥的蓝色石蕊试纸,证明CO2能与水反应的现
象是___________________________________________________________;通过E装置
产生的现象可证明CO2具有_____________________________________的性质。
B
将燃着的木条放在a端,木条熄灭则集满
m处湿润的蓝色石蕊试纸变红,n处干燥的蓝色石蕊试纸不变色
密度比空气大,不燃烧也不支持燃烧
【解析】(1)实验室制取二氧化碳发生装置是固液常温型,故选B;(2)由于二氧化碳的密度比空气大,收集时,应从b端通入,验满的方法是在a端导管口处放燃着的小木条,木条熄灭则集满;(3)干燥的二氧化碳气体不能使蓝色石蕊试纸变色,二氧化碳与水反应生成碳酸,碳酸能使蓝色石蕊试纸变红;由于二氧化碳的密度比空气大,且二氧化碳不燃烧也不支持燃烧,可观察到E装置中蜡烛自下而上依次熄灭。
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 自然界中的水
- 第三节 水分子的变化
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 物质构成的奥秘
- 第一节 原子的构成
- 第二节 元素
- 第三节 物质组成的表示
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去 二氧化碳的实验室制取与性质
