【精选备课】2022-2023学年沪教版(全国)化学九年级上册 第四章单元检测(含解析)
文档属性
| 名称 | 【精选备课】2022-2023学年沪教版(全国)化学九年级上册 第四章单元检测(含解析) |

|
|
| 格式 | doc | ||
| 文件大小 | 361.5KB | ||
| 资源类型 | 试卷 | ||
| 版本资源 | 沪教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-10-08 00:00:00 | ||
图片预览




文档简介
中小学教育资源及组卷应用平台
第四章 单元检测
一、单选题
1.下列有关碳单质的说法错误的是
A.金刚石是天然存在的最硬的物质
B.石墨具有导电性可用作电极
C.金刚石和石墨的化学性质相似
D.C60是由60个碳原子构成的
2.镁带在耐高温的密闭(内含空气)容器中加热,下列图中能正确表示容器里所盛的物质总质量变化的是
A. B.
C. D.
3.石墨具有优异的光学、电学和力学特性,是一种革命性材料。如图为金刚石、石墨和石墨烯的结构模型,图中小球代表碳原子,下列说法正确的是
①石墨烯是一种新型化合物
②三种物质分别在足量的氧气中完全燃烧的产物相同
③金刚石和石墨烯是组成相同但结构不同的两种物质
④构成金刚石和石墨的原子大小不同
A.①④ B.②③ C.①③ D.②③④
4.在一个密闭容器中,有甲、乙、丙、丁四种物质在一定条件下充分反应后,测得反应前后各物质的质量如下表:
物质 甲 乙 丙 丁
反应前质量/g 5 2 20 22
反应后质量/g 待测 11 28 5
下列说法错误的是A.该反应是分解反应 B.甲可能是该反应的催化剂
C.乙、丙变化的质量比为9:8 D.反应后甲的质量为0 g
5.下列对一些事实的解释错误的是
事实 解释
A 书写档案规定必须使用碳素墨水 碳的化学性质常温下稳定
B 石墨能做电池的电极材料 石墨能够导电
C 碳能与二氧化碳反应生成一氧化碳 碳具有氧化性
D 制糖工业中用活性炭来脱色制白糖 活性炭具有吸附性
A.A B.B C.C D.D
6.将一定质量的a、b、c、d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得各物质的质量如表:
物质 a b c d
反应前的质量/g 6.4 14.0 3.2 1.0
反应一段时间后的质量/g 10.0 7.2 X 1.0
下列有关说法正确的是A.a和b是反应物 B.X=3.2
C.该反应属于分解反应 D.d一定是催化剂
7.下列物质的用途错误的是
A.用石墨做墨汁绘画 B.用木炭吸附一些食品里色素
C.金刚石镶在钻探机钻头上 D.活性炭用作防毒面具
8.碳单质的性质与用途对应关系错误的是
A.石墨导电性好可作电池电极 B.活性炭吸附性强可作冰箱除味剂
C.金刚石硬度大可制作铅笔芯 D.炭黑常温化学性质稳定可制墨汁
9.下列有关碳和碳的化合物说法错误的是
A.金刚石、石墨、C60都是碳元素组成的单质
B.在高温条件下,C能与许多金属氧化物反应
C.CO2中混有少量CO,可用点燃的方法除去
D.水墨画长久保存不变色是因为在常温下碳的化学性质不活泼
10.下列图标中属于消防安全标志的是
A.①② B.③④⑤ C.①③⑤ D.②④
11.在“高锰酸钾→锰酸钾+二氧化锰+氧气”反应中,二氧化锰是
A.氧化剂 B.催化剂 C.反应物 D.生成物
12.工业上可以用电解饱和食盐水的方法来制取氯气、氢气及另外一种重要的化工原料,反应方程式2NaCl+2H2O2X+Cl2+H2方程式已配平,则X的化学式为
A.HCl B.NaOH C.NaClO D.
13.下列变化中,不属于缓慢氧化的是。
A.酿酒 B.钢铁生锈 C.木炭燃烧 D.食物腐败
14.某化工厂通过电解食盐(NaCl)水制取一些化学工业的基本原料,此反应的产物中不可能存在的物质是( )
A.氢氧化钠 B.硫酸 C.氢气 D.氯气
二、课内填空
15.石墨是_______色的有金属光泽面不透明的细鳞片状固体,最软的矿物之一,有导电性,润滑性。可用于制铅笔芯、电池的电极、润滑剂等。
三、填空题
16.金刚石、石墨都是由碳元素组成的单质,但是由于他们的______不同,因此它们的______存在差异
17.大型海水淡化厂采用反渗透膜技术淡化海水,但是需要利用化石燃料供能,成本较高。阿拉伯目前正在建设一面巨大的反射镜,这个装置会将太阳光聚集到一个足球场大小的钢制玻璃穹顶上,汇集后的热量可以使其中的海水蒸发。蒸发后海水的溶质质量分数______(选填“变大”或“变小”或“不变”),此过程海水发生的变化是______(选填“物理”或“化学”)变化。
18.汽车使用是人类进步的标志,但生产汽车的材料、使用的能等是人们关注并需解决的问题。
(1)制造汽车的材料以钢铁为主,写出在高温下一氧化碳与氧化铁反应的化学方程式______。
(2)有些汽车新型排气系统中,使用抗腐蚀性能好的钛合金材料。生产钛(Ti)的部分工艺流程图如下:
回答下列问题:
① 二氧化钛中钛元素的化合价为_______价。
② 写出镁与四氯化钛(TiCl4)发生反应的化学方程式_______;该反应类型属于_______。上述反应需在氩气环境中进行,理由是_______。
四、简答题
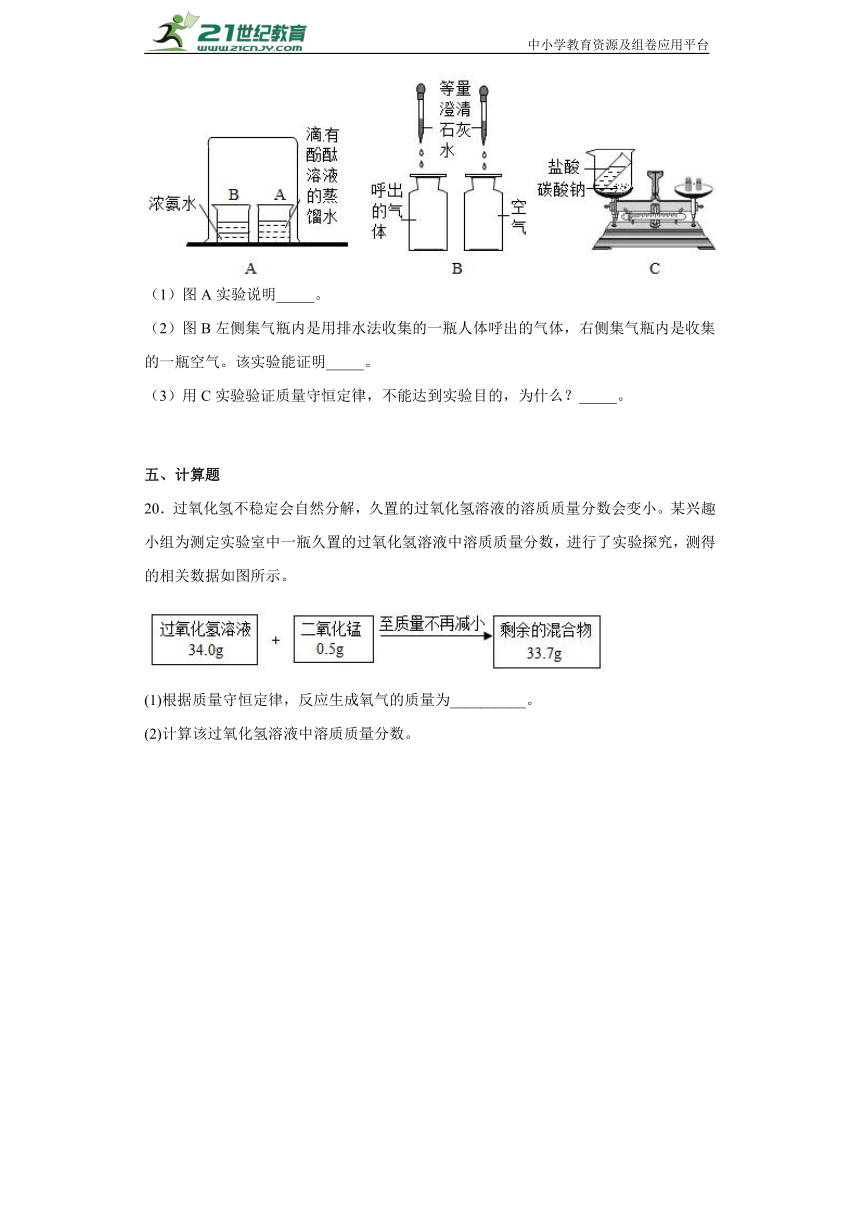
19.有如下图的三个实验。
(1)图A实验说明_____。
(2)图B左侧集气瓶内是用排水法收集的一瓶人体呼出的气体,右侧集气瓶内是收集的一瓶空气。该实验能证明_____。
(3)用C实验验证质量守恒定律,不能达到实验目的,为什么?_____。
五、计算题
20.过氧化氢不稳定会自然分解,久置的过氧化氢溶液的溶质质量分数会变小。某兴趣小组为测定实验室中一瓶久置的过氧化氢溶液中溶质质量分数,进行了实验探究,测得的相关数据如图所示。
(1)根据质量守恒定律,反应生成氧气的质量为__________。
(2)计算该过氧化氢溶液中溶质质量分数。
参考答案:
1.D
【详解】A、 金刚石是自然界最硬的物质,故选项说法正确;
B、石墨有导电性,可制作电极,故选项说法正确;
C、金刚石和石墨都是由碳元素组成的单质,它们的碳原子排列方式不同,导致它们的物理性质有较大的差异,然而它们都是碳的单质,所以,它们的化学性质相似,故选项说法正确;
D、C60是由C60分子构成,一个C60分子是由60个碳原子构成的,故选项说法错误。
故选:D。
2.B
【详解】镁带在耐高温的密闭(内含空气)容器中加热,镁与氧气燃烧生成氧化镁,容器内外的物质没有发生交流,由质量守恒定律可知,容器里所盛的物质总质量保持不变,故选B。
3.B
【详解】①石墨烯是由碳原子构成的,所以是一种新型单质,故①错误;
②三种物质分别在足量的氧气中完全燃烧的产物相同,都是二氧化碳,故②正确;
③金刚石和石墨烯都是由碳元素组成的,但是结构不同的两种物质,故③正确;
④构成金刚石和石墨的原子大小是相同的,故④错误,故②③正确。
故选:B。
4.D
【分析】该反应应用质量守恒定律先计算出待测值,反应前的总质量等于反应后的总质量,5+2+20+22=待测+11+28+5,待测值等于5。
【详解】A、乙、丙物质反应后质量增加了,说明乙、丙物质为生成物,丁物质反应后质量在减少,说明丁物质为反应物,表达式为:,该反应为分解反应,不符合题意;
B、根据表格甲物质反应前后质量不变,所以甲可能是反应的催化剂或杂质,不符合题意;
C、乙反应前后质量的变化值为:11-2=9,丙反应前后质量的变化值为:28-20=8,所以乙、丙变化的质量比为9:8,不符合题意;
D、反应后甲的质量为5g,符合题意;
故选:D。
5.C
【详解】A、碳素墨水中含有炭黑,炭黑的主要成分是碳,碳在常温下化学性质不活泼,故选项说法正确;
B、石墨能够做电池的电极材料,是因为石墨具有良好的导电性,故选项说法正确;
C、碳能与二氧化碳反应生成一氧化碳,说明碳具有还原性,故选项说法错误;
D、制糖工业中用活性炭来脱色以制白糖,是因为活性炭具有吸附性,能吸附色素,故选项说法正确。
故选C。
6.C
【分析】反应前后物质总质量不变,所以X=6.4+14.0+3.2+1.0-10.0-7.2-1.0=6.6。a、c反应后质量增加是生成物,b反应后质量减少,是反应物。d质量不变可能是催化剂也可能不参加反应。
【详解】A、a、c反应后质量增加是生成物,b反应后质量减少,是反应物。错误。
B、X=6.6,错误。
C、该反应是一种物质生成两种物质的反应,是分解反应。正确。
D、d可能是催化剂,也可能是不参加反应的杂质,错误。
故选C。
7.A
【详解】A. 墨汁通常是炭黑制成的,而石墨一般不用来做墨汁,故选项说法错误,符合题意;
B. 木炭具有吸附性,可以吸附一些食品里色素,故选项说法正确,不符合题意;
C. 因为金刚石的硬度很大,所以可以将金刚石镶在钻探机钻头上,故选项说法正确,不符合题意;
D. 因为活性炭具有吸附性,所以活性炭可以用作防毒面具,故选项说法正确,不符合题意。
故选:A。
8.C
【详解】A、石墨导电性好可作电池电极,故选项正确;
B、活性炭吸附性强可作冰箱除味剂是利用了活性炭的吸附性,故选项正确;
C、石墨在刻划时容易留下痕迹,可以制作铅笔芯,故选项错误;
D、常温下,碳单质的化学性质稳定,可制墨汁,故选项正确。
故选:C。
9.C
【详解】A、金刚石、石墨、C60都是由碳元素组成的单质,不符合题意;
B、C有还原性,在加热或高温的条件下,C能与许多金属氧化物如氧化铁、氧化铜反应,不符合题意;
C、CO2不可燃,不支持燃烧,所以二氧化碳中混有少量的CO,不能点燃,所以不可用点燃的方法除去CO,符合题意;
D、水墨画可长久保存不变色,是因为在常温下碳的化学性质不活泼,不符合题意。故选C。
10.C
【详解】①表示禁止吸烟,②是国家节水标志,③表示禁止放易燃物,④表示塑料制品回收标志,⑤表示禁止烟火;所以属于消防安全标志的是①③⑤;
故选C。
11.D
【分析】
【详解】“高锰酸钾加热生成锰酸钾、二氧化锰、氧气”可以看出,二氧化锰是生成物,故选D.
12.B
【详解】由质量守恒定律:反应前后,原子种类、数目均不变。
由反应的化学方程式2NaCl+2H2O2X+Cl2+H2,反应前钠、氯、氢、氧原子个数分别为2、2、4、2,反应后的生成物中钠、氯、氢、氧原子个数分别为0、2、2、0,根据反应前后原子种类、数目不变,则2X分子中含有2个钠原子、2个氢原子和2个氧原子,则每个X分子由1个钠原子、1个氢原子和1个氧原子构成,则物质X的化学式为NaOH。
故选B。
13.C
【详解】木炭燃烧是木炭和氧气进行的发光发热的剧烈的氧化反应,有些氧化反应进行得很慢,甚至不容易被察觉,这种氧化叫做缓慢氧化。如动植物呼吸、食物腐烂、酒和醋的酿造、金属生锈等,故选:C。
14.B
【详解】电解食盐水时,溶液中含有氯化钠和水,氯化钠和水中分别含有的元素是氯元素、钠元素、氢元素、氧元素,不含有硫元素,故产物中不可能有硫酸,故选B。
15.深灰
【详解】石墨是深灰色的有金属光泽面不透明的细鳞片状固体,最软的矿物之一,有导电性,润滑性。可用于制铅笔芯、电池的电极、润滑剂等。
16. 原子排列方式 物理性质
【详解】金刚石、石墨都是由碳元素组成的单质,但是由于他们的原子排列方式不同,因此它们的物理性质存在差异。
17. 变大 物理
【分析】根据题意,这个装置会将太阳光聚集到一个足球场大小的钢制玻璃穹顶上,汇集后的热量可以使其中的海水蒸发,进行分析解答。
【详解】这个装置会将太阳光聚集到一个足球场大小的钢制玻璃穹顶上,汇集后的热量可以使其中的海水蒸发,析出晶体前,溶质的质量不变,溶剂的质量减少,则蒸发后海水的溶质质量分数变大,此过程海水发生的变化,只是水的状态发生改变,没有新物质生成,属于物理变化。
故答案为:①变大;②物理。
【点睛】本题难度不大,明确蒸发前后溶液组成的变化、物理变化和化学变化的判别方法是正确解答本题的关键。
18. 3CO+Fe2O32Fe+3CO2 +4 TiCl4+2Mg2MgCl2+Ti 置换反应 防止高温下Mg(Ti)被氧化
【详解】(1)在高温下一氧化碳与氧化铁反应生成铁和二氧化碳,反应的化学方程为:3CO+Fe2O32Fe+3CO2;(2)化合物中元素的化合价的代数和为零,设钛元素的化合价为x,则x+(-1)×4=0 X=+4;由题中信息可知镁与四氯化钛(TiCl4)发生反应生成氯化镁和钛,反应的化学方程式为:TiCl4+2Mg2MgCl2+Ti;由一中单质和一种化合物生成另一种和另一种化合物的反应叫置换反应。镁与四氯化钛反应需在氩气环境中进行,理由是镁和钛的化学性质活泼,易与氧气反应,为防止高温下Mg(Ti)被氧化,需在氩气环境中进行,利用氩气隔绝氧气。
点睛:写方程式时的易错点①是配平错误,所以一定要计算反应前后原子的个数②忘记标记箭头或条件
19. 分子在不停地运动(或氨分子可以使酚酞溶液变红色) 人体呼出的气体中二氧化碳含量比空气中二氧化碳含量大 盐酸和碳酸钠反应生成的二氧化碳逸散(或挥发、或扩散等)到空气中(或反应没有在密闭容器中进行)
【详解】(1)图A实验中B中氨气分子不断运动扩散到A中,说明分子在不停地运动(或氨分子可以使酚酞溶液变红色);
(2)呼出气体能够使澄清的石灰水变浑浊,澄清的石灰水滴入空气中没有明显变化,因此说明人体呼出的气体中二氧化碳含量比空气中二氧化碳含量大;
(3)用C实验验证质量守恒定律,因为盐酸和碳酸钠反应生成的二氧化碳逸散(或挥发、或扩散等)到空气中(或反应没有在密闭容器中进行)所以不能达到实验目的。
20.(1)0.8g
(2)5%
解:设过氧化氢溶液溶质质量分数为x。
x=5%
答:溶质质量分数5%。
【分析】(1)
反应生成氧气的质量为34.0g+0.5g-33.7g=0.8g,故填:0.8g。
(2)
见答案
第四章 单元检测
一、单选题
1.下列有关碳单质的说法错误的是
A.金刚石是天然存在的最硬的物质
B.石墨具有导电性可用作电极
C.金刚石和石墨的化学性质相似
D.C60是由60个碳原子构成的
2.镁带在耐高温的密闭(内含空气)容器中加热,下列图中能正确表示容器里所盛的物质总质量变化的是
A. B.
C. D.
3.石墨具有优异的光学、电学和力学特性,是一种革命性材料。如图为金刚石、石墨和石墨烯的结构模型,图中小球代表碳原子,下列说法正确的是
①石墨烯是一种新型化合物
②三种物质分别在足量的氧气中完全燃烧的产物相同
③金刚石和石墨烯是组成相同但结构不同的两种物质
④构成金刚石和石墨的原子大小不同
A.①④ B.②③ C.①③ D.②③④
4.在一个密闭容器中,有甲、乙、丙、丁四种物质在一定条件下充分反应后,测得反应前后各物质的质量如下表:
物质 甲 乙 丙 丁
反应前质量/g 5 2 20 22
反应后质量/g 待测 11 28 5
下列说法错误的是A.该反应是分解反应 B.甲可能是该反应的催化剂
C.乙、丙变化的质量比为9:8 D.反应后甲的质量为0 g
5.下列对一些事实的解释错误的是
事实 解释
A 书写档案规定必须使用碳素墨水 碳的化学性质常温下稳定
B 石墨能做电池的电极材料 石墨能够导电
C 碳能与二氧化碳反应生成一氧化碳 碳具有氧化性
D 制糖工业中用活性炭来脱色制白糖 活性炭具有吸附性
A.A B.B C.C D.D
6.将一定质量的a、b、c、d四种物质放入一密闭容器中,在一定条件下反应一段时间后,测得各物质的质量如表:
物质 a b c d
反应前的质量/g 6.4 14.0 3.2 1.0
反应一段时间后的质量/g 10.0 7.2 X 1.0
下列有关说法正确的是A.a和b是反应物 B.X=3.2
C.该反应属于分解反应 D.d一定是催化剂
7.下列物质的用途错误的是
A.用石墨做墨汁绘画 B.用木炭吸附一些食品里色素
C.金刚石镶在钻探机钻头上 D.活性炭用作防毒面具
8.碳单质的性质与用途对应关系错误的是
A.石墨导电性好可作电池电极 B.活性炭吸附性强可作冰箱除味剂
C.金刚石硬度大可制作铅笔芯 D.炭黑常温化学性质稳定可制墨汁
9.下列有关碳和碳的化合物说法错误的是
A.金刚石、石墨、C60都是碳元素组成的单质
B.在高温条件下,C能与许多金属氧化物反应
C.CO2中混有少量CO,可用点燃的方法除去
D.水墨画长久保存不变色是因为在常温下碳的化学性质不活泼
10.下列图标中属于消防安全标志的是
A.①② B.③④⑤ C.①③⑤ D.②④
11.在“高锰酸钾→锰酸钾+二氧化锰+氧气”反应中,二氧化锰是
A.氧化剂 B.催化剂 C.反应物 D.生成物
12.工业上可以用电解饱和食盐水的方法来制取氯气、氢气及另外一种重要的化工原料,反应方程式2NaCl+2H2O2X+Cl2+H2方程式已配平,则X的化学式为
A.HCl B.NaOH C.NaClO D.
13.下列变化中,不属于缓慢氧化的是。
A.酿酒 B.钢铁生锈 C.木炭燃烧 D.食物腐败
14.某化工厂通过电解食盐(NaCl)水制取一些化学工业的基本原料,此反应的产物中不可能存在的物质是( )
A.氢氧化钠 B.硫酸 C.氢气 D.氯气
二、课内填空
15.石墨是_______色的有金属光泽面不透明的细鳞片状固体,最软的矿物之一,有导电性,润滑性。可用于制铅笔芯、电池的电极、润滑剂等。
三、填空题
16.金刚石、石墨都是由碳元素组成的单质,但是由于他们的______不同,因此它们的______存在差异
17.大型海水淡化厂采用反渗透膜技术淡化海水,但是需要利用化石燃料供能,成本较高。阿拉伯目前正在建设一面巨大的反射镜,这个装置会将太阳光聚集到一个足球场大小的钢制玻璃穹顶上,汇集后的热量可以使其中的海水蒸发。蒸发后海水的溶质质量分数______(选填“变大”或“变小”或“不变”),此过程海水发生的变化是______(选填“物理”或“化学”)变化。
18.汽车使用是人类进步的标志,但生产汽车的材料、使用的能等是人们关注并需解决的问题。
(1)制造汽车的材料以钢铁为主,写出在高温下一氧化碳与氧化铁反应的化学方程式______。
(2)有些汽车新型排气系统中,使用抗腐蚀性能好的钛合金材料。生产钛(Ti)的部分工艺流程图如下:
回答下列问题:
① 二氧化钛中钛元素的化合价为_______价。
② 写出镁与四氯化钛(TiCl4)发生反应的化学方程式_______;该反应类型属于_______。上述反应需在氩气环境中进行,理由是_______。
四、简答题
19.有如下图的三个实验。
(1)图A实验说明_____。
(2)图B左侧集气瓶内是用排水法收集的一瓶人体呼出的气体,右侧集气瓶内是收集的一瓶空气。该实验能证明_____。
(3)用C实验验证质量守恒定律,不能达到实验目的,为什么?_____。
五、计算题
20.过氧化氢不稳定会自然分解,久置的过氧化氢溶液的溶质质量分数会变小。某兴趣小组为测定实验室中一瓶久置的过氧化氢溶液中溶质质量分数,进行了实验探究,测得的相关数据如图所示。
(1)根据质量守恒定律,反应生成氧气的质量为__________。
(2)计算该过氧化氢溶液中溶质质量分数。
参考答案:
1.D
【详解】A、 金刚石是自然界最硬的物质,故选项说法正确;
B、石墨有导电性,可制作电极,故选项说法正确;
C、金刚石和石墨都是由碳元素组成的单质,它们的碳原子排列方式不同,导致它们的物理性质有较大的差异,然而它们都是碳的单质,所以,它们的化学性质相似,故选项说法正确;
D、C60是由C60分子构成,一个C60分子是由60个碳原子构成的,故选项说法错误。
故选:D。
2.B
【详解】镁带在耐高温的密闭(内含空气)容器中加热,镁与氧气燃烧生成氧化镁,容器内外的物质没有发生交流,由质量守恒定律可知,容器里所盛的物质总质量保持不变,故选B。
3.B
【详解】①石墨烯是由碳原子构成的,所以是一种新型单质,故①错误;
②三种物质分别在足量的氧气中完全燃烧的产物相同,都是二氧化碳,故②正确;
③金刚石和石墨烯都是由碳元素组成的,但是结构不同的两种物质,故③正确;
④构成金刚石和石墨的原子大小是相同的,故④错误,故②③正确。
故选:B。
4.D
【分析】该反应应用质量守恒定律先计算出待测值,反应前的总质量等于反应后的总质量,5+2+20+22=待测+11+28+5,待测值等于5。
【详解】A、乙、丙物质反应后质量增加了,说明乙、丙物质为生成物,丁物质反应后质量在减少,说明丁物质为反应物,表达式为:,该反应为分解反应,不符合题意;
B、根据表格甲物质反应前后质量不变,所以甲可能是反应的催化剂或杂质,不符合题意;
C、乙反应前后质量的变化值为:11-2=9,丙反应前后质量的变化值为:28-20=8,所以乙、丙变化的质量比为9:8,不符合题意;
D、反应后甲的质量为5g,符合题意;
故选:D。
5.C
【详解】A、碳素墨水中含有炭黑,炭黑的主要成分是碳,碳在常温下化学性质不活泼,故选项说法正确;
B、石墨能够做电池的电极材料,是因为石墨具有良好的导电性,故选项说法正确;
C、碳能与二氧化碳反应生成一氧化碳,说明碳具有还原性,故选项说法错误;
D、制糖工业中用活性炭来脱色以制白糖,是因为活性炭具有吸附性,能吸附色素,故选项说法正确。
故选C。
6.C
【分析】反应前后物质总质量不变,所以X=6.4+14.0+3.2+1.0-10.0-7.2-1.0=6.6。a、c反应后质量增加是生成物,b反应后质量减少,是反应物。d质量不变可能是催化剂也可能不参加反应。
【详解】A、a、c反应后质量增加是生成物,b反应后质量减少,是反应物。错误。
B、X=6.6,错误。
C、该反应是一种物质生成两种物质的反应,是分解反应。正确。
D、d可能是催化剂,也可能是不参加反应的杂质,错误。
故选C。
7.A
【详解】A. 墨汁通常是炭黑制成的,而石墨一般不用来做墨汁,故选项说法错误,符合题意;
B. 木炭具有吸附性,可以吸附一些食品里色素,故选项说法正确,不符合题意;
C. 因为金刚石的硬度很大,所以可以将金刚石镶在钻探机钻头上,故选项说法正确,不符合题意;
D. 因为活性炭具有吸附性,所以活性炭可以用作防毒面具,故选项说法正确,不符合题意。
故选:A。
8.C
【详解】A、石墨导电性好可作电池电极,故选项正确;
B、活性炭吸附性强可作冰箱除味剂是利用了活性炭的吸附性,故选项正确;
C、石墨在刻划时容易留下痕迹,可以制作铅笔芯,故选项错误;
D、常温下,碳单质的化学性质稳定,可制墨汁,故选项正确。
故选:C。
9.C
【详解】A、金刚石、石墨、C60都是由碳元素组成的单质,不符合题意;
B、C有还原性,在加热或高温的条件下,C能与许多金属氧化物如氧化铁、氧化铜反应,不符合题意;
C、CO2不可燃,不支持燃烧,所以二氧化碳中混有少量的CO,不能点燃,所以不可用点燃的方法除去CO,符合题意;
D、水墨画可长久保存不变色,是因为在常温下碳的化学性质不活泼,不符合题意。故选C。
10.C
【详解】①表示禁止吸烟,②是国家节水标志,③表示禁止放易燃物,④表示塑料制品回收标志,⑤表示禁止烟火;所以属于消防安全标志的是①③⑤;
故选C。
11.D
【分析】
【详解】“高锰酸钾加热生成锰酸钾、二氧化锰、氧气”可以看出,二氧化锰是生成物,故选D.
12.B
【详解】由质量守恒定律:反应前后,原子种类、数目均不变。
由反应的化学方程式2NaCl+2H2O2X+Cl2+H2,反应前钠、氯、氢、氧原子个数分别为2、2、4、2,反应后的生成物中钠、氯、氢、氧原子个数分别为0、2、2、0,根据反应前后原子种类、数目不变,则2X分子中含有2个钠原子、2个氢原子和2个氧原子,则每个X分子由1个钠原子、1个氢原子和1个氧原子构成,则物质X的化学式为NaOH。
故选B。
13.C
【详解】木炭燃烧是木炭和氧气进行的发光发热的剧烈的氧化反应,有些氧化反应进行得很慢,甚至不容易被察觉,这种氧化叫做缓慢氧化。如动植物呼吸、食物腐烂、酒和醋的酿造、金属生锈等,故选:C。
14.B
【详解】电解食盐水时,溶液中含有氯化钠和水,氯化钠和水中分别含有的元素是氯元素、钠元素、氢元素、氧元素,不含有硫元素,故产物中不可能有硫酸,故选B。
15.深灰
【详解】石墨是深灰色的有金属光泽面不透明的细鳞片状固体,最软的矿物之一,有导电性,润滑性。可用于制铅笔芯、电池的电极、润滑剂等。
16. 原子排列方式 物理性质
【详解】金刚石、石墨都是由碳元素组成的单质,但是由于他们的原子排列方式不同,因此它们的物理性质存在差异。
17. 变大 物理
【分析】根据题意,这个装置会将太阳光聚集到一个足球场大小的钢制玻璃穹顶上,汇集后的热量可以使其中的海水蒸发,进行分析解答。
【详解】这个装置会将太阳光聚集到一个足球场大小的钢制玻璃穹顶上,汇集后的热量可以使其中的海水蒸发,析出晶体前,溶质的质量不变,溶剂的质量减少,则蒸发后海水的溶质质量分数变大,此过程海水发生的变化,只是水的状态发生改变,没有新物质生成,属于物理变化。
故答案为:①变大;②物理。
【点睛】本题难度不大,明确蒸发前后溶液组成的变化、物理变化和化学变化的判别方法是正确解答本题的关键。
18. 3CO+Fe2O32Fe+3CO2 +4 TiCl4+2Mg2MgCl2+Ti 置换反应 防止高温下Mg(Ti)被氧化
【详解】(1)在高温下一氧化碳与氧化铁反应生成铁和二氧化碳,反应的化学方程为:3CO+Fe2O32Fe+3CO2;(2)化合物中元素的化合价的代数和为零,设钛元素的化合价为x,则x+(-1)×4=0 X=+4;由题中信息可知镁与四氯化钛(TiCl4)发生反应生成氯化镁和钛,反应的化学方程式为:TiCl4+2Mg2MgCl2+Ti;由一中单质和一种化合物生成另一种和另一种化合物的反应叫置换反应。镁与四氯化钛反应需在氩气环境中进行,理由是镁和钛的化学性质活泼,易与氧气反应,为防止高温下Mg(Ti)被氧化,需在氩气环境中进行,利用氩气隔绝氧气。
点睛:写方程式时的易错点①是配平错误,所以一定要计算反应前后原子的个数②忘记标记箭头或条件
19. 分子在不停地运动(或氨分子可以使酚酞溶液变红色) 人体呼出的气体中二氧化碳含量比空气中二氧化碳含量大 盐酸和碳酸钠反应生成的二氧化碳逸散(或挥发、或扩散等)到空气中(或反应没有在密闭容器中进行)
【详解】(1)图A实验中B中氨气分子不断运动扩散到A中,说明分子在不停地运动(或氨分子可以使酚酞溶液变红色);
(2)呼出气体能够使澄清的石灰水变浑浊,澄清的石灰水滴入空气中没有明显变化,因此说明人体呼出的气体中二氧化碳含量比空气中二氧化碳含量大;
(3)用C实验验证质量守恒定律,因为盐酸和碳酸钠反应生成的二氧化碳逸散(或挥发、或扩散等)到空气中(或反应没有在密闭容器中进行)所以不能达到实验目的。
20.(1)0.8g
(2)5%
解:设过氧化氢溶液溶质质量分数为x。
x=5%
答:溶质质量分数5%。
【分析】(1)
反应生成氧气的质量为34.0g+0.5g-33.7g=0.8g,故填:0.8g。
(2)
见答案
同课章节目录
- 第1章 开启化学之门
- 第1节 化学给我们带来什么
- 第2节 化学研究些什么
- 第3节 怎样学习和研究化学
- 第2章 身边的化学物质
- 第1节 性质活泼的氧气
- 第2节 奇妙的二氧化碳
- 第3节 自然界中的水
- 基础实验1 氧气的制取与性质
- 基础实验2 二氧化碳的制取与性质
- 第3章 物质构成的奥秘
- 第1节 构成物质的基本微粒
- 第2节 组成物质的化学元素
- 第3节 物质的组成
- 第4章 认识化学变化
- 第1节 常见的化学反应——燃烧
- 第2节 化学反应中的质量关系
- 第3节 化学方程式的书写与运用
- 基础实验3 物质燃烧的条件
- 第5章 金属的冶炼与利用
- 第1节 金属的性质和利用
- 第2节 金属矿物 铁的冶炼
- 第3节 金属防护和废金属回收
- 基础实验4 常见金属的性质
