高中化学人教版(2019)必修第一册1.3氧化还原反应(共19张ppt)
文档属性
| 名称 | 高中化学人教版(2019)必修第一册1.3氧化还原反应(共19张ppt) |

|
|
| 格式 | zip | ||
| 文件大小 | 2.1MB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版(2019) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-10-08 00:00:00 | ||
图片预览





文档简介
(共19张PPT)
第一章 物质及其变化
第三节 氧化还原反应
第1课时
1、①常用的四种基本反应类型用符号可简单表示如下,请问其分类的标准是什么
化合反应: A + B=AB 置换反应: A+BC= B+ AC
分解反应: AB=A+ B 复分解反应: AB +CD=AD + CB
②以下反应属于四种基本反应类型中的哪种
Fe2O3 + 3CO===2Fe + 3CO2
思考与交流
◆分类标准:根据反应物和生成物的种类和数目的多少。
高温
《九年级化学》
物质与氧发生的反应属于氧化反应。
含氧化合物里的氧被夺去的反应叫做还原反应。
1774年,法国化学家拉瓦锡提出燃烧的氧化学说后,
人们把物质与氧结合的反应叫做氧化反应,
把氧化物失去氧的反应叫做还原反应。
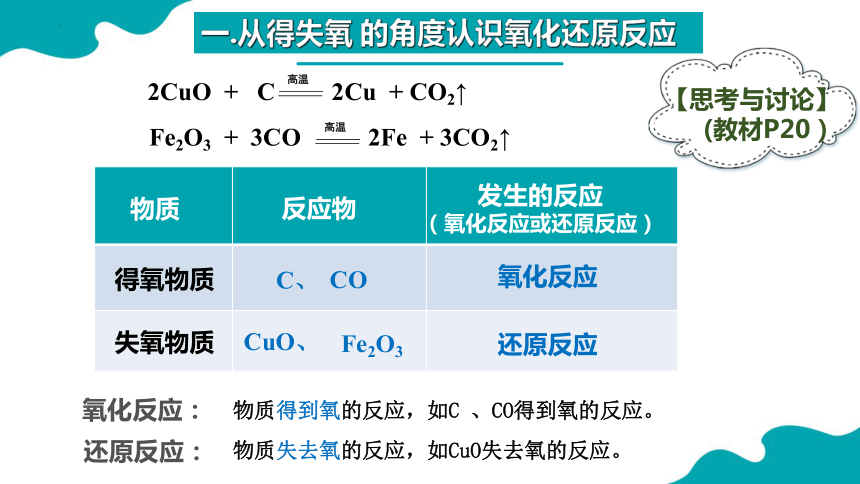
一.从得失氧 的角度认识氧化还原反应
2CuO + C 2Cu + CO2↑
高温
Fe2O3 + 3CO 2Fe + 3CO2↑
高温
物质
得氧物质
失氧物质
反应物
C、
CO
CuO、
Fe2O3
发生的反应
(氧化反应或还原反应)
氧化反应
还原反应
【思考与讨论】
(教材P20)
氧化反应:
物质得到氧的反应,如C 、CO得到氧的反应。
还原反应:
物质失去氧的反应,如CuO失去氧的反应。
思考与交流
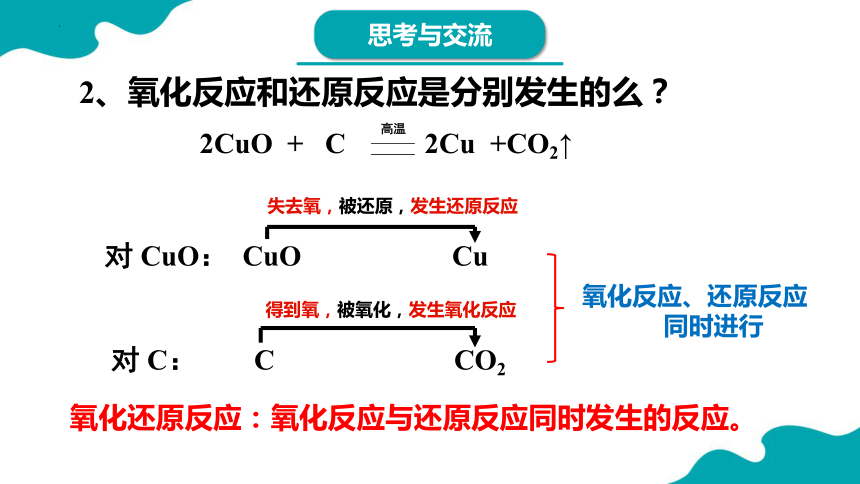
2、氧化反应和还原反应是分别发生的么?
2CuO + C 2Cu +CO2↑
高温
对 CuO: CuO Cu
失去氧,被还原,发生还原反应
对 C: C CO2
得到氧,被氧化,发生氧化反应
氧化反应、还原反应
同时进行
氧化还原反应:氧化反应与还原反应同时发生的反应。
氧化还原反应判断方法:是否有元素化合价的升降(特征)
2CuO + C 2Cu +CO2↑
高温
+2
0
+4
0
Fe2O3 + 3CO 2Fe + 3CO2↑
高温
【思考与讨论】
(教材P20)
标出各物质所含元素的化合价,除了得失氧之外,化合价有什么变化?
+3
0
+4
+2
二. 从化合价的角度认识氧化还原反应
【思考与讨论】
(教材P20)
3、物质发生的氧化反应或还原反应,与物质所含元素化合价的升
高或降低有什么关系?
2CuO + C 2Cu +CO2↑
高温
+2
0
+4
0
对 C: C CO2
0
+4
对 CuO: CuO Cu
+2
0
化合价升高,
被氧化,发生氧化反应
化合价降低,
被还原,发生还原反应
思考与交流
氧化还原反应
从化合价升降的角度
物质所含元素化合价升高,发生氧化反应
物质所含元素化合价降低,发生还原反应
氧化反应:
还原反应:
氧化还原反应:
凡是有元素化合价升降的反应都是。
是否有元素化合价的升降(特征)
【氧化还原反应判断依据】
① Fe+CuSO4=FeSO4+Cu
② 2H2 + O2
③ CaO+H2O = Ca(OH)2
④ 2KClO3 = 2KCl+3O2↑
⑤ CaCO3 = CaO + CO2↑
⑥ Na2CO3+2HCl = 2NaCl+ H2O + CO2↑
点燃
2H2O
判断方法:
是否有元素
化合价的升降(特征)
判断以下反应属于四大基本反应的哪个反应类型,并判断是否为氧化还原反应?
是否属于
氧化还原反应
四大基本反应类型
√
置换
√
√
×
×
×
化合
化合
分解
分解
复分解
尝试画出四大基本反应类型与氧化还原反应的交叉分类示意图:
置换反应
复分解反应
化合反应
分解反应
氧化还原反应
非氧化还原反应
为什么会有元素化合价的升降?
三. 认识氧化还原反应的本质
1、化合价升降原因
失2e-,化合价升高,发生氧化反应
得2e-,化合价降低,发生还原反应
0
0
+1
-1
①对于金属与非金属的反应:
2Na + Cl2 = 2NaCl
点燃
电子的得失
H Cl
+17
+1
+1
+17
H Cl
+1 -1
H
Cl
HCl
共用电子对的偏移
H2 + Cl2 = 2HCl
电子对偏离,化合价升高,发生氧化反应
电子对偏向,化合价降低,发生还原反应
0
0
+1
-1
②对于非金属与非金属的反应:
点燃
1、化合价升降原因
电子的得失
电子对的偏移
偏离
偏向
2、氧化还原反应的实质
电子的转移
2、氧化还原反应的实质
从电子转移的角度(实质)
失去电子或电子对偏离的反应
得到电子或电子对偏向的反应
有电子转移(得失或偏移)的反应
氧化反应:
还原反应:
氧化还原反应:
化合价升高--失去电子--氧化反应
化合价降低--得到电子--还原反应
特 征
本质
【归纳总结】
1、根据下列物质变化中化合价的情况,判断属于还原反应的是 ( )
A.CuO → Cu B. NaCl → HCl
C.C → CO2 D. FeCl2 → FeCl3
A
2、当化合物中的元素被转化成单质中的元素时,该元素 ( )
A.一定被氧化 B.一定被还原
C.可能被氧化,也可能被还原 D.化合价降低为零
C
感受氧化还原反应的存在
第一章 物质及其变化
第三节 氧化还原反应
第1课时
1、①常用的四种基本反应类型用符号可简单表示如下,请问其分类的标准是什么
化合反应: A + B=AB 置换反应: A+BC= B+ AC
分解反应: AB=A+ B 复分解反应: AB +CD=AD + CB
②以下反应属于四种基本反应类型中的哪种
Fe2O3 + 3CO===2Fe + 3CO2
思考与交流
◆分类标准:根据反应物和生成物的种类和数目的多少。
高温
《九年级化学》
物质与氧发生的反应属于氧化反应。
含氧化合物里的氧被夺去的反应叫做还原反应。
1774年,法国化学家拉瓦锡提出燃烧的氧化学说后,
人们把物质与氧结合的反应叫做氧化反应,
把氧化物失去氧的反应叫做还原反应。
一.从得失氧 的角度认识氧化还原反应
2CuO + C 2Cu + CO2↑
高温
Fe2O3 + 3CO 2Fe + 3CO2↑
高温
物质
得氧物质
失氧物质
反应物
C、
CO
CuO、
Fe2O3
发生的反应
(氧化反应或还原反应)
氧化反应
还原反应
【思考与讨论】
(教材P20)
氧化反应:
物质得到氧的反应,如C 、CO得到氧的反应。
还原反应:
物质失去氧的反应,如CuO失去氧的反应。
思考与交流
2、氧化反应和还原反应是分别发生的么?
2CuO + C 2Cu +CO2↑
高温
对 CuO: CuO Cu
失去氧,被还原,发生还原反应
对 C: C CO2
得到氧,被氧化,发生氧化反应
氧化反应、还原反应
同时进行
氧化还原反应:氧化反应与还原反应同时发生的反应。
氧化还原反应判断方法:是否有元素化合价的升降(特征)
2CuO + C 2Cu +CO2↑
高温
+2
0
+4
0
Fe2O3 + 3CO 2Fe + 3CO2↑
高温
【思考与讨论】
(教材P20)
标出各物质所含元素的化合价,除了得失氧之外,化合价有什么变化?
+3
0
+4
+2
二. 从化合价的角度认识氧化还原反应
【思考与讨论】
(教材P20)
3、物质发生的氧化反应或还原反应,与物质所含元素化合价的升
高或降低有什么关系?
2CuO + C 2Cu +CO2↑
高温
+2
0
+4
0
对 C: C CO2
0
+4
对 CuO: CuO Cu
+2
0
化合价升高,
被氧化,发生氧化反应
化合价降低,
被还原,发生还原反应
思考与交流
氧化还原反应
从化合价升降的角度
物质所含元素化合价升高,发生氧化反应
物质所含元素化合价降低,发生还原反应
氧化反应:
还原反应:
氧化还原反应:
凡是有元素化合价升降的反应都是。
是否有元素化合价的升降(特征)
【氧化还原反应判断依据】
① Fe+CuSO4=FeSO4+Cu
② 2H2 + O2
③ CaO+H2O = Ca(OH)2
④ 2KClO3 = 2KCl+3O2↑
⑤ CaCO3 = CaO + CO2↑
⑥ Na2CO3+2HCl = 2NaCl+ H2O + CO2↑
点燃
2H2O
判断方法:
是否有元素
化合价的升降(特征)
判断以下反应属于四大基本反应的哪个反应类型,并判断是否为氧化还原反应?
是否属于
氧化还原反应
四大基本反应类型
√
置换
√
√
×
×
×
化合
化合
分解
分解
复分解
尝试画出四大基本反应类型与氧化还原反应的交叉分类示意图:
置换反应
复分解反应
化合反应
分解反应
氧化还原反应
非氧化还原反应
为什么会有元素化合价的升降?
三. 认识氧化还原反应的本质
1、化合价升降原因
失2e-,化合价升高,发生氧化反应
得2e-,化合价降低,发生还原反应
0
0
+1
-1
①对于金属与非金属的反应:
2Na + Cl2 = 2NaCl
点燃
电子的得失
H Cl
+17
+1
+1
+17
H Cl
+1 -1
H
Cl
HCl
共用电子对的偏移
H2 + Cl2 = 2HCl
电子对偏离,化合价升高,发生氧化反应
电子对偏向,化合价降低,发生还原反应
0
0
+1
-1
②对于非金属与非金属的反应:
点燃
1、化合价升降原因
电子的得失
电子对的偏移
偏离
偏向
2、氧化还原反应的实质
电子的转移
2、氧化还原反应的实质
从电子转移的角度(实质)
失去电子或电子对偏离的反应
得到电子或电子对偏向的反应
有电子转移(得失或偏移)的反应
氧化反应:
还原反应:
氧化还原反应:
化合价升高--失去电子--氧化反应
化合价降低--得到电子--还原反应
特 征
本质
【归纳总结】
1、根据下列物质变化中化合价的情况,判断属于还原反应的是 ( )
A.CuO → Cu B. NaCl → HCl
C.C → CO2 D. FeCl2 → FeCl3
A
2、当化合物中的元素被转化成单质中的元素时,该元素 ( )
A.一定被氧化 B.一定被还原
C.可能被氧化,也可能被还原 D.化合价降低为零
C
感受氧化还原反应的存在
