浙教版2022-2023学年上学期八年级科学分类题型训练:第1章 水和水的溶液 计算题(10)【word,含答案】
文档属性
| 名称 | 浙教版2022-2023学年上学期八年级科学分类题型训练:第1章 水和水的溶液 计算题(10)【word,含答案】 |

|
|
| 格式 | doc | ||
| 文件大小 | 292.5KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 浙教版 | ||
| 科目 | 科学 | ||
| 更新时间 | 2022-10-11 00:00:00 | ||
图片预览



文档简介
1.如图是浓硫酸试剂瓶标签的部分内容。阅读后回答下列问题。
(1)未开启前该瓶液体的质量为_________克。
(2)①欲配置50克溶质的质量分数为20%的稀硫酸,需要这种98%的浓硫酸多少克?(结果保留1位小数)②同时需要水多少克?
2.根据下表氯化钠和硝酸钾的溶解度,回答下列问题:
(1)写出硝酸钾和氯化钠具有相同溶解度时的温度范围(限表中相邻两个温度之间):______________。
(2)在50℃时,向100克水中加A90克硝酸钾,充分搅拌后所得溶液质量为多少?
(3)计算20℃时氯化钠饱和溶液的溶质质量分数。(计算结果精确到0.1%)
3.某工厂在装配一件设备时,不小心把一个精密空心小球掉到一个又深、又小的坚固的水泥小洞中,用各种工具都取不出来,已知该小球的密度为1.64g/cm,有人提出往小洞中倒入某种溶液使小球浮起。现有两种物质的溶解度数据如下表:(溶液体积可认为近似等于水的体积,g取10N/kg)
(1)理论上可用上表中__________物质配制成溶液倒入小洞中使小球浮起。
(2)配制的溶液温度至少应保持_____________℃以上。
(3)小球取出后,擦干,用天平称得其质量为8.2g,若把此球投入水中,则静止时所受浮力为多大?
4.一个不规则的实心物体,质量55g,放入装满纯水的烧杯中,沉入底部,排开0.5N的水。然后向烧杯中加盐并搅拌,直到物体悬浮为止。g=10N/kg。求:
(1)物体在纯水中所受的浮力。
(2)物体的体积。
(3)物体悬浮时盐水的密度。
5.质量分数不同的硫酸溶液其密度不相同,对照表如下:
(1)分析表中数据,可以归纳出硫酸溶液的质量分数与密度的关系是_____。
(2)欲配制300克溶质的质量分数为30%的稀硫酸,需要溶质的质量分数为90%的浓硫酸多少克?水多少克。
6.氯化钠俗名食盐是工业生产和生活的一种重要原料,也是实验室里常见的一种药品。下表是20℃时,氯化钠溶解于水的实验数据,回答下列问题:
(1)表中m=_________;
(2)计算第3次实验得到的氯化钠溶液的溶质质量分数。(写出过程)
(3)20℃时,实验室把100克溶质质量分数为20%的氯化钠溶液释成5%的氯化钠溶液,需加水多少克?(写出过程)
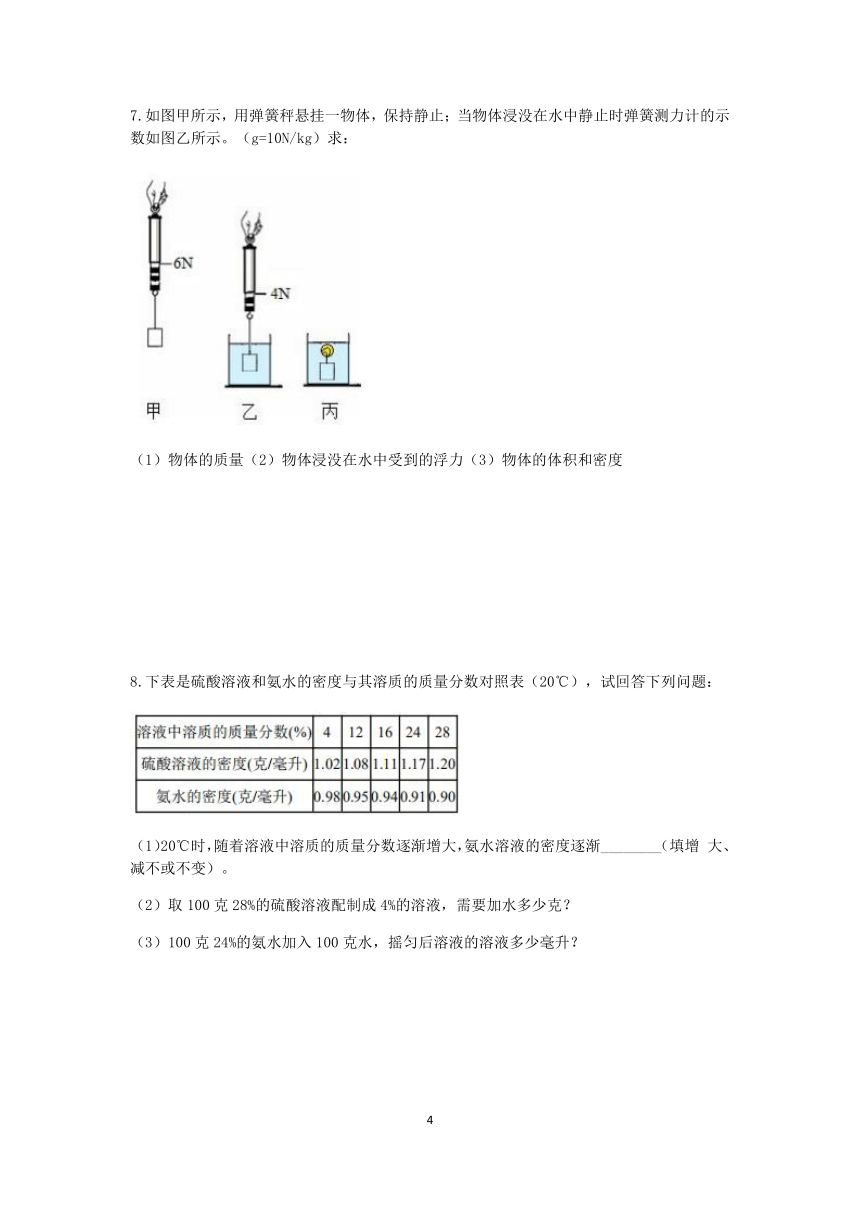
7.如图甲所示,用弹簧秤悬挂一物体,保持静止;当物体浸没在水中静止时弹簧测力计的示数如图乙所示。(g=10N/kg)求:
(1)物体的质量(2)物体浸没在水中受到的浮力(3)物体的体积和密度
8.下表是硫酸溶液和氨水的密度与其溶质的质量分数对照表(20℃),试回答下列问题:
(1)20℃时,随着溶液中溶质的质量分数逐渐增大,氨水溶液的密度逐渐________(填增 大、减不或不变)。
(2)取100克28%的硫酸溶液配制成4%的溶液,需要加水多少克?
(3)100克24%的氨水加入100克水,摇匀后溶液的溶液多少毫升?
9.有一个足够高的底面积为300平方厘米圆柱形容器,在其水平底水平放置一个立方体(如图)。立方体的边长为10厘米,密度为0.7×103kg/m3,(g取10N/kg)求 :(1)向容器内注水,在水位到达5cm时立方体受到水的浮力(2)此时立方体对池底的压力为多大?
10.某同学在实验室进行有关浓硫酸的实验,观察瓶上的标签(如右表所示)。他从瓶中倒出50毫升用于配制成稀硫酸,问:
(1)这50毫升浓硫酸中含溶质硫酸___________克。
(2)他将这50毫升浓硫酸与200克水均匀混合,求所得稀硫酸的质量分数。(结果保留到0.1%)
(3)若实验室用98%的浓硫酸来配制630g溶质质量分数28%的稀硫酸,则需要再加多少毫升的水?
11.如图甲所示,水平放置的方形容器里有一个重为6N、边长为10cm的立方体物块M (开始时容器内无水)。已知容器高20cm,物块M与容器底部不密合,且M底部与容器底部之间用一段5cm长的细线相连,假设细线足够牢固。现以5mL/s的恒定水流向容器内注水,当注水时间t=130s时,可画出容器中水的深度h随注水时间t的变化关系如图乙所示。请解答下列问题:
(1)当t=130s时,物块在水中的状态?(选“浸没”或“部分浸入”,写出计算过程)
(2)图乙中a的值是多少?(要求写出计算过程)
(3)上述过程中容器内的深度h与注水时间t的关系最符合下列哪个选线(假设物块始终保持水平)?答:_________ (选填字母代号)。
12.将一密度比水小的木块,系好绳子后放入甲图容器中,并且绳子的另一端固定在容器的中央。然后沿器壁缓慢匀速倒入水(忽略其他因素影响),容器中水与木块的位置变化如乙图。请你在丙图中画出木块的从加水开始到完全浸没后的过程中浮力随时间的变化情况图,并说出各段变化的理由。(温馨提示:t1时木块恰好离开杯底 t2时绳子刚好拉直 t3时木块完全淹没)
13.下表是硝酸钾在不同温度时的溶解度,根据表中数据回答下列问题。
(1)10℃时,100克水中最多可溶解硝酸钾的质量为_________克。
(2)20℃时,将10克硝酸钾加入40克水中,所得溶液溶质质量分数为____________。
(3)如图是硝酸钾溶液的变化情况,请写出两种可采用的操作方法。(写出计算过程)
参考答案
1.(1)920(2)50×20%=98%m m=10.250-10.2=39.8
2.(1)20-30℃(2)185.5(3)26.5%
3.(1)硝酸钾(2)40(3)0.05N
4.解:(1) F浮=G排水=0.5(2)因为浸没体积=排开水的体积=0.5/密度/g=50立方厘米(取g=10N/kg)(3)悬浮时浮力=重力密度×g×v=55×gv=50立方厘米密度=1.1克/立方厘米
5.(1)硫酸溶液的质量分数越大,密度越大 (2)设需要溶质的质量分数为90%的浓硫酸的质量为X300g×30%=90%˙XX=180g加水的质量为m水=300g-180g=120g 答:需要溶质的质量分数为90%的浓硫酸的质量为180g,水为120g。
6.(1)16g(2)w%=25%(3)m浓×A%=m稀×B%100g×20%=m稀×5%m稀=400gm水=m稀-m浓=400g-100g=300g
7.(1)解:物体的质量m=G/g=6N/10N/kg=0.6kg;(2)解:物体浸没在水中受到的浮力F浮=G-F拉=6N-4N=2N;(3)解:物体的体积V=V排=F浮/ρ水g=2N/103kg/m3×10N/kg=2×10 4m3; 物体的密度ρ=m/V=0.6kg/2×10 4m3=3000kg/m3。
8.(1)减小(2)设需要加水的质量为x, 100g×28%=(100g+x)×4%; 解得:x=600g。(3)根据表格可知,24%的氨水的密度为0.91g/ml; 100g氨水的体积:V氨水=m氨水ρ氨水=100g0.91g/ml≈109.89ml; 100g水的体积:V水=m水ρ水=100g1g/ml=100ml; 那么摇匀后溶液的体积为:V=V氨水+V水=100ml+109.89ml=209.89ml。
9.(1)5N (2)2N
10.(1)90.16(2)30.9%(3)450
11.
12.(1)0-t1 浸入,V排增大,浮力增大(2)t1-t2 漂浮,浮力不变(3)t2-t3 继续浸入,V排增大,浮力增大 (4)t3-t4 浸没,V排不变,浮力不变
13.(1)20.9 (2)20%(3)方法一:设可加入硝酸钾的质量为m1100克×10%=(100克+m1)×25% m1=20克方法二:设可蒸发的水的质量为m2 100克×10%=(100克-m2)×25% m2=60克
《水和溶液》计算训练(10)
(1)未开启前该瓶液体的质量为_________克。
(2)①欲配置50克溶质的质量分数为20%的稀硫酸,需要这种98%的浓硫酸多少克?(结果保留1位小数)②同时需要水多少克?
2.根据下表氯化钠和硝酸钾的溶解度,回答下列问题:
(1)写出硝酸钾和氯化钠具有相同溶解度时的温度范围(限表中相邻两个温度之间):______________。
(2)在50℃时,向100克水中加A90克硝酸钾,充分搅拌后所得溶液质量为多少?
(3)计算20℃时氯化钠饱和溶液的溶质质量分数。(计算结果精确到0.1%)
3.某工厂在装配一件设备时,不小心把一个精密空心小球掉到一个又深、又小的坚固的水泥小洞中,用各种工具都取不出来,已知该小球的密度为1.64g/cm,有人提出往小洞中倒入某种溶液使小球浮起。现有两种物质的溶解度数据如下表:(溶液体积可认为近似等于水的体积,g取10N/kg)
(1)理论上可用上表中__________物质配制成溶液倒入小洞中使小球浮起。
(2)配制的溶液温度至少应保持_____________℃以上。
(3)小球取出后,擦干,用天平称得其质量为8.2g,若把此球投入水中,则静止时所受浮力为多大?
4.一个不规则的实心物体,质量55g,放入装满纯水的烧杯中,沉入底部,排开0.5N的水。然后向烧杯中加盐并搅拌,直到物体悬浮为止。g=10N/kg。求:
(1)物体在纯水中所受的浮力。
(2)物体的体积。
(3)物体悬浮时盐水的密度。
5.质量分数不同的硫酸溶液其密度不相同,对照表如下:
(1)分析表中数据,可以归纳出硫酸溶液的质量分数与密度的关系是_____。
(2)欲配制300克溶质的质量分数为30%的稀硫酸,需要溶质的质量分数为90%的浓硫酸多少克?水多少克。
6.氯化钠俗名食盐是工业生产和生活的一种重要原料,也是实验室里常见的一种药品。下表是20℃时,氯化钠溶解于水的实验数据,回答下列问题:
(1)表中m=_________;
(2)计算第3次实验得到的氯化钠溶液的溶质质量分数。(写出过程)
(3)20℃时,实验室把100克溶质质量分数为20%的氯化钠溶液释成5%的氯化钠溶液,需加水多少克?(写出过程)
7.如图甲所示,用弹簧秤悬挂一物体,保持静止;当物体浸没在水中静止时弹簧测力计的示数如图乙所示。(g=10N/kg)求:
(1)物体的质量(2)物体浸没在水中受到的浮力(3)物体的体积和密度
8.下表是硫酸溶液和氨水的密度与其溶质的质量分数对照表(20℃),试回答下列问题:
(1)20℃时,随着溶液中溶质的质量分数逐渐增大,氨水溶液的密度逐渐________(填增 大、减不或不变)。
(2)取100克28%的硫酸溶液配制成4%的溶液,需要加水多少克?
(3)100克24%的氨水加入100克水,摇匀后溶液的溶液多少毫升?
9.有一个足够高的底面积为300平方厘米圆柱形容器,在其水平底水平放置一个立方体(如图)。立方体的边长为10厘米,密度为0.7×103kg/m3,(g取10N/kg)求 :(1)向容器内注水,在水位到达5cm时立方体受到水的浮力(2)此时立方体对池底的压力为多大?
10.某同学在实验室进行有关浓硫酸的实验,观察瓶上的标签(如右表所示)。他从瓶中倒出50毫升用于配制成稀硫酸,问:
(1)这50毫升浓硫酸中含溶质硫酸___________克。
(2)他将这50毫升浓硫酸与200克水均匀混合,求所得稀硫酸的质量分数。(结果保留到0.1%)
(3)若实验室用98%的浓硫酸来配制630g溶质质量分数28%的稀硫酸,则需要再加多少毫升的水?
11.如图甲所示,水平放置的方形容器里有一个重为6N、边长为10cm的立方体物块M (开始时容器内无水)。已知容器高20cm,物块M与容器底部不密合,且M底部与容器底部之间用一段5cm长的细线相连,假设细线足够牢固。现以5mL/s的恒定水流向容器内注水,当注水时间t=130s时,可画出容器中水的深度h随注水时间t的变化关系如图乙所示。请解答下列问题:
(1)当t=130s时,物块在水中的状态?(选“浸没”或“部分浸入”,写出计算过程)
(2)图乙中a的值是多少?(要求写出计算过程)
(3)上述过程中容器内的深度h与注水时间t的关系最符合下列哪个选线(假设物块始终保持水平)?答:_________ (选填字母代号)。
12.将一密度比水小的木块,系好绳子后放入甲图容器中,并且绳子的另一端固定在容器的中央。然后沿器壁缓慢匀速倒入水(忽略其他因素影响),容器中水与木块的位置变化如乙图。请你在丙图中画出木块的从加水开始到完全浸没后的过程中浮力随时间的变化情况图,并说出各段变化的理由。(温馨提示:t1时木块恰好离开杯底 t2时绳子刚好拉直 t3时木块完全淹没)
13.下表是硝酸钾在不同温度时的溶解度,根据表中数据回答下列问题。
(1)10℃时,100克水中最多可溶解硝酸钾的质量为_________克。
(2)20℃时,将10克硝酸钾加入40克水中,所得溶液溶质质量分数为____________。
(3)如图是硝酸钾溶液的变化情况,请写出两种可采用的操作方法。(写出计算过程)
参考答案
1.(1)920(2)50×20%=98%m m=10.250-10.2=39.8
2.(1)20-30℃(2)185.5(3)26.5%
3.(1)硝酸钾(2)40(3)0.05N
4.解:(1) F浮=G排水=0.5(2)因为浸没体积=排开水的体积=0.5/密度/g=50立方厘米(取g=10N/kg)(3)悬浮时浮力=重力密度×g×v=55×gv=50立方厘米密度=1.1克/立方厘米
5.(1)硫酸溶液的质量分数越大,密度越大 (2)设需要溶质的质量分数为90%的浓硫酸的质量为X300g×30%=90%˙XX=180g加水的质量为m水=300g-180g=120g 答:需要溶质的质量分数为90%的浓硫酸的质量为180g,水为120g。
6.(1)16g(2)w%=25%(3)m浓×A%=m稀×B%100g×20%=m稀×5%m稀=400gm水=m稀-m浓=400g-100g=300g
7.(1)解:物体的质量m=G/g=6N/10N/kg=0.6kg;(2)解:物体浸没在水中受到的浮力F浮=G-F拉=6N-4N=2N;(3)解:物体的体积V=V排=F浮/ρ水g=2N/103kg/m3×10N/kg=2×10 4m3; 物体的密度ρ=m/V=0.6kg/2×10 4m3=3000kg/m3。
8.(1)减小(2)设需要加水的质量为x, 100g×28%=(100g+x)×4%; 解得:x=600g。(3)根据表格可知,24%的氨水的密度为0.91g/ml; 100g氨水的体积:V氨水=m氨水ρ氨水=100g0.91g/ml≈109.89ml; 100g水的体积:V水=m水ρ水=100g1g/ml=100ml; 那么摇匀后溶液的体积为:V=V氨水+V水=100ml+109.89ml=209.89ml。
9.(1)5N (2)2N
10.(1)90.16(2)30.9%(3)450
11.
12.(1)0-t1 浸入,V排增大,浮力增大(2)t1-t2 漂浮,浮力不变(3)t2-t3 继续浸入,V排增大,浮力增大 (4)t3-t4 浸没,V排不变,浮力不变
13.(1)20.9 (2)20%(3)方法一:设可加入硝酸钾的质量为m1100克×10%=(100克+m1)×25% m1=20克方法二:设可蒸发的水的质量为m2 100克×10%=(100克-m2)×25% m2=60克
《水和溶液》计算训练(10)
同课章节目录
- 第1章 水和水的溶液
- 第1节 地球上的水
- 第2节 水的组成
- 第3节 水的浮力
- 第4节 物质在水中的分散状况
- 第5节 物质的溶解
- 第6节 物质的分离
- 第7节 水资源的利用、开发和保护
- 第2章 天气与气候
- 第1节 大气层
- 第2节 气温
- 第3节 大气的压强
- 第4节 风和降水
- 第5节 天气预报
- 第6节 气候和影响气候的因素
- 第7节 我国的气候特征与主要气象灾害
- 第3章 生命活动的调节
- 第1节 植物生命活动的调节
- 第2节 人体的激素调节
- 第3节 神经调节
- 第4节 动物的行为
- 第5节 体温的控制
- 第4章 电路探秘
- 第1节 电荷与电流
- 第2节 电流的测量
- 第3节 物质的导电性与电阻
- 第4节 变阻器
- 第5节 电压的测量
- 第6节 电流与电压、电阻的关系
- 第7节 电路分析与应用
- 研究性学习课题
- 一 测定本地区的“酸雨”情况及分析原因
- 二 太阳黑子活动与本地区降水的关系
- 三 训练小动物建立某种条件反射
- 四 调查在自然界或生命活动中的电现象
