第十一单元《盐化肥》2022-2023学年九年级化学人教版下册(有答案)
文档属性
| 名称 | 第十一单元《盐化肥》2022-2023学年九年级化学人教版下册(有答案) |

|
|
| 格式 | zip | ||
| 文件大小 | 63.1KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 人教版 | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-10-12 00:00:00 | ||
图片预览

文档简介
第十一单元《盐化肥》2022-2023学年九年级化学人教版下册
一、单选题
1.下列物质能用作钾肥的是( )
A.NH4HCO3 B.Ca3(PO4)2 C.K2CO3 D.CO(NH2)2
2.下列化肥从外观即可与其他化肥相区别的是( )
A.硝酸钾 B.氯化铵 C.磷矿粉 D.氯化钾
3.下列物质的名称或俗名,属同一种物质的是
A.生石灰 熟石灰 消石灰 B.冰 干冰 可燃冰
C.烧碱 苛性钠 火碱 D.石灰石 熟石灰 大理石
4.十一世纪,中国就用“卓筒井”凿井技术获取食盐。食盐的主要成分是( )
A.NaHCO3 B.Na2CO3 C.NaCl D.NaOH
5.下列实验目的与所用试剂相符的是
A.证明NaOH溶液中含有Na2CO3――酚酞试剂
B.证明NaOH溶液中含有Na2CO3――澄清石灰水
C.除去NaOH溶液中的Na2CO3杂质――稀盐酸
D.除去NaOH溶液中的Na2CO3杂质――CaCl2溶液
6.以下是Na2CO3、NaHCO3的溶解度表。下列说法中错误的是( )
0℃ 10℃ 20℃ 30℃ 40℃ 50℃ 60℃
Na2CO3的溶解度(g/100g水) 7.1 12.5 21.5 39.7 49.0 48.5 46.0
NaHCO3的溶解度(g/100g水) 6.9 8.1 9.6 11.1 12.7 14.5 16.4
A.40℃的饱和Na2CO3溶液升温到60℃,会析出晶体
B.60℃的NaHCO3溶液蒸干并充分灼烧,可得到NaHCO3晶体
C.30℃的溶质质量分数为25%的Na2CO3溶液降温到20℃,有晶体析出
D.20℃的饱和Na2CO3溶液中通足量CO2,生成的NaHCO3会部分析出
7.中华古代文化蕴含着丰富的化学知识,下列理解不合理的是
选项 文摘 理解
A 露从今夜白,月是故乡明 描述中有物理变化
B 暖暖远人村,依依墟里烟 描述中有化学变化
C 金(即铜)柔锡柔,合两柔则刚 合金的硬度比组成它的纯金属大
D 冬日灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣 其中的碱是指NaOH
A.A B.B C.C D.D
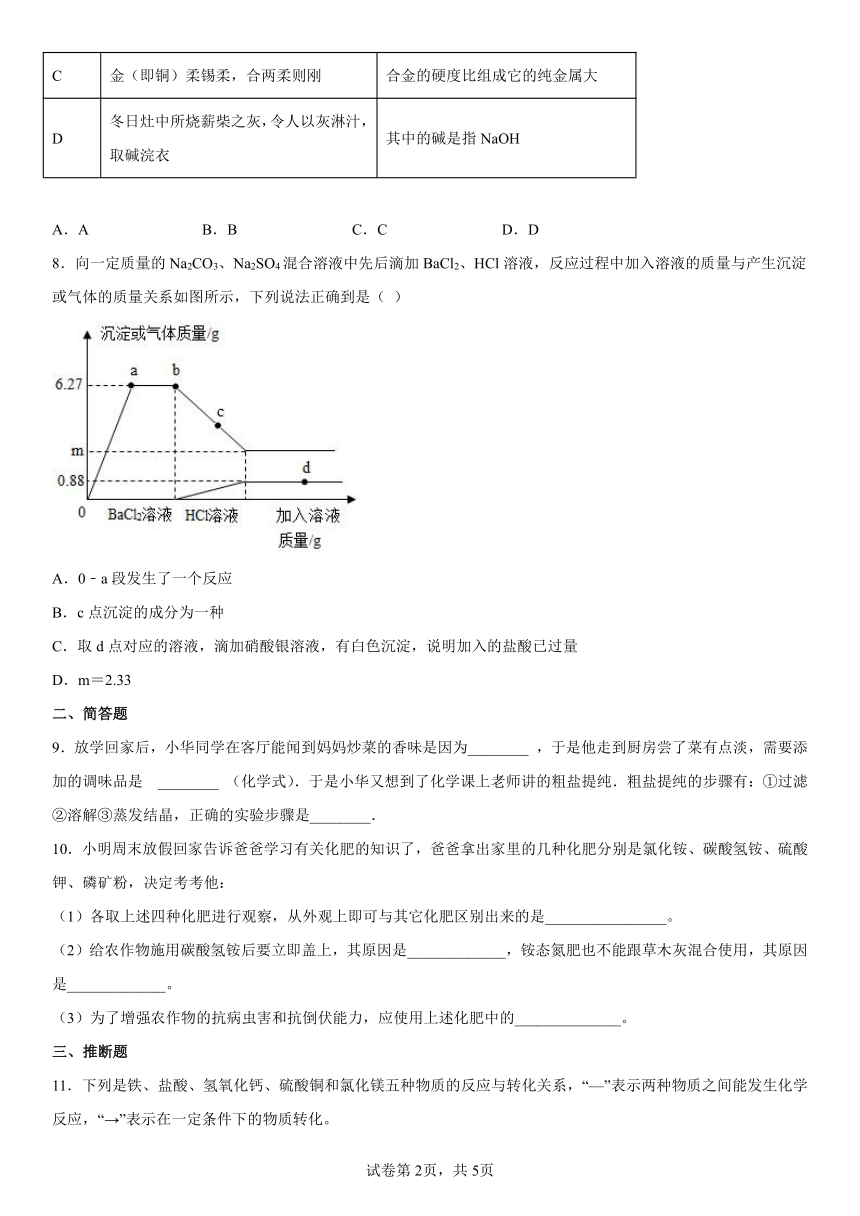
8.向一定质量的Na2CO3、Na2SO4混合溶液中先后滴加BaCl2、HCl溶液,反应过程中加入溶液的质量与产生沉淀或气体的质量关系如图所示,下列说法正确到是( )
A.0﹣a段发生了一个反应
B.c点沉淀的成分为一种
C.取d点对应的溶液,滴加硝酸银溶液,有白色沉淀,说明加入的盐酸已过量
D.m=2.33
二、简答题
9.放学回家后,小华同学在客厅能闻到妈妈炒菜的香味是因为________ ,于是他走到厨房尝了菜有点淡,需要添加的调味品是 ________ (化学式).于是小华又想到了化学课上老师讲的粗盐提纯.粗盐提纯的步骤有:①过滤②溶解③蒸发结晶,正确的实验步骤是________.
10.小明周末放假回家告诉爸爸学习有关化肥的知识了,爸爸拿出家里的几种化肥分别是氯化铵、碳酸氢铵、硫酸钾、磷矿粉,决定考考他:
(1)各取上述四种化肥进行观察,从外观上即可与其它化肥区别出来的是________________。
(2)给农作物施用碳酸氢铵后要立即盖上,其原因是_____________,铵态氮肥也不能跟草木灰混合使用,其原因是_____________。
(3)为了增强农作物的抗病虫害和抗倒伏能力,应使用上述化肥中的______________。
三、推断题
11.下列是铁、盐酸、氢氧化钙、硫酸铜和氯化镁五种物质的反应与转化关系,“—”表示两种物质之间能发生化学反应,“→”表示在一定条件下的物质转化。
(1)D的化学式为_____________。
(2)铁与B反应的实验现象是___________,该反应属于基本反应类型中的_____________反应。
(3)写出A与B反应的化学方程式________________。
(4)从物质反应规律分析,在单质、氧化物、酸、碱和盐中,能与C反应生成D的物质的______(填序号)。
①2类 ②3类 ③4类 ④5类
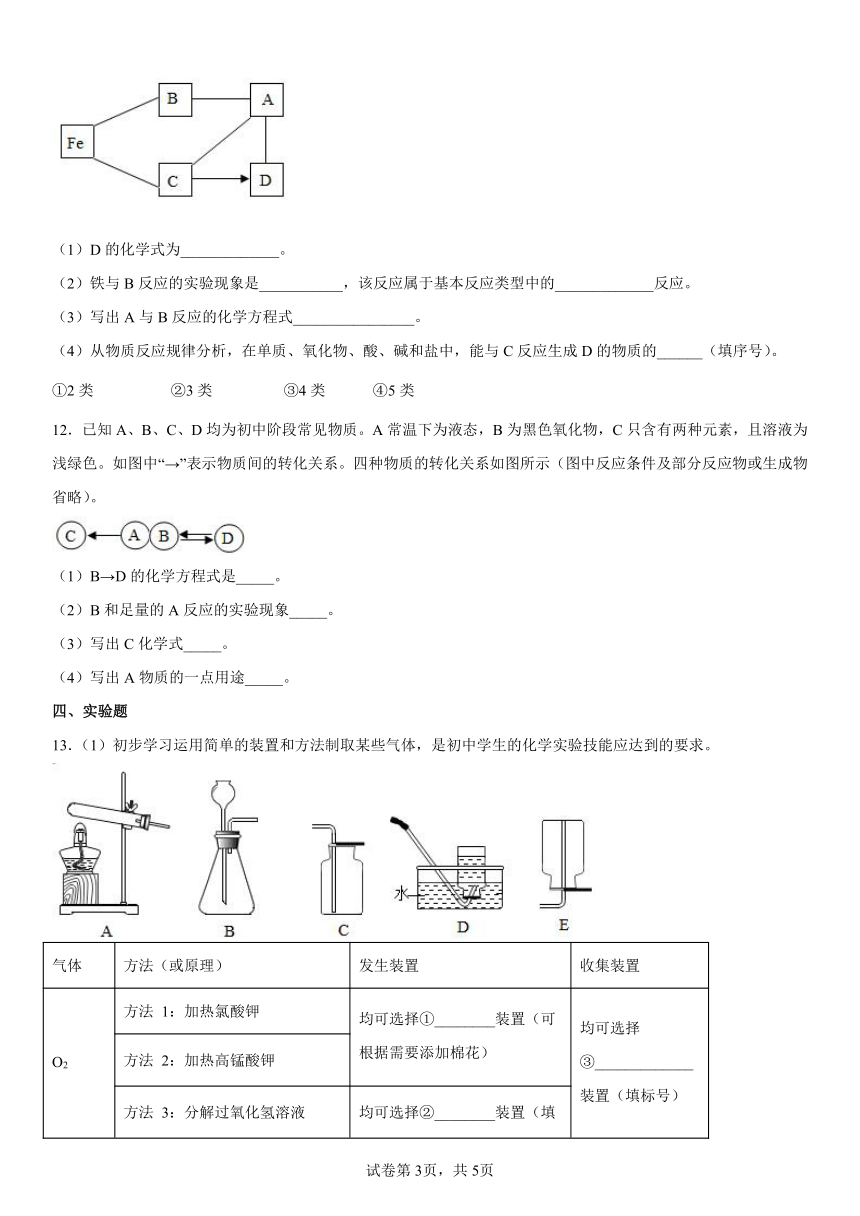
12.已知A、B、C、D均为初中阶段常见物质。A常温下为液态,B为黑色氧化物,C只含有两种元素,且溶液为浅绿色。如图中“→”表示物质间的转化关系。四种物质的转化关系如图所示(图中反应条件及部分反应物或生成物省略)。
(1)B→D的化学方程式是_____。
(2)B和足量的A反应的实验现象_____。
(3)写出C化学式_____。
(4)写出A物质的一点用途_____。
四、实验题
13.(1)初步学习运用简单的装置和方法制取某些气体,是初中学生的化学实验技能应达到的要求。
气体 方法(或原理) 发生装置 收集装置
O2 方法 1:加热氯酸钾 均可选择①________装置(可根据需要添加棉花) 均可选择③_____________装置(填标号)
方法 2:加热高锰酸钾
方法 3:分解过氧化氢溶液 均可选择②________装置(填标号)
CO2 大理石和稀盐酸
(2)粗盐提纯的步骤为:溶解、________、蒸发结晶、转移。每个步骤都要用到的仪器是________。
(3)某同学欲配制100g10%的NaCl溶液,称取NaCl时,指针向左偏,则他应该________。
14.为验证稀H2SO4的化学性质,同学们做了如下实验:
(1)能产生气泡的是_______(填字母,下同) ,不能体现酸的通性的是_____。
(2)写出试管D中发生反应的化学方程式__________。
(3)将试管E中的浊液过滤,为探究滤液的成分,小李设计了如下方案:
方案一:滤液验证滤液中含有HCl和H2SO4。
方案二:滤液 验证滤液中含有HCl和BaCl2。
其中方案_____(填“一”或“二”)不能达到实验目的,应将药品更换为__(填字母)。
a AgNO3溶液
b BaCl2溶液
c NaHCO3固体
d 金属铝
五、计算题
15.现有25 g石灰石样品,请按下面要求计算:
(1)25 g样品与足量的稀盐酸反应放出8.8 gCO2(杂质不溶于酸,且不与酸反应),请计算该样品的纯度(CaCO3的质量分数)是多少________?
(2)若将一定质量的该石灰石样品高温煅烧,有关物质质量随反应时间的变化如表所示:
时间/min t1 t2 t3 t4 t5
CO2质量/g 2.2 4.4 6.6 8.8 8.8
剩余固体质量/g 22.8 20.6 m 16.2 16.2
则m=_____,t3时剩余固体中除杂质外含有的物质是____(填化学式)。
16.实验室现有硫酸镁和硫酸钠的固体混合物样品,诺贝尔同学想测定样品中硫酸镁的质量分数,先称取该混合物样品20g,完全溶于100g水中。然后取用了一定溶质质量分数的氢氧化钠溶液100g平均分四次加入其中,充分振荡,实验所得数据见下表,请你分析并进行有关计算:
次数 1 2 3 4
加入氢氧化钠溶液的质量/g 25 25 25 25
生成沉淀的质量/g 2.9 x 8.7 8.7
(1)上表中x的数值为__________。
(2)求恰好完全反应时,溶液中溶质的质量分数(写出计算过程,结果保留一位小数)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.C
3.C
4.C
5.B
6.B
7.D
8.D
9. 分子是在不断运动的; NaCl; ②①③
10. 磷矿粉 碳酸氢铵性质很不稳定,受热时容易分解,温度越高,分解越快 碱性的草木灰跟铵态氮肥混合使用后,会产生氨气,氨气易挥发,会降低肥效 硫酸钾
11. MgCl2 铁表面有红色物质出现,溶液由蓝色变为浅绿色 置换 Ca(OH)2+CuSO4=Cu(OH)2↓+CaSO4 ③
12. FeO+COFe+CO2(合理即可) 黑色粉末逐渐溶解,溶液变为浅绿色 FeCl2 用于金属表面除锈(合理即可)
13. A C B 过滤 玻璃棒 减少药品直至天平平衡
14. AD E 一 b
15.(1)80%(2)18.4;CaCO3和CaO
16.5.8;
由表格可知第三次氢氧化钠和硫酸镁恰好完全反应,设生成硫酸钠质量为y,硫酸镁的质量为z,
溶质质量为硫酸钠质量=20g-12g+14.2g=22.2g
溶液质量=100g+20g+25g×3-8.7g=186.3g
溶质质量分数为:
答:溶液中溶质的质量分数11.9%。
答案第1页,共2页
答案第1页,共2页
一、单选题
1.下列物质能用作钾肥的是( )
A.NH4HCO3 B.Ca3(PO4)2 C.K2CO3 D.CO(NH2)2
2.下列化肥从外观即可与其他化肥相区别的是( )
A.硝酸钾 B.氯化铵 C.磷矿粉 D.氯化钾
3.下列物质的名称或俗名,属同一种物质的是
A.生石灰 熟石灰 消石灰 B.冰 干冰 可燃冰
C.烧碱 苛性钠 火碱 D.石灰石 熟石灰 大理石
4.十一世纪,中国就用“卓筒井”凿井技术获取食盐。食盐的主要成分是( )
A.NaHCO3 B.Na2CO3 C.NaCl D.NaOH
5.下列实验目的与所用试剂相符的是
A.证明NaOH溶液中含有Na2CO3――酚酞试剂
B.证明NaOH溶液中含有Na2CO3――澄清石灰水
C.除去NaOH溶液中的Na2CO3杂质――稀盐酸
D.除去NaOH溶液中的Na2CO3杂质――CaCl2溶液
6.以下是Na2CO3、NaHCO3的溶解度表。下列说法中错误的是( )
0℃ 10℃ 20℃ 30℃ 40℃ 50℃ 60℃
Na2CO3的溶解度(g/100g水) 7.1 12.5 21.5 39.7 49.0 48.5 46.0
NaHCO3的溶解度(g/100g水) 6.9 8.1 9.6 11.1 12.7 14.5 16.4
A.40℃的饱和Na2CO3溶液升温到60℃,会析出晶体
B.60℃的NaHCO3溶液蒸干并充分灼烧,可得到NaHCO3晶体
C.30℃的溶质质量分数为25%的Na2CO3溶液降温到20℃,有晶体析出
D.20℃的饱和Na2CO3溶液中通足量CO2,生成的NaHCO3会部分析出
7.中华古代文化蕴含着丰富的化学知识,下列理解不合理的是
选项 文摘 理解
A 露从今夜白,月是故乡明 描述中有物理变化
B 暖暖远人村,依依墟里烟 描述中有化学变化
C 金(即铜)柔锡柔,合两柔则刚 合金的硬度比组成它的纯金属大
D 冬日灶中所烧薪柴之灰,令人以灰淋汁,取碱浣衣 其中的碱是指NaOH
A.A B.B C.C D.D
8.向一定质量的Na2CO3、Na2SO4混合溶液中先后滴加BaCl2、HCl溶液,反应过程中加入溶液的质量与产生沉淀或气体的质量关系如图所示,下列说法正确到是( )
A.0﹣a段发生了一个反应
B.c点沉淀的成分为一种
C.取d点对应的溶液,滴加硝酸银溶液,有白色沉淀,说明加入的盐酸已过量
D.m=2.33
二、简答题
9.放学回家后,小华同学在客厅能闻到妈妈炒菜的香味是因为________ ,于是他走到厨房尝了菜有点淡,需要添加的调味品是 ________ (化学式).于是小华又想到了化学课上老师讲的粗盐提纯.粗盐提纯的步骤有:①过滤②溶解③蒸发结晶,正确的实验步骤是________.
10.小明周末放假回家告诉爸爸学习有关化肥的知识了,爸爸拿出家里的几种化肥分别是氯化铵、碳酸氢铵、硫酸钾、磷矿粉,决定考考他:
(1)各取上述四种化肥进行观察,从外观上即可与其它化肥区别出来的是________________。
(2)给农作物施用碳酸氢铵后要立即盖上,其原因是_____________,铵态氮肥也不能跟草木灰混合使用,其原因是_____________。
(3)为了增强农作物的抗病虫害和抗倒伏能力,应使用上述化肥中的______________。
三、推断题
11.下列是铁、盐酸、氢氧化钙、硫酸铜和氯化镁五种物质的反应与转化关系,“—”表示两种物质之间能发生化学反应,“→”表示在一定条件下的物质转化。
(1)D的化学式为_____________。
(2)铁与B反应的实验现象是___________,该反应属于基本反应类型中的_____________反应。
(3)写出A与B反应的化学方程式________________。
(4)从物质反应规律分析,在单质、氧化物、酸、碱和盐中,能与C反应生成D的物质的______(填序号)。
①2类 ②3类 ③4类 ④5类
12.已知A、B、C、D均为初中阶段常见物质。A常温下为液态,B为黑色氧化物,C只含有两种元素,且溶液为浅绿色。如图中“→”表示物质间的转化关系。四种物质的转化关系如图所示(图中反应条件及部分反应物或生成物省略)。
(1)B→D的化学方程式是_____。
(2)B和足量的A反应的实验现象_____。
(3)写出C化学式_____。
(4)写出A物质的一点用途_____。
四、实验题
13.(1)初步学习运用简单的装置和方法制取某些气体,是初中学生的化学实验技能应达到的要求。
气体 方法(或原理) 发生装置 收集装置
O2 方法 1:加热氯酸钾 均可选择①________装置(可根据需要添加棉花) 均可选择③_____________装置(填标号)
方法 2:加热高锰酸钾
方法 3:分解过氧化氢溶液 均可选择②________装置(填标号)
CO2 大理石和稀盐酸
(2)粗盐提纯的步骤为:溶解、________、蒸发结晶、转移。每个步骤都要用到的仪器是________。
(3)某同学欲配制100g10%的NaCl溶液,称取NaCl时,指针向左偏,则他应该________。
14.为验证稀H2SO4的化学性质,同学们做了如下实验:
(1)能产生气泡的是_______(填字母,下同) ,不能体现酸的通性的是_____。
(2)写出试管D中发生反应的化学方程式__________。
(3)将试管E中的浊液过滤,为探究滤液的成分,小李设计了如下方案:
方案一:滤液验证滤液中含有HCl和H2SO4。
方案二:滤液 验证滤液中含有HCl和BaCl2。
其中方案_____(填“一”或“二”)不能达到实验目的,应将药品更换为__(填字母)。
a AgNO3溶液
b BaCl2溶液
c NaHCO3固体
d 金属铝
五、计算题
15.现有25 g石灰石样品,请按下面要求计算:
(1)25 g样品与足量的稀盐酸反应放出8.8 gCO2(杂质不溶于酸,且不与酸反应),请计算该样品的纯度(CaCO3的质量分数)是多少________?
(2)若将一定质量的该石灰石样品高温煅烧,有关物质质量随反应时间的变化如表所示:
时间/min t1 t2 t3 t4 t5
CO2质量/g 2.2 4.4 6.6 8.8 8.8
剩余固体质量/g 22.8 20.6 m 16.2 16.2
则m=_____,t3时剩余固体中除杂质外含有的物质是____(填化学式)。
16.实验室现有硫酸镁和硫酸钠的固体混合物样品,诺贝尔同学想测定样品中硫酸镁的质量分数,先称取该混合物样品20g,完全溶于100g水中。然后取用了一定溶质质量分数的氢氧化钠溶液100g平均分四次加入其中,充分振荡,实验所得数据见下表,请你分析并进行有关计算:
次数 1 2 3 4
加入氢氧化钠溶液的质量/g 25 25 25 25
生成沉淀的质量/g 2.9 x 8.7 8.7
(1)上表中x的数值为__________。
(2)求恰好完全反应时,溶液中溶质的质量分数(写出计算过程,结果保留一位小数)
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.C
2.C
3.C
4.C
5.B
6.B
7.D
8.D
9. 分子是在不断运动的; NaCl; ②①③
10. 磷矿粉 碳酸氢铵性质很不稳定,受热时容易分解,温度越高,分解越快 碱性的草木灰跟铵态氮肥混合使用后,会产生氨气,氨气易挥发,会降低肥效 硫酸钾
11. MgCl2 铁表面有红色物质出现,溶液由蓝色变为浅绿色 置换 Ca(OH)2+CuSO4=Cu(OH)2↓+CaSO4 ③
12. FeO+COFe+CO2(合理即可) 黑色粉末逐渐溶解,溶液变为浅绿色 FeCl2 用于金属表面除锈(合理即可)
13. A C B 过滤 玻璃棒 减少药品直至天平平衡
14. AD E 一 b
15.(1)80%(2)18.4;CaCO3和CaO
16.5.8;
由表格可知第三次氢氧化钠和硫酸镁恰好完全反应,设生成硫酸钠质量为y,硫酸镁的质量为z,
溶质质量为硫酸钠质量=20g-12g+14.2g=22.2g
溶液质量=100g+20g+25g×3-8.7g=186.3g
溶质质量分数为:
答:溶液中溶质的质量分数11.9%。
答案第1页,共2页
答案第1页,共2页
同课章节目录
