第6章《常用的金属和盐》同步练习-2022-2023学年九年级化学沪教版(上海)第二学期(有答案)
文档属性
| 名称 | 第6章《常用的金属和盐》同步练习-2022-2023学年九年级化学沪教版(上海)第二学期(有答案) |
|
|
| 格式 | zip | ||
| 文件大小 | 60.6KB | ||
| 资源类型 | 教案 | ||
| 版本资源 | 沪教版(试用本) | ||
| 科目 | 化学 | ||
| 更新时间 | 2022-10-12 00:00:00 | ||
图片预览



文档简介
第6章《常用的金属和盐》同步练习-2022-2023学年九年级化学沪教版(上海)第二学期
一、单选题
1.金属材料在人类活动中已得到越来越广泛的应用。下列性质属于金属共性的是
A.熔点很高 B.有良好的导电性、导热性
C.银白色的固体 D.硬度很大
2.醋酸(CH3COOH是食醋的成分之一,其水溶液中存在H+和CH3COO-。下列说法正确的是
A.醋酸属于氧化物
B.醋酸不能用于除铁锈
C.醋酸能与镁反应产生氢气
D.醋酸中碳元素的质量分数最大
3.铁是一种重要的金属。下列关于铁的叙述错误的是
A.生铁是纯净物
B.涂油漆可防止铁生锈
C.工业上常用赤铁矿冶炼铁
D.铁与硫酸铜溶液的反应属于置换反应
4.现有甲、乙、丙三种金属,先将三者分别加入到硫酸亚铁溶液中,只有甲可使溶液中析出铁单质。再将三者加入到硝酸银溶液中,只有乙不能使溶液中析出银单质,则三者的金属活动性从强到弱的顺序是
A.甲>乙>丙 B.乙>甲>丙 C.甲>丙>乙 D.无法判断
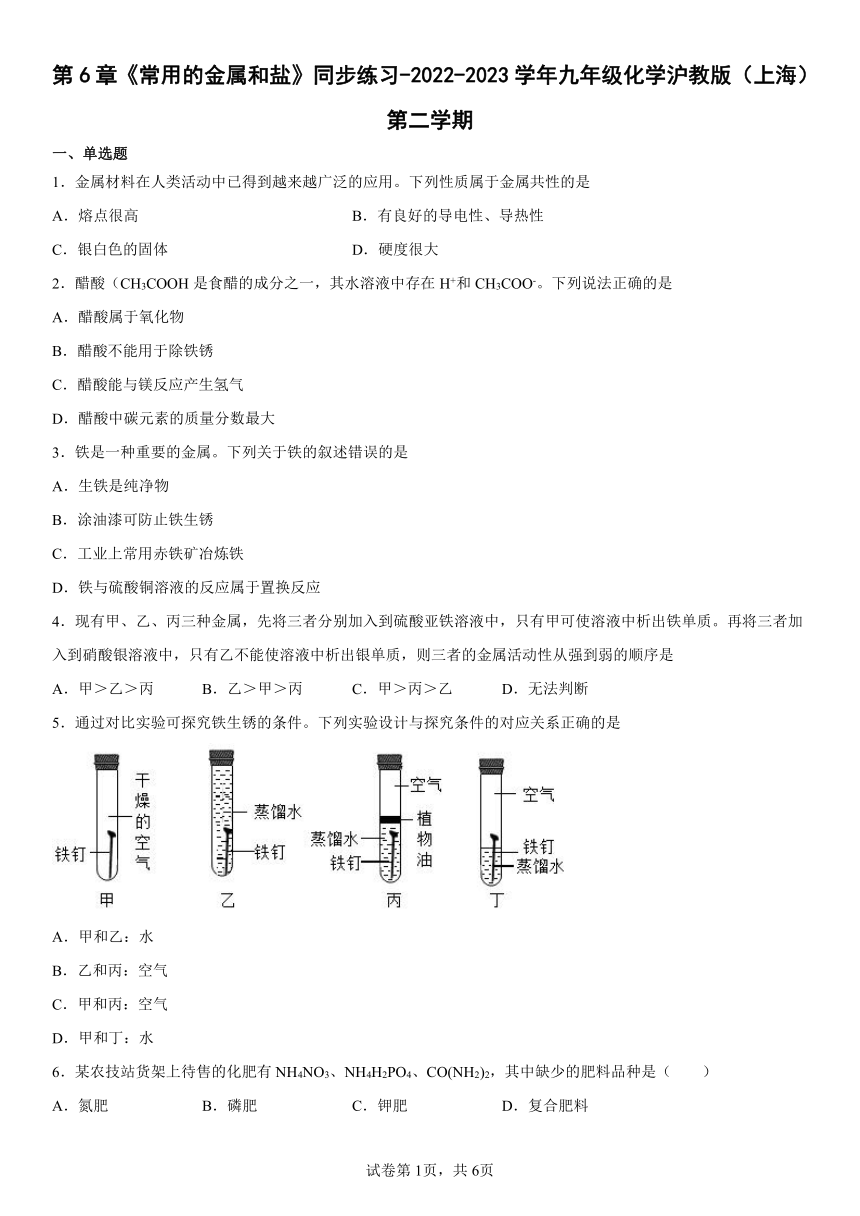
5.通过对比实验可探究铁生锈的条件。下列实验设计与探究条件的对应关系正确的是
A.甲和乙:水
B.乙和丙:空气
C.甲和丙:空气
D.甲和丁:水
6.某农技站货架上待售的化肥有NH4NO3、NH4H2PO4、CO(NH2)2,其中缺少的肥料品种是( )
A.氮肥 B.磷肥 C.钾肥 D.复合肥料
7.“中国高铁,世界第一”,高铁列车车体材料使用了含镍不锈钢,工业上火法炼镍的原理是:,下列说法错误的是( )
A.反应中NiO发生还原反应
B.气体产物中可能有CO
C.该不锈钢中还含有铁和碳
D.该不锈钢合金的硬度小于纯铁
8.下列做法正确的是
A.门捷列夫用定量的方法研究空气的成分
B.生活中可以用煮沸的方法降低水的硬度
C.我国的纯碱资源比较丰富,用纯碱来制取大量食盐
D.发现厨房燃气泄漏时,立即打开排风扇电源开关
9.下列方法中,能达到目的是
选项 物质(括号内为杂质) 除去杂质的方法
A CuSO4溶液(H2SO4) 加足量铜粉,过滤
B CaO(CaCO3) 加足量水溶解、过滤
C CO2(CO) 点燃
D FeC12溶液(CuCl2) 加入过量铁粉,过滤
A.A B.B C.C D.D
10.(2012年山东烟台,18题,2分)电影《黄金大劫案》上映后,里面用“王水”(浓盐酸与浓硝酸的混合液)溶解黄金的情引起了广泛的热议。黄金溶解在“王水”中形成HAuCl4(四氯合金酸),没有氢气产生。根据以上信息,下列有关说法正确的是
①“王水”溶解黄金是化学变化;②金比氢活泼;③HAuCl4中,Au的化合价为+3价;④可以将pH试纸伸入“王水”中测其酸碱度;⑤“王水”可以用铁质容器盛装。
A.①④⑤ B.①②③ C.③④⑤ D.①③
二、简答题
11.请用学过的知识回答下列关于燃烧与灭火的相关问题。
(1)酒精灯内的酒精不小心洒出,在桌面上燃烧起来,应采取的灭火方法是______。
(2)用嘴吹灭燃着的蜡烛,其灭火原理是______。
(3)请写一个氧化产物和还原产物相同的化学方程式______。
(4)将煤制成蜂窝状,其目的是______。
12.如图是某化肥包装袋上的部分说明:
(1)由标签上的注意事项推测一条碳酸氢铵具有的性质;
(2)请谈一点过量施用化肥的弊端。
13.一瓶未贴标签的粉末状常见金属R。为了测定R的相对原子质量,准确称取一定量金属粉末,在坩埚内加强热使其完全氧化,冷却后再称重。重复实验,获得如表数据。请回答:
实验次数 金属质量(g) 金属氧化物质量(g)
l 45.0 84.9
2 45.0 85.1
3 45.0 85.O
平均值 45.0 m
(1)表格中m= 。
(2)该金属氧化物中,R元素和氧元素的质量比为 。
(3)已知R的化合价为+3价,则R的相对原子质量为 。
三、推断题
14.构建知识网络是一种重要的学习方法.如图是关于铁化学性质的知识网络(“→”表示一种物质转化为另一种物质),其中B是密度最小的气体,C为红色固体单质.请回答下列问题:
(1)A物质的化学式为______.
(2)B物质的一种用途是______.
(3)写出反应③的方程式______.
15.A~H是初中化学常见物质。A~G中均含有一种相同元素。H中只含有两种元素,E为铁锈的主要成分,G广泛应用于玻璃、造纸、纺织和洗涤剂的生产等。A、B、C、F、G为五种不同类别物质,反应①放热。它们之间的转化和反应关系如图所示,图中“→”表示一种物质转化为另一种物质,“一”表示相连的两种物质能发生化学反应,部分反应物、生成物及反应条件已略去。请回答:
(1)写出物质化学式:B___________。C___________。
(2)反应②的化学方程式为___________。
(3)物质D在生产、生活中的用途___________(答出一点即可)。
四、实验题
16.如图,利用井穴板、打孔透明盖子、滴管和导管进行微型实验。
(1)井穴1中能证明石灰水和盐酸发生反应的现象是 ______ 。
(2)井穴2发生反应的化学方程式为 ______ 。
(3)欲证明未知粉末X中含有碳酸盐,实验操作为 ______ 。
17.化学小组为探究铁、铜、锌、银的金属活动性顺序,设计如下三个实验(其中金属均已打磨,其形状、大小及同种稀盐酸的用量均相同):
(1)实验①的化学方程式为 ______ ;一段时间后,观察到实验②的铜片表面有银白色固体附着,这说明铜比银的活动性 ______ (填“强”或“弱”)。
(2)甲同学认为通过实验①和③可比较锌和铁的金属活动性,他依据的实验现象是 ______ 。
(3)乙同学认为上述实验方案不足以得出四种金属的活动性顺序,并在上述实验的基础上补充了一个实验(如图所示),实现了探究目的,则乙同学的实验:X是金属 ______ ,Y是 ______ 溶液。
五、计算题
18.小娟想测定Cu-Zn合金和Cu-Ag合金中铜的质量分数,实验室只提供了一瓶稀盐酸和必要的仪器。
(1)你认为她能测出铜的质量分数的合金是_____合金。
(2)小娟取该合金的粉末32.5 g与足量的该盐酸充分反应后,经测定产生了0.4 g气体,请你帮助她计算出该合金中铜的质量分数_____。
19.生铁和钢都是铁和碳的合金,生铁含碳量为2%~4.3%,钢含碳量为0.03%~2%,化学兴趣小组的同学为确定该铁合金是生铁还是钢,他们取11.5g铁合金样品盛放到锥形瓶中,将100g稀盐酸分成5等份,分5次加入锥形瓶,每次待充分反应后记录实验数据。实验数据整理如下表所示:
次数 加盐酸前 第1次 第2次 第3次 第4次 第5次
加入稀盐酸的质量(g) 0 20 20 20 20 20
锥形瓶内物质的总质量(g) 11.5 31.4 m 71.2 91.1 111.1
【查阅资料】碳不与稀盐酸反应。
请回答下列问题:
(1)根据质量守恒定律,该反应中生成气体的总质量为 。
(2)实验数据表中m的值为 。
(3)请通过计算确定该铁合金是生铁还是钢(写出计算过程,计算结果保留到0.1%)。
20.鸡蛋壳的主要成分是碳酸钙。某兴趣小组为了测定鸡蛋壳中CaCO3的含量,取12.5g干燥的鸡蛋壳,捣碎放在烧杯中,然后向其中滴加某浓度的稀盐酸滴加过程中产生气体质量与所加稀盐酸质量的关系如图所示(鸡蛋壳中除CaCO3外的其他成分都不溶于水,也不与稀盐酸反应)。试计算:
(1)产生CO2的质量为 g。
(2)该鸡蛋壳中CaCO3的质量分数;
(3)所用稀盐酸溶质的质量分数。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.C
3.A
4.C
5.D
6.C
7.D
8.B
9.D
10.D
11. 用湿抹布盖灭 降温至蜡烛的着火点以下 增大可燃物与氧气的接触面积,促进燃烧
12.(1)易溶于水。 (2)过量施用化肥,对环境造成严重的影响,特别是水域和土壤的污染。
13.(1)85.0 (2)9:8 (3)27
14. Fe3O4 作燃料或冶炼金属 Fe+CuSO4=FeSO4+Cu
15. 灭火
16. 红色溶液变成无色 6HCl+Fe2O3=2FeCl3 +3H2O 在孔穴6中加入澄清石灰水,将稀盐酸挤入孔穴3
17. 强 锌表面产生气泡快,铁表面产生气泡慢 Fe(或Cu) CuSO4(或HCl)
18.(1)铜锌(2)60%
19.(1)0.4g;(2)51.3;(3)2.6%
20.(1)4.4(2)80%(3)7.3%
答案第1页,共2页
答案第1页,共2页
一、单选题
1.金属材料在人类活动中已得到越来越广泛的应用。下列性质属于金属共性的是
A.熔点很高 B.有良好的导电性、导热性
C.银白色的固体 D.硬度很大
2.醋酸(CH3COOH是食醋的成分之一,其水溶液中存在H+和CH3COO-。下列说法正确的是
A.醋酸属于氧化物
B.醋酸不能用于除铁锈
C.醋酸能与镁反应产生氢气
D.醋酸中碳元素的质量分数最大
3.铁是一种重要的金属。下列关于铁的叙述错误的是
A.生铁是纯净物
B.涂油漆可防止铁生锈
C.工业上常用赤铁矿冶炼铁
D.铁与硫酸铜溶液的反应属于置换反应
4.现有甲、乙、丙三种金属,先将三者分别加入到硫酸亚铁溶液中,只有甲可使溶液中析出铁单质。再将三者加入到硝酸银溶液中,只有乙不能使溶液中析出银单质,则三者的金属活动性从强到弱的顺序是
A.甲>乙>丙 B.乙>甲>丙 C.甲>丙>乙 D.无法判断
5.通过对比实验可探究铁生锈的条件。下列实验设计与探究条件的对应关系正确的是
A.甲和乙:水
B.乙和丙:空气
C.甲和丙:空气
D.甲和丁:水
6.某农技站货架上待售的化肥有NH4NO3、NH4H2PO4、CO(NH2)2,其中缺少的肥料品种是( )
A.氮肥 B.磷肥 C.钾肥 D.复合肥料
7.“中国高铁,世界第一”,高铁列车车体材料使用了含镍不锈钢,工业上火法炼镍的原理是:,下列说法错误的是( )
A.反应中NiO发生还原反应
B.气体产物中可能有CO
C.该不锈钢中还含有铁和碳
D.该不锈钢合金的硬度小于纯铁
8.下列做法正确的是
A.门捷列夫用定量的方法研究空气的成分
B.生活中可以用煮沸的方法降低水的硬度
C.我国的纯碱资源比较丰富,用纯碱来制取大量食盐
D.发现厨房燃气泄漏时,立即打开排风扇电源开关
9.下列方法中,能达到目的是
选项 物质(括号内为杂质) 除去杂质的方法
A CuSO4溶液(H2SO4) 加足量铜粉,过滤
B CaO(CaCO3) 加足量水溶解、过滤
C CO2(CO) 点燃
D FeC12溶液(CuCl2) 加入过量铁粉,过滤
A.A B.B C.C D.D
10.(2012年山东烟台,18题,2分)电影《黄金大劫案》上映后,里面用“王水”(浓盐酸与浓硝酸的混合液)溶解黄金的情引起了广泛的热议。黄金溶解在“王水”中形成HAuCl4(四氯合金酸),没有氢气产生。根据以上信息,下列有关说法正确的是
①“王水”溶解黄金是化学变化;②金比氢活泼;③HAuCl4中,Au的化合价为+3价;④可以将pH试纸伸入“王水”中测其酸碱度;⑤“王水”可以用铁质容器盛装。
A.①④⑤ B.①②③ C.③④⑤ D.①③
二、简答题
11.请用学过的知识回答下列关于燃烧与灭火的相关问题。
(1)酒精灯内的酒精不小心洒出,在桌面上燃烧起来,应采取的灭火方法是______。
(2)用嘴吹灭燃着的蜡烛,其灭火原理是______。
(3)请写一个氧化产物和还原产物相同的化学方程式______。
(4)将煤制成蜂窝状,其目的是______。
12.如图是某化肥包装袋上的部分说明:
(1)由标签上的注意事项推测一条碳酸氢铵具有的性质;
(2)请谈一点过量施用化肥的弊端。
13.一瓶未贴标签的粉末状常见金属R。为了测定R的相对原子质量,准确称取一定量金属粉末,在坩埚内加强热使其完全氧化,冷却后再称重。重复实验,获得如表数据。请回答:
实验次数 金属质量(g) 金属氧化物质量(g)
l 45.0 84.9
2 45.0 85.1
3 45.0 85.O
平均值 45.0 m
(1)表格中m= 。
(2)该金属氧化物中,R元素和氧元素的质量比为 。
(3)已知R的化合价为+3价,则R的相对原子质量为 。
三、推断题
14.构建知识网络是一种重要的学习方法.如图是关于铁化学性质的知识网络(“→”表示一种物质转化为另一种物质),其中B是密度最小的气体,C为红色固体单质.请回答下列问题:
(1)A物质的化学式为______.
(2)B物质的一种用途是______.
(3)写出反应③的方程式______.
15.A~H是初中化学常见物质。A~G中均含有一种相同元素。H中只含有两种元素,E为铁锈的主要成分,G广泛应用于玻璃、造纸、纺织和洗涤剂的生产等。A、B、C、F、G为五种不同类别物质,反应①放热。它们之间的转化和反应关系如图所示,图中“→”表示一种物质转化为另一种物质,“一”表示相连的两种物质能发生化学反应,部分反应物、生成物及反应条件已略去。请回答:
(1)写出物质化学式:B___________。C___________。
(2)反应②的化学方程式为___________。
(3)物质D在生产、生活中的用途___________(答出一点即可)。
四、实验题
16.如图,利用井穴板、打孔透明盖子、滴管和导管进行微型实验。
(1)井穴1中能证明石灰水和盐酸发生反应的现象是 ______ 。
(2)井穴2发生反应的化学方程式为 ______ 。
(3)欲证明未知粉末X中含有碳酸盐,实验操作为 ______ 。
17.化学小组为探究铁、铜、锌、银的金属活动性顺序,设计如下三个实验(其中金属均已打磨,其形状、大小及同种稀盐酸的用量均相同):
(1)实验①的化学方程式为 ______ ;一段时间后,观察到实验②的铜片表面有银白色固体附着,这说明铜比银的活动性 ______ (填“强”或“弱”)。
(2)甲同学认为通过实验①和③可比较锌和铁的金属活动性,他依据的实验现象是 ______ 。
(3)乙同学认为上述实验方案不足以得出四种金属的活动性顺序,并在上述实验的基础上补充了一个实验(如图所示),实现了探究目的,则乙同学的实验:X是金属 ______ ,Y是 ______ 溶液。
五、计算题
18.小娟想测定Cu-Zn合金和Cu-Ag合金中铜的质量分数,实验室只提供了一瓶稀盐酸和必要的仪器。
(1)你认为她能测出铜的质量分数的合金是_____合金。
(2)小娟取该合金的粉末32.5 g与足量的该盐酸充分反应后,经测定产生了0.4 g气体,请你帮助她计算出该合金中铜的质量分数_____。
19.生铁和钢都是铁和碳的合金,生铁含碳量为2%~4.3%,钢含碳量为0.03%~2%,化学兴趣小组的同学为确定该铁合金是生铁还是钢,他们取11.5g铁合金样品盛放到锥形瓶中,将100g稀盐酸分成5等份,分5次加入锥形瓶,每次待充分反应后记录实验数据。实验数据整理如下表所示:
次数 加盐酸前 第1次 第2次 第3次 第4次 第5次
加入稀盐酸的质量(g) 0 20 20 20 20 20
锥形瓶内物质的总质量(g) 11.5 31.4 m 71.2 91.1 111.1
【查阅资料】碳不与稀盐酸反应。
请回答下列问题:
(1)根据质量守恒定律,该反应中生成气体的总质量为 。
(2)实验数据表中m的值为 。
(3)请通过计算确定该铁合金是生铁还是钢(写出计算过程,计算结果保留到0.1%)。
20.鸡蛋壳的主要成分是碳酸钙。某兴趣小组为了测定鸡蛋壳中CaCO3的含量,取12.5g干燥的鸡蛋壳,捣碎放在烧杯中,然后向其中滴加某浓度的稀盐酸滴加过程中产生气体质量与所加稀盐酸质量的关系如图所示(鸡蛋壳中除CaCO3外的其他成分都不溶于水,也不与稀盐酸反应)。试计算:
(1)产生CO2的质量为 g。
(2)该鸡蛋壳中CaCO3的质量分数;
(3)所用稀盐酸溶质的质量分数。
试卷第1页,共3页
试卷第1页,共3页
参考答案:
1.B
2.C
3.A
4.C
5.D
6.C
7.D
8.B
9.D
10.D
11. 用湿抹布盖灭 降温至蜡烛的着火点以下 增大可燃物与氧气的接触面积,促进燃烧
12.(1)易溶于水。 (2)过量施用化肥,对环境造成严重的影响,特别是水域和土壤的污染。
13.(1)85.0 (2)9:8 (3)27
14. Fe3O4 作燃料或冶炼金属 Fe+CuSO4=FeSO4+Cu
15. 灭火
16. 红色溶液变成无色 6HCl+Fe2O3=2FeCl3 +3H2O 在孔穴6中加入澄清石灰水,将稀盐酸挤入孔穴3
17. 强 锌表面产生气泡快,铁表面产生气泡慢 Fe(或Cu) CuSO4(或HCl)
18.(1)铜锌(2)60%
19.(1)0.4g;(2)51.3;(3)2.6%
20.(1)4.4(2)80%(3)7.3%
答案第1页,共2页
答案第1页,共2页
