第3单元溶液复习
图片预览








文档简介
课件29张PPT。溶液复习温故知新溶液溶液的形成 溶液组成的定 量表示配制一定质量分数的溶液 1、定义:一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物,叫做溶液。溶液 2、溶液的宏观特征:
(1)均一性
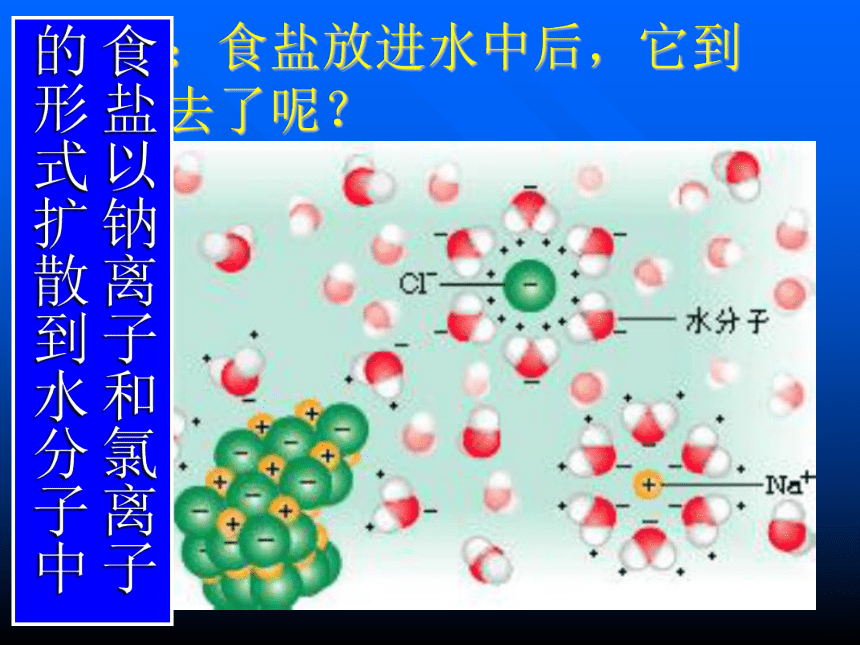
(2)稳定性思考:食盐放进水中后,它到哪里去了呢?食盐以钠离子和氯离子
的形式扩散到水分子中思考:蔗糖放进水中后,它到哪里去了呢?蔗糖分子扩散到水分子中蔗糖是由
蔗糖分子
构成 1、定义:一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物,叫做溶液。溶液 2、溶液的宏观特征:
(1)均一性
(2)稳定性以分子
或离子
的形式溶液的性质:
1.均一性、稳定性
2.某些溶液有导电性(如食盐水);
3.某些溶液有色(硫酸铜-蓝色、碘酒等)
4.形成溶液后沸点升高,
凝固点降低(融雪剂)(3)溶液的组成 ②溶剂:能溶解其它物质的物质叫溶剂。 ①溶质:被溶解的物质叫溶质。(4)溶液中溶质和溶剂的确定溶质: ①是固体、气体、液体
②可以是一种也可以是多种
溶剂:①水是最常用的溶剂,但酒精、
汽油也可以做溶剂;
②一种溶液中只有一种溶剂
③ 有水时,水一定是溶剂M液=M剂+M质 V液90ml豆油90ml酒精
10ml水溶质溶剂KMnO4水碘酒精HCl气体水汽油豆油酒精 水溶液的命名:一般叫做溶质的溶剂溶液。
如碘溶解在酒精中形成的溶液叫做碘的酒精溶液。酒精和水互溶后形成的溶液叫做酒精的水溶液。乳浊液及乳化现象
1.乳浊液:小液滴分散到液体里形成的混合物
叫做乳浊液。如牛奶、豆浆等。
2.乳化现象:在乳浊液中加入洗涤剂以后,油
虽然并没有溶解在水中,但这时形成的乳浊
液却能均匀、稳定地存在而不分层,这种现
象叫乳化现象。
注意:“乳化”不是溶解,只是使油分散成无数细
小的液滴存在于水中而不聚集。乳化现象
是一种物理变化。3.乳化作用在生活、生产中的应用:
(1)洗涤:用乳化剂(洗涤剂)可以将衣服、
餐具上的油垢洗掉;
(2)农药的使用:在农药中加入一定量的乳
化剂后,再溶解在有机溶剂里,混合均
匀后制成的透明液体叫乳油。如敌敌畏
乳油;
(3)生活中常用的乳化剂:肥皂、洗洁精等。溶解作用:汽油洗油污,形成溶液;
乳化作用:洗涤剂洗油污,形成乳浊液。对比记忆洗发膏、洗衣粉、洗衣液等是常见的乳化剂。讨论:试比较悬浊液、乳浊液和溶液的区别分散的微粒分散物状态宏观特征实例溶液悬浊液乳浊液分子或离子固、气、液均一、
稳定食盐水分子集合体固态不均一、
不稳定泥浆分子集合体液态不均一、
不稳定牛奶溶解时的吸热或放热现象探究:NaCl、NH4NO3、 NaOH 三种物质溶于水后溶液的温度改变.为什么会放热或吸热?物质溶解过程中常常伴随着吸热或放热现象.溶质的分子向水中扩散,这一过程吸收热量,溶质的分子和水分子作用,生成水合分子,这一过程放出热量。吸收或放出热量不同,就产生温度的变化.一定温度下,一定量的溶剂中,不能再溶解某种溶质的溶液称为该溶质的饱和溶液。一定温度下,一定量的溶剂中,还能再溶解某种溶质的溶液称为该溶质的不饱和溶液。溶液的饱和与不饱和练习:在T℃时,将100克饱和的蔗糖溶液与100克饱和的氯化钠溶液分混合(两种溶液互溶时不发生化学反应,温度不变),所得溶液( )
A、绿化钠的饱和溶液 B、蔗糖的饱和溶液
C、两者的饱和溶液 D、两者的不饱和溶液D饱和
溶液不饱和
溶液加溶剂 升温加溶质 蒸发溶剂 降温氢氧化钙:温度越高,在水中溶解能力越弱。氢氧化钙反之现有一杯硝酸钾溶液,怎样知道它是否饱和?溶液是否饱和的识别方法:
继续加入少量该溶质,看是否继续溶解。一杯饱和的硝酸钾溶液,是否可以继续溶解其他溶质?如食盐?它是硝酸钾的饱和溶液,不是食盐的饱和溶液,所以它还可以继续溶解食盐。饱和、
不饱和溶液与浓、稀溶液的关系既是不饱和溶液又是浓溶液既是不饱和溶液又是稀溶液既是饱和溶液又是浓溶液既是饱和溶液又是稀溶液判断正误:
1.饱和溶液一定比不饱和溶液浓。
2.同种物质的饱和溶液一定比不饱和溶液浓。
3.同一温度下饱和溶液一定比不饱和溶液浓。
4.同温、同溶质时饱和溶液一定比不饱和溶液浓。
×××√溶质的质量分数表达式 千万别丢下我啊! 谢谢噢!注意:1、溶质、溶剂、溶液的量均以质量表示, 单位要统一,最后计算结果换算成百分数的形式。
2、溶质的质量是指溶解在溶剂中形成溶液 的那部分质量,不包括未溶解的溶质的质量。含义:描述任意状态下溶液中溶质所占整个溶液的比例是多少。(即每100份质量溶液中含a份质量的溶质)
想一想:5%的氯化钠溶液的含义是什么?
公式变形
1、溶质的质量 = 溶液的质量×溶质的质量分数
2、溶液的质量 = 溶质的质量 / 溶质的质量分数
3、溶剂的质量 = 溶液的质量 -溶质的质量 下表是某温度时NaCl溶液中的质量,请填表:5190405%105%15016%1.上下写出原溶液中溶质、溶液的质量
2.判断出上、下是加还是减,并写出
3.计算结果 9g
90g 9g
90g+10g 9%配制溶质质量分数一定的溶液:
1、步骤
(1)计算 (2)称量 (3)溶解( 4)装瓶2. 所用到的仪器:托盘天平、药匙、量筒、 胶头滴管、烧杯、玻璃棒
量取
(1)均一性
(2)稳定性思考:食盐放进水中后,它到哪里去了呢?食盐以钠离子和氯离子
的形式扩散到水分子中思考:蔗糖放进水中后,它到哪里去了呢?蔗糖分子扩散到水分子中蔗糖是由
蔗糖分子
构成 1、定义:一种或几种物质分散到另一种物质里,形成均一的、稳定的混合物,叫做溶液。溶液 2、溶液的宏观特征:
(1)均一性
(2)稳定性以分子
或离子
的形式溶液的性质:
1.均一性、稳定性
2.某些溶液有导电性(如食盐水);
3.某些溶液有色(硫酸铜-蓝色、碘酒等)
4.形成溶液后沸点升高,
凝固点降低(融雪剂)(3)溶液的组成 ②溶剂:能溶解其它物质的物质叫溶剂。 ①溶质:被溶解的物质叫溶质。(4)溶液中溶质和溶剂的确定溶质: ①是固体、气体、液体
②可以是一种也可以是多种
溶剂:①水是最常用的溶剂,但酒精、
汽油也可以做溶剂;
②一种溶液中只有一种溶剂
③ 有水时,水一定是溶剂M液=M剂+M质 V液
10ml水溶质溶剂KMnO4水碘酒精HCl气体水汽油豆油酒精 水溶液的命名:一般叫做溶质的溶剂溶液。
如碘溶解在酒精中形成的溶液叫做碘的酒精溶液。酒精和水互溶后形成的溶液叫做酒精的水溶液。乳浊液及乳化现象
1.乳浊液:小液滴分散到液体里形成的混合物
叫做乳浊液。如牛奶、豆浆等。
2.乳化现象:在乳浊液中加入洗涤剂以后,油
虽然并没有溶解在水中,但这时形成的乳浊
液却能均匀、稳定地存在而不分层,这种现
象叫乳化现象。
注意:“乳化”不是溶解,只是使油分散成无数细
小的液滴存在于水中而不聚集。乳化现象
是一种物理变化。3.乳化作用在生活、生产中的应用:
(1)洗涤:用乳化剂(洗涤剂)可以将衣服、
餐具上的油垢洗掉;
(2)农药的使用:在农药中加入一定量的乳
化剂后,再溶解在有机溶剂里,混合均
匀后制成的透明液体叫乳油。如敌敌畏
乳油;
(3)生活中常用的乳化剂:肥皂、洗洁精等。溶解作用:汽油洗油污,形成溶液;
乳化作用:洗涤剂洗油污,形成乳浊液。对比记忆洗发膏、洗衣粉、洗衣液等是常见的乳化剂。讨论:试比较悬浊液、乳浊液和溶液的区别分散的微粒分散物状态宏观特征实例溶液悬浊液乳浊液分子或离子固、气、液均一、
稳定食盐水分子集合体固态不均一、
不稳定泥浆分子集合体液态不均一、
不稳定牛奶溶解时的吸热或放热现象探究:NaCl、NH4NO3、 NaOH 三种物质溶于水后溶液的温度改变.为什么会放热或吸热?物质溶解过程中常常伴随着吸热或放热现象.溶质的分子向水中扩散,这一过程吸收热量,溶质的分子和水分子作用,生成水合分子,这一过程放出热量。吸收或放出热量不同,就产生温度的变化.一定温度下,一定量的溶剂中,不能再溶解某种溶质的溶液称为该溶质的饱和溶液。一定温度下,一定量的溶剂中,还能再溶解某种溶质的溶液称为该溶质的不饱和溶液。溶液的饱和与不饱和练习:在T℃时,将100克饱和的蔗糖溶液与100克饱和的氯化钠溶液分混合(两种溶液互溶时不发生化学反应,温度不变),所得溶液( )
A、绿化钠的饱和溶液 B、蔗糖的饱和溶液
C、两者的饱和溶液 D、两者的不饱和溶液D饱和
溶液不饱和
溶液加溶剂 升温加溶质 蒸发溶剂 降温氢氧化钙:温度越高,在水中溶解能力越弱。氢氧化钙反之现有一杯硝酸钾溶液,怎样知道它是否饱和?溶液是否饱和的识别方法:
继续加入少量该溶质,看是否继续溶解。一杯饱和的硝酸钾溶液,是否可以继续溶解其他溶质?如食盐?它是硝酸钾的饱和溶液,不是食盐的饱和溶液,所以它还可以继续溶解食盐。饱和、
不饱和溶液与浓、稀溶液的关系既是不饱和溶液又是浓溶液既是不饱和溶液又是稀溶液既是饱和溶液又是浓溶液既是饱和溶液又是稀溶液判断正误:
1.饱和溶液一定比不饱和溶液浓。
2.同种物质的饱和溶液一定比不饱和溶液浓。
3.同一温度下饱和溶液一定比不饱和溶液浓。
4.同温、同溶质时饱和溶液一定比不饱和溶液浓。
×××√溶质的质量分数表达式 千万别丢下我啊! 谢谢噢!注意:1、溶质、溶剂、溶液的量均以质量表示, 单位要统一,最后计算结果换算成百分数的形式。
2、溶质的质量是指溶解在溶剂中形成溶液 的那部分质量,不包括未溶解的溶质的质量。含义:描述任意状态下溶液中溶质所占整个溶液的比例是多少。(即每100份质量溶液中含a份质量的溶质)
想一想:5%的氯化钠溶液的含义是什么?
公式变形
1、溶质的质量 = 溶液的质量×溶质的质量分数
2、溶液的质量 = 溶质的质量 / 溶质的质量分数
3、溶剂的质量 = 溶液的质量 -溶质的质量 下表是某温度时NaCl溶液中的质量,请填表:5190405%105%15016%1.上下写出原溶液中溶质、溶液的质量
2.判断出上、下是加还是减,并写出
3.计算结果 9g
90g 9g
90g+10g 9%配制溶质质量分数一定的溶液:
1、步骤
(1)计算 (2)称量 (3)溶解( 4)装瓶2. 所用到的仪器:托盘天平、药匙、量筒、 胶头滴管、烧杯、玻璃棒
量取
同课章节目录
- 第一单元 步入化学殿堂
- 第一节 化学真奇妙
- 第二节 体验化学探究
- 到实验室去:化学实验基本技能训练(一)
- 第二单元 探秘水世界
- 第一节 运动的水分子
- 第二节 水分子的变化
- 第三节 原子的构成
- 第四节 元素
- 到实验室去:化学实验基本技能训练(二)
- 第三单元 溶液
- 第一节 溶液的形成
- 第二节 溶液组成的定量表示
- 到实验室去:配制一定溶质质量分数的溶液
- 第四单元 我们周围的空气
- 第一节 空气的成分
- 第二节 物质组成的表示
- 第三节 氧气
- 到实验室去:氧气的实验室制取与性质
- 第五单元 定量研究化学反应
- 第一节 化学反应中的质量守恒
- 第二节 化学反应的表示
- 第三节 化学反应中的有关计算
- 到实验室去:探究燃烧的条件
- 第六单元 燃烧与燃料
- 第一节 燃烧与灭火
- 第二节 化石燃料的利用
- 第三节 大自然中的二氧化碳
- 到实验室去:二氧化碳的实验室制取与性质
